Neurosci Biobehav Ds. 2011 Jan; 35 (3): 939-55. doi: 10.1016 / j.neubiorev.2010.10.014. Epub 2010 Nov 2.
- 1Bernard B. Brodie Departement Neurowetenschappen, Universiteit van Cagliari, Cittadella Universitaria, 09042 Monserrato, CA, Italië. [e-pos beskerm]
OPSOMMING
Oksitosien is 'n kragtige inducer van penile ereksie wanneer dit in die sentrale senuweestelsel ingespuit word. By manlike rotte is die sensitiefste breinarea vir die pro-erektiele effek van oksitosien die paraventrikulêre kern van die hipotalamus. Hierdie kern en omliggende streke bevat die selliggame van alle oksitokinergiese neurone wat uitsteek na buitehypothalamiese breinareas en die rugmurg. Hierdie oorsig toon dat oksitosien ook penile ereksie veroorsaak wanneer dit in sommige van hierdie areas ingespuit word (bv. Ventrale tegmentale area, ventrale subikulum van die hippokampus, posteromediale kortikale kern van die amygdala- en thorak-lumbale rugmurg). Mikroinjectiestudies gekombineer met intra-serebrale mikrodialise en dubbele immunofluorescensstudies dui daarop dat oksitosien in hierdie gebiede direk of indirek (hoofsaaklik deur glutamiensuur) mesolimbiese dopaminerge neurone aktiveer. Dopamien vrygestel in die kern accumbens aktiveer op sy beurt neurale weë wat lei tot die aktivering van incerto-hipotalamiese dopaminerge neurone in die paraventrikulêre kern. Dit aktiveer nie net oksitosinergiese neurone wat na die rugmurg en mediasie penile ereksie uitsteek nie, maar ook diegene wat na die bogenoemde ekstrahypothalamiese areas produseer, wat direk of indirek (deur glutamiene suur) die aktiwiteit van mesolimbiese dopaminerge neurone reguleer wat motivering en beloning beheer. Saam kan hierdie neurale bane 'n komplekse hipotetiese kring vorm, wat nie net in die verbruiksfase van seksuele aktiwiteit (erektiele funksie en kopulasie) 'n rol speel nie, maar ook in die motiverende en lonende aspekte van die aanvanklike fase van seksuele gedrag.
1.Introduction
Penile ereksie is 'n manlike seksuele reaksie wat 'n sleutelrol speel in die voortplanting van soogdiere insluitend die mens, en dit kan ook waargeneem word in kontekste wat verskil van dié wat streng verband hou met voortplanting. Afhangende van die konteks waarin penile ereksie voorkom, neem verskillende sentrale en perifere neurale en / of humorale meganismes deel aan die regulering daarvan (sien Meisel en Sachs, 1994, Argiolas en Melis, 1995, 2004, 2005, Sachs, 2000, 2007, McKenna, 2000; Giuliano en Rampin, 2000, 2004; Andersson, 2001; Melis en Argiolas; 1995a; 2003; Hull et al., 2002). Onder sentrale neurotransmitters en neuropeptiede wat penile ereksie beheer, is die bekendste dopamien, serotonien, eksitatoriese aminosure, stikstofoksied, adrenokortikotropien, oksitosien en opioïede peptiede. Hulle kan penile ereksie fasiliteer of inhibeer deur in verskeie breinareas op te tree, dws die mediale preoptiese area, die paraventrikulêre kern van die hipotalamus, die ventrale tegmentale area, die hippokampus, die amygdala, die bedkern van die stria terminusse, die nucleus accumbens, die medulla oblongata en die rugmurg (Tabel 1) (sien Meisel en Sachs, 1994, Witt en Insel, 1994, Stancampiano et al., 1994; Argiolas en Melis; 1995; 2005; Argiolas; 1999; Bancila et al., 2002; Giuliano en Rampin, 2000, McKenna, 2000; Andersson, 2001; Hull et al., 2002; Coolen et al., 2004).
Oksitosien, die neuro-hipofiseale peptied wat bekend staan vir sy hormonale rol in laktasie en bevalling, is teenwoordig in vroue en mans, nie net in neurone met selliggame in die paraventrikulêre en supraoptiese kern van die hipotalamus wat na die neuro-hipofise uitsteek nie, maar ook in neurone wat uitsteek. van die paraventrikulêre kern en omliggende strukture tot ekstrahypothalamiese breinareas (dws die septum, die ventrale tegmentale area, die hippokampus, die amygdala, die medulla oblongata en die rugmurg). Hierdie neurone word vermoedelik betrokke by talle sentrale funksies, soos geheue, leer, affiliatiewe en sosio-seksuele gedrag, insluitende penile ereksie en copulatoriese gedrag (sien Buijs, 1978, Sofroniew, 1983, Argiolas en Gessa, 1991; Pedersen et al . 1992; Carter, 1992; Wagner en Clemens; 1993; Ivell en Russel; 1995; Carter et al., 1997; Tang et al., 1998; Veronneau-Longueville et al., 1999). Inderdaad, oksitosien fasiliteer erektiele funksie en manlike seksuele gedrag in muise, rotte, hase en ape (sien Argiolas en Gessa, 1991, Carter, 1992, Pedersen et al., 1992; Argiolas en Melis, 1995, 2004; Argiolas, 1999). Dit kan ook by mense voorkom, aangesien plasmaoksitosien verhoog word deur seksuele stimuli, veral by ejakulasie (Carmichael et al., 1987, Murphy et al., 1987) en deur die manipulasie van bors en van die genitalieë, wat gewoonlik tydens seksuele gedrag voorkom omgang (Tindall, 1974).
'N Fasilitatiewe effek van oksitosien op manlike seksuele gedrag is eers getoon deur die vermoë van intraveneuse oksitosien om die latensie vir die eerste ejakulasie te verminder en om seksuele uitputting van manlike konyne wat met ontvanklike vroue (Melin en Kihlstrom, 1963) gepaard gaan, te vertraag. Die seksuele effekte van oksitosien is egter eers in die tagtigerjare definitief erken. Oksitosien wat sentraal in nanogram gegee word, is dan gevind om penile ereksie (Argiolas et al., 1985, 1986) te bewerkstellig, en om copulatoriese gedrag (Arletti et al., 1985) by manlike rotte te verbeter en om lordose in vroulike rotte te verhoog (Arletti en Bertolini, 1985, Caldwell et al., 1986), blykbaar deur middel van baarmoeder-oksitosinere reseptore (sien Argiolas en Melis, 1995, 2004, Argiolas, 1999, Melis en Argiolas, 2003 en verwysings daarin). Oksitosien verbeter seksuele gedrag nie net in seksueel sterk manlike rotte (Arletti et al., 1985) nie, maar ook in ouer manlike rotte (Arletti et al., 1990), en in dominante, maar nie in ondergeskikte, manlike eekhorings-ape (Winslow en Insel , 1991).
Die pro-erektiele effek van oksitosien is testosteroon afhanklik, aangesien dit afgeskaf word deur hipofisektomie en kastrasie, en herstel deur aanvulling met testosteroon of sy metaboliete, estradiol en 5_-dihydro-testosteroon wat saam gegee word. (Melis et al., 1994a). Die mees sensitiewe breinarea vir die induksie van penile ereksie deur oksitosien is die paraventrikulêre kern van die hipotalamus (Melis et al., 1986), waaruit alle ekstra hipotalamiese oksitosinêre projeksies ontstaan (sien hierbo). Hier is gevind dat oksitosien penile ereksie (en gaande) kan veroorsaak wanneer dit teen dosisse van so laag as 3 pmol ingespuit word (sien Afdeling 2.1 hieronder). Oksitosien-geïnduksieerde penile ereksie, ook wanneer dit in die CA1-veld van die hippokampus ingespuit word, maar nie in die dorsale subikulum nie (sien Afdeling 2.3 hieronder), die laterale septum, die caudaat-kern, die mediale preoptiese area, die ventromediale kern van die hipotalamus en die supraoptiese kern (Melis et al., 1986). Met betrekking tot die meganisme waarmee oksitosien in die paraventrikulêre kern optree om hierdie seksuele respons te bewerkstellig, dui talle studies daarop dat oksitosien sy eie neurone aktiveer. In ooreenstemming met hierdie hipotese, verhoog seksuele interaksie FOS, die geenproduk van die onmiddellike vroeë geen c-fos in paraventrikulêre oksitosinere neurone wat na die rugmurg uitsteek, wat betrokke is by die beheer van penile ereksie (sien Witt en Insel, 1994 en verwysings daarin) en seksuele impotensie (bv. die onvermoë van 'n volwasse manlike rat om met 'n ovariectomized estrogeen-progesteron-geprimeerde ontvanklike vrou te kopieer) is geassosieer met die manlike rat met lae vlakke van oksitosien mRNA in die paraventrikulêre kern van die hipotalamus (Arletti et al., 1997).
Of oksitosien die voornemende fase of die verbruiksfase van seksuele gedrag beïnvloed, is tans onduidelik. Aangesien oksitosien penile ereksie veroorsaak, en die hoof-effek van oksitosien op kopulatoriese gedrag is 'n afname in die post-ejakulatoriese interval in manlike rotte (Arletti et al., 1985), is dit redelik om te aanvaar dat die peptied seksuele prestasie verbeter. Aangesien oksitosien egter ook sosio-seksuele interaksies verhoog (sien Pedersen et al., 1992, Carter et al., 1997, Ivell en Russel, 1995) en oksitosienreseptorantagoniste voorkom nie-kontak-ereksies (Melis et al., 1999a) word beskou as 'n indeks van seksuele opwinding (sien Sachs, 1997, 2000, 2007, Melis et al., 1998, 1999b en verwysings daarin), 'n moontlike rol van oksitosien in seksuele opwinding en seksuele motivering kan nie uitgesluit word nie.
Hierdie oorsig gee 'n opsomming van gepubliseerde en ongepubliseerde resultate van onlangse studies, wat daarop dui dat oksitosien induceer penile ereksie nie net wanneer dit in die paraventrikulêre kern van die hipotalamus ingespuit word nie, maar ook in ander buite-hipotalamiese breinareas, soos die ventrale tegmentale area (Melis et al., 2007, 2009a, Succu et al., 2008), thy ventrale subikulum van die hippocampus en die posterior kern van die amygdala (Melis et al., 2009b, 2010), wat belangrike bestanddele van die limbiese stelsel is en word beskou as 'n sleutelrol in motivering en beloningsprosesse. Hierdie studies toon aan dat oksitosien deelneem aan neurale stroombane, wat ander neurotransmitters insluit, soos dopamien en glutamiene suur, en ander breinareas behalwe die paraventrikulêre kern, bv. Die ventrale tegmentale area, die nucleus accumbens, die hippocampus en areas wat nog nie geïdentifiseer. Hierdie stroombane sal waarskynlik 'n interaksie tussen die mesolimbiese en die incerto-hipotalamiese dopaminerge sisteem bemiddel en nie net in die verbruiksfase van manlike seksuele gedrag (bv. Penile ereksie en copulasie) speel nie, maar ook in seksuele motivering en seksuele opwekking, dus 'n neurale substraat vir die verduideliking van die motiverende en bevredigende eienskappe van seksuele aktiwiteit.
2. Oksitosien beïnvloed penile ereksie deur in verskillende breinareas op te tree
2.1. Die paraventrikulêre kern van die hipotalamus
Soos hierbo genoem, is die paraventrikulêre kern van die hipotalamus gou geïdentifiseer as die breinarea wat die sensitiefste vir oksitosien is. Wanneer eensydig in hierdie kern geïnjecteer is, is oksitosien aktief gevind teen dosisse so laag as 3 ng (3 pmol) (Melis et al., 1986). Struktuur-aktiwiteitsverhoudingstudies het getoon dat oksitosien-geïnduceerde penile ereksie gemedieer is deur uterinetipe oksitosienreseptore, gekoppel aan 'n Ca2 + -toevoer in die selliggame van oksitosinergiese neurone wat uitsteek na ekstrahypothalamiese breinareas en die aktivering van stikstofoksied-sintase. Koolstofoksied op sy beurt deur op te tree as 'n intrasellulêre boodskapper met 'n nog onbekende meganisme (waarby nie-guanilaat-siklas betrokke is), lei tot die aktivering van oksitosinergiese neurone wat na die rugmurg- en ekstrahypothalamiese breinareas uitsteek, wat penile ereksie veroorsaak (Fig. 1). hieronder en Argiolas en Melis, 1995, 2004, 2005 en verwysings daarin). Die vermoë van oksitosien om sy eie neurone te aktiveer
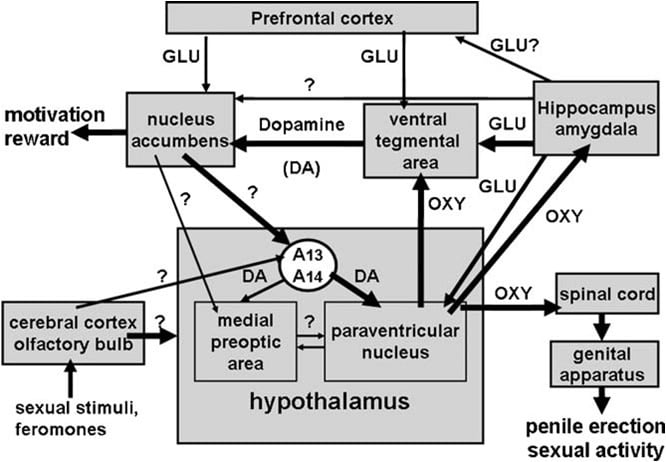
Fig. 1. (MISSING) Skematiese voorstelling van oksitosinergiese neurone, wat ontstaan in die paraventrikulêre kern van die hipotalamus en projekteer na buitehypothalamiese breinareas, soos die rugmurg, die VTA, die hippokampus, die amygdala, ens. Die aktivering van hierdie neurone deur dopamien, opwindende aminosure, oksitosien self, heksarelin analoogpeptiede en VGF-afgeleide peptiede lei tot penis oprigting, wat verminder kan word en / of afgeskaf word deur die stimulering van GABAergic, opioïde en cannabinoïde CB1 reseptore. Die aktivering van oksitosinergiese neurone is sekondêr tot die aktivering van stikstofoksied-sintase teenwoordig in hierdie neurone. Inderdaad, endogene stikstofoksied wat gevorm word deur die stimulering van dopamien-, eksitatoriese aminosuur- of oksitosienreseptore of eksogene stikstofoksied, soos dit afgelei word van stikstofoksieddonante wat direk in die paraventrikulêre kern gegee word, aktiveer oksitokinergiese neurone deur 'n nog onbekende meganisme wat blykbaar nie verband hou met die stimulering van guanilaat-siklas. Dit veroorsaak op sy beurt die vrystelling van oksitosien in die rugmurg en in ekstra-hipotalamiese breinareas. 'N Paar besonderhede oor die meganismes waardeur oksitosien penile ereksie veroorsaak wanneer dit in hierdie gebiede vrygestel word, bv. Die VTA, die ventrale subikulum en die amygdala, word in die onderskeie breinarea-afdelings beskryf. Hier handel oksitosien op sy eie reseptore en verhoog NO produksie, wat lei tot penis oprigting soos in die PVN gevind. In teenstelling met die PVN aktiveer egter in die caudale VTA NO guanilaat-siklas. Dit veroorsaak 'n toename in cGMP konsentrasie wat lei tot die aktivering van mesolimbiese dopaminerge neurone en tot penile ereksie. In die VSA NO aktiveer glutamatergiese neurone wat na buite-hippocampale gebiede, insluitende die VTA, uitsteek. Glutamiene suur in die VTA aktiveer op sy beurt mesolimbiese dopaminerge neurone soos aangetoon met oksitosien. Meganismes soortgelyk aan dié wat hierbo beskryf word, sal waarskynlik ook funksioneer wanneer penile ereksie in fisiologiese kontekste voorkom, naamlik wanneer manlike rotte in die teenwoordigheid van 'n ontoeganklike ontvanklike vrou geplaas word (bv. Niekontakte ereksies) of tydens copulasie.
in die paraventrikulêre kern is ondersteun deur studies wat toon dat: (1) oksitosienreseptore is teenwoordig in hierdie hipotalamiese kern (Freund-Mercier et al., 1987; Freund-Mercier en Stoeckel, 1995); (2) oksitosien fasiliteer sy eie vrystelling in vitro en in vivo (Freund-Mercier en Richard, 1981, 1984; Moos et al., 1984); en (3) oksitosien opgewonde sy eie neurone deur op te tree in die paraventrikulêre kern (Yamashita et al., 1987). Daarbenewens is oksitokinergiese sinapse wat op die selliggame van magnokellulêre oksitosinergiese neurone raak, ook geïdentifiseer in die paraventrikulêre en supraoptiese kern van die hipotalamus (Theodosis, 1985). Ten slotte word die vernietiging van sentrale oksitosinergiese neurone deur elektrolytiese of chemiese eksitotoksiese letsels van die paraventrikulêre kern, wat die oksitosieninhoud heeltemal oor die sentrale senuweestelsel en die rugmurg afbreek, nie net die pro-erektiele effek van oksitosien afskaf nie, maar verminder ook geneesmiddel-geïnduseerde penis oprigting en noncontact ereksies (sien hieronder en Argiolas et al., 1987a, b; Liu et al., 1997 en verwysings daarin). Resultate soortgelyk aan dié wat met letsels van die paraventrikulêre kern voorkom, word aangetref met kragtige en selektiewe oksitosienreseptorantagoniste. Inderdaad, hierdie verbindings wat in die paraventrikulêre kern ingespuit is in nanogramme, het heeltemal oksitosin-geïnduceerde penile ereksie verhoed, terwyl dit in die laterale ventrikels gegee word, het nie net penile ereksies geïnduceerd deur oksitosien self nie, maar ook dwelm-geïnduseerde penile ereksie (sien Afdeling 3 hieronder en Argiolas en Melis, 1995, 2004, 2005 en verwysings daarin) en nie-kontaksie-ereksies (Melis et al., 1999a), en was ook baie effektief in die verswakking van kopulatoriese gedrag van seksueel sterk manlike rotte (Argiolas et al., 1988). Verder verhoog seksuele interaksie FOS, die geenproduk van die onmiddellike vroeë gene c-fos in paraventrikulêre oksitosinere neurone wat na die rugmurg wat betrokke is by die beheer van penile ereksie (sien Witt en Insel, 1994 en verwysings daarin). Ten slotte, seksuele impotensie (bv. die onvermoë van 'n volwasse manlike rat om met 'n estrogeen-progesteron-geprimeerde ontvanklike vrou te kopieer) hsoos ook in die manlike rat geassosieer met lae vlakke van oksitosienmRNA en van stikstofoksiedsintase in die paraventrikulêre kern van die hipotalamus (Benelli et al., 1995; Arletti et al., 1997) (vir 'n uitgebreide oorsig van hierdie studies sien Argiolas, 1999; Argiolas en Melis, 2004, 2005).
2.2. Die ventrale tegmentale area
Die ventrale tegmentale area is eers onlangs as 'n breinwerf ontdek, waarby oksitosien penile ereksie veroorsaak. Hierdie area bevat oksitosinergiese senuwee eindes wat ontstaan in die paraventrikulêre kern en oksitosienreseptore (Freund-Mercier et al., 1987, Vaccari et al., 1998). Meer spesifiek, is oksitosien bevind dat ek in staat isnuwende penile ereksie wanneer dit eensydig in die caudale ingespuit word, maar nie in die rostrale ventrale tegmentale area nie op 'n dosis afhanklike wyse (Melis et al., 2007). Die aktiewe dosisse was hoër as dié wat benodig word wanneer dit in die paraventrikulêre kern ingespuit word en soortgelyk aan die induksie van penile ereksie wanneer dit ingespuit word in die ventrikulêre subikulum van die hippokampus of in die posteremediale kortikale kern van die amygdala (sien hieronder). Klaarblyklik word die pro-erektiele effek bemiddel deur die aktivering van mesolimbiese dopaminerge neurone wat na die dop van die nucleus accumbens uitsteek, wat op sy beurt nog onbekende neurale bane aktiveer wat na die incerto-hipotalamiese dopaminerge neurone impakteer op paraventrikulêre oksitosinere neurone wat penile ereksie bemiddel (Melis et al., 2007, 2009a).
Met betrekking tot die meganisme waardeur oksitosien dopaminerge neurotransmissie in die ventrale tegmentale area aktiveer, dui die beskikbare data aan dat oksitosien stimuleer oksitosinere reseptore wat in die selliggame van mesolimbiese dopaminerge neurone geleë is. Dit verhoog Ca2 + instroming binne die selliggame van dopaminerge neurone, waardeur stikstofoksied-sintase (Succu et al., 2008) geaktiveer word. In teenstelling met die paraventrikulêre kern (sien Afdeling 3 hieronder), aktiveer stikstofoksied op sy beurt guanylaat-siklas, waardeur die konsentrasie van sikliese GMP verhoog word. In ooreenstemming met hierdie meganisme is óf d (CH2) 5Tyr (Me) 2-Orn8-vasotosien, 'n kragtige oksitosienantagonis of S-metiel-tio-l-sitrolien, 'n kragtige inhibitor van neuronale stikstofoksied-sintase, ingespuit in die caudale ventrale tegmentale area voor oksitosien, afskaffing van penile ereksie en die toename in ekstra-sellulêre dopamien konsentrasie in die dop van die nukleosakens veroorsaak deur oksitosien. Daarbenewens induceer 8-broom-sikliese GMP, 'n aktiewe fosfodiesterasebestuurde sikliese GMP-analoog, penile ereksie wanneer dit ingespuit word in die caudale ventrale tegmentale area en verhoog die ekstra-sellulêre dopamien konsentrasie in die dop van die nucleus accumbens, soos gevind met oksitosien geïnjecteerd in die caudale ventrale tegmentale area (Succu et al., 2008; Melis et al., 2009a) (sien ook Fig. 2).
Altyd in lyn met hierdie meganisme, verminder haloperidol, 'n kragtige dopamien D2-reseptor antagonis, wat in die dop van die nucleus accumbens ingespuit word, penile ereksie wat deur oksitosien geïnduceerd word in die ventrale tegmentale area (Melis et al., 2007). Die bogenoemde meganisme word ook ondersteun deur dubbele immuno-fluorescensstudies, wat daarop dui dat oksitosienvezels op die selliggame van dopaminerge neurone in die caudale ventrale tegmentale area, wat voorheen gemerk is met die retrograde-spore Fluorogold wat in die dop van die nukleusbalk ingespuit is, beïnvloed ( Melis et al., 2007; Succu et al., 2008). Die aktiverings van hierdie dopaminerge neurone en van dopamienreseptore in die nukleus-reseptore lei op sy beurt tot die aktivering van neurale bane wat nog geïdentifiseer moet word, wat dopaminerge neuro-hipotalamiese neurone stimuleer om dopamien in die paraventrikulêre kern vry te laat, en sodoende oksitokinergiese neurone te aktiveer wat na die rugmurg en bemiddelende penis oprigting (sien hierbo en Melis et al., 2007; Succu et al., 2007, 2008). Inderdaad, oksitosien wat in die caudale ventrale tegmentale area geïnspireer is teen 'n dosis wat penile ereksie veroorsaak het, het verhoogde ekstrasellulêre dopamienkonsentrasie in die dialisaat verkry, nie net van die nucleus accumbens nie, maar ook van die paraventrikulêre kern (Succu et al., 2007).
2.3. Die seekoei
Die CA1-veld van die hippocampus was die ander breinarea wat ryk is aan oksitosinergiese vesels en reseptore wat geïdentifiseer is deur die vroeëre studies waarin die inspuiting van oksitosien-geïnduksieerde penile ereksie (sien Bujis, 1978, Sofroniew, 1983). In teenstelling met die paraventrikulêre kern, is daar egter oksitosien aangetref wat slegs in staat is om penile ereksie te induceer wanneer dit in bilaterale en hoër dosisse ingespuit word as diegene wat aktief is in die paraventrikulêre kern (Melis et al., 1986; Chen et al., 1992). Inspuitings van oksitosien in die subikulum is in hierdie vroeëre studies onaktief gevind. Onlangse en versigtiger mikroinjectie studies het egter gelei tot die identifikasie van a streek van die ventrale subikulum waarin die inspuiting van oksitosien in 'n dosisafhanklike wyse penile ereksie kon induksie (Melis et al., 2009b). Die pro-erektiele effek van oksitosien wat in hierdie breinarea ingespuit is, is waargeneem by dosisse soortgelyk aan diegene wat aktief was in die ventrale tegmentale area na eensydige inspuiting (Melis et al., 2007), soos gevind in die paraventrikulêre kern. Blykbaar veroorsaak oksitosien wat in die ventrale subikulum ingespuit word penis oprigting deur oksitokinergiese reseptore in neurone wat stikstofoksied-sintase veroorsaak, te aktiveer, wat 'n toename in stikstofoksiedproduksie veroorsaak. Nitriese oksied op sy beurt deur te optree as intersellulêre boodskapper aktiveer glutamiene suur neurotransmissie, wat lei tot penis oprigting, moontlik deur middel van neurale (glutamatergiese) efferente projeksies vanaf die ventrale subikulum na buitehippokampale breinareas wat die aktiwiteit van mesolimbiese dopaminerge neurone modelleer (bv. die ventrale tegmentale area, die voorfrontale korteks, die paraventrikulêre kern) (sien hieronder en Melis, 2007, 2009b, Succu et al., 2008).
Hierdie werkingsmeganisme word ondersteun deur intra-serebrale mikrodialise-eksperimente, wat aantoon dat oksitosien geïnspireer word in die ventrale subikulum by dosisse wat penile ereksie veroorsaak, verhoog die produksie van stikstofoksied en ekstracellulêre glutamiensuurkonsentrasie in die dialisaat vanaf die ventrale subikulum (Melis et al. , 2010) en van ekstrasellulêre dopamien in die nucleus accumbens (Melis et al., 2007). Hierdie antwoorde is nie net deur die oksitosienreseptor-antagonis d (CH2) 5Tyr (Me) 2-Orn8-vasotosien, maar ook deur die neuronale stikstofoksied-sintase-inhibeerder S-metiel-tio-ltritrolien en deur die stikstofoksiedverskillende hemoglobien gegee Enkele minute voor oksitosien in die ventrale subikulum (Melis et al., 2010).
Verder, in ooreenstemming met hierdie meganisme van werking, veroorsaak aktivering van glutamatergiese neurotransmissie deur NMDA wat in die ventrale subikulum ingespuit word, penis oprigting (Melis et al., 2010). Die fenotipe van efferente projeksies van die ventrale subikulum, wat die aktivering van mesolimbiese dopaminerge neurone en die toename in ekstra-sellulêre dopamien in die kernblusse veroorsaak, is tans onbekend. Aangesien penis ereksie geïnduseer word deur oksitosien wat in die ventrale subikulum ingespuit word, vind egter gelyktydig plaas tot 'n toename in ekstrasellulêre glutamiene suur in die dialisaat vanaf die ventrale tegmentale area, maar nie vanaf die nucleus accumbens nie en word deur (+) MK-801 geantagoniseer, 'n kragtige nie-kompeterende antagonis van eksitatoriese aminosuurreseptore van die NMDA-subtipe (Woodruff et al., 1987), ingespuit in die ventrale tegmentale area, maar nie in die nucleus accumbens nie (sien Fig. 2 en Melis et al., 2009b) , Dit is waarskynlik dat hierdie projeksies lei tot die aktivering van glutamatergiese neurotransmissie in die ventrale tegmentale area, wat op sy beurt die mesolimbiese dopaminerge neurone wat na die nucleus accumbens uitsteek, aktiveer. Of die verhoogde konsentrasie glutamienzuur in die ventrale tegmentale area na oksitosien-inspuiting in die ventrale subikulum bevind word, word vrygestel van neurone wat uit die subikulum ontstaan of in ander breinareas (bv. Die prefrontale korteks) is tans onbekend. nietemin, Dit veroorsaak die aktivering van mesolimbiese dopaminerge neurone en 'n verhoogde vrystelling van dopamien in die kernklem. Hier lei die aktivering van dopamienreseptore tot die aktivering van inkerto-hipotalamiese dopaminerge neurone, wat dopamien in die paraventrikulêre kern vrystel, waardeur oksitokinergiese neurone wat na die rugmurg uitsteek en mediasie penile ereksie aktiveer (sien hierbo en Melis et al., 2007, 2009a; Succu et al., 2008).
2.4. Die amygdala
Die amygdala is 'n ander breinarea wat ryk is aan oksitosienvesels en reseptore (sien Freund-Mercier et al., 1987; Vaccari et al., 1998; Uhl-Bronner et al., 2005). Oksitosien word gedink om betrokke te wees by verskillende funksies, van anxiolise, sosiale geheue en kognisie, maatskaplik versterkte leer, emosionele empatie, emosionele gesigverwerking en vrees in die mens vir erektiele funksie en seksuele gedrag (kyk Kondo et al., 1998; Dominguez et Xnumx; Ebner et al., 2001; Huber et al., 2005; Domes et al., 2005; Petrovic et al., 2007; Lee et al., 2008; Donaldson and Young; 2009; Hurlemann et al. , 2009). Die vermoë van oksitosien om penile ereksie by manlike rotte te veroorsaak wanneer dit egter in die posteriemiese kortikale kern van die amygdala geïnduseer word, is eers onlangs ontdek (Melis et al., 2010b). Hierdie reaksie het gelyktydig plaasgevind met 'n toename in ekstra-sellulêre dopamien konsentrasie in die dialisaat wat verkry is uit die dop van die nukleusakkapsel, soos aangetref na oksitosien inspuiting in die ventrale subikulum (Melis et al., 2009b). Die meganisme waardeur oksitosien geïnspireer word in die posteriese kortikale kern van die amygdala, veroorsaak penile ereksie, is tans onbekend. Die beskikbare data toon dat beide penis ereksie en die toename in ekstracellulêre dopamien konsentrasie in die dialysaat verkry vanaf die nukleus accumbens bemiddel word deur die aktivering van oksitosinere reseptore, aangesien beide antwoorde afgeskaf is deur die oksitosienreseptor antagonis d (CH2009) 2Tyr Ek) 5-Orn2-vasotosien geïnjecteerd in die amygdala-kern enkele minute voor oksytocine (Melis et al., 8b).
Wat ookal meganisme oksitosien aktiveer in die posteriese kortikale kern van die amygdala, word die seksuele reaksie wat deur die peptied geïnduksie word, afgeskaf deur die blokkade van alle dopaminerge reseptore met cis-flupenthixol wat in die dop van die nucleus accumbens ingespuit word en deur die blokkade van NMDA-reseptore met ( +) MK-801 ingespuit in die ventrale tegmentale area, maar nie in die nukleusakkapsel nie, soos gevind vir penile ereksie geïnduceerd deur oksitosien geïnspireer in die ventrale subikulum (Melis et al., 2009b). Dit dui daarop dat oksitosien geïnspireer in die posteriese kerne van die amygdala aktiveer glutamiene suur neurotransmissie in die ventrale tegmentale area. Dit veroorsaak weer die aktivering van mesolimbiese dopaminerge neurone wat tot penile ereksie lei. In die lig van studies wat neurale bane toon wat hierdie kern van die amygdala verbind met die ventrale subikulum (Canteras et al., 1995, French and Totterdell, 2003), verhoog hierdie bevindings die moontlikheid dat daar tussen hierdie twee breinareas 'n interaksie bestaan, alhoewel direk paaie van die amygdala na die kernklem of die ventrale tegmentale area is beskryf (Kelley en Domesick, 1982; Witter, 2006).
2.5. Die rugmurg
Die rugmurg is 'n ander area van die sentrale senuweestelsel wat oksitosinergiese vesels en reseptore bevat (Freund-Mercier et al., 1987, Uhl-Bronner et al., 2005), waarin oksitosien penile ereksie veroorsaak (Tang et al., 1998 ; Veronneau-Longueville et al., 1999; Giuliano en Rampin, 2000; Giuliano et al., 2001). Soos hierbo genoem, ontstaan hierdie oksitosinêre vesels in die paraventrikulêre kern van die hipotalamus en dra by tot afnemende bane wat spinale outonome neurone beheer wat mediêre penile ereksie beheer. Inderdaad maak hierdie vesels sinaptiese kontakte in die dorsale horing preganglioniese simpatiese en parasimpatiese selkolomme in die thoraco-lumbale en lumbo-sakrale kanaal met spinale neurone innervating penile cavernous corpora (Marson en McKenna, 1996; Giuliano en Rampin, 2000; Giuliano et al. , 2001). Hierdie sinaptiese kontakte is getoon deur die etikettering van spinale neurone wat van die penis afkomstig is en die rugmurg te bereik met spesifieke retrograde tracers wat in holle korporasies ingespuit is, gekombineer met dubbel immunofluorescensie en konfokale lasermikroskopie studies (Tang et al., 1998; Veronneau-Longueville et al., 1999). In ooreenstemming met hierdie studies het intravaskale inspuiting van kumulatiewe dosisse oksitosien by die lumbo-sakrale, maar nie op die thoraco-lumbaalvlak, by intestekale manlike rotte op 'n dosis afhanklike wyse intrakavernose druk gestyg nie. Hierdie effekte is afgeskaf deur die blokkade van oksitosinere reseptore met d (CH2) 5Tyr (Me) 2-Orn8-vasotosien en deur 'n gedeelte van die bekken senuwees (Giuliano en Rampin, 2000, Giuliano et al., 2001). Hierdie resultate toon dat oksitosien, wat by die lumbosakrale rugmurg optree, die intrakavernose druk verhoog en stel voor dat oksitosien, wat tydens fisiologiese aktivering van die paraventrikulêre kern vrygestel word, 'n kragtige aktivator is van spinale pro-erektiele neurone wat na die korporatiewe korporasie uitsteek. Interessant genoeg, hierdie pro-erektiele spinale neurone waarop oksitosien optree om sy pro-erektiele effek uit te oefen, ontvang ook sinaptiese kontakte van serotoninergiese neurone wat ontstaan in die kernparagigantocellularis van die retikulêre vorming van die medulla oblongata (Marson en McKenna, 1992; Tang et al ., 1998). Vernietiging van hierdie serotoninergiese neurone fasiliteer ejakulasie en penile reflekse in manlike rotte (Marson en McKenna, 1992; Yells et al., 1992). Aangesien dwelms wat 5HT2C reseptore stimuleer, fasiliteer penile ereksie wanneer dit intrakerebroventrikulêr gegee word, maar nie in die paraventrikulêre kern nie, en middels wat 5HT2C-reseptore blokkeer, verminder ook dopamienagonistiese en oksitosien-geïnduceerde penile ereksie, terwyl dopamienantagoniste nie 5HT2C-agonist-geïnduseerde penile ereksie verminder nie. sien Stancampiano et al., 1994 en verwysings daarin), is dit ook voorgestel dat oksitosien die werking van pro-erektiele 5HT2C reseptore op die vlak van die lumbo-sakrale rugmurg (Stancampiano et al., 1994) fasiliteer. Alternatiewelik kan oksitosien die aktiwiteit van spinale dalende serotoninergiese neurone beïnvloed deur direk in die kernparagigantocellularis te werk, waar hierdie neurone ontstaan (sien Stancampiano et al., 1994).
3. Interaksies tussen oksitosien, dopamien en glutamienzuur in die sentrale senuweestelsel en penis oprigting
Soos onthou in Afdeling 1, kom alle oksitosinergiese neurone in die sentrale senuweestelsel af in die paraventrikulêre kern en omliggende strukture. Die aktiwiteit van hierdie neurone is onder die beheer van verskillende neurotransmitters en / of neuropeptiede. Onder die meeste bestudeer op die paraventrikulêre vlak is dopamien, glutamienzuur, gamma-aminobutuursuur (GABA), stikstofoksied, endokannabinoïede, opioïede peptiede, groeihormoon-vrygestelde peptiede, VGF-verwante peptiede en oksitosien self. Dopamien, glutamienzuur, groeihormoon-vrystelling van peptiede, VGF-afgeleide peptiede en oksitosien is stimulerend, bv. Hierdie verbindings en hul agoniste fasiliteer penile ereksie wanneer dit ingespuit word in die paraventrikulêre kern, terwyl GABA, opioïede peptiede en endokannabinoïede inhibeer, bv. Hierdie verbindings of hul agoniste inhibeer penis oprigting (sien Meisel en Sachs, 1994; Witt en Insel; 1994; Argiolas en Melis; 1995; 2004; 2005; Giuliano en Rampin; 2000; 2004; McKenna; 2000; Andersson; 2001; Hull et al., 2002).
Verskeie lyne eksperimentele bewyse dui daarop dat hierdie oksitokinergiese neurone en bogenoemde neurotransmitters en neuropeptides betrokke is in die beheer van erektiele funksie en seksuele gedrag in verskillende fisiologiese kontekste. Daarbenewens kan oksitosien wat vrygestel word in ekstrahypothalamiese breinareas, soos die ventrale tegmentale area, die hippokampus en sy streke, die amygdala en die rugmurg die aktiwiteit van daardie neurone beïnvloed waarop oksitokinergiese sinapse beïnvloed. Op die oomblik is die enigste neurone wat belangrik is vir penile ereksie waarop oksitokinergiese sinapse inwerk, met sekerheid vasgestel, die selliggame van mesolimbiese dopaminerge neurone van die caudale ventrale tegmentale area wat na die dop van die nucleus accumbens uitsteek (Melis et al., 2007 Succu et al., 2008), en die pro-erektiele spinale neurone wat vanaf die lumbo-sakrale kanaal na die cavernous corpora uitsteek (sien Giuliano en Rampin, 2000, Giuliano et al., 2001) (kyk ook Artikels 2.2 en 2.5) . Inderdaad, hoewel oksitokinergiese sinapse en reseptore ook in die ventrale subikulum geïdentifiseer is, is die amygdala en die rugmurg, areas wat almal belangrik is vir penis ereksie (sien hierbo), in hierdie gebiede die tipe neurotransmitter / s wat in die neurone teenwoordig is. watter oksitokinergiese senuwee-eindes belemmer, is nog onbekend.
Hierdie gedeelte van die oorsig gee 'n kort opsomming van die onlangse literatuur oor die meganismes wat onderliggend is aan die pro-erektiele effek van oksitosien wat ingespuit word in die caudale ventrale tegmentale area, die ventrale subikulum van die hippokampus en in die rugmurg. Spesifieke aandag word gegee aan die interaksie van die peptied met dopamien en glutamienzuur in hierdie gebiede en op die rol wat hierdie interaksie in die sentrale beheer van erektiele funksie kan speel. 'N Kort opsomming van die effekte van dopamien en glutamienzuur op oksitosinergiese neurone in die paraventrikulêre kern, wat ook 'n sleutelrol in erektiele funksie speel, word eers verskaf om die leser bewus te maak van die vroeë navorsingstoestand in hierdie veld, soos hierdie studies is reeds omvattend hersien (sien Argiolas en Melis, 1995, 2004, 2005, Melis en Argiolas, 2003). Ook in hierdie geval word veral aandag gegee aan die mees onlangse resultate, wat 'n belangrike rol vir beide 'n dopamien-oksitosien-skakel en 'n glutamien-oksitoksienverbinding, nie net in seksuele prestasie (penile ereksie en copulasie) nie, maar ook in seksuele opwekking en seksuele motivering.
3.1. Dopamien-oksitosien interaksie in die paraventrikulêre kern
Die vermoë van dopamien-agoniste om penile ereksie te bewerkstellig deur sentrale oksitokinergiese neurone te aktiveer is onmiddellik na die ontdekking aangevoer dat apomorfien die penile ereksie veroorsaak wanneer dit in die paraventrikulêre kern (Melis et al., 1987) geïnspireer word wanneer die oksitosienreseptor antagonis d (CH2) 5Tyr (Me) 2-Orn8-vasotosien ingespuit word, intracerebroventricularly (icv) gevind in staat om byna heeltemal penile ereksie te verminder, wat nie net deur oksitosien gegee is nie, maar ook deur apomorfien, subkutane gegee (Argiolas et al., 1987b). Hierdie resultate is gevolg deur dié van ander studies wat soortgelyke resultate toon wanneer d (CH2) 5Tyr (Me) 2-Orn8-vasotosien gegee is icv en apomorfien is direk in die paraventrikulêre kern gegee (Melis et al., 1989b), lnader om voor te stel dat dopamienagoniste penile ereksie veroorsaak deur paraventrikulêre oksitosinergiese neurone te aktiveer wat uitsteek na buitehypothalamiese breinareas en in besonder aan die rugmurg (sien Argiolas en Melis, 1995, 2004, 2005). In ooreenstemming met hierdie hipotese is by anestesie-rotte blokkade van lumbo-sakrale oksitosinere reseptore deur 'n nie-peptiedoksitosienreseptor antagonis onlangs in staat om apomorfien-geïnduceerde stygings in intrakarnêre druk af te lei wat deur die dopamien-agonistiese apomorfien geïnduseer word, wat bewys lewer van 'n paraventriculo-spinale oxytocinergiese pad betrokke by penis oprigting (Baskerville et al., 2009).
Studies gerig op die identifikasie van die dopamienreseptor wat verantwoordelik is vir die induksie van penis ereksie, het getoon dat ook dopamienreseptoragoniste ook in die paraventrikulêre kern penile ereksie veroorsaak deur op dopamienreseptore van die D2-familie op te tree, soos aangetoon met dopamienreseptoragoniste wat sistemies gegee word (sien Melis et al., 1987; Eaton et al., 1991; Melis and Argiolas, 1995a). Gevolglik is apomorfien, 'n kragtige gemengde D1 / D2-reseptor-agonis en quinpirole, 'n sterk selektiewe D2-receptor agonis, maar nie SKF 38393, 'n selektiewe D1-reseptor-agonis, wat in hierdie hipotalamaskern geïnjecteer is, in staat gestel om op 'n dosis afhanklike wyse penile ereksie te veroorsaak nie. , en die seksuele respons wat deur hierdie D2-reseptoragoniste geïnduseer is, is afgeskaf deur D2-reseptorantagoniste, soos haloperidol en l-sulpiride, maar nie deur SCH 23390, 'n selektiewe D1-reseptorantagonis (Melis et al., 1987) nie. Die vermoë van apomorfien om penile ereksie te veroorsaak wanneer dit in die paraventrikulêre kern ingespuit word, is ook bevestig deur telemetrie studies wat toon dat die dopamien-agonis wat in die paraventrikulêre kern gegee word, intravaskulêre druk in wakker manlike rotte kan verhoog sonder om sistemiese bloeddruk te verander. (Chen et al. , 1999, Giuliano en Allard, 2001), soos gevind na sistemiese inspuiting (Bernabè et al., 1999). Hierdie studies ook bevestig 'n hoofrol van D2-reseptore, aangesien D1-reseptoragoniste gewoonlik nie in staat was om intrakavernose druk te verhoog wanneer dit in die paraventrikulêre kern ingespuit word nie. (Chen et al., 1999).
Verskeie lyne van eksperimentele bewyse was toe beskikbaar wat daarop dui dat paraventrikulêre D2-reseptore, wie se stimulasie penile ereksie veroorsaak, op die selliggame van oksitosinergiese neurone geleë is. Eerstens bevat die paraventrikulêre kern dopaminerge senuweesterminale wat tot die sogenaamde incertohypothalamiese dopaminerge neurone behoort. Die selliggame van hierdie neurone is in die A13- en A14-groep van Dahlstrom en Fuxe (1964), word baie uitgebrei en bevat verskeie hipotalamiese strukture, insluitende paraventrikulêre oksitosinere neurone wat na die neuro-hipofise en / of na die ekstra-hipotalamiese breinareas uitsteek (Buijs et al., 1984, Lindvall et al., 1984).
Die betrokkenheid van hierdie dopaminerge neurone op die paraventrikulêre vlak in die beheer van penile ereksie en kopulering word ondersteun deur mikrodialise studies wat toon dat die konsentrasies van ekstrasellulêre dopamien en 3,4-dihydroxyfenylaceticzuur (DOPAC), sy hoofmetaboliet, verhoog word in die dialysaat verkry uit die paraventrikulêre kern van seksueel kragtige manlike rotte wat niekontakte-ereksies toon wanneer dit in die teenwoordigheid van 'n ontoeganklike ovariectomized estrogeen + progesteroon-primed ontvanklike vrou is nie (Melis et al., 2003).
Die toename van die dopamien- en DOPAC-konsentrasies was selfs hoër wanneer die samestelling met die ontvanklike vrou toegelaat word (Melis et al., 2003), soos aangetref in die mediale preoptiese area (Hull et al., 1995) en in die nucleus accumbens (Pfaus en Everitt, 1995). Tweedens, verskeie studies toon dat penis ereksie veroorsaak deur die stimulering van paraventrikulêre D2 reseptore, bemiddel word deur oksitosien vrygestel in hierdie gebiede. Gevolglik is apomorfien wat gegee word by dosisse wat penile ereksie veroorsaak, gevind om oksitosienkonsentrasie te verhoog, nie net in plasma van rotte en ape nie (Melis et al., 1989a, Cameron et al., 1992), maar ook in ekstrahypothalamiese brein gebiede, soos die hippokampus (Melis et al., 1990). In ooreenstemming met hierdie resultate is onlangs aangetoon dat apomorfien in die paraventrikulêre kern geïnspireer word teen 'n dosis wat penile ereksie veroorsaak, wat ook ekstra-sellulêre dopamienkonsentrasie in die nukleusakkumulasie kan verhoog, 'n effek verminder deur die oksitosienreseptor antagonis d (CH2) 5Tyr (Me) 2-Orn8-vasotosien ingespuit in die ventrale tegmentale area (Succu et al., 2007; Melis et al., 2009a) (sien ook Afdeling 4). Derde bilaterale elektrolytiese letsels van die paraventrikulêre kern, wat bykans heeltemal oksitosien uit ekstrahypothalamiese breinareas (Hawthorn et al., 1985) elimineer, apomorfien-geïnduseerde penile ereksie (Argiolas et al., 1987a) en selektiewe oksitosienreseptorantagoniste af te skaf. gegee in die laterale ventrikels, maar nie in die paraventrikulêre kern nie, verminder dosisafhanklik apomorfieninduksie penile ereksie met 'n potensiaal ewewydig aan dié van hierdie verbindings in die blokkeer van oksitosienreseptore (Melis et al., 1989b). Oksitosienreseptor antagoniste is ook uiters kragtig om die fasilitering van manlike seksuele gedrag wat nie net deur oksitosien geïnduseer word nie, maar ook deur apomorfien (Argiolas et al., 1988, 1989) te verminder.
Met betrekking tot die meganisme waardeur D2-reseptore geaktiveer word deur dopamien of deur dopamienreseptoragoniste, verhoog die aktiwiteit van oksitosinergiese neurone, waardeur oksitosien in ekstrahypotalamiese breinareas en in die rugmurg vrygestel word, talle eksperimentele data sverwerp die hipotese dat die stimulering van D2-reseptore die konsentrasie van intrasellulêre Ca2 + -ione binne die selliggame van oksitosinergiese neurone verhoog, wat lei tot die aktivering van stikstofoksied-sintase, 'n Ca2 + -kalmodulien-afhanklike ensiem wat in hierdie selliggame voorkom (Vincent en Kimura, 1992, Torres et al., 1993, Sanchez et al., 1994, Sato-Suzuki et al., 1998). Die verhoogde stikstofoksiedproduksie veroorsaak op sy beurt die aktivering van oksitosinergiese neurone. Gevolglik is (1) apomorfien-geïnduceerde penile ereksie deur organiese kalsiumkanaalblokkers en by-konotoxien GVIA, 'n kragtige en selektiewe blokker van spanning afhanklike Ca2 + kanale van die N-tipe (McCleskey et al., 1987), in die paraventrikulêre kern (sien Argiolas et al., 1990, en verwysings daarin); (2) apomorfien-geïnduseerde penile ereksie is verhoed deur stikstofoksied-sintase-inhibeerders wat in die paraventrikulêre kern gegee is (Melis et al., 1994c); en (3) apomorfien en ander D2-reseptoragoniste gegee by dosisse wat penile ereksie veroorsaak, verhoogde stikstofoksiedproduksie in die paraventrikulêre dialisaat verkry deur intra-cerebrale mikrodialise, 'n toename wat verminder is deur inhibeerders van paraventrikulêre stikstofoksied-sintase, gegee by dosisse wat verminder D2 reseptor agonistinduced penile erection (Melis et al., 1996). Die meganisme waardeur stikstofoksied paraventrikulêre oksitokinergiese neurone aktiveer, is nog onbekend, hoewel beskikbare data suggereer dat stikstofoksied dien as 'n intracellulêre boodskapper en dat guanilaatsiklase nie betrokke is nie. Inderdaad, die aktiewe fosfodiesteraseresistante analoog van sikliese GMP, 8-broom-sikliese GMP, is nie gevind nie om penile ereksie te veroorsaak wanneer dit in die paraventrikulêre kern (Fig. 2) ingedien word (sien Melis en Argiolas, 1995b en verwysings daarin).
Bogenoemde interpretasie word dikwels as nie oortuigend beskou nie, hoofsaaklik omdat die stimulering van dopamien D2 reseptore gewoonlik gekoppel word aan inhibisie eerder as opwekking van die selliggame van die neurone wat hierdie reseptore bevat deur verskillende G-proteïengekoppelde meganismes (sien Sokoloff en Schwartz, 1995). 'N Moontlike verklaring vir hierdie teenstrydigheid, wat in lyn is met 'n direkte stimulasie van paraventrikulêre oksitosinere neurone deur dopamien, is onlangs voorgestel deur die ontdekking van 'n G proteïengekoppelde dopamien D4 reseptor, 'n lid van die D2-reseptorfamilie (D2, D3 en D4). Die stimulering hiervan verhoog Ca2 + -invloei in selpreparate wat 'n gekloneerde weergawe van hierdie reseptorteelt bevat (Moreland et al., 2004). Nog belangriker is 'n selektiewe D4-reseptoragonist (bv. ABT 724) (N-metiel-4- (2-cyanofenyl) piperazynil-3-methylbenzamidmaleaat) wat in staat was om penile ereksie in manlike rotte te veroorsaak wanneer dit stelselmatig gegee word (Brioni et al. 2004). Hierdie effek is nie gevind met die selektiewe D2 reseptor subtypagonist PNU-95666E (R-5,6-dihydro-N, N-dimethyl-4Himidazo [4,5,1-i] kinolien-5-amin) (Hsieh et al., 2004) was ook nie in staat om Ca2 + -toevoer te verhoog in die selpreparate wat die gekloonde weergawe van die D4-reseptorsubtipe bevat nie (Brioni et al., 2004; Moreland et al., 2004). In ooreenstemming met die bostaande hipotese en bevindings, is PD 168,077 (N-metiel-4- (2-cyanofenyl) piperazynil-3-methylbenzamidmaleaat), PIP-3EA (2- [4- (2-metoksyfenyl) piperazine-1-ylmethyl] imidazo [1,2-a] -pyridien) en ander selektiewe D4-reseptoragoniste (Heier et al., 1997, Melis et al., 2006b, Löber et al., 2009), is gevind om penile ereksie te veroorsaak wanneer dit sistemies, ijv en in die paraventrikulêre kern, hoewel minder effektief as apomorfien. Die pro-erektiele effek van hierdie D4-reseptoragoniste is voorkom deur L-745,870 (3- (4- [chlorofenyl] piperazine-1-yl) -methyl-1H-pyrrolo [2,3-B] piridien trihidrochloried), 'n selektiewe D4 reseptor antagonis (Patel et al., 1997; Melis et al., 2005, 2006b; Löber et al., 2009).
Laastens is die pro-erektiele effek van bogenoemde D4-reseptoragoniste ook verminder deur stikstofoksied-sintase-inhibeerders, gegee in die paraventrikulêre kern, en deur d (CH2) 5Tyr (Me) 2-Orn8-vasotosien, 'n selektiewe oksitosienreseptorantagonis gegee icv maar nie in die paraventrikulêre kern nie. Hierdie resultate stem ooreen met die hipotese dat D4-reseptoragoniste ook oksitokinergiese neurone stimuleer deur nitrioksied-sintase te aktiveer en oksitosien in ekstrahypothalamiese breinareas vry te stel, wat op sy beurt penile ereksie fasiliteer, soos aangetoon vir apomorfien en klassieke D2-agoniste (Melis et al. ., 2005, 2006b; Löber et al., 2009).
Bogenoemde bevindings ondersteun ook die hipotese dat dopamien penile ereksie veroorsaak deur op D4-reseptore wat op die selliggame van paraventrikulêre oksitosinergiese neurone voorkom, 'n verhoogde Ca2 + -invloei in die selliggame van oksitosinergiese neurone te veroorsaak, wat lei tot verhoogde stikstofoksiedproduksie. Nitriese oksied aktiveer weer oksitosinergiese neurone om oksitosien in ekstrahypothalamiese breinareas en in die rugmurg te laat ontsluit, soos reeds bespreek. In hierdie verband, Dit is opmerklik dat dopamienreseptore in die selliggame van oksitosinergiese neurone in die paraventrikulêre kern geïdentifiseer is. slegs onlangs deur dubbele immuno-fluorescentie studies met hoë selektiewe D2-, D3- en D4-reseptor teenliggaampies en met oksitosien teenliggaampies. Hierdie studies het die uitdrukking van al drie D2-receptor subtipes (D2, D3 en D4) getoon, wat afsonderlik in die selliggame van oksitosinergiese neurone in die paraventrikulêre kern (en ook in die supraoptiese kern en die mediale preoptiese area) geplaas is (Baskerville en Douglas, 2008; Baskerville et al., 2009).
Dit bied sterk neuroanatomiese ondersteuning aan die moontlikheid dat dopamien- en dopamienreseptoragoniste van die D2-tipe penile ereksie veroorsaak deur direkte oksitokinergiese neurone te aktiveer wat na die ekstrahypotalamiese breinareas wat hierbo genoem word, produseer., bv. die rugmurg, die ventrale tegmentale area, die hippokampus en die amygdala. Hierdie bevindinge bied egter geen hulp vir die identifikasie van die D2-reseptor subtipe / s, wie se stimulasie die erektiele respons veroorsaak nie. Ongelukkig kan geen hulp verkry word selfs van studies wat daarop gemik is om oksitosinergiese neurone te identifiseer wat geaktiveer word deur dopamienreseptoragoniste in die paraventrikulêre kern nie. Trouens, ten spyte van die verskillende aktiwiteit op die verskillende dopamienreseptor-subtipes, kan gemengde dopamienreseptoragoniste (bv. Apomorfien) of selektiewe D2-reseptoragoniste (bv. Quinpirole, wat op alle D2-receptor subtipes optree) of selektiewe D4-receptoragoniste veroorsaak die aktivering van oksitosinergiese neurone, soos gemeet deur die toename van FOS proteïen in parvokellulêre oksitosinere neurone van die paraventrikulêre kern (Bitner et al., 2006). Hierdie bevinding is egter onlangs bevraagteken, aangesien die FOS proteïenverhoging in paraventrikulêre oksitosinergiese neurone slegs gevind is toe penile ereksie deur quinerolane geïnduseer is, wat hoofsaaklik op D2- en D3-receptor subtipes handel, maar nie deur PD 168077, 'n D4-reseptoragonist, ten spyte van die vermoë van beide verbindings om die seksuele respons te bewerkstellig (Baskerville et al., 2009).
Verdere eksperimente met selektiewe agoniste van die ander D2-reseptor subtipes (hoofsaaklik D2 en D3) is dan nodig om die presiese rol van elke dopamienreseptor-subtipe in die beheer van erektiele funksie op die paraventrikulêre vlak te identifiseer. In hierdie verband, soos reeds voorheen herinner, is apomorfien, wat sterk op alle dopamienreseptor-subtipes optree (sien Brioni et al., 2004, en verwysings daarin), veel meer effektief as D4-reseptore-agoniste in die induksie van penile ereksie wanneer dit in die paraventrikulêre kern. Dit kan verklaar word deur 'n hoër affiniteit van apomorfien op D4-reseptore in vergelyking met dié van die getoetsde D4-reseptoragoniste, of alternatiewelik kan D4-reseptoragoniste as D4-receptor partiële agoniste optree, of die gepaardgaande aktivering van verskillende dopamien-receptor subtipes deur apomorfien mag produseer 'n hoër aktivering van oksitosineriese neurone mediasie penile ereksie, as die aktivering deur D2-reseptoragoniste van die D4-reseptorsubtipe.
Interaksies tussen dopamien D1 en D2 reseptore is reeds beskryf in die beheer van seksuele gedrag op die vlak van die mediale preoptiese area (sien Hull et al., 1989). In die geval dat die onvermoë van selektiewe D2-reseptoragoniste om penile ereksie (Hsieh et al., 2004) te bewerkstellig sal bevestig word (maar sien Depoortère et al., 2009), byvoorbeeld selfs na inspuiting van hierdie verbindings in die paraventrikulêre kern , 'n belangrike rol vir D3-reseptore alleen of saam met dié van D4-reseptore by die aktivering van oksitosinere neurone wat mediasie penile ereksie moet analiseer, moet in detail ontleed word (sien Baskerville et al., 2009). Ongelukkig is selektiewe D2- en D3-reseptoragoniste (bv. Wat verskil in hul affiniteit vir hierdie twee reseptor subtipes vir ten minste vier / vyf bestellings van in vitro) nie beskikbaar nie. Om hierdie rede het die onlangse voorstel dat D3-reseptore penile ereksie bemiddel, geïnduceerd deur klassieke D2-reseptoragoniste, wat hoofsaaklik gebaseer is op die vermoë van vermeende D3-reseptorantagoniste wat in vitro-eksperimente gekarakteriseer word, om penile ereksie wat deur klassieke D2-agoniste geïnduceerd word, te verminder, soos apomorfien, quinpirole en pramipexole, wat alle dopamien D2-reseptor subtipes (Collins et al., 2009) sterk aktiveer, moet sekerlik met ander eksperimente bekragtig word. Hierdie validering is ook nodig omdat geen effek van D4-reseptoragoniste op penile ereksie in hierdie studie gevind is nie, in stryd met die resultate van die bogenoemde studies wat 'n pro-erektiele effek van D4-reseptoragoniste toon. Inderdaad, selfs die vermoë van apomorfien om penile ereksie (en gaping) in D4-reseptor-knockout-muise te veroorsaak met 'n potensie wat dieselfde is as wat in wild-tipe D4-receptor-knockout-muise en die vermoë van D3-receptorantagoniste om die apomorfienreaksie in hierdie diere af te skaf ( Collins et al., 2009) kan nie beskou word as 'n definitiewe bewys vir 'n selektiewe rol van die D3-reseptorsubtipe in D2-reseptoragonist-geïnduseerde penile ereksie. Spesiesverskille uitmekaar, studies met neurotransmitter / neuropeptied- en / of neurotransmitter / neuropeptide-reseptor-genablasie (neurotransmitter / neuropeptide en / of neurotransmitter / neuropeptide reseptor uitklopdiere) het gewoonlik meer verwarring en komplikasies bygevoeg in die bevestiging van die vermeende seksuele rol van neurotransmitters en / of neuropeptiede en hul reseptore. Namelyks, oksitosien-gene ablasie produseer oksitosien-knock-out-muise wat normaalweg mate en kopieer, asof oksitosien onnodig was vir paring en copulasie. Ook die homosigotiese vroulike oksitosien-knockout-muise wys normale paring en afskeiding, alhoewel met 'n duidelike inkorting van melkverlies (Nishimori et al., 1996, Young et al., 1996). Die ablasie van die geen wat kodeer vir neuronale stikstofoksiedsintase, produseer ook stikstofoksied-sintase-knock-out-muise wat normaalweg mate en kopieer (Huang et al., 1993). Hierdie bevindings dui egter waarskynlik op 'n belangrike kenmerk van voortplantingsfisiologie, dit wil sê die ontslag van die stelsels betrokke by sy beheer op sentrale en perifere vlak.
Sulke oortolligheid het beslis 'n evolusionêre oorsprong, aangesien dit die genesing van die volgende generasie vir die oorlewing van die spesie waarborg. Die feit dat ablasie van die D4-receptor geen die pro-erektiele effek van apomorfien beïnvloed, dui daarop dat D4-reseptore, soos oksitosien en stikstofoksied, slegs 'n paar van die mediators is wat in die sisteme beheer oor erektiele funksie, eerder as wat daarop dui dat daar geen rol vir hierdie reseptore in die beheer van penile ereksie en seksuele gedrag is nie. Die versuim van D4-agoniste om penile ereksie te veroorsaak wanneer dit sistemies aan manlike rotte van verskillende stamme gegee word, is onlangs aangemeld deur 'n ander studie (Depoortère et al., 2009). In teenstelling met die werk van Collins et al. (2009) en om die rol van die verskillende D2-reseptor subtipes in die beheer van penile ereksie selfs meer verwarrend te maak, toon hierdie studie ook dat vermeende selektiewe D3-reseptorantagoniste wat stelselmatig gegee is, nie in staat was om apomorfien-geïnduseerde penile ereksie te verminder nie. Manlike rotte van die stam wat meer sensitief is vir die pro-erektiele effek van apomorfien, terwyl die seksuele respons (en gaping) deur die selektiewe D2-antagonis L-741,626 (3 - [[4- (4-chlorfenyl) -4-hidroksipiperidien -1-yl] metiel-1H-indool), wat die skrywers voorspel dat D2-reseptore, eerder as D3- en D4-reseptore, diegene speel wat 'n belangrike rol speel in D2-agonist-geïnduceerde penile ereksie (Depoortère et al., 2009). Laastens, die moontlikheid dat die opwekkende effek van dopamienreseptoragoniste op oksitokinergiese neurone mediasie penile ereksie, ten minste gedeeltelik, indirek is, eerder as direk, bv. Bemiddel of beïnvloed word deur veranderinge in die aktiwiteit van ander neurotransmitters, neuropeptiede wat die aktiwiteit van oksitosinere neurone in die paraventrikulêre kern, kan nie heeltemal uitgesluit word nie.
3.2. Glutamien suur-oksitosien interaksie in die paraventrikulêre kern
Die paraventrikulêre kern van die hipotalamus is baie ryk aan sinapse wat 'n opwindende aminosuur bevat as 'n neurotransmitter (bv. Glutamienzuur en asparagine suur) (Van Den Pol, 1991). Opwindende aminosure in hierdie kern is betrokke by talle funksies, insluitende penile ereksie en seksuele gedrag (Roeling et al., 1991, Melis et al., 1994b, 2000, 2004b). Gevolglik is N-metiel-d-asparaginsuur (NMDA), 'n selektiewe agonis van die NMDA-reseptorsubtipe, maar nie (±) -_-aminotoksis-3-hydroxy-5-metielisoksasool-4-propioniensuur (AMPA) , 'n selektiewe agonis van die AMPA-reseptor-subtipe of (±) -trans (1) -amino-1,3-siklopentandi-dikarboksielsuur (ACPD), 'n selektiewe agonis van die metabotropiese reseptorsubtipe, is gevind om penile ereksie te veroorsaak wanneer dit in die paraventrikulêre kern van vrybewegende rotte (Melis et al., 1994b). Die pro-erektiele effek van 948 MR Melis, A. Argiolas / Neurowetenschappen en Biobehavioral Reviews 35 (2011) 939-955 NMDA is voorkom deur (+) MK-801, 'n nie-mededingende NMDA reseptor antagonis (Woodruff et al., 1987 ), ingespuit in die paraventrikulêre kern (Melis et al., 1994b). In ooreenstemming met hierdie resultate, in telemetrie studies wat gemik was op intrakavernose druk, was NMDA baie meer aktief as agoniste van die ander eksitatoriese aminosure-reseptorsubtipes wanneer dit in die paraventrikulêre kern geïnkorporeer word in toenemende intrakavernosale druk in wakker of verdoofde manlike rotte (Zahran et al., 2000; Chen en Chang, 2003).
Soos hierbo voorgestel vir oksitosien en dopamien, is dit waarskynlik dat NMDA-reseptore wat penile ereksie bemiddel, in die selliggame van oksitosinergiese neurone geleë is, aangesien eksitatoriese aminosuur-senuwee-eindings op oksitosinergiese selliggame in die paraventrikulêre kern belemmer. (Van Den Pol, 1991). In analogie tot wat met dopamienreseptoragoniste aangetref word, word die pro-erektiele effek van NMDA blykbaar gemedieer deur die aktivering van oksitosinergiese neurotransmissie, wat afgeskaf word deur die oksigosienantagonist d (CH2) 5Tyr (Me) 2-Orn8-vasotosien gegee icv, maar nie in die paraventrikulêre kern nie (sien Argiolas en Melis, 1995, 2004, 2005 en verwysings daarin). Net so is NMDA-geïnduceerde aktivering van oksitosinergiese neurotransmissie ook sekondêr vir die aktivering van stikstofoksied-sintase, aangesien NMDA-geïnduceerde penile ereksie voorkom word deur stikstofoksied-sintase-inhibeerders (N-Nitro-N-metiel-arginien-metielester en N- metiel-tio-l-sitrolien) in die paraventrikulêre kern gegee, en NMDA ingespuit in die paraventrikulêre kern by dosisse wat penile ereksie veroorsaak, verhoog die produksie van stikstofoksied in die hipotalamiese kern (sien Argiolas en Melis, 1995, 2004, 2005 en verwysings daarin ). Wat die dopamienreseptoragoniste betref, kan die NMDA-geïnduceerde aktivering van stikstofoksiedintese ook sekondêr wees vir 'n verhoogde Ca2 + -toevoer in oksitosinergiese selliggame deur die Ca2 + kanaalgekoppelde NMDA-reseptore, soos getoon in verskeie neurale preparate (vir 'n oorsig sien Snyder, 1992; Southam en Garthwaite, 1993; Schuman en Madison, 1994 en verwysings daarin). Nitriese oksied aktiveer weer oksitosinergiese neurotransmissie (sien hierbo). Die oorsprong van glutamatergiese projeksies wat paraventrikulêre oksitosinêre neurone bemiddelende penile ereksie aktiveer, is onbekend, hoewel sommige neuroanatomiese en elektrofisiologiese bewyse daarop dui dat hulle ten minste gedeeltelik in die hippokampus (Saphier en Feldman, 1987, Chen et al., 1992) . Alhoewel verdere werk nodig is om die oorsprong van die glutamatergiese projeksies aan die paraventrikulêre kern te verbeter, word die betrokkenheid van glutamiene suur in die paraventrikulêre kern in die beheer van penile ereksie en seksuele gedrag duidelik ondersteun deur mikrodialise-studies. Gevolglik is die ekstra-sellulêre konsentrasies van glutamienzuur en asparaginsuur verhoog in die dialysaat verkry uit die paraventrikulêre kern van manlike rotte wat niekontakte-ereksies toon wanneer dit in die teenwoordigheid van ontoeganklike oestrogeen + progesteroon-primed ontvanklike vroulike rotte (Melis et al. 2004b), penis ereksies wat ook bemiddel word deur die aktivering van sentrale oksitosinergiese oordrag (Melis et al., 1999a, b). Sulke verhogings is selfs hoër gevind toe samestelling met die ontvanklike vrou toegelaat is (Melis et al., 2004a). In lyn met die hipotese dat 'n verhoogde aktiwiteit van opwekkerlike aminosure in die paraventrikulêre kern voorkom tydens penile ereksie en copulasie, word beide nie-kontak-ereksies en copulatoriese gedrag (waarteen daar in kopula-penile ereksies voorkom) verminder deur blokkade van NMDA-reseptore in die paraventrikulêre kern , en hierdie vermindering word gevolg deur 'n afname in die toename van stikstofoksiedproduksie wat in hierdie hipotalamiese kern in hierdie fisiologiese kontekste voorkom (Melis et al., 2000). 'N Toename in ekstrasellulêre glutamiesuurkonsentrasie, ondergeskik aan 'n afgeneemde GABA-vrystelling van GABAergiese senuwee-eindpunte wat op eksitatoriese aminosuurergiese sinapse gepaardgaan wat saamgevoeg is aan oksitosinergiese selliggame, is ook gevind in die paraventrikulêre kern na die blokkasie van cannabinoïede CB1-reseptore deur die CB1-antagonis SR 141761A, gegee in die laterale ventrikels of direk in die paraventrikulêre kern by dosisse wat penile ereksie veroorsaak (sien Succu et al., 2006, Castelli et al., 2007). Sodanige toename het gelei tot die aktivering van stikstofoksied-sintase in die selliggame van oksitosinergiese neurone, wat die produksie van stikstofoksied verhoog. Nitriese oksied aktiveer weer oksitosinere neurone wat mediasie penile ereksie bewerkstellig soos hierbo beskryf. In lyn met so 'n meganisme is SR 141761A-geïnduseerde penile ereksie verminder deur die blokkade van NMDA-reseptore en deur stikstofoksied-sintase-inhibeerders, maar nie deur die blokkade van dopamien- of oksitosienreseptore in die paraventrikulêre kern nie, terwyl dit deur die blokkade van sentrale oksitosienreseptore deur oksitosienreseptorantagoniste gegee icv
3.3. Oksitosien-dopamien interaksie in die ventrale tegmentale area
Oksitosien induceer penile ereksie wanneer dit op 'n dosis afhanklike wyse in die caudale deel van die ventrale tegmentale area ingespuit word. (Melis et al., 2007). Die laagste aktiewe dosis wat eensydig ingespuit is, was 20 ng, terwyl die hoogste dosis getoets 100 ng was. Die oksitosien-effek word bemiddel deur die aktivering van oksitosinergiese reseptore, aangesien die seksuele respons afgeskaf word deur die vorige inspuiting van die oksitosienantagonis d (CH2) 5Tyr (Me) 2-Orn8-vasotosien in die caudale ventrale tegmentale area. Hierdie reseptore word gelokaliseer in die selliggame van dopaminerge neurone, wat hoofsaaklik na die dop van die nucleus accumbens kom. Gevolglik toon (1) dubbelimmunfluorescensstudies dat oksitokinergiese vesels in die caudale ventrale tegmentale area in noue kontak is met die selliggame van dopaminerge neurone, waarvan die meerderheid positief gemerk is vir tyrosienhidroksilase en die retrograde-spore Fluorogold voorheen bevat. geïnspireer in die dop van die nucleus accumbens (Melis et al., 2007) en (2) ventrale tegmentale area oksitosien-geïnduceerde penile ereksie vind plaas met 'n toename in die konsentrasie van buite-sellulêre dopamien in die dialisaat wat verkry word uit die dop van die kern accumbens (Melis et al., 2007). Oksitosien-geïnduseerde penile ereksie vind ook gepaard met 'n toename in stikstofoksiedproduksie in die ventrale tegmentale area, aangesien beide antwoorde nie net deur d (CH2) 5Tyr (Me) 2-Orn8-vasotosien en deur die stikstofoksiedsintase-inhibitor S- methyl-thio-l-citrulline, maar ook deur _-conotoxine, 'n spanningsafhanklike Ca2 + -kanaalblokker, en deur ODQ (1H- [1,2,4] oksadiasool [4,3-a] quinoxalin-1-een), 'n kragtige inhibitor van guanilaat siklase, almal gegee in die caudale ventrale tegmentale area voor oksitosien (Succu et al., 2008). Aangesien baie van die Fluorogold-gemerkte dopaminerge selliggame wat deur oksitosinergiese vesele gekontak is, positief was vir tyrosienhidroksilase in die caudale ventrale tegmentale area, is ook positief gemerk vir stikstofoksied-sintase en guanilaat-siklasase (Succu et al., 2008), oksitosien -indukte penis oprigting kan bemiddel word deur die volgende meganisme. Die aktivering van oksitosinergiese reseptore in dopaminerge selliggame deur die peptied verhoog Ca2 + -invloei in die selliggame van dopaminerge neurone. Dit aktiveer stikstofoksied-sintase, 'n Ca2 + -kalmodulien-afhanklike ensiem, wat sodoende die produksie van stikstofoksied verhoog. Nitriese oksied aktiveer weer guanilaat-siklas, wat lei tot 'n verhoogde konsentrasie van sikliese GMP. Sikliese GMP aktiveer dopaminerge neurone wat na die nucleus accumbens uitsteek. Die rol van sikliese GMP in penile ereksie geïnduceerd deur oksitosien geïnspireer in die caudale ventrale tegmentale area word ook ondersteun deur die vermoë van 8-broom-sikliese GMP, 'n aktiewe fosfodiesterase-weerstandige analoog van sikliese GMP, om penile ereksie te veroorsaak wanneer dit ingespuit word in die caudale ventrale tegmentale area, en om ekstra-sellulêre dopamien in die dialisaat vanaf die kernblusse te verhoog (Succu et al., 2008; Melis et al., 2009a). Dit is in teenstelling met die meganisme waardeur stikstofoksied oksitokinergiese neurone in die paraventrikulêre kern aktiveer, synde 8-broom-sikliese GMP wat nie in staat is om penile ereksie te veroorsaak wanneer dit in hierdie kern ingespuit word nie (Melis en Argiolas, 1995b) (Fig. 2). Wat die neurale bane wat deur dopamien geaktiveer word in die kernklemme wat tot penile ereksie lei, is dit nog onbekend. Die beskikbare data dui egter daarop dat hierdie bane dopamien-neurotransmissie in die paraventrikulêre kern van die hipotalamus aktiveer. Gevolglik vind oksitosien-geïnduseerde penile ereksie gelyktydig plaas tot 'n toename in ekstrasellulêre dopamien, nie net in die nukleus accumbens, maar ook in die paraventrikulêre kern, en word geantagoniseer deur die dopamienreseptor antagonist haloperidol wat in die paraventrikulêre kern (Melis et al., 2007) ingespuit word. AAl hierdie resultate ondersteun die idee dat oksitosinere neurone wat uit die paraventrikulêre kern ontstaan en na die caudale ventrale tegmentale area uitsteek, wanneer oksitosien in hierdie area geaktiveer word, en sodoende 'n NO-sikliese GMP seinstelsel, wat op sy beurt aktiveer mesolimbiese dopaminerge neurone (Melis et al., 2007, 2009a; Succu et al., 2008). Dopamien vrygestel in die nucleus accumbens aktiveer op sy beurt neurale bane wat lei tot die aktivering van incerto-hipotalamiese dopaminerge neurone, wat paraventrikulêre oksitosinergiese neurone stimuleer wat na die rugmurgmediasie-penile ereksie uitsteek. Terselfdertyd kan dopamien wat in die paraventrikulêre kern vrygestel word, ook oksitokinergiese neurone aktiveer wat uitsteek na ekstrahypothalamiese breinareas soos die ventrale tegmentale area, die hippokampus, die amygdala en miskien ander breinareas.
Soos hierbo genoem, in ooreenstemming met hierdie hipotese, verhoog apomorfien in die paraventrikulêre kern by 'n dosis wat penile ereksie veroorsaak, ook ekstra-sellulêre dopamien konsentrasie in die kern accumbens, 'n effek verminder deur die oksitosienreseptor antagonis d (CH2) 5Tyr (Me ) 2-Orn8-vasotosien ingespuit in die ventrale tegmentale area (Succu et al., 2007; Melis et al., 2009a). Saam kan die bogenoemde neurale bane 'n hipotetiese neurale kringloop wees wat dopamien, oksitosien en ander neurotransmitters insluit (bv. Glutamienzuur, sien hieronder) wat nie net seksuele prestasie beïnvloed nie, maar ook seksuele motivering en seksuele bevredigende (sien Afdeling 4).
3.4. Oksitosien-glutamiese suur interaksie in die ventrale subikulum van die hippokampus
Oksitosien induceer penile ereksie wanneer dit in die ventrale ingespuit word, maar nie in die dorsale subikulum nie, op 'n dosis afhanklike wyse (Melis et al., 2009b). Die seksuele respons word bemmed deur die stimulering van oksitosienreseptore, wat afgeskaf word deur die vorige inspuiting van d (CH2) 5Tyr (Me) 2-Orn8-vasotosien wat in dieselfde area van oksitosien gegee word, soos in ander breinareas aangetref word (sien hierbo) . Wat die lokalisering van hierdie reseptore betref, dui die beskikbare data daarop dat hulle gelokaliseer word in die selliggame van neurone wat ryk is aan stikstofoksied-sintase.
Gevolglik toon mikrodialise-studies dat oksitosien-geïnduksieerde penile ereksie gelyktydig plaasvind met 'n toename in stikstofoksiedproduksie in die ventrale subikulum, en hierdie toename word afgeskaf, nie net deur die vorige inspuiting van die stikstofoksiedesintase-inhibeerder S-metiel-tio-l-sitrolien en deur die stikstofoksiedverskillende hemoglobien, maar ook deur d (CH2) 5Tyr (Me) 2-Orn8-vasotosien, wat almal op dieselfde plek van oksitosien gegee word by dosisse wat penis ereksie (Melis et al., 2010) teenwerk. Belangrikste oksigosin-geïnduceerde penile ereksie vind ook gepaard met 'n toename in die konsentrasie van ekstrasellulêre glutamienzuur in die ventrale subikulum, wat slegs gedeeltelik deur die nie-mededingende NMDA-receptorantagonis (+) MK-801 in die ventrale subikulum (Melis et al., 2010). Saam dui hierdie resultate daarop dat nuutgevormde stikstofoksied, deur as 'n intersellulêre boodskapper op te tree, glutamiesuur-neurotransmissie aktiveer wat lei tot penile ereksie, moontlik deur neurale efferente projeksies van die ventrale subikulum na ekstra hippokampale breinareas. In lyn met hierdie hipotese, NMDA ingespuit in die ventrale subikulum induceer penile ereksie op 'n dosis afhanklike wyse en hierdie effek word heeltemal deur die vorige inspuiting geantagoniseer in dieselfde plek van (+) MK-801, maar nie deur S-metiel-tio-l-sitrolien , hemoglobien of d (CH2) 5Tyr (Me) 2-Orn8-vasotosien (Melis et al., 2010). Wat die neurale effense paaie betref wat na ekstra hippokampale breinareas wat geaktiveer word deur opwekkende aminosure (dws glutamiene suur) in die ventrale subikulum, is dit waarskynlik dat dit glutamatergies is, asook die meerderheid van hippocampale efferente projeksies. Op die oomblik mag dit slegs voorgestel word dat hierdie projeksies die aktiwiteit van mesolimbiese dopaminerge neurone moduleer, wat op sy beurt die aktiwiteit van incerto-hipotalamiese dopaminerge neurone in die paraventrikulêre kern moduleer, wat lei tot die aktivering van oksitosinergiese neurone bemiddelende penis oprigting soos reeds bespreek (sien hierbo).
Gevolglik vind penile ereksie wat deur ventrale subikulumoksitosien plaasvind, gepaardgaande met 'n toename in die konsentrasie van ekstra-sellulêre dopamien in die dop van die nukleus accumbens. Hierdie toename, soos penile ereksie, word afgeskaf deur d (CH2) 5Tyr (Me) 2- Orn8-vasotosien gegee in die ventrale subikulum voor oksitosien (Melis et al., 2009b). Daarbenewens word oksitosien-geïnduksieerde penile ereksie ook verminder deur (+) MK-801 wat in die ventrale tegmentale area geïnspireer is, maar nie in die nucleus accumbens (Melis et al., 2009b) en kom tegelykertyd voor op 'n toename van ekstra-sellulêre glutamiene suur in die ventrale tegmentale area, maar nie in die nukleusakkumulasie nie, beide reaksies afgeskaf deur d (CH2) 5Tyr (Me) -Orn8-vasotosien, ingespuit in die ventrale subikulum voor oksitosien (sien Fig. 3) Dit is waarskynlik dat die aktivering van mesolimbiese dopaminerge neurone sekondêr is tot 'n verhoogde glutamatergiese neurotransmissie in die ventrale tegmentale area. Dit dui daarop dat 'n glutamiene suur-dopamien interaksie beheer penile ereksie bestaan in die ventrale tegmentale area. Verdere studies is nodig om te bepaal of die pro-erektiele efferente glutametergiese bane van die subikulum na die ventrale tegmentale area direk of indirek is, dws deur die voorfrontale korteks of ander breinareas (sien Melis et al., 2009b en verwysings daarin). Aangesien die paraventrikulêre kern ook glutamatergiese projeksies van die hippokampus ontvang (sien hierbo en Saphier en Feldman, 1987), en glutamiene suur aktiveer paraventrikulêre oksitosinergiese neurone, insluitend dié wat na die ventrale tegmentale area uitsteek (sien Argiolas en Melis, 2005 en verwysings daarin), en oksitosien in die ventrale tegmentale area veroorsaak penis oprigting en verhoog die aktiwiteit van mesolimbiese dopaminerge neurons (sien hierbo), is dit aanloklik om daardie p. te spekuleeraraventrikulêre oksitosinergiese neurone kan ook ten minste gedeeltelik betrokke wees by die aktivering van mesolimbiese dopaminerge neurone deur oksitosien geïnspireer in die ventrale subikulum (sien Afdeling 4).
4. Slotopmerkings
Die bogenoemde studies bevestig en brei vroeë bevindinge uit en laat dit uit dat in manlike rotte oksitosien 'n sleutelrol speel in die sentrale beheer van penile ereksie op die vlak van die paraventrikulêre kern van die hipotalamus en van die rugmurg. In die besonder, die meeste resent ondersoeke toon dat oksitosien penile ereksie beïnvloed ook deur op te tree in ander breinareas, dws die ventrale tegmentale area, die ventrale subikulum en die posteromediale kortikale kern van die amygdala.
Op die paraventrikulêre vlak is die belangrikste nuwe bevinding moontlik die ontdekking van die uitdrukking van alle dopamienreseptore van die D2-familie (D2, D3 en D4) in die selliggame van oksitosinergiese neurone in die paraventrikulêre kern (en in die supraoptiese kern en die mediale preoptiese area) (Baskerville en Douglas, 2008; Baskerville et al., 2009). Dit bied sterk neuroanatomiese steun aan die hipotese dat dopamien- en dopamienreseptoragoniste direk oksitokinergiese neurone wat betrokke is by erektiele funksie, kan aktiveer en nie net op die rugmurg uitwerk nie, maar ook na buitehypothalamiese breinareas. In hierdie verband is dit ook belangrik dat die ontdekking dat dopamienreseptor-agonist-geïnduceerde toename in intrakarnêre druk verminder word deur die blokkade van oksitosinere reseptore in die lumbo-sakrale rugmurg (Baskerville et al., 2009). Inderdaad, alhoewel sulke bewyse verkry is in verdovende manlike rotte, bevestig die bevinding die aktivering van 'n paraventriculo-spinale oksitokinergiese afname wat betrokke is by dopamien-reseptor-agonist-geïnduceerde penile ereksie. Howerver, moet nog vasgestel word of penis oprigting geïnduseer deur die stimulering van dopamienreseptore wat in oksitosinergiese selliggame voorkom, is sekondêr tot die aktivering van 'n spesifieke dopamienreseptor-subtipe van die D2-familie (D2, D3 of D4) of as hierdie reseptor subtipes saamwerk om die erektiele respons te modulerende, moontlik op verskillende maniere, afhangende van die konteks waarin penile ereksie voorkom (sien Moreland et al., 2004; Enguehard-Gueiffier et al., 2006; Melis et al., 2006a, b; Löber et al., 2009; Collins et al., 2009; Depoortère et al., 2009; Baskerville et al., 2009).
Nog 'n belangrike nuwe bevinding is dat oksitosien penile ereksie veroorsaak wanneer dit nie net in die paraventrikulêre kern of die CA1-veld van die hippokampus geïnspireer word nie, maar ook in die ventrale tegmentale area, die ventrale subikulum en die posteromediale kortikale kern van die amygdala. Hierdie breinareas is nie getoets in die vroeëre studies wat getoon het dat oksitosien spontane penile ereksie-episodes in manlike rotte verhoog het nie, alhoewel hulle soos die oksitosinêre rugmurg-oksitosinêre projeksies van die paraventrikulêre kern ontvang. Oksitosien is inderdaad in staat gestel om spontane penis ereksie episodes te verhoog, wat voorkom by volwassenes manlike rotte in die afwesigheid van enige seksuele stimuli, soos dié wat ontstaan uit die teenwoordigheid van 'n toeganklike of ontoeganklike ontvanklike (oestrogeen-progesteroon-geperste) ovariectomized vroulike rat of manipulasie van die genitalieë, in die paraventrikulêre kern en die CA1-veld van die hippokampus, maar nie in die dorsale subikulum nie, die laterale septum, die caudaat-kern, die mediale preoptiese area, die ventromediale kern en die supraoptiese kern (Melis et al. , 1986). In al hierdie studies is penile ereksie gewoonlik getel toe die penis uit die penisskede kom deur 'n waarnemer wat onbewus was van die gegewe behandelings direk tydens die eksperiment of later deur die eksperiment op te neem wat op 'n videoband met 'n videokameraapparaat aangeteken is. Elke penis ereksie-episode duur vir 0.5-1 min en word gewoonlik vergesel van penisversorging en / of hipfleksies. Geen eksperiment word gewoonlik in hierdie rotte gedoen om die effek van seksuele ondervinding, ouderdom te bepaal of as hierdie rotte verdeel kan word in lae of hoë responders op die pro-erektiele effek van oksitosien wat in die verskillende breinareas ingespuit word nie. Dit geld ook vir die meeste studies oor die pro-erektiele effek van ander neuropeptiede en middels wat spontane penile ereksie episodes verhoog, insluitende dopamienagoniste, eksitatoriese aminosure, ACTH-MSH, heksarelin en VGF-peptiede. Die pro-erektiele effek van hierdie verbindings is egter herhaaldelik bevestig deur telemetriemetodes wat die voorkoms van penile ereksie bepaal deur die toename in intrakarnêre druk wat spontaan of na toediening van hierdie verbindings op verskillende roetes plaasvind, dit wil sê sistemies, intracerebroventrikulêr of direk na spesifieke breinkerns, na die inplanting van 'n drukmikrotransducer direk in die cavernous corpora (sien Bernabè et al., 1999). In die ventrale tegmentale area, die ventrale subikulum en die posteromediale kern van die amygdala, veroorsaak oksitosien ook penile ereksie deur op oksitosinere reseptore te reageer. Dit lei tot die aktivering van mesolimbiese dopaminerge neurone van oorsprong in die ventrale tegmentale area en uitsteek na die dop van die nucleus accumbens, soos gemeet deur die toenames in ekstra-sellulêre dopamien konsentrasie in die dialisaat verkry vanaf die dop van die nucleus accumbens en deur die vermindering in die erektiele reaksie wat veroorsaak word deur die peptied wat in hierdie ekstra-hipotalamiese gebiede ingespuit word, wat na die blokkade van dopaminerge reseptore in die kern accumbens (sien hieronder). Wat die meganismes wat deur die stimulering van oksitokinergiese reseptore in hierdie breinareas geaktiveer word, wat lei tot die aktivering van mesolimbiese dopaminerge neurone en tot penile ereksie, is die beste verduidelike diegene wat in die caudale ventrale tegmentale area voorkom. Inderdaad, hier toon farmakologiese en immuno-fluorescensuitslae dat oksitosien-senuwee-eindpunte op die selliggame van dopaminerge neurone uitsteek, wat na die dop van die nucleus accumbens uitsteek (Melis et al., 2007, 2009a, Succu et al., 2008). Baie van hierdie neurone is ryk aan stikstofoksiedsintase en in guanilaat-siklas. Die stimulering van oksitokinergiese reseptore in die selliggame van hierdie dopaminerge neurone veroorsaak die aktivering van stikstofoksiedsintase wat lei tot verhoogde stikstofoksiedproduksie. Koolstofoksied aktiveer weer guanilaat-siklas, waardeur die konsentrasie van sikliese GMP verhoog word, wat lei tot die aktivering van mesolimbiese dopaminerge neurone en tot die vrylating van dopamien in die nukleusakkoue, soos gemeet deur die toename in ekstracellulêre dopamien in die dialisaat vanaf die nucleus accumbens verkry deur intra-cerebrale mikrodialise (Succu et al., 2008 ). Dopamien vrygestel in die kern accumbens aktiveer op sy beurt neurale paaie wat lei tot penis oprigting. Dit word gesteun deur die vermoë van dopamienreseptorantagoniste haloperidol en / of cis-flupentixol wat in die nukleusbuis ingespuit word om die oksitosien-geïnduceerde penile ereksie (Succu et al., 2008) te verminder. Een van die pro-erektiele paaie blyk te wees om dopaminerge neuro-hipotalamiese neurone te aktiveer, veral dié wat na die selliggame van paraventrikulêre oksitosinergiese neurone projekteer. Inderdaad, oksitosien wat in die caudale ventrale tegmentale area ingespuit word verhoog nie alleen ekstracellulêre dopamien nie, maar ook in die paraventrikulêre kern, en die blokkade van dopamienreseptore in die paraventrikulêre kern verminder aansienlik ventrale tegmentale area oksitosien-geïnduceerde penile ereksie (Succu et al. , 2007, 2008, Melis et al., 2007, 2009a). Die bestaan van hierdie kern sluit in dopamien-paraventrikulêre dopamien-paraventrikulêre oksitosien-ventrale tegmentale area oksitosien-dopamien skakels word ook voorgestel deur die vermoë van 'n pro-erektiele dosis apomorfien en van die D4-reseptor-agonis PD 168077 wat in die paraventrikulêre kern ingespuit is om ekstra-sellulêre dopamien in die dop van die nucleus accumbens te verhoog (Succu et al., 2007), respons Dit word afgeskaf deur d (CH2) 5Tyr (Me) -Orn8-vasotosien wat in die ventrale tegmentale area gegee word (Melis et al., 2009a, sien ook hieronder). Nog verdere werk is nodig om die neurale bane te identifiseer wat die kern verbind tot die incerto-hipotalamiese dopaminerge sisteem.
Die meganisme waardeur oksitosien penile ereksie bewerkstellig en mesolimbiese dopaminerge neurone aktiveer wanneer dit in die ventrale subikulum ingespuit word of in die posteriorale kern van die amygdala word slegs gedeeltelik verstaan. In hierdie gebiede aktiveer oksitosien ook sy eie reseptore wat tot die aktivering van stikstofoksied-sintase lei, wat sodoende die produksie van stikstofoksied verhoog. Koolstofoksied aktiveer weer onbekende effense projeksies, wat skynbaar glutamatergiese neurotransmissie in die ventrale tegmentale area verhoog. Glutamiene suur stimuleer dan mesolimbiese dopaminerge neurone wat tot penile ereksie lei. Hierdie hipotese word hoofsaaklik ondersteun deur die vermoë van oksitosien wat in die ventrale subikulum ingespuit word om ekstrasellulêre glutamienzuur in die ventrale tegmentale area te verhoog (Fig. 3) en van die nie-mededingende NMDA-reseptorantagonis (+) MK-801 wat in die ventrale tegmentale area geïnspireer is, maar nie in die nucleus accumbens nie, om penile ereksie wat deur oksitosien geïnduceerd word, in die ventrale subikulum of in die posteromediale kern geïnkorporeer van die amygdala (Melis et al., 2009b). Op die oomblik is meer besonderhede beskikbaar vir die oksitosien-geïnduceerde penile ereksie van die ventrale subikulum. Hier lyk oksitosien-geïnduseerde penile ereksie sekondêr tot die aktivering van oksitosinere reseptore wat in die selliggame van stikstofoksied-sintase-bevattende neurone geleë is. Dit veroorsaak 'n toename in die produksie van stikstofoksied, wat glutamatergiese neurotransmissie aktiveer deur op te tree as 'n intersellulêre boodskapper met 'n meganisme soortgelyk aan dié wat beskryf word vir langtermyn potensiering (sien Snyder, 1992, Southam en Garthwaite, 1993, Schuman en Madison, 2004) . In lyn met hierdie hipotese kom oksitosien-geïnduceerde penile ereksie saam met 'n toename in ekstrasellulêre glutamienzuur in die dialisaat vanaf die ventrale subikulum, en stimulasie van opwekende aminosuurreseptore in die ventrale subikulum deur NMDA, veroorsaak penis-oprigting. Glutamiene suur aktiveer weer neurale efferprojeksies, wat lei tot die aktivering van mesolimbiese dopaminerge neurone in die ventrale tegmentale area, soos hierbo gerapporteer. As hierdie meganismes ook in werking is, is dit ook in die posteriese kerne van die amygdala op die oomblik onbekend. Daarbenewens is verdere studies nodig om te bewys dat (1) oksitosinergiese senuwee-eindpunte en reseptore in die ventrale subikulum en in die posteriemiese kern van die amygdala in selliggame van neurone wat stikstofoksied-sintase, (2) bevat, gelokaliseer word indien hierdie neurone uiteindelik onder die beheer van eksitatoriese aminosuur (glutamatergiese) sinapse en (3) om die seinstelsel geaktiveer deur stikstofoksied te identifiseer. In hierdie verband is dit opmerklik dat oksitosien se vermoë om stikstofoksied-sintase-aktiwiteit in die selliggame van dopaminerge neurone in die caudale ventrale tegmentale area en van nog onbekende neurone in die ventrale subikulum en die posteromediale kern van die amygdala te herinner, herinner die vermoë van oksitosien om stikstofoksied-sintase in die selliggame van oksitosinergiese neurone in die paraventrikulêre kern te aktiveer (Melis et al., 1997). Alhoewel die verhoogde produksie van stikstofoksied in die selliggame van dopaminerge neurone in die ventrale tegmentale area lei tot die aktivering van hierdie neurone deur die gebruik van guanilaat-siklas en toenemende sikliese GMP, kom dit nie voor in die paraventrikulêre kern nie. Gevolglik veroorsaak 8-broom-sikliese GMP wat in die paraventrikulêre kern ingespuit word, nie penile ereksie nie, terwyl dit in die ventrale tegmentale area ingespuit word. Nog 'n seinroete wat verskil van die stikstofoksied-sikliese GMP-stelsel is dan by die paraventrikulêre vlak betrokke by die aktivering van oksitosinere neurone wat mediasie penile ereksie veroorsaak deur endogene en / of eksogene stikstofoksied (Melis en Argiolas, 1995b; Melis et al., 1997) . 1). Aan die ander kant blyk dit dat cykliese GMP in die ventrale tegmentale area ook 'n sleutelrol speel in die aktivering van mesolimbiese dopaminerge neurone en in die toename in ekstra-sellulêre dopamien wat voorkom in die dialisaat wat verkry word uit die dop van die kernkloppers van manlike rotte geselekteer vir die vertoon of nie-kontak van penis ereksies wanneer dit in die teenwoordigheid van 'n ontoeganklike ovariectomized ontvanklike (estrogeen + progesteroon behandelde) vroulike rot is. In hierdie eksperimentele toestande word manlike rotte wat nie-kontak-penile ereksies toon, 'n toename in ekstra-sellulêre dopamien konsentrasie gevind soos verwag, en hierdie toename word verder verhoog, alhoewel slegs beskeie deur fosfodiesterase-remmers in die caudale ventrale tegmentale area (Sanna et al., 2009).
Die vermoë van oksitosien wat ingespuit word in die ventrale tekentarea, in die ventrale subikulum en in die posteriederiële kortikale kern van die amygdala, tesame met die van dopamienagoniste wat in die paraventrikulêre kern ingespuit word, om penile ereksie te veroorsaak en om mesolimbiese dopaminerge neurone te aktiveer, verdien 'n mate van kommentaar . Eerstens, meganismes soortgelyk aan dié wat hierbo genoem word, kan van toepassing wees wanneer penile ereksie in fisiologiese kontekste voorkom, soos tydens samestelling (wanneer daar in kopulapile ereksies voorkom) of tydens nie-kontak penile ereksies. Hierdie ereksies is feromoon-gemedieerde penis ereksies wat nie onderskei word aan diegene wat deur dwelms of oksitosien geïnduceerd word, wat voorkom wanneer seksueel sterk manlike rotte in die teenwoordigheid van 'n ontoeganklike ontvanklike (ovariectomized estrogeen + progesteron-primed) vroulike rot is en as 'n seksuele indeks beskou word nie. opwekking (Sachs, 1997, 2007). Inderdaad, hoewel hierdie resultate nie aantoon dat oksitosien in hierdie gebiede 'n rol speel in penile ereksie wat plaasvind in fisiologiese kontekste of na dwelmadministrasie nie, voeg hulle nog sterker by tot vroeë bevindinge wat daarop dui dat hierdie breinareas behoort aan diegene waar oksitosien wat sentraal toegepas word, verhoog Nie net spontane penis ereksie episodes gesien pro-erektiele dwelms, maar ook om manlike (en vroulike) seksuele gedrag te verbeter (sien Argiolas en Melis, 2004 en verwysings daarin). Gevolglik verhoog die oksitosienkonsentrasie in die hippokampus van manlike rotte wat behandel word met 'n pro-erektiele dosis apomorfien, 'n klassieke dopamienagonis (Melis et al., 1990) en d (CH2) 5Tyr (Me) -Orn8-vasotosien, wat oksitosien blokkeer. reseptore, is uiters doeltreffend, nie net vir die verswakking van copulatoriese gedrag (Argiolas et al., 1987a) nie, maar ook die fasiliterende effek van apomorfien op manlike kopulatoriese gedrag (Argiolas et al., 1987b) by seksueel sterk manlike rotte, tydens die copula penile ereksie gebeur. d (CH2) 5Tyr (Me) -Orn8-vasotosien is ook uiters sterk in die vermindering van niekontakte-ereksies in seksueel sterk manlike rotte, wanneer dit in nanogramme in die laterale ventrikels gegee word, maar nie in die PVN (Melis et al., 1999a) nie.
Tweedens speel mesolimbiese dopaminerge neurone 'n sleutelrol in die motiverende en lonende eienskappe van natuurlike versterkende stimuli, soos voedsel, water en seksuele aktiwiteit (Fibiger en Phillips, 1988, Wise and Rompre, 1989, Everitt, 1990). In die besonder word dopamien wat vrygestel is van hierdie neurone, gedink om die omsettings van die motiveringsaspekte van natuurlike stimuli in doelgerigte gedrag te bemiddel, byvoorbeeld in die geval van seksuele aktiwiteit, die soeke na 'n seksuele vennoot en seksuele omgang om beloning en bevrediging te bereik (Goto and Grace, 2005). Gevolglik verhoog die ekstrasellulêre dopamienkonsentrasie in dialysaat vanaf die kernkloppers van seksueel kragtige manlike rotte tydens blootstelling aan 'n ontoeganklike ovariectomized estrogeen + progesteroon-primed ontvanklike vroulike rot, en so 'n toename was selfs hoër toe die manlike rat toegelaat word om te kopieer met die ontvanklike vroulike (Pfaus en Everitt, 1995).
Derdens ondersteun die huidige resultate die hipotese dat 'n neurale kring die paraventrikulêre kern met die ventrale tegmentale area direk of indirek verbind (deur die ventrale subikulum en / of die posteromediale kortikale kern van die amygdala) en die nucleus accumbens en van hier af deur onbekende weë terug na die paraventrikulêre kern om die aktiwiteit van oksitosinergiese neurone wat na die rugmurgmediasie-penile ereksie uitsteek, en oksitokinergiese neurone wat na die ventrale tegmentale area, die ventrale subikulum en die posteromediale kortikale kern van die amygdala uitsteek, te moduleer. aktiwiteit van mesolimbiese dopaminerge neurone (Fig. 4). Hierdie komplekse neurale kring kan 'n rol speel in die integrasie van neurale aktiwiteite wat betrokke is by die beheer van die verbruikende (erektiele-ejakulatoriese) en anticiperende (motiverende en bevredigende) aspekte van manlike seksuele gedrag in fisiologiese kontekste. Inderdaad, ekstracellulêre dopamien neem toe in die nucleus accumbens (Pfaus en Everitt, 1995) en in die paraventrikulêre kern van seksueel sterk manlike rotte tydens blootstelling aan 'n ontoeganklike ontvanklike vroulike rat, wanneer ongeskonde ereksies voorkom, en selfs meer wanneer kopulasie toegelaat word, bv. wanneer daar in copula penile ereksies voorkom (Melis et al., 2003). Alhoewel verdere studies nodig is om die rol van endogene oksitosien in die ventrale tegmentale area, die ventrale subikulum en die amygdala tydens ongeskonde ereksies en seksuele gedrag te verduidelik, kan dit dus redelik wees om aan te neem dat hierdie hipotetiese neurale kring, terwyl dit bydra tot die verbruikende aspekte van seksuele gedrag, kan die mesolimbiese dopaminerge sisteem ook 'n neurale substraat aktiveer om die belonende eienskappe van seksuele aktiwiteit te verduidelik (Everitt, 1990, Pfaus en Everitt, 1995). In hierdie opsig is dit opmerklik dat die mesolimbiese dopaminerge sisteem wat geaktiveer word deur oksitosien geïnspireer in die ventrale tegmentale area, geaktiveer word deur dwelmmiddels soos opiate, kannabinoïede, amfetamien, kokaïen en alkohol (Tanda et al., 1997) en dat oksitosien gevind is om die verdraagsaamheid en afhanklikheid van kokaïen, morfien, alkohol en cannabinoïede te verminder (Kovacs et al., 1998; Cui et al., 2001). Ten slotte blyk dit dat oksitosien vrygestel word nie net in die ventrale tegmentale area nie, maar ook in die ventrale subikulum en die posteromediale kortikale kern van die amygdala, kan mesolimbiese dopaminerge neurone aktiveer, wat betrokke kan wees by die aptytende en lonende effekte van seksuele aktiwiteit . Die aktivering van mesolimbiese dopaminerge neurone kan direk deur oksitokinergiese reseptore in die selliggame van mesolimbiese dopaminerge neurone, of indirekte deur die aktivering van glutamiene suur-neurotransmissie in die ventrale tegmentale area.
Dopamien vrygestel in die nucleus accumbens dop modulateer op sy beurt die aktiwiteit van die incerto-hipotalamiese dopaminerge neurone in die paraventrikulêre kern wat penile ereksie veroorsaak (via aktivering van oksitosinergiese neurone wat na die rugmurg uitsteek) of seksuele motivering en beloning (via aktivering van oksitosinergiese neurone wat na die ventrale tegmentale area, die ventrale subikulum of die posteromediale kortikale kern van die amygdala uitsteek). Aangesien dopamien ook vrygestel word in die nukleus accumbens-dop en in die paraventrikulêre kern wanneer penile ereksie in fisiologiese kontekste voorkom (bv. Nie-kontak-ereksies en kopulasie) (Succu et al., 2007, Melis et al., 2003, 2007) waarskynlik dat sentrale oksitokinergiese neurone aan neurale bane deelneem wat 'n interaksie tussen die mesolimbiese en die incerto-hipotalamiese dopaminerge sisteem bemiddel. Hierdie neurale stroombane kan nie net in die verbruiksfase van seksuele gedrag (bv. Penis oprigting en kopulasie) speel nie, maar ook in seksuele motivering, seksuele opwinding en seksuele beloning.
Skematiese voorstelling van hipotetiese neurale kringe wat oksitosien beïnvloed wat seksuele motivering, beloning en seksuele prestasie beïnvloed, soos voorgestel deur die resultate van hierdie hoofstuk en vorige verslae. Oksitokinergiese neurone wat uit die paraventrikulêre kern ontstaan en na die rugmurg uitsteek wanneer dit byvoorbeeld deur dopamien en glutamienzuur (maar ook deur ander neurotransmitters en / of neuropeptiede) geaktiveer word, fasiliteer penile ereksie en seksuele prestasie deur oksitokinergiese neurone wat na die rugmurg uitsteek, te aktiveer. Dopamien en glutamienzuur (maar ook neurotransmitters en neuropeptides) in die paraventrikulêre kern aktiveer ook oksitosinergiese neurone wat na die ventrale tegmentale area uitsteek, waardeur mesolimbiese dopaminerge neurone geprojekteer word wat na die nucleus accumbens uitwerk, seksuele motivering en beloning moduleer. Dopamien vrygestel in die nucleus accumbens (NAs) aktiveer op sy beurt steeds onbekende neurale weë, wat die aktiwiteit van dwelm-dopaminerge neurone (wat uit die A13-A14-groepe van Dahlstrom en Fuxe) voorkom, verhoog die aktiwiteit van oksitosinergiese neurone, insluitend diegene wat na die rugmurg wat tot penile ereksie lei. Hierdie stroombaan kan ook geaktiveer word deur oksitosien geïnspireer nie net in die caudale ventrale tegmentale area nie, maar ook in die ventrale subikulum en in die amygdala, wat ook 'n oksitokinergiese innervasie van die paraventrikulêre kern ontvang, moontlik deur direkte of indirekte glutamatergiese efferent na die ventrale tegmentale area, wat lei tot die modulasie van beide seksuele motivering en penis oprigting. Laastens kan bogenoemde kringe ook deur seksuele stimuli en feromone geaktiveer word, aangesien ekstracellulêre dopamien en glutamiene suur in die paraventrikulêre kern (en in die mediale preoptiese area) tydens feromoon gemedieerde nie-kontak-ereksies en copulasie toeneem. (Vir toepaslike verwysings sien die Verwysingslys).
Erkennings Hierdie werk is gedeeltelik ondersteun deur 'n toekenning van die Italiaanse Ministerie van die Universiteit en van Navorsing aan AA en MRM
Verwysings
Andersson, KE, 2001. Farmakologie van penis oprigting. Pharmacol. Op 53, 417-450. Argiolas, A., 1994. Stikstofoksied is 'n sentrale bemiddelaar van penis oprigting. Neurofarmakologie 33, 1339-1344. Argiolas, A., 1999. Neuropeptides en seksuele gedrag. Neurosci. Biobehav. Op 23, 1127-1142. Argiolas, A., Gessa, GL, 1991. Sentrale funksies van oksitosien. Neurosci. Biobehav. Op 15, 217-231. Argiolas, A., Melis, MR, 1995. Neuromodulasie van penis oprigting: 'n oorsig van die rol van neurotransmitters en neuropeptides. Prog. Neurobiol. 47, 235-255. Argiolas, A., Melis, MR, 2004. Die rol van oksitosien en die paraventrikulêre kern in die seksuele gedrag van manlike soogdiere. Physiol. Behav. 83, 309-317. Argiolas, A., Melis, MR, 2005. Sentrale beheer van penis oprigting: rol van die paraventrikulêre kern van die hipotalamus. Prog. Neurobiol. 76, 1-21. Argiolas, A., Collu, M., Gessa, GL, Melis, MR, Serra, G., 1988. Die oksitosienantagonis d (CH2) 5Tyr (Me) -Orn8-vasotosien antagoniseer manlike kopulatoriese gedrag by rotte. E. J. Pharmacol. 149, 389-392. Argiolas, A., Collu, M., D'Aquila, P., Gessa, GL, Melis, MR, Serra, G., 1989. Apomorfiene stimulasie van manlike kopulatoriese gedrag word verhoed deur die oksitosienantagonis d (CH2) 5Tyr (Me) -Orn8-vasotosien in rotte. Pharmacol. Biochem. Behav. 33, 81-83. Argiolas, A., Melis, MR, Gessa, GL, 1985. Intraventrikulêre oksitosien induceer gaai en penis ereksie by rotte. E. J. Pharmacol. 117, 395-396. Argiolas, A., Melis, MR, Gessa, GL, 1986. Oksitosien: 'n uiters sterk inducer van penis ereksie en gaaf in manlike rotte. E. J. Pharmacol. 130, 265-272. Argiolas, A., Melis, MR, Mauri, A., Gessa, GL, 1987a. Paraventrikulêre nukleuslees voorkom dat gaai en penis ereksie geïnduseer word deur apomorfien en oksitosien, maar nie deur ACTH by rotte nie. Brein Res. 421, 349-352. Argiolas, A., Melis, MR, Vargiu, L., Mauri, A., Gessa, GL, 1987b. d (CH2) 5Tyr (Me) -Orn8-vasotosien, 'n kragtige oksitosienantagonis, benadeel penis ereksie en gaaf veroorsaak deur oksitosien en apomorfien, maar nie deur ACTH 1-24 nie. E. J. Pharmacol. 134, 221-224. Argiolas, A., Melis, MR, Stancampiano, R., Gessa, GL, 1990. _ -Konotoxien verhoed apomorfien- en oksitosien-geïnduceerde penile ereksie en gaaf in manlike rotte. Pharmacol. Biochem. Behav. 37, 253-257. Arletti, R., Bertolini, A., 1985. Oksitosien stimuleer lordose gedrag by vroulike rotte. Neuropeptides 6, 247-255. Arletti, R., Bazzani, C., Castelli, M., Bertolini, A., 1985. Oksitosien verbeter manlike kopulatoriese prestasie by rotte. Horm. Behav. 19, 14-20. Arletti, R., Benelli, A., Bertolini, A., 1990. Seksuele gedrag van verouderde manlike rotte word deur oksitosien gestimuleer. E. J. Pharmacol. 179, 377-382. Arletti, R., Calzà, L., Giardino, L., Benelli, A., Cavazzutti, E., Bertolini, A., 1997. Seksuele impotensie word geassosieer met 'n verminderde produksie van oksitosien en 'n verhoogde produksie van opioïede peptiede in die paraventrikulêre kern van die hipotalamus. Neurosci. Lett. 233, 65-68. Bancila, M., Giuliano, F., Rampin, O., Mailly, P., Brisorgueil, MJ, Clas, A., Verge, D., 2002. Bewys vir 'n direkte projeksie vanaf die paraventrikulêre kern van die hipotalamus tot vermeende serotoninergiese neurone van die kernparagigantocellularis betrokke by die beheer van ereksie by rotte. E. J. Neurosci. 16, 1240-1249. Burnett, AL, Lowenstein, CJ, Bredt, DS, Chang, TSK, Snyder, SH, 1992. Nitriese oksied: 'n fisiologiese mediator van penis oprigting. Wetenskap 257, 401-403. Baskerville, TA, Douglas, AJ, 2008. Interaksie tussen dopamien en oksitosien in die beheer van seksuele gedrag. Prog. Brein Res. 170, 277-289. Baskerville, TA, Allard, J., Wayman, C., Douglas, AJ, 2009. Dopamien-oksitosien interaksie in penis oprigting. E. J. Neurosci. 30, 2151-2164. Benelli, A., Bertolini, A., Poggioli, R., Cavazzutti, E., Calzà, L., Giardino, L., Arletti, R., 1995. Stikstofoksied is betrokke by manlike seksuele gedrag van rotte. E. J. Pharmacol. 294, 505-510. Bernabè, J., Rampin, O., Sachs, BD, Giuliano, F., 1999. Intravaskale druk tydens ereksie by rotte: 'n integrerende benadering gebaseer op telemetriese opname. Am. J. Physiol. 276, R441-R449. Bitner, RS, Nikkel, AL, Otte, S., Martino, B., Barlow, EH, Bhatia, P., Stewart, AO, Brioni, JD, Decker, MW, Moreland, RB, 2006. Dopamien D4 reseptor sein in die rat paraventrikulêre hipotalamus kern: bewyse van natuurlike koppeling wat onmiddellike vroeë gene induksie en mitogeen geaktiveerde proteïenkinase fosforilering behels. Neurofarmakologie 50, 521-531. Brioni, JD, Moreland, RB, Cowart, M., Hsieh, GC, Stewart, AO, Hedlund, P., Donnelly-Roberts, DL, Nakane, M., Lynch 3rd., J., Kolasa, T., Polakowski , JS, Osinski, MA, Marsh, K., Andersson, KE, Sullivan, JP, 2004. Aktivering van dopamien D4 reseptore deur ABT-724 veroorsaak penis ereksie by rotte. Proc. Natl. ACAD. Sci. VSA 101, 6758-6763. Buijs, RM, 1978. Intra- en ekstra-hipotalamiese vasopressien- en oksitosienbane in die rat. Selweefsel Res. 192, 423-435. Buijs, RM, Geffard, M., Pool, CW, Hoorneman, EMD, 1984. Die dopaminerge innervasie van die supraoptiese en paraventrikulêre kern. 'N Lig- en elektronmikroskopiese studie. Brein Res. 323, 65-72. Caldwell, JD, Prange, AJ, Pedersen, CA, 1986. Oksitosien fasiliteer die seksuele ontvanklikheid van estrogeen-behandelde vroulike rotte. Neuropeptides 7, 175-189. Cameron, JL, Pomerantz, SM, Layden, LM, Amico, JA, 1992. Dopaminerge stimulering van oksitosienkonsentrasies in die plasma van manlike en vroulike ape deur apomorfien en 'n D2-reseptoragonist. J. Clin. Endocrinol. Metab. 75, 855-860. Canteras, NS, Simerly, RB, Swanson, LW, 1995. Organisasie van projeksies uit die mediale kern van die amygdala: 'n PHAL-studie in die rot. J. Comp. Neurol. 360, 213-245. Carmichael, MS, Humbert, R., Dixen, J., Palmisano, G., Greeleaf, W., Davidson, JM, 1987. Plasma oksitosien toeneem in menslike seksuele respons. J. Clin. Endocrinol. Metab. 64, 27-31. Carter, CS, 1992. Oksitosien en seksuele gedrag. Neurosci. Biobehav. Op 16, 131-144. Carter, CS, Lederhendler, II, Kirkpatrick, B., 1997. Die Interaktiewe Neurobiologie van Affiliasie, Annale van die New York Academy of Sciences, vol. 807. Die New York Akademie van Wetenskappe, New York. Castelli, LP, Piras, AP, Melis, T., Succu, S., Sanna, F., Melis, MR, Collu, S., Ennas, MG, Diaz, G., Mackie, K., Argiolas, A. , 2007. Cannabinoïde CB1-reseptore in die paraventrikulêre kern en sentrale beheer van penile ereksie: immunokytochemie, autoradiografie en gedragstudies. Neurowetenskap 147, 197-206. Chen, KK, Chang, LS, 2003. Effek van eksitatoriese aminosuurreseptoragoniste op penile ereksie na toediening in paraventrikulêre kern van die hipotalamus by rotte. J. Urol. 62, 575-580. Chen, KK, Chan, JYH, Chang, LS, Chen, MT, Chang, SHH, 1992. Uitnodiging van penis oprigting na aktivering van die seekoei-vorming in die rat. Neurosci. Lett. 141, 218-222. Chen, KK, Chan, JYH, Chang, LS, 1999. Dopaminerge neurotransmissie by die paraventrikulêre kern van die hipotalamus in sentrale regulering van penile ereksie in die rat. J. Urol. 162, 237-242. Collins, GT, Truccone, A., Haji-Abdi, F., Newman, AH, Grundt, P., Rice, KC, Mans, SM, Greedy, BM, Enguehard-Gueiffer, C., Gueiffer, A., Chen , J., Wang, S., Katz, JL, Grandy, DK, Sunahara, RK, Woods, JH, 2009. Pro-erektiele effekte van dopamienD2-agoniste word bemiddel deur die D3-reseptor by rotte en muise. J. Pharmacol. Exp. En daar. 329, 210-217. Coolen, LM, Allard, J., Truitt, WA, McKenna, KE, 2004. Sentrale regulering van ejakulasie. Physiol. Behav. 83, 203-215. Cui, SS, Bowen, RC, Gu, GB, Hannesson, BK, Yu, PH, Zhang, X., 2001. Voorkoming van kannabinoïed onttrekkingsindroom deur litium: betrokkenheid van oksitosinergiese neuronale aktivering. J. Neurosci. 21, 9867-9876. Dahlstrom, A., Fuxe, K., 1964. Bewys vir die bestaan van monoamienbevattende neurone in die sentrale senuweestelsel. I. Demonstrasie van monoamiene in die selliggame van breinstam neurone. Acta Physiol. Scand. 62 (Suppl. 232), 1-54. Depoortère, R., Bardin, L., Rodrigues, M., Abrial, E., Aliaga, M., Newman-Tancredi, A., 2009. Penile ereksie en gaping veroorsaak deur dopamien D2-agtige reseptoragoniste by rotte: invloed van spanning en bydrae van dopamien D2, maar nie D3- en D4-reseptore nie. Behav. Pharmacol. 20, 303-311. Domes, G., Heinrichs, M., Buchel, C., Braus, DF, Herpertz, SC, 2007. Oksitosien verswak amygdala-reaksies op emosionele gesigte ongeag valensie. Biol. Psigiatrie 62, 11871190. Dominguez, J., Riolo, JV, Xu, Z., Hull, ME, 2001. Regulering deur die mediale amygdala van kopulasie en mediale preoptiese dopamien vrystelling. J. Neurosci. 21, 349-355. Donaldson, ZR, Young, LJ, 2009. Oksitosien, vasopressien en die neurogenetika van sosialiteit. Wetenskap 322, 900-904. Eaton, RG, Markowski, VF, Lumley, LA, Thompson, JT, Moses, J., Hull, EM, 1991. D2-reseptore in die paraventrikulêre kern reguleer genitale response en kopulasie by manlike rotte. Pharmacol. Biochem. Behav. 39, 177-181. Ebner, K., Bosch, OJ, Krömer, SA, Singewald, N., Neumann, ID, 2005. Vrystelling van oksitosien in die rat sentrale amigdala moduleer stres-coping gedrag en die vrylating van opwindende aminosure. Neuropsigofarmacologie 30, 223-230. Enguehard-Gueiffier, C., Hübner, H., El Hakmaoui, A., Allouchi, H., Gmeiner, P., Argiolas, A., Melis, MR, Gueiffier, A., 2006. 2 - [(4-Fenylpiperazine-1-yl) metiel] imidazo (di) asiene as selektiewe D4-ligande. Induksie van penis oprigting deur 2- [4- (2-methoxyphenyl) piperazine-1-ylmethyl] imidazo [1,2-a] -pyridien (PIP3EA), 'n kragtige en selektiewe D4-agonis. J. Med. Chem. 49, 3938-3947. Everitt, BJ, 1990. Seksuele motivering: 'n neurale en gedragsontleding van die meganismes onderliggend aan aanvullende en copulatoriese response, manlike rotte. Neurosci. Biobehav. Op 14, 217-232. Fibiger, HC, Phillips, AG, 1988. Mesokortikolimbiese dopamienstelsel en beloning. Ann. N. Y. ACAD. Sci. 5, 206-215. Frans, SJ, Totterdell, S., 2003. Individuele nucleus accumbens-projeksie neurone ontvang beide basolaterale amygdala en ventrale subikulêre afferente in rotte. Neurowetenskap 119, 19-31. 954 MR Melis, A. Argiolas / Neurowetenschappen en Biobehaviorale Reviews 35 (2011) 939-955 Freund-Mercier, MJ, Richard, P., 1981. Opwindende effekte van intraventrikulêre inspuitings van oksitosien op die melkuitwerpingsrefleks in die rat. Neurosci. Lett. 23, 193-198. Freund-Mercier, MJ, Richard, P., 1984. Elektrofisiologiese bewyse vir die fasilitering van oksitosienneurone deur oksitosien tydens die suig in die rot. J. Physiol. (Lond.) 352, 447-466. Freund-Mercier, MJ, Stoeckel, ME, 1995. Somatodendritiese autoreceptors op oksitosienneurone. In: Ivell, R., Russel, JA (Eds.), Oksitosien, sellulêre en molekulêre benaderings in medisyne en navorsing. Adv. Exp. Med. Biol., 365. Plenum Press, New York en Londen, pp. 185-194. Freund-Mercier, MJ, Stoeckel, ME, Palacios, JM, Pazos, JM, Richard, PH, Porte, A., 1987. Farmakologiese eienskappe en anatomiese verspreiding van 3H oksitosien bindingsplekke in die Wistar rat brein bestudeer deur autoradiografie. Neurowetenskap 20, 599-614. Giuliano, F., Rampin, O., 2000. Sentrale beheer van penis oprigting. Neurosci. Biobehav. Op 24, 517-533. Giuliano, F., Allard, J., 2001. Dopamien en seksuele funksie. Int. J. Impotensie Res. 13 (Suppl. 3), 18-28. Giuliano, F., Rampin, O., 2004. Neurale beheer van oprigting. Physiol. Behav. 83, 189-201. Giuliano, F., Bernabè, J., McKenna, KE, Longueville, F., Rampin, O., 2001. Spinale prokektiele effek van oksitosien in verdovende rotte. Am J. Physiol. Regul. Integ. Comp. Physiol. 280, R1870-R1877. Gaan, Y., Grace, AA, 2005. Dopaminerge modulasie van limbiese en kortikale dryfkrag van kernklemme in doelgerigte gedrag. Nat. Neurosci. 8, 805-812. Hawthorn, J., Ang, VT, Jenkins, JS, 1985. Effekte van letsels in die hipotalamiese paraventrikulêre, supraoptiese en suprachiasmatiese kerne op vasopressien en oksitosien in rotbrein en rugmurg. Brein Res. 346, 51-57. Hier, RF, Dolak, LA, Duncan, JN, Hyslop, DK, Lipton, MF, Martin, LJ, Mauragis, MA, Piercey, MF, Nichols, NF, Schreur, PJ, Smith, MW, Maan, MW, 1997. Sintese en biologiese aktiwiteite van (R) -5,6-dihydro-N, N-dimethyl-4H-imidazo [4,5,1-ij] kinolien-5-amin) en sy metaboliete. J. Med. Chem. 40, 639-646. Hsieh, GC, Hollingsworth, PR, Martino, B., Chang, R., Terranova, MA, O'Neill, AB, Lynch, JJ, Moreland, RB, Donnelly-Roberts, DL, Kolasa, T., Mikusa, JP , McVey, JM, Marsh, KC, Sullivan, JP, Brioni, JD, 2004. Sentrale meganismes wat penile ereksie in bewuste rotte reguleer: die dopaminerge stelsels wat verband hou met die prokektiele effek van apomorfien. J. Pharmacol. Exp. En daar. 308, 330-338. Huang, PL, Dawson, TM, Bredt, DS, Snyder, SH, Fishman, MC, 1993. Gerigte ontwrigting van die neuronale stikstofoksied-sintasegen. Sel 75, 1273-1286. Huber, D., Veinante, P., Stoop, R., 2005. Vasopressien en oksitosien verwek afsonderlike neuronale bevolkings in die sentrale amygdala. Wetenskap 308, 245-248. Hull, EM, Warner, RK, Bazzett, TJ, Eaton, RC, Thompson, JT, 1989. D2 / D1 verhouding in die mediale preoptiese area beïnvloed die samestelling van manlike rotte. J. Pharmacol. Exp. En daar. 251, 422-427. Hull, EM, Du, J., Lorrain, DS, Matuszewich, L., 1995. Ekstra-sellulêre dopamien in die mediale preoptiese area: implikasies vir seksuele motivering en hormonale beheer van kopulasie. J. Neurosci. 15, 7465-7471. Hull, EM, Meisel, RL, Sachs, BD, 2002. Manlike seksuele gedrag. In: Pfaff, DW, Arnold, AP, Etgen, AM, Fahrbach, SE, Rubin, RT (Eds.), Hormone, Brein en Gedrag. Akademiese Pers, New York, pp. 3-137. Hurlemann, R., Patin, A., Onur, OA, Cohen, MX, Baumgartner, T., Metzler, S., Dziobek, I., Gallinat, J., Wagner, M., Maier, W., Kendrick, KM, 2010. Oksitosien verhoog amigdala-afhanklike, maatskaplik versterkte leer en emosionele empatie by mense. J. Neurosci. 30, 4999-5007. Ivell, R., Russel, JA, 1995. Oksitosien: Sellulêre en Molekulêre Benaderings in Geneeskunde en Navorsing. Voorskotte in eksperimentele geneeskunde en biologie, vol. 395. Plenum Press, New York. Kelley, AE, Domesick, VB, 1982. Die verspreiding van die projeksie vanaf die hippocampale vorming na die kernklem in die rot: 'n anterograde- en retrograde-peperwortelperoksidase-studie. Neurowetenskap 7, 2321-2335. Kimura, Y., Naitou, Y., Wanibuchi, F., Yamaguchi, T., 2008. 5-HT (2C) reseptor aktivering is 'n algemene meganisme op prokektiele effekte van apomorfien, oksitosien en melanotan-II by rotte. E. J. Pharmacol. 589, 157-162. Kondo, Y., Sachs, BD, Sakuma, Y., 1998. Die belangrikheid van die mediale amygdala in die rat-penile ereksie veroorsaak deur afgeleë stimuli van estrouse vroue. Behav. Brein Res. 91, 215-222. Kovacs, GL, Sarnyai, Z., Szabo, G., 1998. Oksitosien en verslawing: 'n oorsig. Psychoneuroendocrinology 23, 945-962. Lee, HJ, Macbeth, AH, Pagani, JH, Scott Young 3rd, W., 2009. Oksitosien: die groot fasiliteerder van die lewe. Prog. Neurobiol. 88, 127-151. Lindvall, O., Bjorklund, A., Skagerberg, G., 1984. Selektiewe istochemiese demonstrasie van dopamien-terminale stelsels in ratdi- en telencephalon: nuwe bewyse vir dopaminerge innervasie van hipotalamiese neurosekretoriese kerne. Brein Res. 306, 19-30. Liu, YC, Salamone, JD, Sachs, BD, 1997. Verswakte seksuele respons na letsels van die paraventrikulêre kern van die hipotalamus by manlike rotte. Behav. Neurosci. 111, 1361-1367. Löber, S., Tschammer, N., Hübner, H., Melis, MR, Argiolas, A., Gmeiner, P., 2009. Die azulene raamwerk as 'n nuwe bioisostere: ontwerp van sterk dopamien D4 reseptor ligande wat penile ereksie veroorsaak. Chem. Med. Chem. 4, 325-328. McCleskey, EW, Fox, AP, Feldman, DH, Cruz, LJ, Olivera, BM, Tsien, RW, Yoshikami, D., 1987. _ -Konotoksien: direkte en aanhoudende blokkade van spesifieke tipes kalsiumkanale in neurone, maar nie spiere nie. Prot. Nat. ACAD. Sci. VSA 84, 4327-4331. McKenna, KE, 2000. Enkele voorstelle rakende die organisasie van die sentrale senuweestelsel beheer van penis oprigting. Neurosci. Biobehav. Op 24, 535-540. Marson, L., McKenna, KE, 1992. 'N rol vir 5-hidroksryptryptamine in dalende remming van ruggraat seksuele reflekse. Exp. Brein Res. 88, 313-318. Marson, L., McKenna, KE, 1996. SSS selgroepe wat betrokke is by die beheer van die ischiocavernosus- en bulbospongiosusspiere: 'n transneuronale opsporingstudie met behulp van pseudorabiesvirus. J. Comp. Neurol. 374, 161-179. Meisel, RL, Sachs, BD, 1994. Die fisiologie van manlike seksuele gedrag. In: Knobil, E., Neil, J. (Eds.), The Physiology of Reproduction, vol. 2, tweede uitgawe. Raven Press, New York, pp. 3-96. Melin, P., Kihlstrom, JE, 1963. Invloed van oksitosien op seksuele gedrag by manlike konyne. Endokrinologie 73, 433-435. Melis, MR, Argiolas, A., 1995a. Dopamien en seksuele gedrag. Neurosci. Biobehav. Op 19, 19-38. Melis, MR, Argiolas, A., 1995b. Nitroksoksied donateurs veroorsaak penile ereksie en gaap wanneer dit in die sentrale senuweestelsel van manlike rotte ingespuit word. E. J. Pharmacol. 294, 1-9. Melis, MR, Argiolas, A., 2003. Sentrale oksitokinergiese neurotransmissie: 'n geneesmiddel teiken vir die terapie van psykogene erektiele disfunksie. Kur. Dwelmteikens 4, 55-66. Melis, MR, Argiolas, A., Gessa, GL, 1986. Oksitosien-geïnduseerde gaai en penis ereksie: werkplek in die brein. Brein Res. 398, 259-265. Melis, MR, Argiolas, A., Gessa, GL, 1987. Apomorfien-geïnduseerde gaai en penis ereksie: werkplek in die brein. Brein Res. 415, 98-104. Melis, MR, Argiolas, A., Gessa, GL, 1989a. Apomorfien verhoog plasmaoksitosienvlakke by rotte. Neurosci. Lett. 98, 351-355. Melis, MR, Argiolas, A., Gessa, GL, 1989b. Bewys dat apomorfien indringing van penis en gaaf veroorsaak deur oksitosien in die sentrale senuweestelsel vry te stel. E. J. Phamacol. 164, 565-570. Melis, MR, Argiolas, A., Stancampiano, R., Gessa, GL, 1990. Effek van apomorfien op oksitosienkonsentrasies in verskillende breinareas en plasma van manlike rotte. E. J. Pharmacol. 182, 101-107. Melis, MR, Mauri, A., Argiolas, A., 1994a. Apomorfien- en oksitosien-geïnduseerde penile ereksie en gaaf in ongeskonde en gekastreerde manlike rotte: effek van seksuele steroïede. Neuroendocrinology 59, 349-354. Melis, MR, Stancampiano, R., Argiolas, A., 1994b. Penile ereksie en gaaf veroorsaak deur paraventrikulêre NMDA inspuitings word bemiddel deur oksitosien. Pharmacol. Biochem. Behav. 48, 203-207. Melis, MR, Stancampiano, R., Argiolas, A., 1994c. Voorkoming deur NG-nitro-l-arginien-metiel ester van apomorfien- en oksitosien-geïnduceerde penile ereksie en gaai: werkplek in die brein. Pharmacol. Biochem. Behav. 48, 799-804. Melis, MR, Succu, S., Argiolas, A., 1996. Dopamien-agoniste verhoog die produksie van stikstofoksied in die paraventrikulêre kern van die hipotalamus: korrelasie met penis oprigting en gaai. E. J. Neurosci. 8, 2056-2063. Melis, MR, Succu, S., Iannucci, U., Argiolas, A., 1997. Oksitosien verhoog die produksie van stikstofoksied in die paraventrikulêre kern van die hipotalamus: korrelasie met penis oprigting en gaai. Reg. Peptides 69, 105-112. Melis, MR, Succu, S., Mauri, A., Argiolas, A., 1998. Produksie van stikstofoksied word verhoog in die paraventrikulêre kern van die hipotalamus van manlike rotte tydens nie-kontak penis ereksies en copulasie. E. J. Neurosci. 10, 1968-1974. Melis, MR, Spano, MS, Succu, S., Argiolas, A., 1999a. Die oksitosienantagonis d (CH2) 5Tyr (Me) 2-Orn8-vasotosien verminder penile ereksies wat nie in kontak is met manlike rotte nie. Neurosci. Lett. 265, 171-174. Melis, MR, Succu, S., Spano, MS, Argiolas, A., 1999b. Morfien wat ingespuit word in die paraventrikulêre kern van die hipotalamus, verhoed kontak-ereksies en verlaag die samestelling: betrokkenheid van stikstofoksied. E. J. Neurosci. 11, 1857-1864. Melis, MR, Spano, MS, Succu, S., Argiolas, A., 2000. Effek van eksitatoriese aminosuur-, dopamien- en oksitosienreseptor antagoniste op nie-kontak penis ereksies en paraventrikulêre stikstofoksied produksie in manlike rotte. Behav. Neurosci. 114, 849-857. Melis, MR, Succu, S., Mascia, MS, Cortis, L., Argiolas, A., 2003. Ekstra-sellulêre dopamien neem toe tydens die seksuele aktiwiteit in die paraventrikulêre kern van manlike rotte. E. J. Neurosci. 17, 1266-1272. Melis, MR, Succu, S., Mascia, MS, Argiolas, A., 2004a. Antagonisme van cannabinoïede CB1-reseptore in die paraventrikulêre kern van manlike rotte veroorsaak penis oprigting. Neurosci. Lett. 359, 17-20. Melis, MR, Succu, S., Mascia, MS, Cortis, L., Argiolas, A., 2004b. Ekstra-sellulêre eksitatoriese aminosure styg in die paraventrikulêre kern van manlike rotte tydens seksuele aktiwiteit: hoofrol vanNMDA-reseptore in erektiele funksie. E. J. Neurosci. 19, 2569-2575. Melis, MR, Succu, S., Mascia, MS, Argiolas, A., 2005. PD-168,077, 'n selektiewe dopamien D4-reseptor-agonis, veroorsaak penile ereksie wanneer dit in die paraventrikulêre kern van manlike rotte ingespuit word. Neurosci. Lett. 379, 59-62. Melis, MR, Succu, S., Mascia, MS, Sanna, F., Melis, T., Succu, S., Castelli, MP, Argiolas, A., 2006a. SR 141716A-geïnduceerde penile ereksie by manlike rotte: betrokkenheid van paraventrikulêre glutamienzuur en stikstofoksied. Neurofarmakologie 50, 219-228. Melis, M., Succu, S., Sanna, F., Mascia, MS, Melis, T., Enguehard-Gueiffier, C., Hubner, H., Gmenier, P., Gueiffier, A., Argiolas, A., 2006b. PIP3EA en PD168077, twee selektiewe dopamien D4-reseptoragoniste, veroorsaak penile ereksie by manlike rotte: plek en werkingsmeganisme in die brein. E. J. Neurosci. 24, 2021-2030. Melis, MR, Melis, T., Cocco, C., Succu, S., Sanna, F., Pillolla, G., Boi, A., Ferri, GL, Argiolas, A., 2007. Oksitosien wat in die ventrale tegmentale area ingespuit word, veroorsaak penile ereksie en verhoog die ekstra-sellulêre dopamien in die kernkolom MR Melis, A. Argiolas / Neurowetenschappen en Biobehaviorale Reviews 35 (2011) 939-955 955 en paraventrikulêre kern van die hipotalamus van manlike rotte. E. J. Neurosci. 26, 1026-1035. Melis, MR, Sanna, F., Succu, S., Zarone, P., Boi, A., Argiolas, A., 2009a. Die rol van oksitosien in die aanvangs- en verbruiksfases van manlike rotse seksuele gedrag. In: Jastrow, H., Feuerbach, D. (Eds.), Handboek van Oksitosiennavorsing: Sintese, berging en vrystelling, aksies en geneesmiddels. Nova Publishers Inc, New York, VSA, pp. 109-125. Melis, MR, Succu, S., Sanna, F., Boi, A., Argiolas, A., 2009b. Oksitosien wat ingespuit word in die ventrale subikulum of die posteromediale kortikale kern van die amygdala, veroorsaak penile ereksie en verhoog ekstrasellulêre dopamien in die kernkloppers van manlike rotte. E. J. Neurosci. 30, 1349-1357. Melis, MR, Succu, S., Cocco, C., Caboni, E., Sanna, F., Boi, A., Ferri, GL, Argiolas, A., 2010. Oksitosien induceer penile ereksie wanneer dit in die ventrale subikulum ingespuit word: rol van stikstofoksied en glutamienzuur. Neurofarmakologie 58, 1153-1160. Moreland, RB, Nakane, M., Donnelly-Roberts, DL, Miller, LN, Chang, R., Uchic, ME, Terranova, MA, Gubbins, EJ, Helfrich, RJ, Namovic, MT, El-Kouhen, OF, Meesters, JN, Brioni, JD, 2004. Vergelykende farmakologie van menslike dopamien D (2) -like reseptor stabiele sellyne gekoppel aan kalsium vloed deur Galpha (qo5). Biochem. Pharmacol. 68, 761-772. Moos, F., Freund-Mercier, MJ, Guerne, Y., Guerne, JM, Stoeckel, ME, Richard, P., 1984. Vrystelling van oksitosien en vasopressien deur magnokellulêre kerne in vitro: spesifieke fasiliterende effek van oksitosien op eie vrylating. J. Endocrinol. 102, 63-72. Murphy, MR, Seckl, JR, Burton, S., Checkley, SA, Lightman, SL, 1987. Veranderinge in oksitosien- en vasopressiensekresie tydens seksuele aktiwiteit by mans. J. Clin. Endocrinol. Metab. 65, 738-741. Nishimori, K., Young, LJ, Guo, Q., Wang, Z., Insel, TR, Matzuk, MM, 1996. Oksitosien word benodig vir verpleegkunde, maar nie noodsaaklik vir bevalling of voortplantingsgedrag nie. Proc. Natl. ACAD. Sci. VSA 93, 11699-11704. Patel, S., Freedman, S., Chapman, KL, Emms, F., Fletcher, AE, Knowles, M., Marwood, R., McCallister, G., Myers, J., Curtis, J., Kulagowski, JJ, Leeson, PD, Ridgill, M., Graham, M., Matheson, S., Rathbone, D., Watt, AP, Bristow, LJ, Rupniak, NM, Baskin, E., Lynch, JJ, Ragan, Cl , 1997. Biologiese profiel van L 745,870, 'n selektiewe antagonis met hoë affiniteit vir die dopamien D4 reseptor. J. Pharmacol. Exp. En daar. 283, 636-647. Pedersen, CA, Caldwell, JD, Jirikowski, GF, Insel, TR, 1992. Oksitosien in Materale, Seksuele en Sosiale Gedrag, Annale van die New York Academy of Sciences, vol. 652. Die New York Akademie van Wetenskappe, New York. Petrovic, P., Kalisch, R., Sanger, T., Dolan, RJ, 2008. Oksitosien verswak affektiewe evaluasies van gekondisioneerde gesigte en amygdala-aktiwiteit. J. Neurosci. 28, 6607-6615. Pfaus, JG, Everitt, BJ, 1995. Die psigofarmakologie van seksuele gedrag. In: Knobil, FE, Kupfer, DJ (Eds.), Psigofarmakologie: die vierde generasie van vordering. Raven Press, New York, pp. 742-758. Rajfer, J., Aronson, WJ, Bush, PA, Dorey, FJ, Ignarro, LJ, 1992. Nitriese oksied as mediator van die verslapping van die corpus cavernosum in reaksie op nieadrenerge, niecholinergiese neurotransmissie. N. Engl. J. Med. 326, 90-94. Roeling, TAP, Van Erp, AMM, Meelis, W., Kruk, MR, Veening, JG, 1991. Gedragsgevolge van NMDA ingespuit in die hipotalamiese paraventrikulêre kern van die rat. Brein Res. 550, 220-224. Sachs, BD, 1997. Oprigting wat in manlike rotte opgewek word deur die luggeur van estrouse vroue. Physiol. Behav. 62, 921-924. Sachs, BD, 2000. Kontekstuele benaderings tot die fisiologie en klassifikasie van erektiele funksie, erektiele disfunksie en seksuele opwinding. Neurosci. Biobehav. Op 24, 541-560. Sachs, BD, 2007. 'N Kontekstuele definisie van manlike seksuele opwinding. Horm. Behav. 51, 569-578. Sanchez, F., Alonso, JR, Arevalo, R., Blanco, E., Aijon, J., Vazquez, R., 1994. Sameksistensie van NADPH-diaphorase met vasopressien en oksitosien in die hipotalamiese magnosellulêre neurosekretoriese kern van die rat. Selweefsel Res. 276, 31-34. Sanna, F., Succu, S., Boi, A., Melis, MR, Argiolas, A., 2009. Fosfodiesterase-tipe 5-inhibeerders fasiliteer nie-kontak-ereksies by manlike rotte: werkplek in die brein en meganisme van werking. J. Seks. Med. 6, 2680-2689. Saphier, D., Feldman, S., 1987. Effekte van septal en hippocampale stimuli op paraventrikulêre kern neurone. Neurowetenskap 20, 749-755. Sato-Suzuki, I., Kita, I., Oguri, M., Arita, H., 1998. Stereotipe gaafreaksies veroorsaak deur elektriese en chemiese stimulasie van paraventrikulêre kern van die rat. J. Neurophysiol. 80, 2765-2775. Schuman, EM, Madison, DV, 1994. Nitriese oksied en sinaptiese funksie. Ann. Op Neurosci. 17, 153-183. Snyder, SH, 1992. Nitriese oksied: eerste in 'n nuwe klas neurotransmitters? Wetenskap 254, 494-496. Sofroniew, MV, 1983. Vasopressien en oksitosien in die soogdierbrein en rugmurg. Neigings Neurosci. 6, 467-472. Sokoloff, P., Schwartz, JC, 1995. Nuwe dopamienreseptore 'n halwe dekade later. Neigings Pharmacol. Sci. 16, 270-275. Southam, E., Garthwaite, J., 1993. Die stikstofoksied-sikliese GMP seinroete in rotbrein. Neurofarmakologie 32, 1267-1277. Stancampiano, R., Melis, MR, Argiolas, A., 1994. Penile ereksie en gaping veroorsaak deur 5-HT1c agoniste in manlike rotte: verhouding met dopaminerge en oksitosinergiese oordrag. E. J. Pharmacol. 261, 149-155. Succu, S., Mascia, MS, Sanna, F., Melis, T., Argiolas, A., Melis, MR, 2006. Die kannabinoïede CB1-reseptor antagonis SR 141716A veroorsaak penis ereksie deur ekstra-sellulêre glutamienzuur in die paraventrikulêre kern van manlike rotte te verhoog. Behav. Brein Res. 169, 274-281. Succu, S., Sanna, F., Melis, T., Boi, A., Argiolas, A., Melis, MR, 2007. Stimulering van dopamienreseptore in die paraventrikulêre kern van die hipotalamus van manlike rotte veroorsaak penile ereksie en verhoog ekstrasellulêre dopamien in die nukleusakkels: betrokkenheid van sentrale oksitosien. Neurofarmakologie 52, 1034-1043. Succu, S., Sanna, F., Cocco, C., Melis, T., Boi, A., Ferri, GL, Argiolas, A., Melis, MR, 2008. Oksitosien induceer penile ereksie wanneer dit ingespuit word in die ventrale tegmentale area van manlike rotte: rol van stikstofoksied en sikliese GMP. E. J. Neurosci. 28, 813-821. Tanda, G., Pontieri, FE, Di Chiara, G., 1997. Kannabinoïede en heroïenaktivering van mesolimbiese dopamien-oordrag deur 'n algemene mu1-opioïed-reseptormeganisme. Wetenskap 276, 2048-2050. Tang, Y., Rampin, O., Calas, A., Facchinetti, P., Giuliano, F., 1998. Oksitosinergiese en serotoninergiese innervasie van geïdentifiseerde lumbosakrale kerne wat penile ereksie in die manlike rat beheer. Neurowetenskap 82, 241-254. Teodose, DT, 1985. Oksitosien-immunoreaktiewe terminale sinkaps op oksitosienneurone in die supraoptiese kerne. Natuur (Londen) 313, 682-684. Tindall, JS, 1974. Stimuli wat die vrystelling van oksitosien veroorsaak. In: Geiger, SR, Knobil, E., Sawyer, WH, Greef, R., Astwood, EB (Eds.), Handboek van Fisiologie. Sekte. 7, Endokrinologie, vol. IV. American Physiology Society, Washington DC, pp. 257-267. Torres, G., Lee, S., Rivier, C., 1993. Ontogenie van die rat hipotalamien stikstofoksied sintase en kolokalisering met neuropeptides. Mol. Sel. Neurosci. 4, 155-163. Uhl-Bronner, S., Waltisperger, E., Martinez-Lorenzana, G., Condes, LM, Freund-Mercier, MJ, 2005. Seksueel dimorfe uitdrukking van oksitosien bindingsplekke in voorhoede en rugmurg van die rat. Neurowetenskap 135, 147-154. Vaccari, C., Lolait, SJ, Ostrowski, NL, 1998. Vergelykende verspreiding van vasopressien V1b en oksitosienreceptor messenger ribonukleïensure in die brein. Endokrinologie 139, 5015-5033. Van Den Pol, A., 1991. Glutamaat- en aspartaat-immunoreaktiwiteit in hipotalamiese presynaptiese aksone. J. Neurosci. 11, 2087-2101. Veronneau-Longueville, F., Rampin, O., Freund-Mercier, MJ, Tang, Y., Calas, A., Marson, L., McKenna, KE, Stoeckel, ME, Benoit, G., Giuliano, F. , 1999. Oksitokinergiese innervering van outonome kerne wat penile ereksie in die rat beheer. Neurowetenskap 93, 1437-1447. Vincent, SR, Kimura, H., 1992. Histochemiese kartering van stikstofoksied sintase in die rotbrein. Neurowetenskap 46, 755-784. Wagner, CK, Clemens, LG, 1993. Neurofisien-bevattende weg vanaf die paraventrikulêre kern van die hipotalamus na 'n seksueel-dimorfe motoriese kern in die rugmurg. J. Comp. Neurol. 336, 106-116. Winslow, JT, Insel, TR, 1991. Sosiale status in pare manlike eekhorings ape bepaal die gedragsreaksie op sentrale oksitosienadministrasie. J. Neurosci. 11, 2032-2038. Wyslik, RA, Rompre, P.-P., 1989. Brein dopamien en beloning. Ann. Op Psychol. 40, 191-225. Witt, DM, Insel, TR, 1994. Manlike seksuele gedrag aktiveer c-fos-agtige proteïene in oksitosienneurone in die paraventrikulêre kern van die hipotalamus. J. Neuroendocrinol. 6, 13-18. Witter, MP, 2006. Verbindings van die subikulum van die rot: topografie in verhouding tot kolomme en laminêre organisasie. Behav Brain Res. 174, 251-264. Woodruff, GN, Foster, AC, Gill, R., Kemp, JA, Wong, EH, Iversen, LL, 1987. Die interaksie tussen MK-801 en reseptore vir N-metiel-d-aspartaat: funksionele gevolge. Neurofarmakologie 26, 903-909. Yamashita, H., Shigeru, O., Inenaga, K., Kasai, M., Uesugi, S., Kannan, H., Kaneko, T., 1987. Oksitosien verwek oorwegend veronderstelende oksitosienneurone in die rat supraoptiese kern in vitro. Brein Res. 416, 364-368. Skree, DP, Hendricks, SE, Prendergast, MA, 1992. Lesies van die kernparagigantocellularis: effekte op paringsgedrag by manlike rotte. Brein Res. 596, 73-79. Young, WS, Shepard, E., Amico, J., Hennighausen, L., LaMarca, ME, McKinney, C., Ginns, EI, 1996. Tekort aan muis oksitosien verhoed melkuitwerping, maar nie vrugbaarheid of bevalling nie. J. Neuroendocrinol. 8, 847-854. Zahran, AR, Vachon, P., Courtois, F., Carrier, S., 2000. Toenames in intrakavernous penile druk na inspuitings van eksitatoriese aminosuurreseptoragoniste in die hipotalamiese paraventrikulêre kern van verdovende rotte. J. Urol.