Přední. Psychiatrie, 25 únor 2016 | http://dx.doi.org/10.3389/fpsyt.2016.00024
Jaride Goodmane a Mark G. Packard*
- Department of Psychology, Texas A&M Institute for Neuroscience, Texas A&M University, College Station, TX, USA
Názor, že anatomicky odlišné paměťové systémy odlišně přispívají k rozvoji drogové závislosti a relapsu, získal rozsáhlou podporu. Tato stručná zpráva se vrací k této hypotéze, protože byla původně navržena před 20 lety (1) a zdůrazňuje několik nedávných událostí. Rozsáhlý výzkum využívající různé paradigmata učení na zvířatech ukazuje, že oddělitelné neurální systémy zprostředkovávají odlišné typy učení a paměti. Každý paměťový systém potenciálně přispívá jedinečnými složkami k naučenému chování podporujícímu závislost na drogách a relapsu. Zejména přechod od rekreačního užívání drog k nutkavému užívání drog může odrážet neuroanatomický posun od kognitivního řízení chování zprostředkovaného hipokampem / dorsomediální striatum směrem k obvyklé kontrole chování zprostředkované dorsolaterálním striatem (DLS). Kromě toho stres / úzkost mohou představovat kofaktor, který usnadňuje paměť závislou na DLS, a to může sloužit jako neurobehaviorální mechanismus, který je základem zvýšeného užívání drog a recidivy u lidí po stresových životních událostech. Důkazy podporující systémový pohled na závislost na drogách pocházejí převážně ze studií učení a paměti, které využívají jako posilovače návykových látek, které jsou často zvažovány v kontextu výzkumu drogové závislosti, včetně kokainu, alkoholu a amfetaminů. Nedávné důkazy navíc naznačují, že přístup k paměťovým systémům může být také užitečný pro pochopení aktuálních zdrojů závislosti, které odrážejí nové zdravotní problémy, včetně užívání marihuany, diety s vysokým obsahem tuku a hraní videoher.
Úvod
Vyšetřovatelé se často dívají na mechanismy učení a chování, aby vysvětlili, jak je lidská psychopatologie získávána a vyjadřována. Příklad takové aplikace poskytl Norman M. White, který použil principy klasické teorie učení a experimentálních důkazů podporujících existenci více paměťových systémů v mozku, aby poskytl nový, vlivný přístup k drogové závislosti (1). Konkrétně White uvedl, že drogy mohou hrát roli „zesilovačů“, které, podobně jako jídlo nebo voda, ve vzdělávacím úkolu, posilují asociace mezi stimuly souvisejícími s drogami, kontextem a chováním na podporu užívání drog a postupem času závislost. Bílý také zahrnoval vznikající hypotézu, že existují různé typy paměti, které jsou zprostředkovány disociovatelnými neuronovými systémy. Podle tohoto nového pohledu mohou léky přímo modulovat více nervových systémů a tyto nervové systémy jdou na kódovat odlišné složky paměti související s drogami, které, když jsou exprimovány, podporují další užívání drog.
V roce 2016 označuje 20th výročí více paměťových systémů pohled na drogové závislosti, jak popisuje White. Současná revize přehodnocuje tuto vlivnou hypotézu a zároveň vyzdvihuje některé důležité nedávné události, které nejen zdůvodnily původní hypotézu, ale také vytvořily další pohled na to, jak systémy s více paměti potenciálně podporují drogovou závislost.
Zobrazení více závislých systémů paměti
Konvergující důkazy ze studií využívajících lidi a nižší zvířata ukazují, že paměť savců je zprostředkována relativně nezávislými neurálními systémy [recenze, viz Ref. (2-4)]. Časné experimenty disociující více paměťových systémů byly primárně prováděny v radiálním bludišti a ukázaly jedinečné mnemonické funkce pro hipokampus, dorzální striatum a amygdalu (5, 6). Hipokampus zprostředkovává kognitivní / prostorovou formu paměti, zatímco dorzální striatum zprostředkovává paměť vzruchu - odezvy (S – R). Amygdala zprostředkovává Pavloviánské a stimulační a asociativní vztahy (6, 7), a zároveň podporuje modulační úlohu emocionálního vzrušení na jiných typech paměti (8-12).
V kontextu vícenásobného systémového pohledu na paměť, bílá (1) navrhl, že hipokampus, dorzální striatum a amygdala kódují jedinečné složky vzpomínek souvisejících s léky (viz obrázek 1). Hippokampus kóduje explicitní znalosti vztahující se ke vztahu mezi narážkami a událostmi (tj. Asociace stimulačních stimulů) v kontextu drog. Důležité je, že hipokampus nekóduje behaviorální odezvy, ale informace získané hipokampem mohou být použity pro generování vhodných reakcí na chování, aby se dostalo zesílení léčiva. Na druhé straně dorzální striatum kóduje asociace mezi stimuly souvisejícími s drogami a reakcemi na chování. To může umožnit prezentaci podnětu souvisejícího s drogami pro aktivaci automatické odezvy na chování, která má za následek užívání drog (např. Běžící přiblížení nebo nástrojový pákový lis). Amygdala kóduje Pavlovian-asociativní vztahy, což umožňuje neutrální narážky v kontextu drog, aby se staly spojeny s odměnou za léky. Zvířata později reagují na tyto podmíněné podněty podobně, jako původně reagovaly na léčivo. Podmíněné podněty aktivizují podmíněné emocionální reakce, včetně vnitřních afektivních stavů a podmíněného přístupu k podmíněnému podnětu (nebo v některých případech k vyhýbání se). Další kritickou složkou Bílé hypotézy je, že léky mohou modulovat paměťovou funkci každé z těchto oblastí mozku. Léky tak mohou potenciálně posílit svou vlastní samosprávu prostřednictvím posílení konsolidace vzpomínek souvisejících s léky kódovaných hipokampem, amygdala a dorzálním striatem (viz obrázek 1).
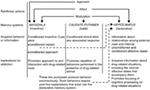
Obrázek 1. Bílé (1vícečetné paměťové systémy pohled na drogovou závislost. Stejně jako přírodní posilovače mají návykové léky několik „posilovacích akcí“, včetně schopnosti vyvolat pozitivní / negativní vliv, přístupu a modulace paměťových systémů. Amygdala, caudate-putamen (tj. Hřbetní striatum) a hipokampus zprostředkovávají disociální paměťové systémy a každý paměťový systém pravděpodobně kóduje jedinečné komponenty pamětí souvisejících s drogami. Vzhledem k jejich modulačním vlastnostem v paměti mohou návykové léky potenciálně zlepšit jejich vlastní správu zvýšením funkce těchto systémů. (Přetištěno od Whitea se svolením John Wiley & Sons.)
V souladu s pohledem na závislost na drogách s více paměťovými systémy, rozsáhlé důkazy naznačují kritické role pro hipokampus, dorzální striatum a amygdalu v závislosti na drogách a relapsy u různých zneužívaných látek [viz přehled Ref. (13)]. Zdá se, že dorzální hipokampus hraje roli v kontextuální kontrole hledání drog pro kokain (14-16). Boční oblast dorzálního striata (DLS) zprostředkovává S – R obvyklý pákový tlak pro kokain a alkohol (17, 18), a basolaterální amygdala (BLA) zprostředkovává podmíněné hledání drog pro kokain, alkohol a heroin (19-22). Také shodovat se s Whiteovou hypotézou, látky zneužívání mohou modulovat mnemonic funkce hippocampus, hřbetní striatum, a amygdala (\ t23-31).
Nedávné studie přispěly k novým změnám v přístupu k systémovým drogovým závislostem. Klíčové rysy tohoto současného pohledu zahrnují (1) neuroanatomický posun v čase k DLS-závislý paměť paměti, (2) kompetitivní interakce mezi paměťovými systémy, (3) role stresu a úzkosti ve zvyšování obvyklého hledání drogy, a (4) uplatnění této hypotézy na nově vznikající zdroje závislosti.
Neuroanatomický posun od poznání k zvyku
V experimentálních situacích učení subjekty obvykle používají účelné chování, když zpočátku řeší úkol. Po rozsáhlém výcviku se však chování stává autonomním a může být prováděno s malou pozorností, záměrem nebo kognitivním úsilím, což představuje „zvyk“ [pro přezkoumání viz Ref. (32)]. V časných demonstracích tohoto posunu od kognitivního řízení chování ke zvyku byli hlodavci trénováni za použití odměny za jídlo ve dvojitém řešení plus bludiště úkolu (33-35). V tomto úkolu byli potkani propuštěni ze stejné výchozí pozice (např. Z jižního ramene) a museli udělat konzistentní otočení těla na křižovatce bludiště, aby dostávali potravinovou odměnu vždy umístěnou ve stejném brankovišti (např. Vždy udělali levici). v západním rameni). Potkani by mohli tento úkol vyřešit buď učením konzistentní odezvy těla, nebo jakoukoliv reakcí nezbytnou k tomu, aby šli do stejné prostorové polohy. K určení, kterou strategii krysy použili, provedli vyšetřovatelé sondový test, ve kterém byla zvířata uvolněna z opačného startovacího ramene (např. Severní rameno). Jestliže zvířata udělala opačné tělo-otočení jít originální umístění cíle, oni byli poznáni jako studenti místa. Pokud zvířata udělala to samé otočení těla jako při tréninku (tj. Jdoucí k rameni naproti původnímu cílovému umístění), zvířata byla identifikována jako žáci odpovědí. Důkazy naznačují, že po nějakém tréninku většina zvířat vykazuje učení na místě, zatímco po rozsáhlém školení přecházejí zvířata na učení obvyklé reakce (34-36). Je zajímavé, že tento posun od učení se místu k učení učení může odrážet neuroanatomický posun. Počáteční využití místního učení v tomto úkolu je zprostředkováno hipokampem a dorsomediální striatum [DMS (36, 37)], zatímco využití odezvového učení po prodlouženém vzdělávání je zprostředkováno DLS (36).
Kromě předčasných demonstrací pomocí plus-bludiště (34, 35), posun chování k paměti zvyku byl později demonstrován pomocí operativních pákových lisovacích paradigmat (38-42). V těchto instrumentálních učebních úkolech zvířata zpočátku účelně stisknou, aby dosáhla výsledku, a poté, co dojde k devalvaci potravinového výsledku, přestanou tlačit páky. Po rozsáhlých tréninkových zvířatech však dojde k přechodu na obvyklou reakci a bude pokračovat v stisknutí páky i po devalvaci výsledku potravy (40). Jak bylo původně prokázáno v bludisku plus (36), přechod od poznání k návyku v úlohách instrumentálního učení může být také přičítán neuroanatomickému posunu. Počáteční kognitivní kontrola chování v těchto instrumentálních učebních úlohách je zprostředkována hipokampem a DMS (43, 44), zatímco pozdější obvyklá reakce je zprostředkována DLS (18, 45, 46).
Četné vyšetřovatelé navrhli, že neuroanatomický posun k paměti zvyku demonstrovaný v bludišti a nástrojových učebních úlohách by také mohl být základem přechodu od rekreačního užívání drog k nutkavému zneužívání drog (13, 47-50). V souladu s touto hypotézou vyšetřovatelé prokázali pro řadu zneužitých látek, že DMS zprostředkovává cílené reakce na zesílení drog a DLS zprostředkovává obvyklou reakci na posílení drog (18, 31, 51-53).
Vzhledem k vysokému potenciálu zneužití některých léků navrhovatelé navrhli, že návykové léky mohou zvýšit funkci paměti závislé na DLS a tím urychlit přechod od kognitivních k obvyklým kontrolám chování. V souladu s touto hypotézou opakovaná expozice amfetaminu nebo kokainu usnadňuje přechod z cílené na obvyklou reakci na posílení potravy v instrumentálních pákových lisovacích úkolech (31, 54-59). Kromě toho, pákový tlak na návykové látky (např. Alkohol nebo kokain) versus odměna za potraviny je spojován s větší obvyklou reakcí versus cílené reakce (24, 60, 61). U lidí vykazují osoby závislé na alkoholu větší obvyklou odezvu v úloze instrumentálního učení vzhledem k jednotlivcům, kteří nejsou závislí na kontrole (62). Toto vylepšení paměti závislé na DLS návykovými léky bylo také pozorováno v úlohách učení hlodavců hlodavců. Expozice kokainu, amfetaminu a alkoholu byla spojena se zvýšeným učením v bludných úkolech závislých na DLS nebo s větším využíváním strategií odpovědí závislých na DLS ve verzích dvojitého řešení bludiště (25, 63, 64). U lidí, použití zneužívaných látek, včetně alkoholu a tabáku, byl korelovaný s větším použitím dorsal striatum-závislé navigační strategie ve virtuálním bludišti (\ t65). Některé drogy zneužívání by tedy mohly zvýšit paměť závislou na DLS a toto zvýšené zapojení paměťového systému DLS by mohlo urychlit přechod z rekreačního užívání drog na obvyklé užívání drog. Tento navrhovaný mechanismus je v souladu s \ t1) původní tvrzení, že drogy zneužívání mohou někdy usnadnit jejich vlastní samosprávu tím, že zlepší funkci paměťových systémů.
Konkurence mezi paměťovými systémy
I když je možné, že návykové léky zvyšují paměť návyku přímo zlepšením funkce DLS [např. Ref. (29)], další možností je, že drogy zneužívání zvyšují návykové návyky nepřímo prostřednictvím modulace jiných paměťových systémů. Tento alternativní mechanismus se dovolává hypotézy, že v některých situacích učení systémy paměti soutěží o kontrolu učení a že narušením funkce jednoho paměťového systému může být rozšířena funkce jiného neporušeného systému (11, 66). Pozoruhodně, hippocampus a DLS může někdy soutěžit o kontrolu učení, přičemž léze hipokampu zvyšuje DLS-dependentní paměťovou funkci (5, 6, 67, 68). Konkurenční interakce mohou být také demonstrovány v úlohách s duálním řešením, kdy poškození jednoho paměťového systému má za následek využití strategie zprostředkované jiným neporušeným systémem. Například zvířata, kterým byla podána DMS léze, vykazují obvyklou reakci závislou na DLS pro odměnu za jídlo v instrumentálních učebních úkolech (44).
S ohledem na konkurenční interakce, které někdy vznikají mezi paměťovými systémy, je jednou z možností, že některé léky zneužívání by mohly nepřímo zvyšovat paměť závislou na DLS, a to narušením kognitivních paměťových mechanismů zprostředkovaných DMS a hippocampem. Jak již bylo zmíněno dříve, alkohol je spojen s větším využíváním paměti závislé na DLS v bludišti a operativních pákových lisovacích paradigmatech (24, 61, 62, 64, 65). Důkazy také naznačují, že alkohol narušuje učení v úlohách prostorové paměti závislých na hipokampu [(64, 69-72); viz rev. (73)], stejně jako v úlohách reverzního učení závislých na DMS (74-77). V souladu s konkurenční interakcí mezi paměťovými systémy se předpokládalo, že alkohol může usnadnit paměť závislou na DLS nepřímo prostřednictvím poškození mechanismů kognitivní paměti (78).
Je třeba poznamenat, že kromě alkoholu jsou četné léky spojeny s deficitem kognitivní paměti. Vystavení morfinu, heroinu, metamfetaminu, MDMA (extáze) nebo chronickému kokainu podobně způsobuje postižení prostorové paměti závislé na hipokampu napříč různými úkoly (79-89). Je lákavé spekulovat, že, jak bylo navrženo pro alkohol, poruchy kognitivní paměti způsobené návykovými drogami mohou nepřímo zvyšovat paměť závislou na DLS a že to může být jeden mechanismus, který umožní, aby se drogová samospráva stala obvyklou u lidí užívajících drogy. Na druhé straně je také možné, že se prostorové poruchy učení způsobené návykovými látkami mohou vyskytovat nepřímo prostřednictvím zlepšení paměťových procesů závislých na DLS. V souladu s touto hypotézou stimuluje aktivita CREB v DLS prostorovou paměť závislou na hipokampu (90), zatímco inhibice aktivity CREB v DLS zvrátí poruchy prostorové paměti produkované morfinem (91).
Role stresu a úzkosti
Další úvaha týkající se přístupu vícečetných paměťových systémů k drogové závislosti je úlohou stresu. Konvergující důkazy naznačují, že silné emocionální vzrušení usnadňuje paměť závislou na DLS u hlodavců a lidí [viz recenze Ref. (9-12)]. Podávání anxiogenních léčiv zvyšuje učení závislé na DLS ve vodě plus bludiště (92-97). Toto zvýšení paměti závislé na DLS je také pozorováno po vystavení nepodmíněným behaviorálním stresorům [např. Chronické omezení, ocasní šok, pach dravců atd. (98-101)] a vystavení se strachem podmíněným podnětům [tón dříve spárovaný s šokem (102, 103)]. Ačkoli byl původně prokázán u hlodavců (92), toto zvýšení paměti zvyku vyvolané silným emocionálním vzrušením bylo také rozsáhle prokázáno u lidí (99, 104-110).
Mechanismy umožňující stres / úzkost usnadňující paměť zvyků zůstávají do značné míry neznámé; důkazy však ukazují kritickou modulační úlohu BLA (93-95, 100). V souladu s konkurenční interakcí mezi paměťovými systémy, některé důkazy také naznačují, že stres / úzkost může zvýšit paměť závislou na DLS závislost nepřímo narušením funkce hipokampu (94, 95).
Zlepšení paměti návyku po stresu nebo úzkosti může být důležité pro pochopení některých významných faktorů vedoucích ke zneužívání drog. Zejména stresové životní události nebo chronické prodloužené doby stresu / úzkosti jsou spojeny se zvýšenou zranitelností vůči drogové závislosti a relapsem u lidí (111-117), a podobná pozorování byla prováděna na zvířecích modelech samopodávání léčiv [pro přezkoumání viz Ref. (118)]. Vyšetřovatelé navrhli, že je konzistentní s vlivem emocionálního vzrušení na více paměťových systémech (10) akutní nebo chronický stres může zvýšit závislost na drogách a recidivu u lidí zapojením procesů paměťové závislosti závislých na DLS (9, 49, 119). V souladu s tímto návrhem je stres u jedinců závislých na kokainu spojen se sníženou aktivitou závislou na hladině kyslíku (BOLD) v hipokampu a se zvýšenou aktivitou v dorzálním striatu a tyto změny aktivity BOLD jsou spojeny se stresem vyvolanou chutí kokainu. (120).
Rozvíjející se zdroje závislosti
Kromě drog zneužívání, hypotéza více paměťových systémů byla také nedávno použita pro pochopení dalších vznikajících zdrojů závislosti. Například vzestup obezity v posledních několika desetiletích vedl ke srovnatelnému nárůstu experimentálního zájmu, kdy mnoho výzkumníků čerpalo paralely mezi závislostí na drogách a přejídáním [pro přezkoumání viz Ref. (121-123)]. Některé nedávné důkazy naznačují, že podobně jako drogová závislost může být závislost na potravinách částečně způsobena zvýšeným zapojením paměti závislé na DLS. U potkanů umožňuje spotřeba potravy podobná flámům přechod od kognitivních k obvyklým kontrolám chování (124, 125). Kromě toho je obvyklé chování u zvířat s falešnými účinky spojeno se zvýšenou aktivitou DLS a může být zabráněno blokováním receptorů AMPA nebo dopaminu D1 v DLS (125). Obezita vyvolaná dietou byla také v nedávné době spojena s použitím paměti zvyků v úkolu Y-bludiště (126).
Další objevující se porucha chování, která je v souladu s některými rysy drogové závislosti, je patologické hraní videohry nebo závislost na videohře [pro přezkoumání viz Ref. (127)]. Podobně jako drogová závislost, dlouhodobé nadměrné hraní videohry bylo spojeno se sníženou vazbou na dopaminový receptor D2 v dorzálním striatu (128). Hraní videogame také souvisí se zvýšenou aktivací dorzálního striata (129, 130) a větší objemy hřbetních striatálních předpovědí ukazují vyšší úroveň dovedností videohry (131). Lidé, kteří pravidelně hrají akční videohry, mají větší pravděpodobnost, že budou ve virtuálním bludišti používat paměť závislou na hřbetním striatu (132), a předškolní videohry vedou k obvyklé reakci na cílené reakce v dvoustupňovém rozhodovacím úkolu (133). Tak, jak navrhoval pro drogy zneužívání, hraní videoher by mohlo zlepšit závislost videohry přes zapojení DLS-závislý systém paměti paměti.
Konečně, přístup k systémům s více paměti může být také užitečný pro pochopení závislosti na marihuaně. Ačkoli marihuana může mít nižší potenciál zneužívání než jiné nelegální látky klasicky uvažované v kontextu výzkumu drogových závislostí (např. Kokain, morfin, heroin atd.), Těžké užívání konopí může přesto podporovat závislost na drogách a abstinenční příznaky pozorované u jiných drog zneužití (134-137). Nedávno bylo navrženo, že závislost na marihuaně může být částečně způsobena zvýšeným zapojením paměti závislé na DLS (138). Vzhledem k tomu, že akutní expozice kanabinoidů zhoršuje paměťovou funkci závislou na DLS (139, 140), opakovaná expozice kanabinoidu vede k větší obvyklé reakci závislé na DLS v úloze instrumentálního učení (141). Silní uživatelé konopí navíc vykazují větší aktivaci dorzálního striata ve srovnání s neuživateli při provádění verze implicitní asociační úlohy marihuany (142), a účastníci s anamnézou užívání konopí častěji používají virtuální paměť závislou na hřbetním striatu ve virtuálním bludišti (65).
Vzhledem k úspěšné aplikaci přístupu paměťových systémů k nově vznikajícím zdrojům závislosti je rozumné předpokládat, že systémy s více paměti mohou být také zapojeny do jiných patologických jevů spojených se závislostí, jako je nutkavé nakupování, závislost na internetu a závislost na sexu. Skutečnost, zda přístup založený na paměťových systémech může být užitečný pro pochopení patologického hráčství, také získal určitou pozornost (143, 144).
Proč investovat do čističky vzduchu?
Dvacet let experimentálních důkazů do značné míry potvrdilo Whiteovy (1vícečetné paměťové systémy přístup k drogové závislosti. Důkazy naznačují, že hipokampus zprostředkovává kontextovou kontrolu užívání drog, DLS zprostředkovává obvyklou reakci S-R na zesílení léků a amygdala zprostředkovává podmíněné hledání léčiv. Následný výzkum navíc vedl k dalším poznatkům o pohledu na závislost na drogách s více paměťovými systémy, včetně přechodu na paměť zvyklostí, konkurence mezi paměťovými systémy a role stresu a úzkosti.
Budoucí výzkum by se měl pokusit o integraci přístupu paměťových systémů s dalšími teoriemi závislosti, jako jsou například motivační procesy soupeře (145). Bylo by také užitečné začlenit do paměťových systémů další znaky závislosti, jako je závislost na drogách, tolerance a abstinence. Ačkoliv se tento přehled převážně zaměřil na oblasti mozku původně uvažované Whiteem (tj. Hipokampus, dorzální striatum a amygdala), je třeba poznamenat, že další oblasti mozku související s učením a pamětí byly také kriticky zapojeny do drogové závislosti a relapsu. , včetně mediálního prefrontálního kortexu a nucleus accumbens [viz přehled Ref. (13)]. Konečně, i když mimo rámec tohoto přehledu, je třeba uznat, že rozsáhlé důkazy naznačují, že buněčné a molekulární změny v dopaminergním systému středního mozku také přispívají k závislosti (146).
Ačkoliv může být obtížné kontrolovat zvyky v paměti, některé důkazy naznačují, že paměť, závislá na DLS, může být za určitých okolností potlačena (147) nebo dokonce obrácené (148, 149). Je tedy možné, že farmakologické manipulace a behaviorální postupy vedoucí ke zvratu nebo potlačení paměťové návyky na zvířecích modelech učení mohou být potenciálně uzpůsobeny k léčbě drogové závislosti a relapsu u lidí.
Autorské příspěvky
JG a MP oba přispěli nápady a psaní současného mini-recenze.
Prohlášení o konfliktu zájmů
Autoři prohlašují, že výzkum byl proveden bez obchodních či finančních vztahů, které by mohly být považovány za potenciální střet zájmů.
Reference
1. Bílá NM. Návykové léky jako zesilovače: více dílčích akcí na paměťových systémech. Závislost (1996) 91(7):921–50. doi: 10.1111/j.1360-0443.1996.tb03586.x
2. White NM, McDonald RJ. Mnohočetné paralelní paměťové systémy v mozku krysy. Neurobiol Learn Mem (2002) 77(2):125–84. doi:10.1006/nlme.2001.4008
3. Squire LR. Paměťové systémy mozku: stručná historie a současná perspektiva. Neurobiol Learn Mem (2004) 82(3):171–7. doi:10.1016/j.nlm.2004.06.005
4. White NM, Packard MG, McDonald RJ. Disociace paměťových systémů: příběh se odvíjí. Behav Neurosci (2013) 127(6):813–34. doi:10.1037/a0034859
5. Packard MG, Hirsh R, bílá NM. Diferenciální účinky lézí fornixu a caudate nucleus na dva radiální úlohy: důkaz pro více paměťových systémů. J Neurosci (1989) 9(5): 1465-72.
6. McDonald RJ, White NM. Trojitá disociace paměťových systémů: hippocampus, amygdala a dorsální striatum. Behav Neurosci (1993) 107(1):3–22. doi:10.1037/0735-7044.107.1.3
7. Maren S. Neurobiology z Pavlovian strach předurčení. Annu Rev Neurosci (2001) 24(1):897–931. doi:10.1146/annurev.neuro.24.1.897
8. McGaugh JL. Amygdala moduluje konsolidaci vzpomínek na emocionálně vzrušující zážitky. Annu Rev Neurosci (2004) 27: 1 – 28. doi: 10.1146 / annurev.neuro.27.070203.144157
9. Packard MG. Úzkost, poznání a zvyk: perspektiva více systémů paměti. Brain Res (2009) 1293: 121 – 8. doi: 10.1016 / j.brainres.2009.03.029
10. Packard MG, Goodman J. Emoční vzrušení a mnohočetné paměťové systémy v mozku savců. Přední Behav Neurosci (2012) 6: 14. doi: 10.3389 / fnbeh.2012.00014
11. Packard MG, Goodman J. Faktory, které ovlivňují relativní použití více paměťových systémů. Hippocampus (2013) 23(11):1044–52. doi:10.1002/hipo.22178
12. Schwabe L. Stres a zapojení více paměťových systémů: integrace studií na zvířatech a člověka. Hippocampus (2013) 23(11):1035–43. doi:10.1002/hipo.22175
13. Everitt BJ, Robbins TW. Neuronové systémy posilování drogové závislosti: od akcí k návykům. Nat Neurosci (2005) 8(11):1481–9. doi:10.1038/nn1579
14. Fuchs RA, Evans KA, Ledford CC, Parker MP, Case JM, Mehta RH, et al. Úloha dorsomediálního prefrontálního kortexu, basolaterální amygdaly a dorzálního hipokampu v kontextuálním návratu kokainového vyhledávání u potkanů. Neuropsychopharmacology (2005) 30(2):296–309. doi:10.1038/sj.npp.1300579
15. Fuchs RA, Eaddy JL, Su ZI, Bell GH. Interakce basolaterální amygdaly s dorzálním hipokampem a dorsomediálním prefrontálním kortexem regulují navrácení kokainu u potkanů v souvislosti s drogami. Eur J Neurosci (2007) 26(2):487–98. doi:10.1111/j.1460-9568.2007.05674.x
16. Kramar CP, Barbano MF, Medina JH. Dopaminové receptory D1 / D5 v dorzálním hipokampu jsou potřebné pro získání a expresi paměti spojené s kokainem v jedné studii. Neurobiol Learn Mem (2014) 116: 172 – 80. doi: 10.1016 / j.nlm.2014.10.004
17. Zapata A, Minney VL, Shippenberg TS. Přechod od cíleného k obvyklému hledání kokainu po dlouhodobých zkušenostech u potkanů. J Neurosci (2010) 30(46):15457–63. doi:10.1523/JNEUROSCI.4072-10.2010
18. Corbit LH, Nie H, Janak PH. Obvyklé hledání alkoholu: časový průběh a přínos subregionů hřbetního striata. Biol Psychiatry (2012) 72(5):389–95. doi:10.1016/j.biopsych.2012.02.024
19. Whitelaw RB, Markou A, Robbins TW, Everitt BJ. Excitotoxické léze basolaterální amygdaly narušují získání kokainového chování v rámci programu posilování druhého řádu. Psychofarmakologie (1996) 127(1–2):213–24. doi:10.1007/BF02805996
20. Alderson HL, Robbins TW, Everitt BJ. Účinky excitotoxických lézí basolaterální amygdaly na získávání chování hledajícího heroin u potkanů. Psychofarmakologie (2000) 153(1):111–9. doi:10.1007/s002130000527
21. Gabriele A, viz RE. Reverzibilní inaktivace basolaterální amygdaly, nikoli však dorsolaterální kaudát putamen, zmírňuje konsolidaci asociativního učení kokain-cue v modelu navrácení drogy. Eur J Neurosci (2010) 32(6):1024–9. doi:10.1111/j.1460-9568.2010.07394.x
22. Sciascia JM, Reese RM, Janak PH, Chaudhri N. Hledání alkoholu vyvolané diskrétními pavlovskými narážkami je povzbuzeno alkoholovým kontextem a zprostředkováno glutamátovou signalizací v basolaterální amygdale. Neuropsychopharmacology (2015) 40: 2801 – 12. doi: 10.1038 / npp.2015.130
23. Packard MG, Teather LA. Amygdala modulace více paměťových systémů: hippocampus a caudate-putamen. Neurobiol Learn Mem (1998) 69(2):163–203. doi:10.1006/nlme.1997.3815
24. Dickinson A, Wood N, Smith JW. Hledání alkoholu u potkanů: akce nebo zvyk? QJ Exp Psychol B (2002) 55(4):331–48. doi:10.1080/0272499024400016
25. Udo T, Ugalde F, DiPietro N, Eichenbaum HB, Kantak KM. Účinky perzistentní kokainové aplikace na amygdala-dependentní a dorzální striatum závislé učení u potkanů. Psychofarmakologie (2004) 174(2):237–45. doi:10.1007/s00213-003-1734-1
26. Wood SC, Fay J, Sage JR, Anagnostaras SG. Kokain a Pavlovian strach kondicionování: analýza dávka-účinek. Behav Brain Res (2007) 176(2):244–50. doi:10.1016/j.bbr.2006.10.008
27. Dřevo SC, Anagnostaras SG. Paměť a psychostimulancia: modulace Pavlovianovy strachové kondice amfetaminem u myší C57BL / 6. Psychofarmakologie (2009) 202(1–3):197–206. doi:10.1007/s00213-008-1185-9
28. Iñiguez SD, Charntikov S., Baella SA, Herbert MS, Bolaños-Guzmán CA, Crawford CA. Expozice kokainu po tréninku usnadňuje konsolidaci prostorové paměti u myší C57BL / 6. Hippocampus (2012) 22(4):802–13. doi:10.1002/hipo.20941
29. DePoy L, Daut R, Brigman JL, MacPherson K, Crowley N, Gunduz-Cinar O, et al. Chronický alkohol produkuje neuroadaptace k prvotnímu dorzálnímu striatálnímu učení. Proc Natl Acad Sci USA (2013) 110(36):14783–8. doi:10.1073/pnas.1308198110
30. Leri F, Nahas E, Henderson K, Limebeer CL, Parker LA, White NM. Účinky post-tréninkového heroinu a d-amfetaminu na konsolidaci učení a udržení strachu. J Psychopharmacol (2013) 27(3):292–301. doi:10.1177/0269881112472566
31. Schmitzer-Torbert N, Apostolidis S, Amoa R, O'Rear C, Kaster M, Stowers J a kol. Podávání kokainu po tréninku usnadňuje učení a vyžaduje infralimbický kortex a dorsolaterální striatum. Neurobiol Learn Mem (2015) 118: 105 – 12. doi: 10.1016 / j.nlm.2014.11.007
32. Knowlton BJ. Bazální ganglia: tvorba zvyků. V: Jaeger D, Jung R, redaktoři. Encyklopedie výpočetních neurověd. New York: Springer (2014). str. 1 – 17.
33. Tolman EC, Ritchie BF, Kalish D. Studie v prostorovém učení. IV. Přenos místního učení na jiné výchozí cesty. J Exp Psychol (1947) 37(1):39–47. doi:10.1037/h0062061
34. Ritchie BF, Aeschliman B, Pierce P. Studie v prostorovém učení. VIII. Místo výkonu a získání místa dispozice. J Comp Physiol Psychol (1950) 43(2):73–85. doi:10.1037/h0055224
35. Hicks LH. Vliv přetrénování na získání a zvrat učení místa a reakce. Psychol Rep (1964) 15(2):459–62. doi:10.2466/pr0.1964.15.2.459
36. Packard MG, McGaugh JL. Inaktivace hippocampu nebo caudate jádra lidokainem odlišně ovlivňuje expresi místa a učení se odezvy. Neurobiol Learn Mem (1996) 65(1):65–72. doi:10.1006/nlme.1996.0007
37. Yin HH, Knowlton BJ. Příspěvky striatálních subregionů k učení místa a reakce. Naučte se Mem (2004) 11(4):459–63. doi:10.1101/lm.81004
38. Adams CD, Dickinson A. Instrumentální reakce po zesílení zesilovače. QJ Exp Psychol (1981) 33B: 109-12. dva: 10.1080 / 14640748108400816
39. Adams CD, Dickinson A. Akce a zvyky: variace v asociativních reprezentacích během instrumentálního učení. V: Spear NE, Miller RR, redaktoři. Zpracování informací ve zvířatech: Mechanismy paměti. Hillsdale, NJ: Erlbaum (1981). str. 143 – 65.
40. Adams CD. Variace v citlivosti instrumentální reakce na devalvaci posilovače. QJ Exp Psychol (1982) 34B: 77-98. dva: 10.1080 / 14640748208400878
41. Dickinson A, Nicholas DJ. Nevýznamné pobídkové učení během instrumentální úpravy: úloha vazby zesilovače a odezvy zesilovače. QJ Exp Psychol (1983) 35B: 249-63. dva: 10.1080 / 14640748308400909
42. Dickinson A, Nicholas DJ, Adams CD. Účinky instrumentální podmíněnosti na náchylnost k devalvaci posilovače. QJ Exp Psychol (1983) 35B: 35-51. dva: 10.1080 / 14640748308400912
43. Corbit LH, Balleine BW. Úloha hippokampu v instrumentální kondici. J Neurosci (2000) 20(11): 4233-9.
44. Yin HH, Ostlund SB, Knowlton BJ, Balleine BW. Úloha dorsomediálního striata v instrumentální kondici. Eur J Neurosci (2005) 22:513–23. doi:10.1111/j.1460-9568.2005.04218.x
45. Yin HH, Knowlton BJ, Balleine BW. Léze dorsolaterálního striatu zachovávají očekávání výsledku, ale narušují tvorbu návyků v instrumentálním učení. Eur J Neurosci (2004) 19:181–9. doi:10.1111/j.1460-9568.2004.03095.x
46. Quinn JJ, Pittenger C, Lee AS, Pierson JL, Taylor JR. Návyky závislé na striatu jsou necitlivé jak na zvýšení, tak na snížení hodnoty zesílení u myší. Eur J Neurosci (2013) 37: 1012 – 21. doi: 10.1111 / ejn.12106
47. Jin HH. Od akcí ke zvyklostem: neuroadaptace vedoucí k závislosti. Alkohol Res Health (2008) 31(4): 340-4.
48. Belin D, Jonkman S, Dickinson A, Robbins TW, Everitt BJ. Paralelní a interaktivní procesy učení v bazálních gangliach: význam pro pochopení závislosti. Behav Brain Res (2009) 199(1):89–102. doi:10.1016/j.bbr.2008.09.027
49. Schwabe L, Dickinson A, Wolf OT. Stres, návyky a drogová závislost: psychoneuroendokrinologická perspektiva. Exp Clin Psychopharmacol (2011) 19(1):53–63. doi:10.1037/a0022212
50. Hogarth L, Balleine BW, Corbit LH, Killcross S. Mechanismy asociativního učení podporující přechod od rekreačního užívání drog k závislosti. Ann. NY Acad Sci (2013) 1282(1):12–24. doi:10.1111/j.1749-6632.2012.06768.x
51. Murray JE, Belin D, Everitt BJ. Dvojitá disociace dorsomediální a dorsolaterální striatální kontroly nad získáváním a výkonem při hledání kokainu. Neuropsychopharmacology (2012) 37(11):2456–66. doi:10.1038/npp.2012.104
52. Clemens KJ, Castino MR, Cornish JL, Goodchild AK, Holmes NM. Behaviorální a neurální substráty tvorby návyků u potkanů intravenózně podávajících nikotin. Neuropsychopharmacology (2014) 39: 2584 – 93. doi: 10.1038 / npp.2014.111
53. Corbit LH, Nie H, Janak PH. Obvyklá reakce na alkohol závisí na signalizaci AMPA a D2 receptoru v dorsolaterálním striatu. Přední Behav Neurosci (2014) 8: 301. doi: 10.3389 / fnbeh.2014.00301
54. Schoenbaum G, Setlow B. Kokain činí akce necitlivé na výsledky, ale ne zánik: důsledky pro změnu orbitofrontální funkce amygdalar. Cereb Cortex (2005) 15(8):1162–9. doi:10.1093/cercor/bhh216
55. Nelson A, Killcross S. Expozice amfetaminu zvyšuje tvorbu návyků. J Neurosci (2006) 26(14):3805–12. doi:10.1523/JNEUROSCI.4305-05.2006
56. Nordquist RE, Voorn P., De Mooij-van Malsen JG, Joosten RNJMA, Pennartz CMA, Vanderschuren LJMJ. Zvýšená hodnota zesílení a zrychlená tvorba návyku po opakované léčbě amfetaminem. Eur Neuropsychopharmacol (2007) 17(8):532–40. doi:10.1016/j.euroneuro.2006.12.005
57. LeBlanc KH, Maidment NT, Ostlund SB. Opakovaná expozice kokainu umožňuje vyjádření motivační motivace a navozuje obvyklou kontrolu u potkanů. PLoS One (2013) 8: e61355. doi: 10.1371 / journal.pone.0061355
58. Nelson AJ, Killcross S. Zrychlená tvorba návyku po expozici amfetaminu je reverzována přípravkem D1, ale zesílena antagonisty receptoru D2. Přední Neurosci (2013) 7: 76. doi: 10.3389 / fnins.2013.00076
59. Corbit LH, Chieng BC, Balleine BW. Účinky opakovaného vystavení kokainu na návykové učení a zvrat N-acetylcysteinem. Neuropsychopharmacology (2014) 39(8):1893–901. doi:10.1038/npp.2014.37
60. Miles FJ, Everitt BJ, Dickinson A. Orální vyhledávání kokainu u potkanů: akce nebo zvyk? Behav Neurosci (2003) 117(5):927–38. doi:10.1037/0735-7044.117.5.927
61. Mangieri RA, Cofresí RU, Gonzales RA. Hledání etanolu u krys Long Evans není vždy cílené chování. PLoS One (2012) 7: e42886. doi: 10.1371 / journal.pone.0042886
62. Sjoerds Z, De Wit S, Van Den Brink W, Robbins TW, Beekman ATF, Penninx BWJH, et al. Behaviorální a neuroimaging důkaz pro overreliance na zvyku učení u alkohol-závislý pacienti. Transl Psychiatrie (2013) 3(12): e337. doi: 10.1038 / tp.2013.107
63. Packard MG, McGaugh JL. Posttraining s podáváním chinpirolu a d-amfetaminu zlepšuje paměť na prostorové a cuedové diskriminaci ve vodním bludišti. Psychobiologie (1994) 22(1): 54-60.
64. Matthews DB, Ilgen M, White AM, Nejlepší PJ. Podávání akutního ethanolu zhoršuje prostorový výkon při současném usnadnění nonspatálního výkonu u potkanů. Neurobiol Learn Mem (1999) 72(3):169–79. doi:10.1006/nlme.1998.3900
65. Bohbot VD, Balso D, Conrad K, Konishi K, Leyton M. Navigační strategie závislé na jádru kyanátu jsou spojeny se zvýšeným užíváním návykových látek. Hippocampus (2013) 23(11):973–84. doi:10.1002/hipo.22187
66. Poldrack RA, Packard MG. Konkurence mezi systémy s více paměti: konvergence důkazů ze studií na zvířatech a lidském mozku. Neuropsychologia (2003) 41(3):245–51. doi:10.1016/S0028-3932(02)00157-4
67. Matthews DB, Best PJ. Léze fimbrie / fornix usnadňují učení se o úkolu nonspatial response. Psychon Bull Rev (1995) 2(1):113–6. doi:10.3758/BF03214415
68. Schroeder JP, Wingard JC, Packard MG. Post-tréninková reverzibilní inaktivace hippokampu odhaluje interference mezi paměťovými systémy. Hippocampus (2002) 12(2):280–4. doi:10.1002/hipo.10024
69. Matthews DB, Simson PE, Nejlepší PJ. Akutní ethanol narušuje prostorovou paměť, ale není stimulační / odezvová paměť u krysy. Alcohol Clin Exp. Res (1995) 19(4):902–9. doi:10.1111/j.1530-0277.1995.tb00965.x
70. White AM, Elek TM, Beltz TL, Nejlepší PJ. Prostorová výkonnost je citlivější na ethanol než nonspatial výkon bez ohledu na blízkost cue. Alcohol Clin Exp. Res (1998) 22(9):2102–7. doi:10.1111/j.1530-0277.1998.tb05922.x
71. Matthews DB, Morrow AL, Tokunaga S, McDaniel JR. Podávání akutního ethanolu a podávání akutního allopregnanolonu zhoršují prostorovou paměť při plnění Morrisovy vody. Alcohol Clin Exp. Res (2002) 26(11):1747–51. doi:10.1111/j.1530-0277.2002.tb02479.x
72. Berry RB, Matthews DB. Podávání akutního ethanolu selektivně narušuje prostorovou paměť u myší C57BL / 6J. Alkohol (2004) 32(1):9–18. doi:10.1016/j.alcohol.2003.09.005
73. Silvers JM, Tokunaga S, Berry RB, White AM, Matthews DB. Poruchy v prostorovém učení a paměti: ethanol, allopregnanolone a hippocampus. Brain Res Rev (2003) 43(3):275–84. doi:10.1016/j.brainresrev.2003.09.002
74. Badanich KA, Becker HC, Woodward JJ. Účinky chronické intermitentní expozice ethanolu na orbitofrontální a mediální prefrontální kortex-závislé chování u myší. Behav Neurosci (2011) 125(6):879–91. doi:10.1037/a0025922
75. Coleman LG Jr, He J, Lee J, Styner M, Crews FT. Dospívající binge pití mění dospělou mozkovou neurotransmitter genovou expresi, chování, mozkové regionální objemy a neurochemistry u myší. Alcohol Clin Exp. Res (2011) 35(4):671–88. doi:10.1111/j.1530-0277.2010.01385.x
76. Kuzmin A, Liljequist S, Meis J, Chefer V, Shippenberg T, Bakalkin G. Opakované mírné dávky ethanolových záchvatů zhoršují kognitivní funkce u krys Wistar. Addict Biol (2012) 17(1):132–40. doi:10.1111/j.1369-1600.2010.00224.x
77. Coleman LG, Liu W, Oguz I, Styner M, Posádky FT. Léčba ethanolu u dospívajících pacientů mění regionální objemy dospělých mozků, protein kortikální extracelulární matrix a flexibilitu chování. Pharmacol Biochem Behav (2014) 116: 142 – 51. doi: 10.1016 / j.pbb.2013.11.021
78. Matthews DB, Silvers JR. Využití akutního podání ethanolu jako nástroje pro zkoumání více paměťových systémů. Neurobiol Learn Mem (2004) 82(3):299–308. doi:10.1016/j.nlm.2004.06.007
79. Broening HW, Morford LL, Inman-Wood SL, Fukumura M, Vorhees CV. 3, 4-methylendioxymetamfetamin (extáze) indukované učení a poruchy paměti závisí na věku expozice během raného vývoje. J Neurosci (2001) 21(9): 3228-35.
80. Williams MT, Morford LL, Wood SL, Wallace TL, Fukumura M, Broening HW, et al. Vývojová léčba d-metamfetaminem selektivně indukuje poruchy prostorové navigace v referenční paměti ve vodním bludisku Morris, zatímco šetří pracovní paměť. Synapse (2003) 48(3):138–48. doi:10.1002/syn.10159
81. CV, Reed TM, Skelton MR, Williams MT. Expozice 3, 4-methylenedioxymetamfetaminu (MDMA) v postnatálních dnech 11-20 indukuje referenční, ale nikoli funkční paměťové deficity ve vodním bludisku Morris u potkanů: důsledky předchozího učení. Int J Dev Neurosci (2004) 22(5):247–59. doi:10.1016/j.ijdevneu.2004.06.003
82. Cohen MA, Skelton MR, Schaefer TL, Gudelsky GA, Vorhees CV, Williams MT. Učení a paměť po neonatální expozici 3, 4-methylendioxymetamfetaminu (extáze) u potkanů: interakce s expozicí v dospělosti. Synapse (2005) 57(3):148–59. doi:10.1002/syn.20166
83. Skelton MR, Williams MT, CV. Léčba pomocí MDMA z P11-20 narušuje prostorovou výuku a učení integrace cest u dospívajících potkanů, ale pouze prostorové učení u starších krys. Psychofarmakologie (2006) 189(3):307–18. doi:10.1007/s00213-006-0563-4
84. Ma MX, Chen YM, He J, Zeng T, Wang JH. Účinky morfinu a jeho stažení na prostorové rozpoznávací paměti Y-bludiště u myší. Neurovědy (2007) 147(4):1059–65. doi:10.1016/j.neuroscience.2007.05.020
85. Belcher AM, Feinstein EM, O'Dell SJ, Marshall JF. Metamfetamin ovlivňuje rozpoznávací paměť: srovnání eskalujících a jednodenních dávkovacích režimů. Neuropsychopharmacology (2008) 33(6):1453–63. doi:10.1038/sj.npp.1301510
86. Tramullas M, Martínez-Cué C, Hurlé MA. Chronické podávání heroinu myším vyvolává upregulaci proteinů souvisejících s apoptózou mozku a narušuje prostorové učení a paměť. Neurofarmakologie (2008) 54(4):640–52. doi:10.1016/j.neuropharm.2007.11.018
87. North A, Swant J, Salvatore MF, Gamble-George J, Prins P., Butler B a kol. Chronická expozice metamfetaminu způsobuje zpožděný, dlouhodobý paměťový deficit. Synapse (2013) 67(5):245–57. doi:10.1002/syn.21635
88. Fole A, Martin M, Morales L, Del Olmo N. Účinky chronické léčby kokainem během dospívání u krys Lewis a Fischer-344: nové poškození rozpoznávání polohy a změny synaptické plasticity v dospělosti. Neurobiol Learn Mem (2015) 123: 179 – 86. doi: 10.1016 / j.nlm.2015.06.001
89. Zhou M, Luo P, Lu Y, Li CJ, Wang DS, Lu Q a kol. Nerovnováha exprese HCN1 a HCN2 v oblasti hipokampálního CA1 narušuje prostorové učení a paměť u potkanů s chronickou expozicí morfinu. Prog Neuropsychopharmacol Biol Psychiatry (2015) 56: 207 – 14. doi: 10.1016 / j.pnpbp.2014.09.010
90. Kathirvelu B, Colombo PJ. Účinky exprese CREB zprostředkované lentivirem v dorsolaterálním striatu: vylepšení paměti a důkaz pro kompetitivní a kooperativní interakce s hippokampem. Hippocampus (2013) 23(11):1066–74. doi:10.1002/hipo.22188
91. Baudonnat M, Guillou JL, Husson M, Vandesquille M, Corio M., Decorte L, et al. Narušení účinku odměny vyvolané léčivem na prostorovou, ale ne cue-řízenou výuku: implikace striatální protein kinázy A / cAMP vazebné proteinové dráhy vazebného elementu. J Neurosci (2011) 31:16517–28. doi:10.1523/JNEUROSCI.1787-11.2011
92. Packard MG, Wingard JC. Amygdala a „emocionální“ modulace relativního využití více paměťových systémů. Neurobiol Learn Mem (2004) 82(3):243–52. doi:10.1016/j.nlm.2004.06.008
93. Elliott AE, Packard MG. Intra-amygdala anxiogenní infuze léčiva před vyhledáním zkreslí krysy směrem k použití paměti habitu. Neurobiol Learn Mem (2008) 90(4):616–23. doi:10.1016/j.nlm.2008.06.012
94. Wingard JC, Packard MG. Amygdala a emocionální modulace konkurence mezi kognitivní a návykovou pamětí. Behav Brain Res (2008) 193(1):126–31. doi:10.1016/j.bbr.2008.05.002
95. Packard MG, Gabriele A. Periferní anxiogenní injekce léků odlišně ovlivňují kognitivní a habitativní paměť: role basolaterální amygdaly. Neurovědy (2009) 164(2):457–62. doi:10.1016/j.neuroscience.2009.07.054
96. Leong KC, Goodman J, Packard MG. Buspiron blokuje zesilující účinek anxiogenního léku RS 79948-197 na konsolidaci paměti habitu. Behav Brain Res (2012) 234(2):299–302. doi:10.1016/j.bbr.2012.07.009
97. Goodman J, Leong KC, Packard MG. Zvýšení glukózové závislosti na dorsolaterální striatu závisí na současném noradrenergním účinku. Neurovědy (2015) 311: 1 – 8. doi: 10.1016 / j.neuroscience.2015.10.014
98. Kim JJ, Lee HJ, Han JS, Packard MG. Amygdala je rozhodující pro modulaci hippokampální dlouhodobé potenciace a učení vyvolané stresem. J Neurosci (2001) 21(14): 5222-8.
99. Schwabe L, Dalm S, Schächinger H, Oitzl MS. Chronický stres moduluje využití prostorových a stimulačních strategií učení u myší a člověka. Neurobiol Learn Mem (2008) 90(3):495–503. doi:10.1016/j.nlm.2008.07.015
100. Leong KC, Packard MG. Expozice zápachu predátorem ovlivňuje relativní využití systémů s více paměti: role basolaterální amygdaly. Neurobiol Learn Mem (2014) 109: 56 – 61. doi: 10.1016 / j.nlm.2013.11.015
101. Taylor SB, Anglin JM, Paode PR, Riggert AG, Olive MF, Conrad CD. Chronický stres může usnadnit nábor neuropatiků souvisejících s návyky a závislostí prostřednictvím neuronální restrukturalizace striata. Neurovědy (2014) 280: 231 – 42. doi: 10.1016 / j.neuroscience.2014.09.029
102. Leong KC, Goodman J, Packard MG. Opakované vystavení po tréninku obavám podmíněných podnětů zvyšuje konsolidaci paměti a ovlivňuje krysy směrem k využití dorsolaterálního učení závislého na striatu. Behav Brain Res (2015) 291: 195 – 200. doi: 10.1016 / j.bbr.2015.05.022
103. Goode TE, Leong KC, Goodman J, Maren S, Packard MG. Zvýšení paměti závislé na striatu podmíněným strachem je zprostředkováno beta-adrenergními receptory v bazolaterální amygdale. Neurobiologie stresu (v tisku). doi: 10.1016 / j.ynstr.2016.02.004
104. Schwabe L, Oitzl MS, Philippsen C, Richter S, Bohringer A, Wippich W, et al. Stres moduluje využití strategie prostorového versus stimulačního učení u lidí. Naučte se Mem (2007) 14(1–2):109–16. doi:10.1101/lm.435807
105. Schwabe L, Schächinger H, de Kloet ER, Oitzl MS. Kortikosteroidy fungují jako přepínač mezi paměťovými systémy. J Cogn Neurosci (2010) 22(7):1362–72. doi:10.1162/jocn.2009.21278
106. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Současná glukokortikoidní a noradrenergní aktivita posune instrumentální chování z cílené kontroly na obvyklou. J Neurosci (2010) 30(24):8190–6. doi:10.1523/JNEUROSCI.0734-10.2010
107. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Blokáda receptorů mineralokortikoidů zabraňuje modulaci více paměťových systémů vyvolaných stresem v lidském mozku. Biol Psychiatry (2013) 74(11):801–8. doi:10.1016/j.biopsych.2013.06.001
108. Schwabe L, Wolf OT. Stres vyvolává u lidí návykové chování. J Neurosci (2009) 29(22):7191–8. doi:10.1523/JNEUROSCI.0979-09.2009
109. Schwabe L, Wolf OT. Společensky hodnocený studený tlakový stres po instrumentálním učení upřednostňuje zvyky před cílenou akcí. Psychoneuroendokrinologie (2010) 35(7):977–86. doi:10.1016/j.psyneuen.2009.12.010
110. Guenzel FM, Wolf OT, Schwabe L. Glukokortikoidy zvyšují tvorbu paměti stimulační reakce u lidí. Psychoneuroendokrinologie (2014) 45: 21 – 30. doi: 10.1016 / j.psyneuen.2014.02.015
111. Higgins RL, Marlatt GA. Strach z interpersonálního hodnocení jako determinant konzumace alkoholu u mužských sociálních konzumentů. J Abnorm Psychol (1975) 84(6):644–51. doi:10.1037/0021-843X.84.6.644
112. Marlatt GA, Gordon JR. Determinanty relapsu: implikace pro udržení změny chování. In: Davidson PO, Davidson SM, editory. Behaviorální medicína: Změna životního stylu. New York: Brunne / Mazel (1980). str. 410 – 52.
113. Newcomb MD, Bentler PM. Vliv užívání drog dospívajícími a sociální podpora na problémy mladých dospělých: longitudinální studie. J Abnorm Psychol (1988) 97:64–75. doi:10.1037/0021-843X.97.1.64
114. Wallace BC. Psychologické a environmentální determinanty relapsu u kuřáků v cracku. J zneužívání zneužívání substrátu (1989) 6(2):95–106. doi:10.1016/0740-5472(89)90047-0
115. Kaplan HB, Johnson RJ. Vztahy mezi okolnostmi, které souvisejí s počátečním užíváním nelegálních drog a eskalací užívání drog: zmírnění účinků pohlaví a časných zkušeností dospívajících. In: Glantz M, Pickens R, redaktoři. Zranitelnost vůči zneužívání drog. Washington, DC: Americká psychologická asociace (1992). str. 200 – 358.
116. Harrison PA, Fulkerson JA, Beebe TJ. Použití více látek mezi dospívajícími oběťmi fyzického a sexuálního zneužívání. Zneužívání zneužívání dětí (1997) 21:529–39. doi:10.1016/S0145-2134(97)00013-6
117. Chilcoat HD, Breslau N. Posttraumatická stresová porucha a poruchy drog: testování kauzálních cest. Arch Gen Psychiatrie (1998) 55(10):913–7. doi:10.1001/archpsyc.55.10.913
118. Piazza PV, Le Moal M. Úloha stresu v samosprávě drog. Trends Pharmacol Sci (1998) 19(2):67–74. doi:10.1016/S0165-6147(97)01115-2
119. Goodman J, Leong KC, Packard MG. Emoční modulace systémů s více paměti: implikace pro neurobiologii posttraumatické stresové poruchy. Rev Neurosci (2012) 23(5–6):627–43. doi:10.1515/revneuro-2012-0049
120. Sinha R, Lacadie C, Skudlarski P, Fulbright RK, Rounsaville BJ, Kosten TR a kol. Neurální aktivita spojená se stresem indukovanou touhou po kokainu: funkční zobrazovací studie magnetické rezonance. Psychofarmakologie (2005) 183(2):171–80. doi:10.1007/s00213-005-0147-8
121. Avena NM, Rada P, Hoebel BG. Důkazy pro závislost na cukru: behaviorální a neurochemické účinky přerušovaného, nadměrného příjmu cukru. Neurosci Biobehav Rev (2008) 32(1):20–39. doi:10.1016/j.neubiorev.2007.04.019
122. Gearhardt AN, Corbin WR, Brownell KD. Potravinová závislost: zkoumání diagnostických kritérií závislosti. J Addict Med (2009) 3(1):1–7. doi:10.1097/ADM.0b013e318193c993
123. Smith DG, Robbins TW. Neurobiologické základy obezity a nadměrného stravování: zdůvodnění přijetí modelu závislosti na potravinách. Biol Psychiatry (2013) 73(9):804–10. doi:10.1016/j.biopsych.2012.08.026
124. de Jong JW, Meijboom KE, Vanderschuren LJ, Adan RA. Nízká kontrola nad příjemným příjmem potravy u potkanů je spojena s obvyklým chováním a zranitelností relapsu: individuální rozdíly. PLoS One (2013) 8(9): e74645. doi: 10.1371 / journal.pone.0074645
125. Furlong TM, Jayaweera HK, Balleine BW, Corbit LH. Konzumativní konzumace chutného jídla urychluje obvyklou kontrolu chování a je závislá na aktivaci dorsolaterálního striata. J Neurosci (2014) 34(14):5012–22. doi:10.1523/JNEUROSCI.3707-13.2014
126. Hargrave SL, Davidson TL, Zheng W, Kinzig KP. Západní diety indukují únik hematoencefalické bariéry a mění prostorové strategie u potkanů. Behav Neurosci (2016) 130(1):123–35. doi:10.1037/bne0000110
127. Smith KL, Hummer TA, Hulvershorn LA. Patologické videohry a jejich vztah k poruchám užívání návykových látek. Curr Addict Rep (2015) 2(4):302–9. doi:10.1007/s40429-015-0075-6
128. Weinstein AM. Závislost na počítačových hrách a videohrách - srovnání mezi uživateli hry a uživateli, kteří nejsou členy hry. Am J zneužívání alkoholu drogami (2010) 36(5):268–76. doi:10.3109/00952990.2010.491879
129. Kätsyri J, Hari R, Ravaja N, Nummenmaa L. Zástupce oponenta: zvýšené fMRI odměny odezvy na výhru proti člověku proti počítačovému soupeři během interaktivního hraní videohry. Cereb Cortex (2013) 23(12):2829–39. doi:10.1093/cercor/bhs259
130. Kätsyri J, Hari R, Ravaja N, Nummenmaa L. Jen pozorování hry nestačí: striatální fMRI odměňuje reakce na úspěchy a neúspěchy ve videohře během aktivního a zprostředkovaného hraní. Přední Hum Neurosci (2013) 7: 278. dva: 10.3389 / fnhum.2013.00278
131. Erickson KI, Boot WR, Basak C, Neider MB, Prakash RS, Voss MW a kol. Striatální objem předpovídá úroveň získávání dovedností videohry. Cereb Cortex (2010) 20: 2522 – 30. doi: 10.1093 / cercor / bhp293
132. West GL, Drisdelle BL, Konishi K, Jackson J, Jolicoeur P, Bohbot VD. Obvyklé akční videohry jsou spojeny s navigačními strategiemi závislými na caudate nucleus. Proc R Soc B (2015) 282(1808). doi: 10.1098 / rspb.2014.2952
133. Liu S, Schad DJ, Kuschpel MS, Rapp MA, Heinz A. Hudba a video hry během přestávek: vliv obvyklého versus cíleného rozhodování. Papír prezentován na 45th výroční setkání společnosti pro neurovědy. Chicago, IL: Společnost pro neurovědy (2015).
134. de Fonseca FR, Carrera MRA, Navarro M, Koob GF, Weiss F. Aktivace faktoru uvolňujícího kortikotropin v limbickém systému během vysazování kanabinoidů. Věda (1997) 276(5321):2050–4. doi:10.1126/science.276.5321.2050
135. Cornelius JR, Chung T, Martin C, Wood DS, Clark DB. Odchod z konopí je běžný u adolescentů, kteří vyhledávají léčbu konopí se závislostí na konopí a velkou depresí, a je spojen s rychlým relapsem závislosti. Addict Behav (2008) 33(11):1500–5. doi:10.1016/j.addbeh.2008.02.001
136. Greene MC, Kelly JF. Prevalence vysazování konopí a jeho vliv na odpověď a výsledky léčby adolescentů: prospektivní šetření 12-měsíc. J Addict Med (2014) 8: 359 – 67. doi: 10.1097 / ADM.0000000000000064
137. Wagner FA, Anthony JC. Od prvního užívání drog po drogovou závislost; vývojových období rizika závislosti na marihuaně, kokainu a alkoholu. Neuropsychopharmacology (2002) 26:479–88. doi:10.1016/S0893-133X(01)00367-0
138. Goodman J, Packard MG. Vliv kanabinoidů na procesy učení a paměti dorzálního striata. Neurobiol Learn Mem (2015) 125: 1 – 14. doi: 10.1016 / j.nlm.2015.06.008
139. Rueda-Orozco PE, Soria-Gomez E, Montes-Rodriguez CJ, Martínez-Vargas M, Galicia O, Navarro L, et al. Potenciální funkce endokanabinoidů při výběru navigační strategie potkanů. Psychofarmakologie (2008) 198(4):565–76. doi:10.1007/s00213-007-0911-z
140. Goodman J, Packard MG. Periferní a intra-dorsolaterální injekce striata agonistu kanabinoidního receptoru WIN 55,212-2 zhoršují konsolidaci paměti odezvy stimulu. Neurovědy (2014) 274: 128 – 37. doi: 10.1016 / j.neuroscience.2014.05.007
141. Nazzaro C, Greco B, Cerovic M, Baxter P, Rubino T, Trusel M, et al. Modulace SK kanálu zachraňuje striatální plasticitu a kontrolu nad návykem v toleranci na kanabinoidy. Nat Neurosci (2012) 15: 284 – 93. doi: 10.1038 / nn.3022
142. Ames SL, Grenard JL, Stacy AW, Xiao L, He Q, Wong SW a kol. Funkční zobrazování implicitních asociací marihuany při výkonu implicitního asociačního testu (IAT). Behav Brain Res (2013) 256: 494 – 502. doi: 10.1016 / j.bbr.2013.09.013
143. Redish AD, Jensen S, Johnson A. Jednotný rámec pro závislost: zranitelnosti v procesu rozhodování. Behav Brain Sci (2008) 31(04):415–37. doi:10.1017/S0140525X0800472X
144. Brevers D, Bechara A, Cleeremans A, Noël X. Iowa Gambling Task (IGT): dvacet let poté - porucha hazardních her a IGT. Front Psychol (2013) 4: 665. doi: 10.3389 / fpsyg.2013.00665
145. Koob GF, Le Moal M. Neurobiologické mechanismy pro motivační procesy soupeře v závislosti. Philos Trans R Soc B Biol Sci (2008) 363(1507):3113–23. doi:10.1098/rstb.2008.0094
146. Hyman SE, Malenka RC, Nestler EJ. Neurální mechanismy závislosti: role učení a paměti související s odměnou. Annu Rev Neurosci (2006) 29: 565 – 98. doi: 10.1146 / annurev.neuro.29.051605.113009
147. Goodman J, Packard M. Paměťový systém používaný během akvizice určuje účinnost různých protokolů extinkce. Přední Behav Neurosci (2015) 9: 314. doi: 10.3389 / fnbeh.2015.00314
148. Palencia CA, Ragozzino ME. Přínos NMDA receptorů v dorsolaterálním striatu k egocentrickému učení odezvy. Behav Neurosci (2005) 119(4):953–60. doi:10.1037/0735-7044.119.4.953
149. Rueda-Orozco PE, Montes-Rodriguez CJ, Soria-Gomez E, Méndez-Díaz M., Prospéro-García O. Poškození aktivity endokanabinoidů v dorsolaterálním striatu prodlužuje zánik chování v procesu procedurální paměti u potkanů. Neurofarmakologie (2008) 55(1):55–62. doi:10.1016/j.neuropharm.2008.04.013
Klíčová slova: paměť, drogová závislost, hipokampus, striatum, amygdala, stres, úzkost
Citace: Goodman J a Packard MG (2016) paměťové systémy a závislý mozek. Přední. Psychiatrie 7: 24. dva: 10.3389 / fpsyt.2016.00024
Přijato: 01 prosinec 2015; Přijato: 11 únor 2016;
Publikováno: 25 únor 2016
Úprava:
Vincent David, Centre National de la Recherche Scientifique (CNRS), Francie
Recenze:
Jacques Micheau, Univerzita Bordeaux 1, Francie
Roberto Ciccocioppo, University of Camerino, Itálie
Copyright: © 2016 Goodman a Packard. Jedná se o článek s otevřeným přístupem distribuovaný podle podmínek Creative Commons Attribution License (CC BY). Používání, distribuce nebo reprodukce na jiných fórech je přípustné za předpokladu, že jsou připočítáni původní autoři nebo nositelé licence a že je uvedena původní publikace v tomto časopise v souladu s uznávanou akademickou praxí. Není povoleno použití, distribuce nebo reprodukce, která nesplňuje tyto podmínky.
Korespondence: Mark G. Packard, [chráněno e-mailem]
