COMMENTAIRES: Comme des études ultérieures le révéleront, DeltaFosB est le commutateur moléculaire commun pour les toxicomanies et les dépendances comportementales. C'est un facteur de transcription, ce qui signifie qu'il affecte les gènes activés ou désactivés. Comme indiqué ailleurs, les drogues addictives ne font que détourner les mécanismes normaux. C'est pourquoi il est ridicule de suggérer que les dépendances comportementales ne peuvent pas exister.
Proc Natl Acad Sci US A. 2001 Septembre 25; 98 (20): 11042 – 11046.
doi: 10.1073 / pnas.191352698.
Eric J. Nestler *, Michel Barrot et David W. Self
Département de psychiatrie et Center for Basic Neuroscience, Centre médical Southwestern de l'Université du Texas, 5323, boulevard Harry Hines, Dallas, TX 75390-9070
Abstract
La longévité de certaines des anomalies comportementales qui caractérisent la toxicomanie a suggéré que la régulation de l'expression des gènes neuronaux pourrait être impliquée dans le processus par lequel les drogues abusives provoquent un état de dépendance. jeDe plus en plus de preuves suggèrent que le facteur de transcription ΔFosB représente un mécanisme par lequel les drogues faisant l’abus génèrent des modifications cérébrales relativement stables qui contribuent au phénotype de la dépendance. ΔFosB, membre de la famille des facteurs de transcription Fos, s’accumule dans un sous-ensemble de neurones du noyau accumbens et du striatum dorsal (régions du cerveau importantes pour la dépendance) après l’administration répétée de nombreux types de drogues. Une accumulation similaire de ΔFosB se produit après une course compulsive, ce qui suggère que ΔFosB peut s'accumuler en réponse à de nombreux types de comportements compulsifs.. Fait important, ΔFosB persiste dans les neurones pendant des périodes relativement longues en raison de son extraordinaire stabilité. Par conséquent, ΔFosB représente un mécanisme moléculaire qui pourrait initier et ensuite maintenir des changements dans l'expression des gènes qui persistent longtemps après la fin de l'exposition au médicament.. Des études sur des souris transgéniques inductibles qui surexpriment ΔFosB ou un inhibiteur négatif dominant de la protéine fournissent des preuves directes que ΔFosB provoque une sensibilité accrue aux effets comportementaux des drogues d’abus et, éventuellement, un comportement accru à la recherche de drogues. Ces travaux corroborent l’opinion selon laquelle ΔFosB fonctionne comme un type de «commutateur moléculaire» prolongé qui convertit progressivement les réactions aiguës aux médicaments en adaptations relativement stables contribuant à la plasticité neuronale et comportementale à long terme qui sous-tend la dépendance.
La recherche sur la toxicomanie est centrée sur la compréhension des manières complexes par lesquelles les drogues en abus modifient le cerveau pour provoquer des anomalies comportementales qui caractérisent la toxicomanie. L'un des défis critiques sur le terrain consiste à identifier les modifications du cerveau induites par les médicaments, relativement stables, afin de prendre en compte les anomalies comportementales particulièrement durables. Par exemple, un toxicomane humain peut courir un risque accru de rechute, même après des années d'abstinence.
La stabilité de ces anomalies comportementales a conduit à penser qu'elles pourraient être médiées, du moins en partie, par des modifications de l'expression des gènes (1 – 3). Selon ce point de vue, l'exposition répétée à une drogue d'abus perturbe de manière répétée la transmission au niveau de certaines synapses cérébrales sensibles. Ces perturbations finissent par se signaler via des cascades de messagers intracellulaires vers le noyau, où ils initient puis maintiennent les modifications de l'expression de gènes spécifiques. Un mécanisme principal par lequel les voies de transduction du signal influencent l'expression des gènes est la régulation des facteurs de transcription, des protéines qui se lient aux régions régulatrices des gènes et modifient leur transcription.
Par conséquent, l'un des objectifs de la recherche sur la toxicomanie était d'identifier les facteurs de transcription qui sont modifiés dans les régions du cerveau impliquées dans la toxicomanie après l'administration chronique de drogues. Plusieurs facteurs de transcription de ce type ont été identifiés au cours de la dernière décennie (1 – 6). Cette revue est centrée sur un facteur de transcription particulier appelé ΔFosB.
Induction de ΔFosB par des drogues d'abus
ΔFosB, codé par le gène fosB, fait partie de la famille des facteurs de transcription Fos, qui comprennent également c-Fos, FosB, Fra1 et Fra2 (7). Ces protéines de la famille Fos hétérodimérisent avec des protéines de la famille Jun (c-Jun, JunB ou JunD) pour former des facteurs de transcription actifs AP-1 (protéine activatrice-1) qui se lient aux sites AP-1 (séquence consensus: TGAC / GTCA) présents dans les promoteurs de certains gènes pour réguler leur transcription.
Ces protéines de la famille Fos sont induites rapidement et de manière transitoire dans des régions spécifiques du cerveau après l'administration aiguë de nombreux médicaments d'abus (Fig. 1) (8 – 11). Les régions importantes sont le noyau accumbens et le striatum dorsal, qui sont des médiateurs importants des réactions comportementales aux médicaments, en particulier de leurs effets stimulants et locomoteurs (12, 13). Ces protéines reviennent aux niveaux de base quelques heures après l'administration du médicament.
Figure 1
Schéma montrant l’accumulation progressive de ΔFosB par rapport à l’induction rapide et transitoire d’autres protéines de la famille Fos en réponse à l’abus de drogues. (A) L'autoradiogramme illustre l'induction différentielle de ces différentes protéines par stimulation aiguë (1 – 2 heure après une exposition unique à un médicament) par rapport à la stimulation chronique (1 jour après une exposition répétée à un médicament). (B) Plusieurs vagues de protéines de type Fos [composées d'isoformes c-Fos (52 à 58-kDa), FosB (Isoformes de 46 à 50-kDa), ΔFosB (33-kDa) et Fra1 ou Fra2 (Fra40) 35 kDa)] sont induits dans le noyau accumbens et les neurones striataux dorsaux par l'administration aiguë d'un médicament faisant l'objet d'abus. Les isoformes de ΔFosB modifiées biochimiquement (37 – XNUMX kDa) sont également induites. ils sont également induits (bien qu'à des niveaux faibles) après une administration aiguë de médicament, mais persistent dans le cerveau pendant de longues périodes en raison de leur stabilité. (C) Avec une administration répétée (par exemple deux fois par jour) du médicament, chaque stimulus aigu induit un faible niveau des isoformes stables de ΔFosB, ce qui est indiqué par le jeu inférieur de lignes se chevauchant qui indiquent ΔFosB induit par chaque stimulus aigu. Le résultat est une augmentation graduelle des niveaux totaux de ΔFosB avec des stimuli répétés au cours du traitement chronique, ce qui est indiqué par la ligne croissante en gradins dans le graphique.
Des réactions très différentes sont observées après l’administration chronique de drogues d’abus (Fig. 1). Les isoformes de ΔFosB modifiées biochimiquement (masse moléculaire 35 – 37 kDa) s'accumulent dans les mêmes régions du cerveau après une exposition répétée au médicament, alors que tous les autres membres de la famille Fos présentent une tolérance (c'est-à-dire une induction réduite par rapport aux expositions initiales au médicament). Une telle accumulation de ΔFosB a été observée pour la cocaïne, la morphine, l’amphétamine, l’alcool, la nicotine et la phencyclidine.e (11, 14 – 18). Certaines preuves suggèrent que cette induction est sélective pour le sous-ensemble de neurones à épines moyennes contenant de la dynorphine / substance P situés dans ces régions du cerveau (15, 17), bien que des travaux supplémentaires soient nécessaires pour l'établir avec certitude. Les isoformes de ΔFosB de 35 à 37-kDa se dimérisent principalement avec JunD pour former un complexe AP-1 actif et durable dans ces régions du cerveau (19, 20). Ces isoformes de ΔFosB s'accumulent lors d'une exposition chronique au médicament en raison de leur demi-vie extrêmement longue (21) et persistent donc dans les neurones pendant plusieurs semaines au moins après la fin de l'administration du médicament. Il est intéressant de noter que ces isoformes de ΔFosB sont des produits hautement stables d’un gène précoce immédiat (fosB). La stabilité des isoformes de ΔFosB fournit un nouveau mécanisme moléculaire par lequel les modifications de l’expression des gènes induites par le médicament peuvent persister malgré des périodes de retrait du médicament relativement longues.
Bien que le noyau accumbens joue un rôle crucial dans les effets bénéfiques des drogues, il semble fonctionner normalement en régulant les réactions aux renforçateurs naturels, tels que les aliments, les boissons, le sexe et les interactions sociales (12, 13). En conséquence, le rôle possible de cette région cérébrale dans d'autres comportements compulsifs (par exemple, une surconsommation pathologique, le jeu, l'exercice, etc.) suscite un intérêt considérable. Pour cette raison, nous avons examiné si ΔFosB est régulé dans un modèle animal de course compulsive. En effet, les isoformes stables de ΔFosB de 35 à 37-kDa sont induites sélectivement dans le noyau accumbens chez des rats qui présentent un comportement compulsif en course. †
Identité Biochimique Des Isoformes ΔFosB Stables
Comme mentionné ci-dessus, les isoformes ΔFosB qui s'accumulent après l'administration chronique d'un médicament d'abus ou de course compulsive indiquent une masse moléculaire de 35 – 37 kDa. Ils peuvent être différenciés de l'isoforme 33-kDa de ΔFosB, qui est induit rapidement mais de façon transitoire après une exposition à un médicament (Fig. 1) (14, 19, 22). Les preuves actuelles suggèrent que l'isoforme 33-kDa est la forme native de la protéine, qui est modifiée pour former les produits plus stables 35 à 37-kDa (19, 21). Cependant, la nature de la modification biochimique qui convertit l'isoforme instable 33-kDa en isoformes stables 35- en 37-kDa est restée obscure. On a supposé que la phosphorylation pourrait être responsable (11). Par exemple, l'induction de ΔFosB est atténuée chez les souris dépourvues de DARPP-32, une protéine enrichie en striatum (23, 24). DARPP-32 régulant l'activité catalytique de la protéine phosphatase-1 et de la protéine kinase A (25, 26), la nécessité pour cette protéine d'accumuler normalement les isoformes stables de ΔFosB suggère un rôle possible de la phosphorylation dans la production de ces produits stables.
Rôle de ΔFosB dans la plasticité comportementale face aux drogues d'abus
Le rôle de ΔFosB dans la toxicomanie est en grande partie issu de l’étude de souris transgéniques dans lesquelles ΔFosB peut être induit sélectivement dans le noyau accumbens et dans d’autres régions striatales d’animaux adultes (27, 28). Il est important de noter que ces souris surexpriment ΔFosB sélectivement dans les neurones à épine moyenne contenant de la dynorphine / substance P, où les médicaments sont supposés induire la protéine. Le tableau 1 résume le phénotype comportemental des souris surexprimant ΔFosB, qui ressemble à bien des égards aux animaux après une exposition chronique au médicament. Les souris présentent une réponse locomotrice augmentée à la cocaïne après une administration aiguë et chronique (28). Ils montrent également une sensibilité accrue aux effets bénéfiques de la cocaïne et de la morphine dans les tests de conditionnement sur place (11, 28) et s'auto-administrent des doses de cocaïne plus faibles que celles de leurs compagnons qui ne surexpriment pas ΔFosB. sensibilisation à la cocaïne et apprentissage spatial normal dans le labyrinthe aquatique de Morris (28). TCes données indiquent que ΔFosB augmente la sensibilité d'un animal à la cocaïne et peut-être à d'autres drogues abusives et peut représenter un mécanisme de sensibilisation relativement prolongée aux drogues.
 striatum
striatum
| Augmentation de l'activation locomotrice en réponse à l'administration aiguë et répétée de cocaïne. |
| Augmentation des réponses enrichissantes à la cocaïne et à la morphine dans les essais de conditionnement sur place. |
| Augmentation de l'auto-administration de faibles doses de cocaïne. |
| Motivation accrue de la cocaïne dans les dosages à rapports progressifs. |
| Augmentation des réponses anxiolytiques à l'alcool. |
| Augmentation du comportement de course compulsif. |
Basé sur les données dans les références. 28 et 29.† ‡ §¶
Plasticité comportementale induite par ΔFosB dans le striatum du noyau accumbens-dorsal
IDe plus, il existe des preuves préliminaires que les effets de ΔFosB peuvent aller bien au-delà d’une régulation de la sensibilité aux médicaments en soi à des comportements plus complexes liés au processus de toxicomanie. Les souris exprimant ΔFosB travaillent plus fort à s'auto-administrer de la cocaïne dans les dosages à auto-administration àen supposant que ΔFosB peut sensibiliser les animaux aux propriétés de motivation de la cocaïne, ce qui les incite à la motivation, et donc à une propension à la rechuteLes souris exprimant L. ‡ ΔFosB présentent également des effets anxiolytiques améliorés de l'alcool, § un phénotype associé à une augmentation de la consommation d'alcool chez l'homme. Ensemble, ces premiers résultats suggèrent que ΔFosB, en plus de sensibiliser davantage aux drogues faisant l’abus de drogues, produit des changements qualitatifs dans le comportement qui favorisent les comportements de recherche de drogues. Ainsi, ΔFosB peut fonctionner comme un «commutateur moléculaire» soutenu qui aide à initier puis à maintenir les aspects cruciaux de l’état de dépendance. Une question importante à l’étude est de savoir si l’accumulation de ΔFosB pendant l’exposition au médicament favorise le comportement de recherche de drogue après des périodes d’attente prolongées, même après que les niveaux de ΔFosB se soient normalisés (voir ci-dessous).
Adulte les souris qui surexpriment ΔFosB de manière sélective dans le noyau accumbens et le striatum dorsal présentent également une course compulsive supérieure à celle des patients de contrôle. † Ces observations soulèvent la possibilité intéressante que l’accumulation de ΔFosB dans ces neurones joue un rôle plus général dans la formation et le maintien de souvenirs d’habitude et de troubles compulsifs. comportements, peut-être en renforçant l'efficacité des circuits neuronaux dans lesquels ces neurones fonctionnent.
Le ΔFosB s'accumule dans certaines régions du cerveau en dehors du noyau accumbens et du striatum dorsal après une exposition chronique à la cocaïne. Parmi eux les régions sont l'amygdale et le cortex préfrontal médial (15). Un des principaux objectifs de la recherche actuelle est de comprendre les contributions de l'induction de ΔFosB dans ces régions au phénotype de la dépendance.
Des travaux antérieurs sur des souris knock-out fosB ont révélé que ces animaux ne développent pas de sensibilisation aux effets locomoteurs de la cocaïne, ce qui est cohérent avec les découvertes des souris surexprimant ΔFosB mentionnées ci-dessus (22). Cependant, les mutants fosB ont montré une sensibilité accrue aux effets aigus de la cocaïne, ce qui est incompatible avec ces autres résultats. L'interprétation des résultats avec les mutants fosB, cependant, est compliquée par le fait que ces animaux manquent non seulement de ΔFosB, mais également de FosB pleine longueur. De plus, les mutants manquent à la fois de protéines dans tout le cerveau et dès les premiers stades de développement. En effet, des travaux plus récents soutiennent les conclusions des souris surexprimant ΔFosB: la surexpression inductible d'un mutant tronqué de c-Jun, qui agit comme un antagoniste négatif dominant de ΔFosB, sélectivement dans le noyau accumbens et le striatum dorsal montre une sensibilité réduite aux effets gratifiants de la cocaïne .¶ Ces résultats soulignent la prudence qui doit être utilisée dans l'interprétation des résultats de souris présentant des mutations constitutives et illustrent l'importance des souris présentant des mutations inductibles et spécifiques au type cellulaire dans les études de plasticité dans le cerveau adulte.
Gènes cibles pour ΔFosB
Puisque ΔFosB est un facteur de transcription, il est probable que la protéine provoque une plasticité comportementale par le biais de modifications de l’expression d’autres gènes. Le ΔFosB est généré par l'épissage alternatif du gène fosB et manque d'une partie du domaine de transactivation C-terminal présent dans le gène FosB de pleine longueur. En conséquence, il a été initialement proposé que ΔFosB fonctionne comme un répresseur de transcription (29). Cependant, les travaux en culture cellulaire ont clairement démontré que le ΔFosB peut induire ou réprimer Transcription médiée par AP-1 en fonction du site particulier AP-1 utilisé (21, 29 – 31). Le FosB de pleine longueur exerce les mêmes effets que le ΔFosB sur certains fragments de promoteur, mais des effets différents sur les autres. Des travaux supplémentaires sont nécessaires pour comprendre les mécanismes sous-jacents à ces actions variées de ΔFosB et de FosB.
Notre groupe a utilisé deux approches pour identifier les gènes cibles pour ΔFosB. L'un est l'approche du gène candidat. Nous avons initialement considéré les récepteurs du glutamate de l'acide α-amino-3-hydroxy-5-méthyl-4-isoxazolepropionique (AMPA) comme des cibles putatives, étant donné le rôle important de la transmission glutamatergique dans le noyau accumbens. Les travaux à ce jour ont indiqué qu'une sous-unité de récepteur de glutamate AMPA particulière, GluR2, peut être une cible de bonne foi pour ΔFosB (figure 2). L'expression de GluR2, mais pas l'expression d'autres sous-unités du récepteur AMPA, est augmentée dans le noyau accumbens (mais pas dans le striatum dorsal) lors de la surexpression de ΔFosB (28), et l'expression d'un mutant négatif dominant atténue la capacité de la cocaïne à induire la protéine.¶ De plus, le promoteur du gène GluR2 contient un site consensus AP-1 qui se lie à ΔFosB (28). La surexpression de GluR2 dans le noyau accumbens, par l'utilisation d'un transfert de gène à médiation virale, augmente la sensibilité d'un animal aux effets gratifiants de la cocaïne, imitant ainsi une partie du phénotype observé chez les souris exprimant ΔFosB (28). L'induction de GluR2 pourrait expliquer la sensibilité électrophysiologique réduite des neurones du noyau accumbens aux agonistes des récepteurs AMPA après l'administration chronique de cocaïne (32), car les récepteurs AMPA contenant GluR2 montrent une conductance globale réduite et une perméabilité au Ca2 + réduite. La réactivité réduite de ces neurones aux entrées excitatrices peut alors améliorer les réponses à une drogue d'abus. Cependant, les façons dont les signaux dopaminergiques et glutamatergiques dans le noyau accumbens régulent le comportement addictif restent inconnues; cela nécessitera un niveau de compréhension du circuit neuronal, qui n'est pas encore disponible.
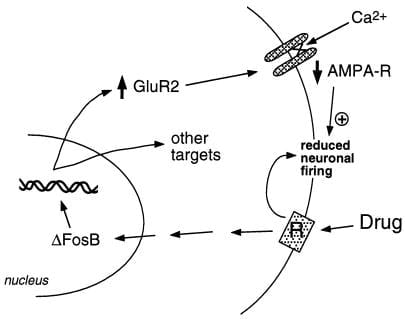
Figure 2
La sous-unité du récepteur du glutamate AMPA, GluR2, est une cible putative pour ΔFosB. On montre comment l'induction médiée par ΔFosB de GluR2 peut modifier la réactivité physiologique des neurones du noyau accumbens et conduire à des réponses sensibilisées aux drogues d'abus. Selon ce schéma, les drogues abusives produisent leurs effets de renforcement aigus via l'inhibition des neurones du noyau accumbens. Avec une exposition répétée, les médicaments induisent ΔFosB, qui régule de nombreux gènes cibles, y compris GluR2. Cela augmente la proportion de récepteurs AMPA (AMPA-R) sur les neurones du noyau accumbens qui contiennent la sous-unité GluR2, ce qui entraîne une réduction du courant AMPA global et du courant Ca2 +. Cette excitabilité réduite pourrait rendre les neurones plus sensibles aux effets inhibiteurs aigus des médicaments et donc aux effets de renforcement des médicaments.
Une autre cible potentielle de ΔFosB est le gène codant pour la dynorphine. Comme indiqué précédemment, la dynorphine est exprimée dans le sous-ensemble de neurones épineux de noyau accumbens qui présentent une induction de ΔFosB. La dynorphine semble fonctionner dans une boucle de rétroaction intercellulaire: sa libération inhibe les neurones dopaminergiques qui innervent les neurones épineux moyens, via des récepteurs opioïdes κ présents sur les terminaisons nerveuses dopaminergiques dans le noyau accumbens, ainsi que sur les corps cellulaires et les dendrites dans la région tegmentale ventrale (Fig. 3) (33 – 35). Cette idée est compatible avec la capacité d'un agoniste des récepteurs K, lors de son administration dans l'une ou l'autre de ces deux régions cérébrales, de diminuer la réactivité du médicament.d (35).
RDes travaux récents ont montré que ΔFosB diminue l’expression de la dynorphine ‖, ce qui pourrait contribuer à l’amélioration des mécanismes de récompense observés lors de l’induction de ΔFosB. Fait intéressant, un autre facteur de transcription régulé par un médicament, CREB (2, 3), exerce l'effet inverse: il induit l'expression de la dynorphine dans le noyau accumbens et réduit les propriétés valorisantes de la cocaïne et de la morphine. (4). **
BL'activation du CREB induite par le médicament se dissipant rapidement après l'administration du médicament, une telle régulation réciproque de la dynorphine par CREB et ΔFosB pourrait expliquer les changements de comportement réciproques qui se produisent pendant les phases de sevrage précoces et tardives, avec des symptômes émotionnels négatifs et une sensibilité réduite au médicament prédominante au cours des phases précoces de sevrage et de sensibilisation aux effets de motivation prédominants et stimulants des médicaments prédominants ultérieurement.
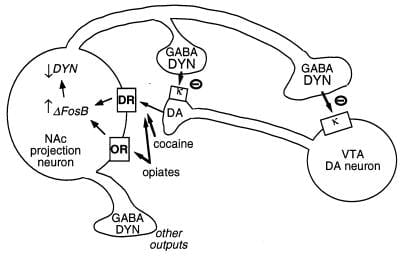
Figure 3
La dynorphine est une cible putative de ΔFosB. Le neurone de la dopamine (DA) de la région tegmentale ventrale (VTA) innervant une classe de neurones de projection GABAergiques du noyau accumbens (NAc) exprimant la dynorphine (DYN). La dynorphine sert de mécanisme de rétroaction dans ce circuit: la dynorphine, libérée des terminaux des neurones NAc, agit sur les récepteurs opioïdes κ situés sur les terminaux nerveux et les corps cellulaires des neurones DA pour inhiber leur fonctionnement. ΔFosB, en inhibant l’expression de la dynorphine, peut réguler négativement cette boucle de rétroaction et améliorer les propriétés gratifiantes des drogues. L’effet réciproque de CREB sur ce système n’est pas démontré: CREB améliore l’expression de la dynorphine et atténue ainsi les propriétés enrichissantes des drogues d’abus. (4). GABA, acide γ-aminobutyrique; DR, récepteur de la dopamine; OU, récepteur opioïde.
La deuxième approche utilisée pour identifier les gènes cibles pour ΔFosB implique l'analyse de puces à ADN. La surexpression inductible de ΔFosB augmente ou diminue l'expression de nombreux gènes dans le noyau accumbens (36). Bien qu'un travail considérable soit maintenant nécessaire pour valider chacun de ces gènes en tant que cibles physiologiques de ΔFosB et pour comprendre leur contribution au phénotype de la dépendance, une cible importante semble être Cdk5 (kinase-5 dépendant de la cycline). Ainsi, Cdk5 a été initialement identifié comme ΔFosB-régulé par l'utilisation de microréseaux, et plus tard il a été montré qu'il était induit dans le noyau accumbens et le striatum dorsal après une administration chronique de cocaïne (37). ΔFosB active le gène cdk5 via un site AP-1 présent dans le promoteur du gène (36). Ensemble, ces données soutiennent un schéma dans lequel la cocaïne induit l'expression de Cdk5 dans ces régions du cerveau via ΔFosB. L'induction de Cdk5 semble altérer la signalisation dopaminergique au moins en partie via une phosphorylation accrue de DARPP-32 (37), qui est converti d'un inhibiteur de la protéine phosphatase-1 en un inhibiteur de la protéine kinase A lors de sa phosphorylation par Cdk5 (26).
Rôle de ΔFosB dans la médiation de la plasticité «permanente» aux drogues d'abus
Bien que le signal ΔFosB ait une durée de vie relativement longue, il n’est pas permanent. Le ΔFosB se dégrade progressivement et ne peut plus être détecté dans le cerveau après un mois de sevrage du médicament 1 – 2, bien que certaines anomalies comportementales persistent pendant des périodes beaucoup plus longues. Par conséquent, ΔFosB en tant que tel ne semblerait pas capable de médier ces anomalies comportementales semi-permanentes. La difficulté à trouver les adaptations moléculaires qui sous-tendent les changements de comportement extrêmement stables associés à la dépendance est analogue aux défis rencontrés dans le domaine de l'apprentissage et de la mémoire. Bien qu’il existe d’élégants modèles d’apprentissage et de mémoire cellulaires et moléculaires, il n’a pas encore été possible d’identifier des adaptations moléculaires et cellulaires suffisamment longues pour rendre compte de mémoires comportementales extrêmement stables. En effet, ΔFosB est la plus longue adaptation connue pour se produire dans le cerveau adulte, non seulement en réponse à l'abus de drogues, mais aussi à toute autre perturbation (qui n'implique pas de lésions). Deux propositions ont évolué, à la fois dans les domaines de la toxicomanie et de l'apprentissage et de la mémoire, pour expliquer cet écart.
Une possibilité est que davantage de changements transitoires dans l'expression des gènes, tels que ceux induits par ΔFosB ou d'autres facteurs de transcription (par exemple, CREB), peut médier des changements de longue durée dans la morphologie neuronale et la structure synaptique. Par exemple, une augmentation de la densité des épines dendritiques (en particulier une augmentation des épines à deux têtes) accompagne la efficacité accrue des synapses glutamatergiques neurones pyramidaux de l'hippocampe au cours d'une potentialisation à long terme (38 – 40) et est parallèle à l'amélioration de la sensibilité comportementale à la cocaïne induite par la neurone au niveau des neurones épineux moyens du noyau accumbens (41). On ignore si ces changements structurels durent suffisamment longtemps pour expliquer des changements de comportement très stables, bien que ces derniers persistent pendant au moins un mois 1 de sevrage du médicament. Des preuves récentes laissent penser que ΔFosB et son induction de Cdk5 sont un médiateur des modifications induites par le médicament de la structure synaptique du noyau accumbens (Fig. 4). ‡‡ Ainsi, l’inhibition d’un inhibiteur de Cdk5 dans le noyau accumbens empêche la exposition répétée à la cocaïne pour augmenter la densité de la colonne vertébrale dendritique dans cette région. Cela concorde avec l'idée selon laquelle Cdk5, qui est enrichi dans le cerveau, régule la structure et la croissance neuronale (voir les références 36 et 37). Il est possible, bien que nullement prouvé, que de tels changements dans la morphologie neuronale puissent durer plus longtemps que le signal ΔFosB lui-même.
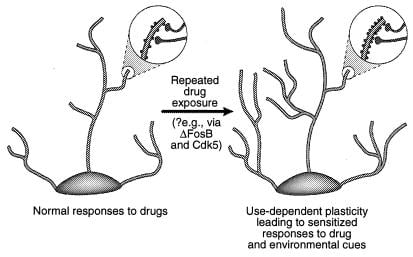
Figure 4
Régulation de la structure dendritique par les drogues d'abus. On voit l'expansion de l'arbre dendritique d'un neurone après une exposition chronique à une drogue d'abus, comme cela a été observé avec la cocaïne dans le noyau accumbens et le cortex préfrontal (41). Les zones de grossissement montrent une augmentation des épines dendritiques, qui est supposée se produire en conjonction avec des terminaisons nerveuses activées. Cette augmentation de la densité de la colonne dendritique peut être médiée via ΔFosB et l'induction conséquente de Cdk5 (voir texte). De telles altérations de la structure dendritique, qui sont similaires à celles observées dans certains modèles d'apprentissage (par exemple, potentialisation à long terme), pourraient médier des réponses sensibilisées à long terme aux drogues d'abus ou aux signaux environnementaux. [Reproduit avec l'autorisation de la référence. 3 (Copyright 2001, Macmillian Magazines Ltd.)].
Une autre possibilité est que l’induction transitoire d’un facteur de transcription (par exemple, ΔFosB, CREB) conduit à des changements plus permanents dans l'expression des gènes par la modification de la chromatin. On pense que ces facteurs de transcription et de nombreux autres activent ou répriment la transcription d'un gène cible en favorisant l'acétylation ou la désacétylation, respectivement, des histones situées à proximité du gène (42). Bien que cette acétylation et cette désacétylation des histones puissent apparemment se produire très rapidement, il est possible que AFOSB ou CREB produisent des adaptations plus durables dans le mécanisme enzymatique qui contrôle l'acétylation des histones. ΔFosB ou CREB peuvent également favoriser des modifications plus longues de l’expression génique en régulant d’autres modifications de la chromatine (par exemple, la méthylation de l’ADN ou de l’histone) qui ont été impliquées dans les modifications permanentes de la transcription génique survenues au cours du développement (voir références 42 et 43). . Bien que ces possibilités restent spéculatives, elles pourraient fournir un mécanisme par lequel des adaptations transitoires à une drogue d'abus (ou à une autre perturbation) entraînent des conséquences comportementales essentiellement tout au long de la vie.
Bibliographie
- ↵
- Nestler EJ,
- Hope BT,
- Widnell KL
(1993) Neuron 11: 995 – 1006.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Berke JD,
- Hyman SE
(2000) Neuron 25: 515 – 532.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Nestler EJ
(2001) Rev Neurosci 2: 119 – 128.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Carlezon WA Jr,
- Thome J,
- Olson VG,
- Lane-Ladd SB,
- Brodkin ES,
- Hiroi N,
- Duman RS,
- Neve RL,
- Nestler EJ
(1998) Science 282: 2272 – 2275.
Résumé / Texte intégral GRATUIT
- O'Donovan KJ,
- Tourtellotte WG,
- Millbrandt J,
- Baraban JM
(1999) Trends Neurosci 22: 167 – 173.
- ↵
- Mackler SA,
- Korutla L,
- Cha XY,
- Koebbe MJ,
- Fournier KM,
- Bowers MS,
- Kalivas PW
(2000) J Neurosci 20: 6210 – 6217.
Résumé / Texte intégral GRATUIT
- ↵
- Morgan JI,
- Curran T
(1995) Trends Neurosci 18: 66 – 67.
- ↵
- Young ST,
- Porrino LJ,
- Iadarola MJ
(1991) Proc Natl Acad Sci USA 88: 1291 – 1295.
Résumé / Texte intégral GRATUIT
- Graybiel AM,
- Moratalla R,
- Robertson HA
(1990) Proc Natl Acad Sci USA 87: 6912 – 6916.
Résumé / Texte intégral GRATUIT
- Hope B,
- Kosofsky B,
- Hyman SE,
- Nestler EJ
(1992) Proc Natl Acad Sci USA 89: 5764 – 5768.
Résumé / Texte intégral GRATUIT
- ↵
- Kelz MB,
- Nestler EJ
(2000) Curr Opin Neurol 13: 715 – 720.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Koob GF,
- Sanna PP,
- Bloom FE
(1998) Neuron 21: 467 – 476.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Sage RA
Dépendance à l'alcool à la drogue 1998: 51 – 13.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Hope BT,
- Nye HE,
- Kelz MB,
- Self DW,
- Iadarola MJ,
- Nakabeppu Y,
- Duman RS,
- Nestler EJ
(1994) Neuron 13: 1235 – 1244.
- ↵
- Nye H,
- Hope BT,
- Kelz M,
- Iadarola M,
- Nestler EJ
(1995) J Pharmacol Exp Ther 275: 1671 – 1680.
Résumé / Texte intégral GRATUIT
- Nye HE,
- Nestler EJ
(1996) Mol Pharmacol 49: 636 – 645.
- ↵
- Moratalla R,
- Elibol B,
- Vallejo M,
- Graybiel AM
(1996) Neuron 17: 147 – 156.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Pich EM,
- Pagliusi SR,
- Tessari M,
- Talabot-Ayer D,
- Hooft van Huijsduijnen R,
- Chiamulera C
(1997) Science 275: 83 – 86.
Résumé / Texte intégral GRATUIT
- ↵
- Chen JS,
- Nye HE,
- Kelz MB,
- Hiroi N,
- Nakabeppu Y,
- Hope BT,
- Nestler EJ
(1995) Mol Pharmacol 48: 880 – 889.
- ↵
- Hiroi N,
- Brown J,
- Ye H,
- Saudou F,
- Vaidya VA,
- Duman RS,
- Greenberg ME,
- Nestler EJ
(1998) J Neurosci 18: 6952 – 6962.
Résumé / Texte intégral GRATUIT
- ↵
- Chen J,
- Kelz MB,
- Hope BT,
- Nakabeppu Y,
- Nestler EJ
(1997) J Neurosci 17: 4933 – 4941.
Résumé / Texte intégral GRATUIT
- ↵
- Hiroi N,
- Brown J,
- Haile C,
- Ye H,
- Greenberg ME,
- Nestler EJ
(1997) Proc Natl Acad Sci USA 94: 10397 – 10402.
Résumé / Texte intégral GRATUIT
- ↵
- Fienberg AA,
- Hiroi N,
- Mermelstein P,
- Chanson WJ,
- Snyder GL,
- Nishi A,
- Cheramy A,
- O'Callaghan JP,
- Miller D,
- Cole DG,
- et al.
(1998) Science 281: 838 – 842.
Résumé / Texte intégral GRATUIT
- ↵
- Hiroi N,
- Feinberg A,
- Haile C,
- Greengard P,
- Nestler EJ
(1999) Eur J Neurosci 11: 1114 – 1118.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Greengard P,
- Allen PB,
- Nairn AC
(1999) Neuron 23: 435 – 447.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Le juge Bibb,
- Snyder GL,
- Nishi A,
- Yan Z,
- Meijer L,
- Fienberg AA,
- Tsai LH,
- Kwon YT,
- Le juge Girault,
- Czernik AJ,
- et al.
(1999) Nature (Londres) 402: 669 – 671.
- ↵
- Chen JS,
- Kelz MB,
- Zeng GQ,
- Sakai N,
- Steffen C,
- Shockett PE,
- Picciotto M,
- Duman RS,
- Nestler EJ
(1998) Mol Pharmacol 54: 495 – 503.
Résumé / Texte intégral GRATUIT
- ↵
- Kelz MB,
- Chen JS,
- Carlezon WA,
- Whisler K,
- Gilden L,
- Beckmann AM,
- Steffen C,
- Zhang YJ,
- Marotti L,
- Self SW,
- et al.
(1999) Nature (Londres) 401: 272 – 276.
- ↵
- Dobrazanski P,
- Noguchi T,
- Kovary K,
- Rizzo CA,
- Lazo PS,
- Bravo R
(1991) Mol Cell Biol 11: 5470 – 5478.
Résumé / Texte intégral GRATUIT
- Nakabeppu Y,
- Nathans D
(1991) Cellule 64: 751 – 759.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Yen J,
- Sagesse RM,
- Tratner I,
- Verma IM
(1991) Proc Natl Acad Sci USA 88: 5077 – 5081.
Résumé / Texte intégral GRATUIT
- ↵
- Blanc FJ,
- Hu XT,
- Zhang XF,
- Wolf ME
(1995) J Pharmacol Exp Ther 273: 445 – 454.
Résumé / Texte intégral GRATUIT
- ↵
- Hyman SE
(1996) Neuron 16: 901 – 904.
- Kreek MJ
(1997) Pharmacol Biochem Behav 57: 551 – 569.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Shippenberg TS,
- Rea W
(1997) Pharmacol Biochem Behav 57: 449 – 455.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Chen JS,
- Zhang YJ,
- Kelz MB,
- Steffen C,
- Ang ES,
- Zeng L,
- Nestler EJ
(2000) J Neurosci 20: 8965 – 8971.
Résumé / Texte intégral GRATUIT
- ↵
- Le juge Bibb,
- Chen JS,
- Taylor JR,
- Svenningsson P,
- Nishi A,
- Snyder GL,
- Yan Z,
- Sagawa ZK,
- Nairn AC,
- Nestler EJ,
- et al.
(2001) Nature (Londres) 410: 376 – 380.
- ↵
- Luscher C,
- Nicoll RA,
- Malenka RC,
- Muller D
(2000) Nat Neurosci 3: 545 – 550.
CrossRefMedlineDÉVELOPPEMENT de la science
- Malinow R,
- Mainen ZF,
- Hayashi Y
(2000) Actus Neurobiol 10: 352 – 357.
CrossRefMedlineDÉVELOPPEMENT de la science
- ↵
- Scannevin RH,
- Huganir RL
(2000) Rev Neurosci 1: 133 – 141.
CrossRefMedlineDÉVELOPPEMENT de la science
Robinson, TE et Kolb, B. (1999) (1997) EUR. J. Neurosci.11 1598-1604.
- ↵
- Carey M,
- Smale ST
(2000) Régulation transcriptionnelle chez les eucaryotes (Cold Spring Harbor Lab. Press, Plainview, NY).
- ↵
- Spencer VA,
- Davie JR
(1999) Gène 240: 1 – 12.
CrossRefMedlineDÉVELOPPEMENT de la science
Articles hébergés par HighWire Press citant cet article
- Natural and Drug Rewards Act sur les mécanismes de plasticité neuronale courants avec {Delta} FosB en tant que médiateur clé J. Neurosci. 2013 33 (8) 3434-3442
- Drogues, crime et épigénétique de l'allostase hédonique Journal de la justice pénale contemporaine 2012 28 (3) 314-328
- Abstract
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- Abstract
- Texte intégral (HTML)
- Texte intégral (PDF)
- La Morphine Active La Voie Des Facteurs De Réponse Du Sérum Facteur De Transcription De Twingt Six Comme X-XUMX / Sérum via Des Kinases Extracellulaires De Signal Régulé-Signal 1 / 1 Dans Des Cellules F2 Dérivées De Neurones Des Ganglions Racinaires Dorsaux J. Pharmacol. Exp. Ther. 2012 342 (1) 41-52
- Mécanisme moléculaire pour une drogue d'introduction: changements épigénétiques initiés par l'expression génique de la nicotine par la cocaïne Sci Transl Med 2011 3 (107) 107ra109
- Auto-administration améliorée du saccharose et de la cocaïne et recherche de drogues induite par un indice après la perte de VGLUT2 dans les neurones de la dopamine du cerveau moyen chez la souris J. Neurosci. 2011 31 (35) 12593-12603
- L'hypoxie intermittente chronique augmente la pression artérielle et l'expression de FosB / {Delta} FosB dans les régions autonomes centrales Un m. J. Physiol. Regul. Intégré. Comp. Physiol. 2011 301 (1) R131-R139
- L'absence du récepteur GPR37 / PAEL altère la phosphorylation striatale de l'Akt et ERK2, l'expression du {Delta} FosB et la préférence de l'endroit conditionné pour l'amphétamine et la cocaïne FASEB J. 2011 25 (6) 2071-2081
- La relation entre la durée de l’exposition initiale à l’alcool et la persistance de la tolérance moléculaire est nettement non linéaire J. Neurosci. 2011 31 (7) 2436-2446
- Imagerie De Bioluminescence In Vivo Révèle L'activation De Protéine-1 Activateur Redox Régulé Dans Le Noyau Paraventriculaire De Souris Avec L'hypertension Rénovasculaire Hypertension 2011 57 (2) 289-297
- Surexpression striatale de {Delta} FosB reproduit des mouvements involontaires chroniques induits par la lévodopa J. Neurosci. 2010 30 (21) 7335-7343
- Médiation épigénétique des influences environnementales dans les troubles psychotiques majeurs Schizophr Bull 2009 35 (6) 1045-1056
- Sondes IRM à base d'ADN pour la détection spécifique de l'exposition chronique à l'amphétamine dans le cerveau vivant J. Neurosci. 2009 29 (34) 10663-10670
- Modification De La Plasticité De La Colonne Dendritique Chez Des Rats Retirés À La Cocaïne J. Neurosci. 2009 29 (9) 2876-2884
- Écran De Surexpression Chez La Drosophile Identifie Les Rôles Neuronaux De GSK-3 {beta} / shaggy Comme Régulateur De La Plasticité Du Développement Dépendante De AP-1 Génétique 2008 180 (4) 2057-2071
- Transcription MRI: Une nouvelle vision du cerveau vivant Neuroscientifique 2008 14 (5) 503-520
- {Delta} Induction FosB Dans Le Cortex Orbitofrontal Indique La Tolérance Aux Dysfonctions Cognitives Induites Par La Cocaïne J. Neurosci. 2007 27 (39) 10497-10507
- Vulnérabilité persistante au rétablissement du comportement de recherche de méthamphétamine chez des souris mutantes du facteur neurotrophique dérivé de lignées cellulaires gliales FASEB J. 2007 21 (9) 1994-2004
- {Delta} FosB dans le noyau Accumbens réglemente le comportement et la motivation instrumentaux renforcés par les aliments J. Neurosci. 2006 26 (36) 9196-9204
- Régulation de la stabilité {Delta} FosB par phosphorylation. J. Neurosci. 2006 26 (19) 5131-5142
- Expression Des Récepteurs NMDA Mutants Dans Les Cellules Contenant Des Récepteurs De La Dopamine D1 Empêche La Sensibilisation De La Cocaïne Et Diminue La Préférence De La Cocaïne J. Neurosci. 2005 25 (28) 6651-6657
- Récepteurs De La Dopamine D1 Modulent {Delta} Induction FosB Dans Le Striatum De Rat Après L'administration De Morphine Intermittente J. Pharmacol. Exp. Ther. 2005 314 (1) 148-154
- Neurobiologie Des Souris Sélectionnées Pour Une Activité Volontaire Volant Élevée Intégré. Comp. Biol. 2005 45 (3) 438-455
- Effets de la privation d'eau et de la réhydratation sur la coloration de c-Fos et FosB dans le noyau supraoptique du rat et la région de la lamina terminalis Un m. J. Physiol. Regul. Intégré. Comp. Physiol. 2005 288 (1) R311-R321
- Induction Transcriptionnelle Du Gène FosB / {Delta} FosB Par Le Stress Mécanique Chez Les Ostéoblastes J Biol Chem 2004 279 (48) 49795-49803
- Induction de {Delta} FosB dans les structures cérébrales liées aux récompenses après un stress chronique J. Neurosci. 2004 24 (47) 10594-10602
- Le dosage du gène Sim1 module la réponse alimentaire homéostatique à une augmentation des graisses alimentaires chez la souris Un m. J. Physiol. Endocrinol. Metab. 2004 287 (1) E105-E113
- Analyse par micropuce d'ADN de l'expression des gènes dans les astrocytes de la tête du nerf optique chez l'homme en réponse à la pression hydrostatique Physiol. Génomique 2004 17 (2) 157-169
- Superoxyde Est Impliqué Dans L'activation Du Système Nerveux Central Et Sympathoexcitation De L'insuffisance Cardiaque Induite Par L'infarctus Du Myocarde Circ. Res. 2004 94 (3) 402-409
- Récepteurs de l'adénosine A2A dans la neuroadaptation à une stimulation dopaminergique répétée: implications pour le traitement des dyskinésies dans la maladie de Parkinson Neurologie 2003 61 (90116) S74-81
- Cytoplasmic Versus Nuclear Localisation De Protéines Liés à Fos Chez La Grenouille, Rana Esculenta, Testicules: In Vivo Et Direct In Vitro Effet D'un Agoniste De L'hormone De Libération Des Gonadotropines Biol. Reprod. 2003 68 (3) 954-960
- Des souris péri-adolescentes présentent une régulation à la hausse de Delta FosB en réponse à la cocaïne et à l'amphétamine J. Neurosci. 2002 22 (21) 9155-9159
- Delta FosB régule la roue J. Neurosci. 2002 22 (18) 8133-8138
- L’activité de CREB dans la coquille du noyau accumbens contrôle la synchronisation des réponses comportementales aux stimuli émotionnels Proc. Natl. Acad. Sci. États-Unis 2002 99 (17) 11435-11440
- Psychogénomique: Opportunités pour comprendre la dépendance J. Neurosci. 2001 21 (21) 8324-8327