KOMMENTAREN: Wéi spéider Studien weisen, ass DeltaFosB de gemeinsame molekulare Schalter fir béid Drogen- a Verhalenssucht. Et ass en Transkriptiounsfaktor wat heescht datt et beaflosst wéi eng Genen op oder ausgeschalt ginn. Wéi soss anzwousch gesot, süchteg Drogen kapéieren nëmmen normale Mechanismen. Dofir ass et domm ze suggeréieren datt Verhalenssucht net existéiere kënnen.
Proc Natl Acad Sci US A. 2001 25. September; 98 (20): 11042-11046.
doi: 10.1073/pnas.191352698.
Eric J. Nestler*, Michel Barrot, and David W. Self
Department of Psychiatry and Center for Basic Neuroscience, University of Texas Southwestern Medical Center, 5323 Harry Hines Boulevard, Dallas, TX 75390-9070
mythologesch
D'Längegkeet vun e puer vun de Verhalensabnormalitéiten, déi Drogenofhängegkeet charakteriséieren, huet virgeschloen datt d'Reguléierung vum neurale Genausdrock an de Prozess involvéiert ka sinn, duerch deen Drogen vu Mëssbrauch e Staat vun der Sucht verursaachen. echSteigerend Beweiser hindeit datt den Transkriptiounsfaktor ΔFosB ee Mechanismus duerstellt, duerch deen Drogen vu Mëssbrauch relativ stabil Verännerungen am Gehir produzéieren, déi zum Suchtphenotyp bäidroen. ΔFosB, Member vun der Fos Famill vun Transkriptiounsfaktoren, accumuléiert an engem Ënnerdeel vun Neuronen vum Nukleus accumbens an dorsalen Striatum (Gehirregiounen wichteg fir Sucht) no widderholl Administratioun vu villen Aarte vu Mëssbrauch. Ähnlech Akkumulation vun ΔFosB geschitt nom compulsive Lafen, wat suggeréiert datt ΔFosB ka accumuléieren an Äntwert op vill Aarte vu compulsive Behuelen. Wichteg ass datt ΔFosB an Neuronen fir relativ laang Perioden bestoe wéinst senger aussergewéinlecher Stabilitéit. Dofir stellt ΔFosB e molekulare Mechanismus duer, dee Verännerungen am Genausdrock kéint initiéieren an dann erhalen, déi laang no der Drogenbelaaschtung ophalen. Studien an induzéierbaren transgene Mais, déi entweder ΔFosB oder e dominanten negativen Inhibitor vum Protein iwwerausdrécken, liwweren direkt Beweiser datt ΔFosB erhéicht Sensibilitéit fir d'Verhalenseffekter vun Drogen vu Mëssbrauch verursaacht a méiglecherweis erhéicht Medikament sichen Verhalen. Dës Aarbecht ënnerstëtzt d'Vue datt ΔFosB funktionéiert als eng Zort nohalteg "molekulare Schalter", déi graduell akut Medikamentreaktiounen an relativ stabile Adaptatiounen konvertéiert, déi zu der laangfristeg neural a Verhalensplastizitéit bäidroen, déi d'Sucht ënnersträicht.
Suchtfuerschung konzentréiert sech op d'komplizéiert Weeër ze verstoen, wéi Drogen vu Mëssbrauch d'Gehir änneren fir Verhalensabnormalitéiten ze verursaachen, déi Sucht charakteriséieren. Ee vun de kriteschen Erausfuerderungen am Feld ass relativ stabil Drogen-induzéiert Verännerungen am Gehir z'identifizéieren fir dës Verhalensabnormalitéiten ze berechnen, déi besonnesch laang liewen. Zum Beispill, e Mënsch Sucht kann e erhéicht Risiko fir Réckwee sinn och no Joere vun Abstinenz.
D'Stabilitéit vun dëse Verhalensabnormalitéiten huet zum Virschlag gefouert datt se op d'mannst deelweis duerch Verännerungen am Genausdrock vermëttelt kënne ginn (1-3). No dëser Vue stéiert widderholl Belaaschtung vun engem Medikament vu Mëssbrauch ëmmer erëm d'Transmissioun bei bestëmmte Synapsen am Gehir, déi sensibel fir d'Droge sinn. Esou Perturbatiounen signaliséieren schlussendlech iwwer intrazellulär Messenger Kaskaden un de Kär, wou se als éischt d'Verännerungen am Ausdrock vu spezifesche Genen initiéieren an dann erhalen. E primäre Mechanismus, duerch deen d'Signaltransduktiounsweeër den Genausdrock beaflossen, ass d'Regulatioun vun Transkriptiounsfaktoren, Proteinen déi sech un reglementaresche Regioune vun Genen binden an hir Transkriptioun änneren.
Ee Zil vun der Suchtfuerschung war dofir d'Transkriptiounsfaktoren z'identifizéieren, déi an de Gehirregiounen verännert ginn, déi an der Sucht implizéiert sinn no chronescher Verwaltung vun Drogen vu Mëssbrauch. Verschidde sou Transkriptiounsfaktoren goufen an de leschte Jorzéngt identifizéiert (1-6). De Fokus vun dëser Iwwerpréiwung ass op ee bestëmmte Transkriptiounsfaktor genannt ΔFosB.
Induktioun vun ΔFosB duerch Drogen vu Mëssbrauch
ΔFosB, kodéiert vum fosB Gen, ass e Member vun der Fos Famill vun Transkriptiounsfaktoren, déi och c-Fos, FosB, Fra1, a Fra2 enthalen (7). Dës Fos Famill Proteinen heterodimerize mat Jun Famill Proteinen (c-Jun, JunB oder JunD) fir aktiv AP-1 (Aktivator Protein-1) Transkriptiounsfaktoren ze bilden, déi un AP-1 Site binden (Konsens Sequenz: TGAC / GTCA) präsent an d'Promoteuren vu bestëmmte Genen fir hir Transkriptioun ze reguléieren.
Dës Fos-Famillproteine ginn séier a transient an spezifesch Gehirregiounen induzéiert no enger akuter Verwaltung vu villen Drogen vu Mëssbrauch (Fig. 1) (8-11). Prominent Regiounen sinn den Nukleus accumbens an dorsalen Striatum, déi wichteg Vermëttler vu Verhalensreaktiounen op d'Drogen sinn, besonnesch hir belountend a lokomotoraktivéierend Effekter (12, 13). Dës Proteine ginn zréck op de Basalniveau bannent Stonnen no der Drogenverwaltung.
Figure 1
Schema weist déi graduell Akkumulation vun ΔFosB versus déi séier an transient Induktioun vun anere Fos Famill Proteinen als Äntwert op Drogen vu Mëssbrauch. (A) Den Autoradiogramm illustréiert d'Differentialinduktioun vun dëse verschiddene Proteinen duerch akuter Stimulatioun (1-2 Stonnen no enger eenzeger Drogenbelaaschtung) versus chronescher Stimulatioun (1 Dag no widderholl Drogenexpositioun). (B) Verschidde Wellen vu Fos-ähnlechen Proteinen [besteet aus c-Fos (52- bis 58-kDa Isoformen), FosB (46- bis 50-kDa Isoformen), ΔFosB (33-kDa Isoform), a Fra1 oder Fra2 ( 40 kDa)] ginn an nucleus accumbens an dorsale striatal Neuronen induzéiert duerch akuter Administratioun vun engem Medikament vu Mëssbrauch. Och induzéiert sinn biochemesch modifizéiert Isoforme vun ΔFosB (35-37 kDa); och si ginn induzéiert (obwuel op nidderegen Niveauen) no akuter Drogenverwaltung, awer behalen am Gehir fir laang Perioden wéinst hirer Stabilitéit. (C) Mat widderholl (zB zweemol deeglech) Drogenverwaltung, induzéiert all akute Stimulus e nidderegen Niveau vun de stabile ΔFosB Isoformen, wat duerch den ënneschten Set vun iwwerlappende Linnen ugewise gëtt, déi ΔFosB induzéiert vun all akuter Reiz. D'Resultat ass eng graduell Erhéijung vun den Gesamtniveauen vun ΔFosB mat widderholl Reizen während engem Cours vun der chronescher Behandlung, wat duerch d'Erhéijung vun der gesteppte Linn an der Grafik uginn.
Ganz ënnerschiddlech Äntwerte ginn no chronescher Verwaltung vun Drogen vu Mëssbrauch gesi (Fig. 1). Biochemesch modifizéiert Isoforme vun ΔFosB (molekulare Mass 35-37 kDa) accumuléieren an deene selwechte Gehirregiounen no widderholl Drogenbelaaschtung, wärend all aner Fos Familljemembere Toleranz weisen (dat ass reduzéiert Induktioun am Verglach mat initialen Drogenexpositiounen). Esou Akkumulation vun ΔFosB gouf fir Kokain, Morphin, Amphetamin, Alkohol, Nikotin a Phencyclidin observéiert.e (11, 14–18). Et gëtt e puer Beweiser datt dës Induktioun selektiv ass fir den Dynorphin / Substanz P-haltege Subset vu mëttleren spiny Neuronen, déi an dëse Gehirregiounen lokaliséiert sinn (15, 17), obwuel méi Aarbecht gebraucht gëtt fir dëst mat Sécherheet ze etabléieren. D'35- bis 37-kDa Isoforme vun ΔFosB dimeriséieren haaptsächlech mat JunD fir en aktiven a laang dauerhafte AP-1 Komplex an dëse Gehirregiounen ze bilden (19, 20). Dës ΔFosB Isoformen accumuléieren mat chronescher Drogenbelaaschtung wéinst hiren aussergewéinlech laangen Hallefzäiten (21), a bestoe sech dofir an den Neuronen op d'mannst e puer Wochen no der Stéierung vun der Medikamentverwaltung. Et ass interessant ze notéieren datt dës ΔFosB Isoformen héich stabil Produkter vun engem direkt fréi Gen (fosB) sinn. D'Stabilitéit vun den ΔFosB Isoformen liwwert en neie molekulare Mechanismus, duerch deen Drogen-induzéiert Verännerungen am Genausdrock kënne bestoe trotz relativ laangen Perioden vum Medikamententzuch.
Och wann de Nukleus accumbens eng kritesch Roll bei de belountende Effekter vun Drogen vu Mëssbrauch spillt, gëtt ugeholl datt se normalerweis funktionnéieren andeems d'Reaktiounen op natierleche Verstäerker reguléieren, wéi Iessen, Drénken, Sex a sozial Interaktiounen (12, 13). Als Resultat gëtt et e wesentlechen Interessi un eng méiglech Roll vun dëser Gehirregioun an aner compulsive Verhalen (zB pathologesch Iwwereess, Spillen, Übung, etc.). Aus dësem Grond hu mir iwwerpréift ob ΔFosB an engem Déiermodell vu compulsive Lafen geregelt ass. Tatsächlech ginn déi stabil 35- bis 37-kDa Isoforme vun ΔFosB selektiv am Nukleus accumbens a Ratten induzéiert, déi compulsivt Lafverhalen weisen.†
Biochemesch Identitéit vu stabile ΔFosB Isoformen
Wéi uewen ernimmt, weisen d'ΔFosB Isoformen, déi no chronescher Verwaltung vun engem Medikament vu Mëssbrauch oder compulsive Lafen accumuléieren, eng molekulare Mass vun 35-37 kDa. Si kënne vun der 33-kDa Isoform vun ΔFosB differenzéiert ginn, déi séier awer transient no enger eenzeger Drogenbelaaschtung induzéiert gëtt (Fig. 1) (14, 19, 22). Aktuell Beweiser hindeit datt d'33-kDa Isoform déi gebierteg Form vum Protein ass, wat geännert gëtt fir déi méi stabil 35- bis 37-kDa Produkter ze bilden (19, 21). Wéi och ëmmer, d'Natur vun der biochemescher Modifikatioun déi déi onbestänneg 33-kDa Isoform an déi stabil 35- bis 37-kDa Isoforme konvertéiert ass obskur bliwwen. Et gouf spekuléiert datt d'Phosphorylatioun verantwortlech ass (11). Zum Beispill, Induktioun vun ΔFosB ass ofgeschwächt bei Mais déi DARPP-32 feelen, e striatal-beräichert Protein (23, 24). Well DARPP-32 d'katalytesch Aktivitéit vu Proteinphosphatase-1 a Proteinkinase A (25, 26) reguléiert, proposéiert d'Ufuerderung fir dëst Protein fir déi normal Akkumulation vun de stabile ΔFosB Isoformen eng méiglech Roll fir Phosphorylatioun bei der Generatioun vun dëse stabile Produkter.
D'Roll vun ΔFosB an der Verhalensplastizitéit zu Drogen vu Mëssbrauch
Asiicht an d'Roll vun ΔFosB an der Drogenofhängeger ass gréisstendeels aus der Studie vun transgene Mais komm, an deenen ΔFosB selektiv an de Nukleus accumbens an aner striatal Regioune vun erwuessene Déieren induzéiert kënne ginn (27, 28). Wichteg sinn dës Mais ΔFosB selektiv an den Dynorphin / Substanz P-haltege mëttleren spiny Neuronen auszedrécken, wou d'Drogen gegleeft ginn de Protein ze induzéieren. De Verhalensphenotyp vun den ΔFosB-iwwerexpresséierende Mais, déi op vill Manéiere wéi Déieren no chronescher Drogenbelaaschtung ähnelt, gëtt an der Tabell 1 zesummegefaasst. D'Mais weisen augmentéiert Lokomotorreaktiounen op Kokain no akuter a chronescher Administratioun (28). Si weisen och eng verstäerkte Sensibilitéit fir déi belountend Effekter vu Kokain a Morphin a Plazbedéngungsanalysen (11, 28) a wäerte selbstverständlech méi niddereg Dosen Kokain verwalten wéi d'Littermates déi ΔFosB net iwwerausdrécken. ‡ Am Géigesaz weisen dës Déieren normal bedingte Lokomotor Sensibiliséierung fir Kokain an normal raimlech Léieren am Morris Waasserlabyrint (28). TDës Donnéeë weisen datt ΔFosB d'Sensibilitéit vun engem Déier fir Kokain a vläicht aner Drogen vu Mëssbrauch erhéicht a kann e Mechanismus representéieren fir relativ länger Sensibiliséierung fir d'Drogen.
 Striatum
Striatum
| Erhéicht Lokomotoraktivéierung als Äntwert op akuter a widderholl Kokainverwaltung. |
| Erhéicht belountend Äntwerten op Kokain a Morphin a Plazbedingungsanalysen. |
| Erhéicht Selbstverwaltung vu geréng Dosen Kokain. |
| Erhéicht Motivatioun fir Kokain a progressive Verhältnis Assays. |
| Erhéicht anxiolytesch Reaktiounen op Alkohol. |
| Erhéicht compulsive Lafverhalen. |
Baséiert op Daten an Ref. 28 an 29.†‡§¶
Verhale Plastizitéit vermittelt duerch ΔFosB am Nucleus accumbens-dorsal Striatum
IZousätzlech gëtt et virleefeg Beweiser datt d'Effekter vum ΔFosB wäit iwwer eng Reguléierung vun der Drogenempfindlechkeet per se op méi komplex Verhalen am Zesummenhang mam Suchtprozess kënne verlängeren. Mais, déi ΔFosB ausdrécken, schaffen méi haart fir Kokain selwer ze verwalten a progressive Verhältnis Selbstverwaltungsanalysen, suGestioun datt ΔFosB Déiere fir d'Incitatiounsmotivatiounseigenschaften vu Kokain sensibiliséieren kann an doduerch zu enger Tendenz fir Réckwee nom Drogenentzéiung féierenl.‡ ΔFosB-ausdréckende Mais weisen och verstäerkte anxiolytesch Effekter vum Alkohol, § e Phänotyp dee mat enger verstäerkter Alkoholkonsum bei Mënschen assoziéiert gouf. Zesummen suggeréieren dës fréi Erkenntnisser datt ΔFosB, nieft der Erhéijung vun der Sensibilitéit fir Drogen vu Mëssbrauch, qualitativ Verännerungen am Verhalen produzéiert, déi Drogen-Sich Verhalen förderen. Also kann ΔFosB als en nohaltege "molekulare Schalter" funktionnéieren deen hëlleft entscheedend Aspekter vum süchtege Staat ze initiéieren an dann z'erhalen. Eng wichteg Fro ënner der aktueller Untersuchung ass ob ΔFosB Akkumulation wärend der Drogenbelaaschtung d'Drogen-Sich Verhalen fördert no verlängerten Réckzuchsperioden, och nodeems d'ΔFosB Niveauen normaliséiert sinn (kuckt hei ënnen).
erwuessener Mais déi ΔFosB selektiv am Nucleus accumbens an dorsalen Striatum iwwerausdrécken, weisen och méi compulsive Lafen am Verglach mat Kontrolllittermates. Verhalen, vläicht duerch d'Verstäerkung vun der Effizienz vun neurale Circuiten, an deenen dës Neuronen funktionnéieren.
ΔFosB accumuléiert a bestëmmte Gehirregiounen ausserhalb vum Nukleus accumbens an dorsalen Striatum no chronescher Belaaschtung fir Kokain. Prominent ënnert dësen Regioune sinn d'Amygdala a medial prefrontal Cortex (15). E wichtegt Zil vun der aktueller Fuerschung ass d'Bäiträg vun der ΔFosB Induktioun an dëse Regiounen zum Suchtphenotyp ze verstoen.
Fréier Aarbechten op fosB Knockout Mais hunn opgedeckt datt dës Déieren d'Sensibiliséierung fir d'Lokomotor Effekter vu Kokain net entwéckelen, wat konsequent mat den Erkenntnisser vun den ΔFosB-iwwerexpressende Mais uewe genannt ass (22). Wéi och ëmmer, d'fosB Mutanten hunn eng verstäerkte Sensibilitéit fir den akuten Effekter vum Kokain gewisen, wat inkonsequent mat dësen anere Befunde ass. D'Interpretatioun vun de Befunde mat de fosB Mutanten ass awer komplizéiert vun der Tatsaach datt dës Déieren net nëmmen ΔFosB feelen, awer och FosB voll Längt. Ausserdeem feelen d'Mutanten béid Proteinen am ganze Gehir a vun de fréiste Stadien vun der Entwécklung. Tatsächlech ënnerstëtzt méi rezent Aarbecht Conclusiounen vun den ΔFosB iwwerausdrockende Mais: induzéierbar Iwwerexpressioun vun engem ofgeschniddene Mutant vum c-Jun, deen als dominante negativen Antagonist vun ΔFosB wierkt, selektiv am Nukleus accumbens an dorsalen Striatum weist reduzéiert Sensibilitéit fir d'belountend Effekter vu Kokain. .¶ Dës Erkenntnisser ënnersträichen d'Virsicht, déi benotzt musse bei der Interpretatioun vu Resultater vu Mais mat konstitutiven Mutatiounen an illustréieren d'Wichtegkeet vu Mais mat induzéierbaren an Zelltypspezifesche Mutatiounen an Studien iwwer Plastizitéit am erwuessene Gehir.
Zil Genen fir ΔFosB
Well ΔFosB en Transkriptiounsfaktor ass, verursaacht vermutlech de Protein Verhalensplastizitéit duerch Ännerungen am Ausdrock vun anere Genen. ΔFosB gëtt generéiert duerch alternativ Splicing vum fosB Gen a feelt en Deel vum C-terminalen Transaktivéierungsdomän präsent a voller Längt FosB. Als Resultat gouf et ursprénglech proposéiert datt ΔFosB als Transkriptiounsrepressor funktionnéiert (29). Wéi och ëmmer, d'Aarbecht an der Zellkultur huet kloer bewisen datt ΔFosB kann entweder induzéieren oder represséieren AP-1-mediéiert Transkriptioun ofhängeg vun der bestëmmter AP-1 Site benotzt (21, 29-31). Voll-Längt FosB übt déiselwecht Effekter wéi ΔFosB op bestëmmte Promoteur Fragmenter, awer verschidden Effekter op anerer. Weider Aarbecht ass gebraucht fir d'Mechanismen ze verstoen, déi dës variéiert Handlunge vun ΔFosB a FosB ënnersträichen.
Eis Grupp huet zwou Approche benotzt fir Zilgenen fir ΔFosB z'identifizéieren. Eent ass d'Kandidat Gen Approche. Mir hunn ufanks α-Amino-3-Hydroxy-5-Methyl-4-Isoxazolpropionsäure (AMPA) Glutamatrezeptoren als putativ Ziler ugesinn, wéinst der wichteger Roll vun der glutamatergescher Iwwerdroung am Nukleus accumbens. Aarbecht bis haut huet uginn datt eng bestëmmten AMPA Glutamat Rezeptor Ënnerunitéit, GluR2, e bona fide Zil fir ΔFosB ka sinn (Fig. 2). GluR2 Ausdrock, awer net den Ausdrock vun aneren AMPA Rezeptor Ënnerunitéiten, gëtt am Nucleus accumbens erhéicht (awer net dorsalen Striatum) op Iwwerexpressioun vun ΔFosB (28), an Ausdrock vun engem dominanten negativen Mutant attenuéiert d'Fäegkeet vu Kokain fir de Protein ze induzéieren.¶ Zousätzlech enthält de Promoteur vum GluR2 Gen e Konsens AP-1 Site deen ΔFosB bindt (28). Iwwerexpressioun vu GluR2 am Nukleus accumbens, duerch Benotzung vu viral-mediéierten Gentransfer, erhéicht d'Sensibilitéit vun engem Déier fir déi belountend Effekter vu Kokain, an doduerch en Deel vum Phänotyp, deen an den ΔFosB-ausdréckende Mais gesi gëtt (28). D'Induktioun vu GluR2 konnt d'reduzéiert elektrophysiologesch Sensibilitéit vun den Nukleus accumbens Neuronen op AMPA Rezeptor Agonisten no chronescher Kokainverwaltung (32) berücksichtegen, well AMPA Rezeptoren enthalen GluR2 weisen reduzéierter Gesamtkonduktioun a reduzéierter Ca2+ Permeabilitéit. Reduzéiert Reaktiounsfäegkeet vun dësen Neuronen op excitatoresch Input kënnen dann d'Äntwerten op e Medikament vu Mëssbrauch verbesseren. Wéi och ëmmer, d'Weeër wéi dopaminergesch a glutamatergesch Signaler am Nukleus accumbens süchteg Verhalen reguléieren bleiwen onbekannt; dëst wäert en neurale Circuitniveau vum Verständnis erfuerderen, wat nach net verfügbar ass.
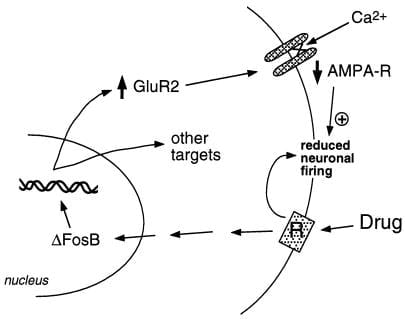
Figure 2
D'AMPA Glutamat Rezeptor Ënnerunitéit, GluR2, ass e putativt Zil fir ΔFosB. Gewise gëtt wéi ΔFosB-mediéiert Induktioun vu GluR2 d'physiologesch Reaktiounsfäegkeet vun den Nukleus accumbens Neuronen verännere kann an zu sensibiliséierte Reaktiounen op Drogen vu Mëssbrauch féieren. No dësem Schema produzéieren Drogen vu Mëssbrauch hir akut Verstäerkungseffekter iwwer Inhibitioun vun Nukleus accumbens Neuronen. Mat widderholl Belaaschtung induzéieren d'Drogen ΔFosB, wat vill Zilgenen reguléiert, dorënner GluR2. Dëst erhéicht den Undeel vun AMPA Rezeptoren (AMPA-R) op Nukleus accumbens Neuronen, déi d'GluR2 Ënnerunitéit enthalen, wat reduzéiert allgemeng AMPA Stroum a reduzéiert Ca2+ Stroum verursaacht. Dës reduzéiert Excitabilitéit kéint d'Neuronen méi sensibel maachen fir déi akut hemmend Effekter vun den Drogen an doduerch op d'Verstäerkungseffekter vun den Drogen.
En anert putativt Zil fir ΔFosB ass de Gen deen Dynorphin kodéiert. Wéi virdru scho gesot, gëtt Dynorphin an der Ënnergrupp vun Nucleus accumbens mëttlere spiny Neuronen ausgedréckt, déi Induktioun vun ΔFosB weisen. Dynorphin schéngt an enger interzellulärer Feedback Loop ze funktionéieren: seng Verëffentlechung hemmt déi dopaminergesch Neuronen, déi déi mëttel spiny Neuronen innervéieren, iwwer κ opioid Rezeptoren, déi op dopaminergesche Nerveterminalen am Nukleus accumbens präsent sinn an och op Zellkierper an Dendriten am ventrale tegmental Beräich. (Fig. 3) (33-35). Dës Iddi ass konsequent mat der Fäegkeet vun engem κ Rezeptor Agonist, bei der Administratioun an entweder vun dësen zwou Gehirregiounen, Drogenrewarnung ze reduzéierend (35).
Recent Aarbecht huet uginn datt ΔFosB den Ausdrock vun Dynorphin erofgeet,‖ wat zu der Verbesserung vun de Belounungsmechanismen bäidroe kann mat ΔFosB Induktioun gesi ginn. Interessanterweis huet en aneren Drogen-geregelten Transkriptiounsfaktor, CREB (cAMP Response Element Binding Protein) (2, 3), de Géigendeel Effekt: et induzéiert Dynorphin Ausdrock am Nukleus accumbens a reduzéiert d'belountend Eegeschafte vu Kokain a Morphin (4).**
BWéinst Drogen-induzéierter Aktivatioun vum CREB verschwënnt séier no der Drogenverwaltung, sou eng géigesäiteg Reguléierung vun Dynorphin vum CREB an ΔFosB kéint déi géigesäiteg Verhalensverännerungen erklären, déi an de fréien a spéiden Phasen vum Réckzuch optrieden, mat negativen emotionalen Symptomer a reduzéierter Drogenempfindlechkeet, déi an de fréie Phasen dominéiert. vum Réckzuch, a Sensibiliséierung fir déi belountend an stimuléierend motivational Effekter vun Drogen, déi zu spéider Zäitpunkte dominéieren.
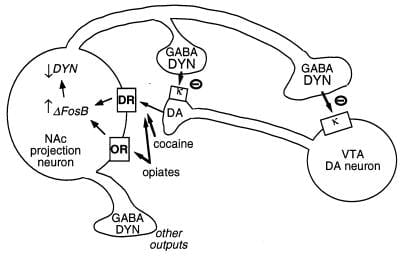
Figure 3
Dynorphin ass e putativt Zil fir ΔFosB. Gewise gëtt e ventraltegmental Gebitt (VTA) Dopamin (DA) Neuron, deen eng Klass vun Nukleus accumbens (NAc) innervéiert GABAergesch Projektiounsneuron déi Dynorphin (DYN) ausdréckt. Dynorphin servéiert e Feedbackmechanismus an dësem Circuit: Dynorphin, verëffentlecht vun den Terminaler vun den NAc Neuronen, wierkt op κ Opioid Rezeptoren, déi op Nerve Terminals an Zellkierper vun den DA Neuronen lokaliséiert sinn, fir hir Funktioun ze hemmen. ΔFosB, andeems d'Dynorphin Ausdrock hemmt, kann dës Feedback-Loop erofreguléieren an d'belountend Eegeschafte vun Drogen vu Mëssbrauch verbesseren. Net gewisen ass de géigesäitege Effekt vum CREB op dësem System: CREB verbessert d'Dynorphin-Ausdrock an schwächt doduerch déi belountend Eegeschafte vun Drogen vu Mëssbrauch (4). GABA, γ-Aminobutyrsäure; DR, Dopamin Rezeptor; ODER, opioid Rezeptor.
Déi zweet Approche benotzt fir Zilgenen fir ΔFosB z'identifizéieren involvéiert DNA Mikroarray Analyse. Inducibel Iwwerexpressioun vun ΔFosB erhéicht oder reduzéiert den Ausdrock vu ville Genen am Nukleus accumbens (36). Och wa bedeitend Aarbecht elo gebraucht gëtt fir all eenzel vun dësen Genen als physiologesch Ziler vun ΔFosB ze validéieren an hire Bäitrag zum Suchtphenotyp ze verstoen, schéngt e wichtegt Zil Cdk5 (cyclin-ofhängeg Kinase-5) ze sinn. Also gouf Cdk5 ufanks als ΔFosB-reguléiert duerch d'Benotzung vu Mikroarrays identifizéiert, a spéider gewisen datt se an Nukleus accumbens an dorsalen Striatum no chronescher Kokainverwaltung induzéiert ginn (37). ΔFosB aktivéiert den cdk5 Gen iwwer eng AP-1 Site präsent am Gen Promoteur (36). Zesummen ënnerstëtzen dës Donnéeën e Schema an deem Kokain den Cdk5 Ausdrock an dëse Gehirregiounen iwwer ΔFosB induzéiert. D'Induktioun vu Cdk5 schéngt d'Dopaminergesch Signaliséierung op d'mannst deelweis iwwer eng verstäerkte Phosphorylatioun vun DARPP-32 (37) z'änneren, déi vun engem Inhibitor vu Proteinphosphatase-1 an en Inhibitor vu Proteinkinase A op senger Phosphorylatioun duerch Cdk5 ëmgewandelt gëtt (26).
D'Roll vum ΔFosB bei der Mediatioun vun "permanent" Plastizitéit zu Drogen vu Mëssbrauch
Och wann den ΔFosB Signal relativ laang lieweg ass, ass et net permanent. ΔFosB degradéiert graduell a kann net méi am Gehir no 1-2 Méint vum Medikamententzug erkannt ginn, och wa verschidde Verhalensabnormalitéite fir vill méi laang Perioden bestoe bleiwen. Dofir schéngt ΔFosB per se net fäeg ze sinn dës semipermanent Verhalensabnormalitéiten ze vermëttelen. D'Schwieregkeet fir d'molekulare Adaptatiounen ze fannen, déi den extrem stabile Verhalensverännerunge mat der Sucht ënnersträichen, ass analog zu den Erausfuerderungen am Léier- a Gedächtnisfeld. Och wann et elegant cellulär a molekulare Modeller vu Léieren a Gedächtnis sinn, ass et bis elo net méiglech molekulare a cellulär Adaptatiounen z'identifizéieren déi genuch laang lieweg sinn fir héich stabil Verhalenserënnerungen ze berechnen. Tatsächlech ass ΔFosB déi längst lieweg Adaptatioun, déi bekannt ass am Erwuessene Gehir, net nëmmen als Äntwert op Drogen vu Mëssbrauch, awer och op all aner Stéierung (déi keng Läsionen involvéiert). Zwou Virschléi hunn evoluéiert, souwuel am Sucht a Léier- a Gedächtnisfelder, fir dës Diskrepanz ze berechnen.
Eng Méiglechkeet ass datt méi transient Verännerungen am Genausdrock, sou wéi déi vermittelt iwwer ΔFosB oder aner Transkriptiounsfaktoren (zB CREB), kënne méi laanglieweg Verännerungen an der neuronaler Morphologie a synaptescher Struktur vermëttelen. Zum Beispill, eng Erhéijung vun der Dicht vun dendritesch Wirbelsäule (besonnesch eng Erhéijung vun zwee-Kapp Wirbelsäule) begleet de erhéicht Effizienz vu glutamatergesche Synapsen bei hippocampal Pyramidal Neuronen während laangfristeg Potenzéierung (38-40), a parallel zu der verstäerkter Verhalensempfindlechkeet fir Kokain, déi um Niveau vun de mëttlere spiny Neuronen vun den Nukleus accumbens vermëttelt ginn (41). Et ass net bekannt ob esou strukturell Ännerungen genuch laang lieweg sinn fir héich stabile Verhalensverännerungen ze berechnen, obwuel déi lescht op d'mannst 1 Mount vum Medikamententzug bestoe bleiwen. Rezent Beweiser erhéijen d'Méiglechkeet datt ΔFosB, a seng Induktioun vu Cdk5, ee Vermëttler vun Drogen-induzéierter Verännerungen an der synaptescher Struktur am Nukleus accumbens ass (Fig. 4). Fäegkeet vun der widderholl Kokain Belaaschtung fir dendritesch Wirbelsäule Dicht an dëser Regioun ze erhéijen. Dëst ass konsequent mat der Meenung datt Cdk5, déi am Gehir beräichert ass, d'neural Struktur a Wuesstem reguléiert (kuckt Ref. 5 an 36). Et ass méiglech, obwuel op kee Fall bewisen ass, datt sou Ännerungen an der neuronaler Morphologie d'ΔFosB Signal selwer iwwerliewen.
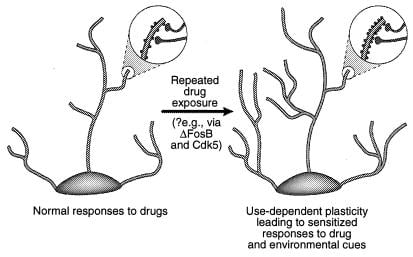
Figure 4
Reguléierung vun dendritesch Struktur duerch Drogen vu Mëssbrauch. Gewise gëtt d'Expansioun vun engem dendritesche Bam vun engem Neuron no chronescher Belaaschtung vun engem Medikament vu Mëssbrauch, wéi mat Kokain am Nukleus accumbens a prefrontal Cortex observéiert gouf (41). D'Gebidder vun der Vergréisserung weisen eng Erhéijung vun dendritesche Wirbelsäule, déi postuléiert gëtt a Verbindung mat aktivéierten Nerveterminalen. Dës Erhéijung vun der dendritescher Wirbelsituatioun kann iwwer ΔFosB vermëttelt ginn an déi konsequent Induktioun vu Cdk5 (kuckt Text). Esou Ännerungen an der dendritescher Struktur, déi ähnlech sinn wéi déi, déi an e puer Léiermodeller observéiert ginn (zB laangfristeg Potenzéierung), kéinte laanglieweg sensibiliséiert Äntwerten op Drogen vu Mëssbrauch oder Ëmweltstécker vermëttelen. [Reproduzéiert mat Erlaabnis vum Ref. 3 (Copyright 2001, Macmillian Magazines Ltd.)].
Eng aner Méiglechkeet ass datt déi transient Induktioun vun engem Transkriptiounsfaktor (zB ΔFosB, CREB) féiert zu méi permanente Verännerungen am Genausdrock duerch d'Modifikatioun vu Chromatin. Dës a vill aner Transkriptiounsfaktoren ginn ugeholl datt d'Transkriptioun vun engem Zilgen aktivéiert oder ënnerdréckt gëtt andeems d'Acetylatioun respektiv Deacetylatioun vun Histonen an der Géigend vum Gen fördert (42). Och wann esou Acetylatioun an Deacetylatioun vun Histonen anscheinend ganz séier kënne geschéien, ass et méiglech datt ΔFosB oder CREB méi laang dauerhaft Adaptatiounen an der enzymatesch Maschinn produzéieren déi d'Histone Acetylatioun kontrolléiert. ΔFosB oder CREB kënnen och méi laang lieweg Verännerungen am Genausdrock förderen andeems aner Chromatinmodifikatioune reguléieren (zB DNA oder Histon-Methylatioun), déi an de permanente Verännerunge vun der Gen-Transkriptioun implizéiert goufen, déi während der Entwécklung optrieden (kuckt Ref. 42 an 43) . Och wann dës Méiglechkeeten spekulativ bleiwen, kënnen se e Mechanismus ubidden, duerch deen transiente Adaptatiounen un e Medikament vu Mëssbrauch (oder eng aner Perturbatioun) zu wesentlech liewenslaang Verhalenskonsequenzen féieren.
Referenze
- ↵
- Nestler EJ,
- Hoffen BT,
- Widnell KL
(1993) Neuron 11:995-1006.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Berke JD,
- Hyman SE
(2000) Neuron 25:515-532.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Nestler EJ
(2001) Nat Rev Neurosci 2:119–128.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Carlezon WA Jr,
- Thome J,
- Olson VG,
- Lane-Ladd SB,
- Brodkin ES,
- Hiroi N,
- Duman RS,
- Neen RL,
- Nestler EJ
(1998) Science 282:2272-2275.
- O'Donovan KJ,
- Tourtellotte WG,
- Millbrandt J,
- Baraban JM
(1999) Trends Neurosci 22: 167-173.
- ↵
- Mackler SA,
- Korutla L,
- Cha XY,
- Koebbe MJ,
- Fournier KM,
- Bauer MS,
- Kalivas PW
(2000) J Neurosci 20:6210-6217.
- ↵
- Morgan JI,
- Curran T
(1995) Trends Neurosci 18: 66-67.
- ↵
- Young ST,
- Porrino LJ,
- Iadarola MJ
(1991) Proc Natl Acad Sci USA 88:1291-1295.
- Greybiel AM,
- Moratalla R,
- Robertson HA
(1990) Proc Natl Acad Sci USA 87:6912-6916.
- Hoffnung B,
- Kosofsky B,
- Hyman SE,
- Nestler EJ
(1992) Proc Natl Acad Sci USA 89:5764-5768.
- ↵
- Kelz MB,
- Nestler EJ
(2000) Curr Opin Neurol 13: 715-720.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Kob GF,
- Sanna PP,
- Blumm FE
(1998) Neuron 21:467-476.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Weis RA
(1998) Drogen Alkohol Ofhängegkeet 51: 13-22.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Hoffen BT,
- Nei HE,
- Kelz MB,
- Selbst DW,
- Iadarola MJ,
- Nakabeppu Y,
- Duman RS,
- Nestler EJ
(1994) Neuron 13:1235-1244.
- ↵
- Nei H,
- Hoffen BT,
- Kellz M,
- Iadarola M,
- Nestler EJ
(1995) J Pharmacol Exp Ther 275:1671-1680.
- Nei HE,
- Nestler EJ
(1996) Mol Pharmacol 49:636-645.
- ↵
- Moratalla R,
- Elibol B,
- Vallejo M,
- Greybiel AM
(1996) Neuron 17:147-156.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Pich EM,
- Pagliusi SR,
- Tessari M,
- Talabot-Ayer D,
- Hooft van Huijsduijnen R,
- Chiamulera C
(1997) Science 275:83-86.
- ↵
- Chen JS,
- Nei HE,
- Kelz MB,
- Hiroi N,
- Nakabeppu Y,
- Hoffen BT,
- Nestler EJ
(1995) Mol Pharmacol 48:880-889.
- ↵
- Hiroi N,
- Braun J,
- Ye H,
- Saudou F,
- Vaidya VA,
- Duman RS,
- Greenberg ME,
- Nestler EJ
(1998) J Neurosci 18:6952-6962.
- ↵
- Chen J,
- Kelz MB,
- Hoffen BT,
- Nakabeppu Y,
- Nestler EJ
(1997) J Neurosci 17:4933-4941.
- ↵
- Hiroi N,
- Braun J,
- Haile C,
- Ye H,
- Greenberg ME,
- Nestler EJ
(1997) Proc Natl Acad Sci USA 94:10397-10402.
- ↵
- Fienberg AA,
- Hiroi N,
- Mermelstein P,
- Lied WJ,
- Schneider GL,
- Nishi A,
- Cheramy A,
- O'Callaghan JP,
- Miller D,
- Cole DG,
- et al.
(1998) Science 281:838-842.
- ↵
- Hiroi N,
- Feinberg A,
- Haile C,
- Greengard P,
- Nestler EJ
(1999) Eur J Neurosci 11:1114-1118.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Greengard P,
- Allen PB,
- Nairn AC
(1999) Neuron 23:435-447.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Bibb JA,
- Schneider GL,
- Nishi A,
- Yan Z,
- Meijer L,
- Fienberg AA,
- Tsai LH,
- Kwon YT,
- Girault JA,
- Czernik AJ,
- et al.
(1999) Natur (London) 402:669-671.
- ↵
- Chen JS,
- Kelz MB,
- Zeng GQ,
- Sakai N,
- Steffen C,
- Schockett PE,
- Picciotto M,
- Duman RS,
- Nestler EJ
(1998) Mol Pharmacol 54:495-503.
- ↵
- Kelz MB,
- Chen JS,
- Carlezon WA,
- Whisler K,
- Gilden L,
- Beckmann AM,
- Steffen C,
- Zhang YJ,
- Marotti L,
- Selbst SW,
- et al.
(1999) Natur (London) 401:272-276.
- ↵
- Dobrazanski P,
- Noguchi T,
- Kovari K,
- Rizzo CA,
- Lazo PS,
- Bravo R
(1991) Mol Zell Biol 11: 5470-5478.
- Nakabeppu Y,
- Nathans D
(1991) Zell 64: 751-759.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Yen J,
- Wäisheet RM,
- Tratner I,
- Verma IM
(1991) Proc Natl Acad Sci USA 88:5077-5081.
- ↵
- Wäiss FJ,
- Hu XT,
- Zhang XF,
- Wolf ME
(1995) J Pharmacol Exp Ther 273:445-454.
- ↵
- Hyman SE
(1996) Neuron 16:901-904.
- Kreek MJ
(1997) Pharmacol Biochem Behav 57: 551-569.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Schiffenberg TS,
- Reen W
(1997) Pharmacol Biochem Behav 57: 449-455.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Chen JS,
- Zhang YJ,
- Kelz MB,
- Steffen C,
- Eng ES,
- Zeng L,
- Nestler EJ
(2000) J Neurosci 20:8965-8971.
- ↵
- Bibb JA,
- Chen JS,
- Taylor JR,
- Svenningsson P,
- Nishi A,
- Schneider GL,
- Yan Z,
- Sagawa ZK,
- Nairn AC,
- Nestler EJ,
- et al.
(2001) Natur (London) 410:376-380.
- ↵
- Luscher C,
- Nicoll RA,
- Malenka RC,
- Muller D
(2000) Nat Neurosci 3:545-550.
CrossRefMedlineweb vun der Wëssenschaft
- Malinow R,
- Mainen ZF,
- Haishi Y
(2000) Curr Opin Neurobiol 10: 352-357.
CrossRefMedlineweb vun der Wëssenschaft
- ↵
- Scannevin RH,
- Huganir RL
(2000) Nat Rev Neurosci 1:133–141.
CrossRefMedlineweb vun der Wëssenschaft
Robinson, TE & Kolb, B. (1999) (1997) EUR. J. Neurosci.11, 1598-1604.
- ↵
- Carey M,
- Kleng ST
(2000) Transkriptiounsreguléierung an Eukaryoten (Cold Spring Harbor Lab. Press, Plainview, NY).
- ↵
- Spencer VA,
- Davis JR
(1999) Gene 240:1–12.
CrossRefMedlineweb vun der Wëssenschaft
HighWire Press-gehaasst Artikelen an Artikelen
- Natierlech a Drogen Reweisen Gesetz iwwer gemeinsame Neural Plastizitéit Mechanismen mat {Delta} FosB als Key Mediator J. Neurosci. 2013 33 (8) 3434-3442
- Drogen, Kriminalitéit an d'Epigenetik vun der Hedonescher Allostasis Journal of Contemporary Criminal Justice 2012 28 (3) 314-328
- mythologesch
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- mythologesch
- Ganz Text (HTML)
- Komplett Text (PDF)
- Morphin Aktivéiert den E Twenty Six-Like Transcription Factor-1 / Serum Response Factor Pathway iwwer extrazellulär Signal-Reguléiert Kinasen 1/2 an F11 Zellen ofgeleet vun Dorsal Root Ganglia Neuronen J. Pharmacol. Exp. Ther. 2012 342 (1) 41-52
- Molekulare Mechanismus fir e Gateway Medikament: Epigenetesch Verännerungen initiéiert vum Nikotin Prime Gene Expression vu Kokain Sci Transl Med 2011 3 (107) 107ra109
- Verbesserte Saccharose a Kokain Selbstverwaltung a Cue-induzéiert Drogen Sich no Verloscht vu VGLUT2 an Midbrain Dopamin Neuronen a Mais J. Neurosci. 2011 31 (35) 12593-12603
- Chronesch intermittéiert Hypoxie erhéicht de Blutdrock an den Ausdrock vu FosB / Delta FosB an zentrale autonome Regiounen Am. J. Physiol. Regul. Integr. Komp. Physiol. 2011 301 (1) R131-R139
- Absence vum GPR37 / PAEL Rezeptor behënnert striatal Akt an ERK2 Phosphorylatioun, {Delta} FosB Ausdrock, a bedingte Plaz Präferenz fir Amphetamin a Kokain FASEB J. 2011 25 (6) 2071-2081
- D'Relatioun tëscht der Dauer vun der initialer Alkoholbeliichtung an der Persistenz vu molekulare Toleranz ass däitlech net-linear J. Neurosci. 2011 31 (7) 2436-2446
- In Vivo Biolumineszenz Imaging Enthüllt Redox-Reguléiert Aktivator Protein-1 Aktivatioun am Paraventrikuläre Nukleus vu Mais mat Renovaskulär Hypertonie Hypertonie 2011 57 (2) 289-297
- Striatal Iwwerausdréck vu {Delta} FosB reproduzéiert chronesch Levodopa-induzéiert ongewollte Bewegungen J. Neurosci. 2010 30 (21) 7335-7343
- Epigenetesch Mediatioun vun Ëmweltinfluenzen a Major Psychotic Disorders Schizophr Bull 2009 35 (6) 1045-1056
- DNA-baséiert MRI Sonde fir spezifesch Detektioun vu chronescher Belaaschtung fir Amphetamin a liewegen Gehirn J. Neurosci. 2009 29 (34) 10663-10670
- Verännert dendritesch Wirbelsäule Plastizitéit bei Kokain zréckgezunn Ratten J. Neurosci. 2009 29 (9) 2876-2884
- Overexpression Écran an Drosophila identifizéiert Neuronal Rollen vum GSK-3 {beta} / shaggy als Regulator vun AP-1-ofhängeg Entwécklungsplastizitéit Genetik 2008 180 (4) 2057-2071
- Transkription MRI: E Neie Bléck op de Living Brain Neuroscientist 2008 14 (5) 503-520
- {Delta} FosB Induktioun am Orbitofrontal Cortex vermëttelt Toleranz fir Kokain-induzéiert kognitiv Dysfunktioun J. Neurosci. 2007 27 (39) 10497-10507
- D'Verlängerung vu Schwieregkeeten fir d'Wiederhuelung vum Methamphetaminsusverhalen am glialen Zellzeil vun der neurotrophen Faktore mutéiert Mais FASEB J. 2007 21 (9) 1994-2004
- {Delta} FosB am Nucleus Accumbens regelt Nahrung verstäerkt Instrumental Verhalt an Motivatioun J. Neurosci. 2006 26 (36) 9196-9204
- Reglement vun {Delta} FosB Stabilitéit duerch Phosphorylatioun. J. Neurosci. 2006 26 (19) 5131-5142
- Ausdrock vu Mutant NMDA Rezeptoren an Dopamin D1 Rezeptor-enthale Zellen verhënnert Kokain Sensibiliséierung a reduzéiert Kokain Präferenz J. Neurosci. 2005 25 (28) 6651-6657
- D1 Dopamine Receptoren Moduléieren {Delta} FosB Induktioun am Rots Striatum no der intermittierender Morphinatiounsverwaltung J. Pharmacol. Exp. Ther. 2005 314 (1) 148-154
- Neurobiologie vu Mäuser déi fir eng fräiwëlleg Wiel aktiv sinn Integr. Komp. Biol. 2005 45 (3) 438-455
- Effekter vu Waasserdeprivatioun a Rehydratioun op c-Fos a FosB Faarwen am Ratten supraoptesche Kär a Lamina terminalis Regioun Am. J. Physiol. Regul. Integr. Komp. Physiol. 2005 288 (1) R311-R321
- Transkriptiounsinduktioun vu FosB/{Delta}FosB Gen duerch mechanesch Stress an Osteoblasten J Biol Chem 2004 279 (48) 49795-49803
- Induktioun vu {Delta}FosB a Belounungsrelatéierte Gehirstrukturen nom chronesche Stress J. Neurosci. 2004 24 (47) 10594-10602
- Sim1 Gen Doséierung moduléiert déi homeostatesch Ernärungsreaktioun op erhéicht Diätfett bei Mais Am. J. Physiol. Endokrinol. Metab. 2004 287 (1) E105-E113
- DNA Mikroarray Analyse vum Genausdrock a mënschlechen Optiknerv Kapp Astrocyten als Äntwert op hydrostateschen Drock Physiol. Genomics 2004 17 (2) 157-169
- Superoxid ass an der Aktivatioun vum Zentralnervensystem a Sympathoexcitatioun vu myokardeschen Infarkt-induzéierten Häerzversoen involvéiert Circ. Res. 2004 94 (3) 402-409
- Adenosin A2A Rezeptoren an der Neuroadaptatioun op widderholl dopaminergesch Stimulatioun: Implikatioune fir d'Behandlung vun Dyskinesien bei der Parkinson Krankheet Neurologie 2003 61 (90116) S74-81
- Cytoplasmesch Versus Nuklear Lokaliséierung vu Fos-Zesummenhang Proteinen am Frog, Rana esculenta, Testis: In Vivo an Direkt In Vitro Effekt vun engem Gonadotropin-Release Hormon Agonist Biol. Reprod. 2003 68 (3) 954-960
- Periaadolescent Mais weisen eng verbessert Delta FosB Upregulatioun als Äntwert op Kokain an Amphetamin J. Neurosci. 2002 22 (21) 9155-9159
- Delta FosB Reguléiert Rad Lafen J. Neurosci. 2002 22 (18) 8133-8138
- D'Aktivitéit CREB am Nukleus Accumbens Shell kontrolléiert d'Opreegung vu Verhalen op emotional Reizen Proc. Natl. Acad. Sci. USA 2002 99 (17) 11435-11440
- Psychogenomics: Méiglechkeete fir Sucht ze verstoen J. Neurosci. 2001 21 (21) 8324-8327
