Biolpsykiatri. 2008 Dec 1; 64 (11): 941-50. Epub 2008 Jul 26.
Teegarden SL, Nestler EJ, Bale TL.
Källa
Institutionen för djurbiologi, University of Pennsylvania, Philadelphia, PA 19104-6046, USA.
Abstrakt
BAKGRUND:
Känslighet för belöning har blivit implicerad som en predisponeringsfaktor för beteenden relaterade till drogmissbruk såväl som överspädning. De underliggande mekanismerna som bidrar till att belöna känsligheten är emellertid okända. Vi antydde att en dysregulering i dopamin-signalering kan vara en bakomliggande orsak till ökad känslighet för belöningen, varigenom belöningsstimuler kan fungera för att normalisera systemet.
METODER:
Vi använde en genetisk musmodell med ökad känslighet för känslighet, den Delta FosB-överuttryckta musen, för att undersöka belöningsbanans förändringar som svar på en godtagbar fetthaltig diet. Markörer av belöningssignalering i dessa möss undersöktes både basalt och efter 6-veckor av godtagbar dietsexponering. Möss undersöktes i ett beteendestest efter hög fetthaltig borttagning av dieten för att bedöma sårbarheten hos denna modell för att avlägsna givande stimuli.
RESULTAT:
Våra resultat visar förändrad belöningsvägsaktivering längs kärnans accumbens-hypotalamus-ventral tegmental-krets som resulterar från överuttryck av Delta FosB i kärnan accumbens och striatala regioner. Nivåer av fosforylerat cykliskt adenosinmonofosfat (cAMP) responselementbindande protein (PCREB), hjärnavledd neurotrofisk faktor (BDNF), och dopamin och cykliskt adenosinmonofosfatreglerat fosfoprotein med en molekylvikt av 32 kDa (DARPP-32) i nukleär accumbens reducerades i Delta FosB-möss, vilket tyder på minskad dopamin-signalering. Sex veckors hög fetthaltsexponering förbättrade dessa skillnader fullständigt, vilket avslöja den potentiella givande förmågan hos en smaklig diet. Delta FosB-möss visade också en signifikant ökning av lokomotorisk aktivitet och ångestrelaterade reaktioner 24 timmar efter högt fettuttag.
SLUTSATSER:
Dessa resultat etablerar en underliggande känslighet för förändringar i belöning relaterad till dysregulering av Delta FosB och dopamin signalering som kan normaliseras med smakliga dieter och kan vara en predisposerande fenotyp i vissa former av fetma.
Beskrivning
Trots vår ökande kunskap om neurala system som styr aptit och mättnad, fortsätter fetthalten att öka i USA. Nuvarande läkemedelsbehandlingar har begränsad effekt, och beteendemässiga modifikationer lider av minimal långvarig efterlevnad (1). Konsumtionen av kaloritäta, välsmakande livsmedel har kopplats till förändringar i stress- och belöningsbanor i hjärnan, vilket tyder på att de givande egenskaperna hos sådana livsmedel kan överstiga energibalanssignaler (2-4). Livsmedel med hög fetthalt verkar som naturliga belöningar, som aktiverar hjärnbelöningscentra på ett sätt som liknar missbruksmissbruk, och som sådana har använts i självadministrationsparadigmer (5-8). Det är sålunda troligt att beteenden och motivationen för överätning och drogmissbruk delar gemensamma underliggande mekanismer, vilket möjligen öppnar nya behandlingsmetoder för båda förhållandena.
När man studerar förhållandet mellan smakliga livsmedel och vägar som reglerar belöning och stress i hjärnan, Vi har tidigare identifierat molekylära och biokemiska markörer med reducerad belöning och ökad stress efter återtagning från en smaklig hög fet diet (HF). På samma sätt som missbruk av droger resulterade exponeringen för en godtagbar diet i våra studier i ökade nivåer av transkriptionsfaktorn ΔFosB i Nuclear Accumbens (NAc), en central hjärnbelöningsstruktur (9, 10). Möss som inducerar överuttryckt ΔFosB visar ökat instrumentalt svar på en matbelöning (11), vilket gör dem till ett värdefullt verktyg för att undersöka rollen av belöningssensitivitet och långsiktig dysregulering av belöningssystemet i de molekylära och biokemiska reaktionerna på en godtagbar diet.
I den föreliggande studien använde vi ΔFosB-överuttryckta möss för att undersöka långsiktiga förändringar i markörer av belöning i NAc-hypotalamus-ventral tegmental-området (VTA) neurokretsen som svar på en välsmakande HF-diet. Baserat på tidigare studier i dessa belöningskänsliga möss antog vi att ΔFosB-inducerade förändringar i belöningssensitivitet involverar en dysregulering vid dopamin-signalering resulterande från NAc-återkoppling till VTA. Vidare förutsåg vi att exponering för en naturlig belöning för en energität HF-diet skulle normalisera det dopaminerga systemet i dessa möss, vilket resulterade i ett överdriven svar på stressen vid tillbakadragande från denna HF-diet. Den unika aspekten av att använda en välsmakande diet som en givande substans tillåter oss att inkludera hypotalamiska ingångar för att belöna kretsloppet i en fenotyp som kan vara prediktiv för en population som är utsatt för behandlingsresistent fetma. För att undersöka denna hypotes studerade vi markörer för dopamin-neurotransmission, inklusive pCREB, BDNF och DARPP-32 i NAc och tyrosinhydroxylas och dopamintransportören i VTA, efter HF-exponering. Vi undersökte också specifika markörer av energibalans som är kända för att påverka dopaminproduktionen, inklusive leptin- och orexinreceptorer i VTA- och orexinuttrycket inom lateral hypotalamus.
Material och metoder
djur
Manliga bitransgena möss som inducerat överuttryckt ΔFosB i dynorfin-positiva neuroner i NAc och dorsalstriatum (Kelz et al., 1999) genererades på en blandad bakgrund (ICR: C57Bl6 / SJL) vid University of Texas Southwestern Medical Center och upprätthölls och testad vid University of Pennsylvania. Alla möss behölls på doxycyklin (100 μg / ml i dricksvattnet) tills de kom till University of Pennsylvania. För att inducera överuttryck avlägsnades doxycyklin (n = 23) (12). Kontrollmöss (n = 26) fortsatte att ta emot läkemedlet. Mössen tilldelades dietgrupper åtta veckor efter avlägsnandet av doxycylin vid vilken tidpunkt expression har visat sig nå maximala nivåer (13). Möss upprätthölls på en 12: 12 ljusmörk cykel (lampor på 0700) med mat och vatten tillgängligt ad libitum. Alla studier utfördes enligt experimentella protokoll godkända av University of Pennsylvania Institutionella djurvård och användningskommitté, och alla förfaranden genomfördes i enlighet med institutionella riktlinjer.
Diet exponering
Möss behölls på house chow (n = 16) eller placerades på HF (n = 16-17) under sex veckor. House Chow (Purina Lab Diet, St. Louis, MO) innehöll 4.00 kcal / g, bestående av 28% protein, 12% fett och 60% kolhydrat. HF-diet (forskningsdiett, New Brunswick, NJ) innehöll 4.73 kcal / g, bestående av 20% protein, 45% fett och 35% kolhydrat.
Biokemi och genuttryck
Möss analyserades efter sex veckors dietsexponering. Hjärnor avlägsnades från skalle och antingen fryst hel på torris eller NAc-dissekerad (ungefär 0.5 - 1.75 mm från bregma, vid ett djup av 3.5 - 5.5 mm) och fryst i flytande kväve. Vävnad lagrades vid -80 ° C tills det analyserades.
Biokemiska analyser
Metoder för Western blots beskrivs i kompletterande material. Antikropparna som användes var: Cdk5, CREB och BDNF (1: 500, Santa Cruz-bioteknik, Santa Cruz, CA) och fosfor-CREB (pCREB) (Ser 133) (1: 500, Cell Signaling Technology, Danvers, MA).
Receptor autoradiografi
Detaljerade metoder för autoradiografi beskrivs i kompletterande material. Ligander som användes var 2 nM H3 - SCH 23390 och 5 nM H3-spiperon (PerkinElmer, Boston, MA).
In situ hybridisering
Vävnadsbehandling och hybridisering utfördes såsom tidigare beskrivits (14). DARPP-32 sonden gavs vänligen av P. Greengard (Rockefeller University) och orexinsonden av J. Elmquist (University of Texas Southwestern Medical Center). Diabilder analyserade för DARPP-32 tilläts att filma för 3 dagar och diabilder analyserade för orexin fick appli-kation till film för 4-dagar. Kvantifiering av filmbilder utfördes såsom tidigare beskrivits (10).
QRT-PCR
RNA isolerades från VTA och uttryck av individuella gener som bedömdes med användning av TaqMan-genuttrycksanalyser (Applied Biosystems, Foster City, CA). Detaljerade metoder och statistiska analyser kan hittas i kompletterande material.
Beteendeanalyser
För att undersöka effekterna av belöningssensitivitet på diet-inducerade beteendeförändringar, togs en delmängd av möss ut från HF efter fyra veckors exponering och återvände till huschow (n = 9-kontroll, n = 8 ΔFosB). Tjugofyra timmar efter återkallandet utsattes möss för öppna fältprov i enlighet med vårt tidigare publicerade dietary withdrawal paradigm (10). Kort sagt placerades musen i mitten av öppenfältapparaten och övervakades i fem minuter. Totalt linjekors, fekal boli, tid i mitten och korsningar i mitten uppmättes.
Statistik
Alla data utom Western blots analyserades med användning av en tvåvägs ANOVA följt av Fishers PLSD-test med doxycyklinbehandling (ΔFosB-uttryck) och dietförhållande som de oberoende variablerna. För RT-PCR-analyser användes ett reducerat P-värde för att korrigera för flera jämförelser inom grupper av relaterade gener (se kompletterande material). Western-blotting analyserades med användning av en elevs t-test med doxycyklinbehandling som den oberoende variabeln, jämförande optiska densiteter inom samma blot. Alla data presenteras som medelvärde ± SEM.
Resultat
Basala biokemiska skillnader
För att belysa de molekylära vägarna som ligger till grund för den ökade belöningskänsligheten i ΔFosB-överuttryckande möss undersöktes nivåer av flera viktiga signalmolekyler i NAc. Det fanns en trend för ökade nivåer av Cdk5 i NAc hos ΔFosB-möss jämfört med djur som kullkamrat kontrollerades på doxycyklin (F = 5.1, P = 0.08; Fig. 1A). ΔFosB-möss uttryckte signifikant reducerade nivåer av pCREB (F = 7.4, P <0.05; Fig. 1B) såväl som totala nivåer av CREB (F = 5.4, P = 0.05; Fig. 1C). En signifikant minskning av BDNF observerades också i NAc hos ΔFosB-möss (F = 10.6, P <0.05; Fig. 1D).
Figur 1
Möss som överuttryckte ΔFosB uppvisade biokemiska markörer av reducerad dopamin-signalering i NAc
Matintag och kroppsvikt på hög fetthalt
Därefter undersökte vi effekterna av en naturligt givande HF-diet på förändringar i signalmolekyler i ΔFosB-överuttryckande möss. Det fanns inga skillnader mellan ΔFosB-möss och kontroller i matintag på varken hus eller HF. Det fanns emellertid en total minskning av kaloriintaget normaliserat till kroppsvikt vid exponering för HF som var specifikt för ΔFosB-mössen (F = 11.2, P <0.01; Fig. 2A). I slutet av sex veckors dietexponering vägde möss som fick HF väsentligt mer än de som hade chow-diet (F = 17.2, P <0.001) och ΔFosB-möss vägde totalt sett mindre än kontrollerna (F = 5.6, P <0.05; Fig. 2B). Denna effekt var specifik för skillnader mellan grupper på chow-dieten (P <0.05).
Figur 2
ΔFosB överuttryckta möss visade inga skillnader i matintag på antingen Chow eller High Fat (HF) diet
Biokemiska skillnader på fetthaltig diet
För att bestämma hur basala skillnader i NAc-signaler kan förändras med HF-diet undersöktes samma signalproteiner som studerades vid baslinjen hos djur som hade fått sex veckor av HF. Det fanns inga signifikanta skillnader i Cdk5-nivåer (Fig. 3A). Nivåerna av pCREB och totalt CREB var inte längre olika efter sex veckor av HF (Fig. 3B, C). Nivåerna av BDNF var signifikant förhöjda i FFB-möss efter sex veckors exponering av HF (F = 6.5, P = 0.05; Fig. 3D).
Figur 3
Högfett (HF) dietreducerade signaleringsskillnader observerade i NAc hos ΔFosB-överuttryckta möss
Dopaminreceptorautadiografi
Vi använde receptorautoradiografi för att bedöma om de ΔFosB-inducerade förändringarna i dopaminsignalering i NAc är relaterade till förändringar i dopaminreceptoruttryck (Fig. 4A). Kost med hög fetthalt verkade öka densiteten av D1-dopaminreceptorbindning något (P = 0.14), och denna skillnad var större hos ΔFosB-möss (fig. 4B). Det fanns också en trend mot en ökning av D1-bindningsområdet efter HF (P = 0.06), och post-hoc-testning visade att detta var signifikant i ΔFosB-mössen (P <0.05; Fig. 4C). Till skillnad från D1-receptorer, inga förändringar i D2-receptorbindningsdensitet (kontrollchow = 97.6 ± 6.9, kontroll HF = 101.1 ± 8.2, ΔFosB chow = 91.6 ± 1.0, ΔFosB HF = 94.8 ± 9.5) eller bindningsområde (kontrollchow = 47.3 ± 3.4, kontroll HF = 53.8 ± 6.0, ΔFosB chow = 51.9 ± 3.7, ΔFosB HF = 49.0 ± 3.3) i NAc observerades.
Figur 4
Hög fet diet (HF) ledde till förändringar i D1-dopaminreceptorbindning och DARPP-32-uttryck i nukleär accumbens (NAc) av ΔFosB-överuttryckta möss
DARPP-32-uttryck i NAc
In situ-hybridisering användes för att bestämma expressionsnivåer av DARPP-32 i NAc (fig. 4D). Kost med hög fetthalt ökade signifikant DARPP-32-uttrycket i denna hjärnregion (F = 5.1, P <0.05), och det fanns en signifikant interaktion mellan diet och ΔFosB-uttryck (F = 8.9, P <0.05), med ΔFosB-möss som visade en större dietinducerad förändring (fig. 4E). En basal skillnad i DARPP-32-expression mellan kontroll- och ΔFosB-möss avslöjades genom post hoc-testning (P <0.01), liksom en signifikant ökning av DARPP-32-uttryck i ΔFosB-möss på HF (P <0.01).
Genuttryck i VTA
QRT-PCR användes för att bedöma förändringar i genuttryck i VTA, inriktad på flera nyckelgener som tidigare var inblandade i regleringen av belöning. Alla prover normaliserades till β-aktin. För att säkerställa att β-aktinuttryck inte förändrades genom behandling genomfördes en separat analys för att jämföra β-aktin med en andra intern kontroll, GAPDH. Det fanns inga signifikanta skillnader i β-aktinuttryck (ΔCT-värden, β-aktin - GAPDH: kontrollchow = 2.29 ± 0.21, kontroll HF = 2.01 ± 0.04, ΔFosB chow = 2.32 ± 0.49, ΔFosB HF = 2.37 ± 0.10).
En trend för en interaktion mellan ΔFosB-expression och dietbehandling observerades för expression av tyrosinhydroxylas (F = 3.6, P <0.06; Fig. 5A). Sex veckors exponering för HF tycktes minska tyrosinhydroxylasuttrycket i kontrollmöss och öka expressionen i AFOSB-möss. En signifikant interaktion mellan ΔFosB-uttryck och dietexponering observerades för expression av dopamintransportören (F = 6.7, P <0.03; Fig. 5B). I likhet med tyrosinhydroxylas minskade exponering för HF dopamintransporteruttryck i kontrollmöss och signifikant ökat uttryck i ΔFosB-möss (P <0.05). Den grundläggande skillnaden i dopamintransportöruttryck mellan kontroll och ΔFosB-möss nådde inte betydelse (P = 0.16), men efter 6 veckor HF uttryckte ΔFosB-möss signifikant förhöjda nivåer av dopamintransportör jämfört med kontroller (P <0.05).
Figur 5
HF-exponering och ΔFosB-uttryck ledde till förändringar i uttryck av ett antal nyckelmolekyler i VTA
Det fanns en trend som indikerade en effekt av ökat ΔFosB-uttryck för att minska TrkB-nivåerna i VTA (F = 5.7, P <0.04; Fig. 5C). Även om det inte fanns några huvudeffekter på k-opioidreceptoruttryck, fanns det en trend mot minskat uttryck i ΔFosB-möss (P = 0.08; Fig. 5D). Uttryck av leptinreceptorn bestämdes också i VTA. En signifikant effekt av dietexponering hittades (F = 6.1, P <0.03), med HF som signifikant minskade nivåerna av leptinreceptorn i VTA i både AFOSB- och kontrollmöss (Fig. 5E). Uttryck av orexinreceptor 1 i VTA undersöktes också. Det fanns en signifikant effekt av diet på expression av orexinreceptorn (F = 9.0, P <0.02), med möss som exponerades för HF uttryckte högre nivåer i VTA (Fig. 5F). Det fanns också en trend för ΔFosB-möss att uttrycka övergripande högre nivåer av orexinreceptor 1 i denna hjärnregion (P <0.05).
Orexinuttryck i lateral hypotalamus
Vi mätte nivåerna av orexin i lateral hypothalamus, ursprunget till orexinerg innervering av VTA, genom hybridisering in situ (Fig. 6A). Det fanns en signifikant interaktion mellan ΔFosB-uttryck och dietexponering på orexinuttryck (F = 9.1, P <0.01), med HF som signifikant ökade orexinnivåerna i kontrollmöss (P <0.05) och minskat uttryck i ΔFosB-möss (Fig. 6B). Även om det inte fanns några signifikanta skillnader i orexinuttryck i basaltillståndet, efter 6 veckor HF, uttryckte ΔFosB-möss signifikant reducerade nivåer av orexin jämfört med kontroller (P <0.05).
Figur 6
Hög fetthalt (HF) diet hade differentialeffekter på orexinuttryck i kontroll (Ctrl) och ΔFosB överuttryckta möss
Behavioralanalyser
För att utvärdera förändringar i upphetsning och känslomässighet på grund av kostförändring exponerades möss för testet på öppna fält 24 timmar efter att HF-dieten hade dragits tillbaka (10). Totala linjekorsningar, som gjordes som ett mått på upphetsning, påverkades signifikant av ΔFosB-uttryck (F = 6.6, P <0.05) och diet (F = 4.6, P <0.05; Fig. 7A). ΔFosB-möss var mer aktiva i den nya miljön än sammandragningar, och post-hoc-testning visade att möss som drogs tillbaka från HF var signifikant mer aktiva än de som exponerades för chow (P <0.05). Fekal boli räknades som ett mått på ångestliknande beteende (10). Det fanns en huvudeffekt av ΔFosB-uttryck (F = 10.2, P <0.01), med ΔFosB-överuttryckande möss som producerade mer fekal boli i den nya miljön, särskilt i hushålls- och HF-tillbakadragningsgrupper (Fig. 7B). ΔFosB-möss som hölls på HF-diet producerade färre fekala boli än de som bibehölls vid chow och de som drogs tillbaka 24 timmar före testet. Kontrollmöss verkade inte påverkas av kosten. Det fanns inga signifikanta effekter av varken ΔFosB-uttryck eller diet på den tid som tillbringades i mitten av det öppna fältet (kontrollchow = 14.5 ± 3.1 sek, kontroll HF = 18.0 ± 3.2 sek, kontroll W / D = 15.4 ± 1.9 sek, ΔFosB chow = 16.9 ± 2.4 sek, ΔFosB HF = 13.1 ± 3.9 sek, ΔFosB W / D = 19.8 ± 2.6 sek).
Figur 7
Möss överuttryckande ΔFosB var mer känsliga för effekterna av hög fetthalt (HF) uttag
Diskussion
Vid fetma behandling finns det ett kritiskt behov av att identifiera faktorer som påverkar mottagligheten för övermålning och viktökning. Hjärnbelöningsbanor spelar en viktig roll i motivationen för och svaret på godtagbara livsmedel och kostförändringar (6, 10, 15, 16). Eftersom orexigena och anorexigena signaler kan direkt påverka belöningssignaler via en hypotalamus-VTA-NAc-krets kan belysningen av gener som är mottagliga för energirika smakliga dieter inom belöningscentra ge nya terapeutiska mål i fetmabehandling (17, 18). Därför undersökte vi biokemiska och molekylära markörer av belöning och energibalanssignalering längs hypotalamus-VTA-NAc-kretsen som svar på en HF-diet i ΔFosB-överuttryckta möss som en modell för förbättrad känslighet för förändringar i belöning (13, 19, 20) , och beteendemässig känslighet efter dietuttag. Vi antog att basal dysregulering av dopamin-signalering i ΔFosB-möss skulle normaliseras genom de fördelaktiga effekterna av en HF-diet, som omfattar skärningspunkten för energibalanssignaler och dopamin-systemet.
För att undersöka markörer som indikerar en dysregulering vid dopamin-signalering i NAc, undersökte vi D1-receptornivåer och nedströms effektorer. Även om det inte fanns några signifikanta skillnader i D1-receptorbindning, Det fanns en trend för HF-exponering för att öka bindningsområdet i ΔFosB-mössen. Detta är intressant som induktion av ΔFosB genom läkemedel och naturliga belöningar verkar dominera i den dynorfin-positiva subtypen av medelstarka nervceller som primärt uttrycker D1-receptorer (9, 21). Nivåerna av det nedströms dopamin-signalerings-målet pCREB reducerades avsevärt i FFB-möss, som stödde reducerad D1-receptoraktivering i denna hjärnområde (22, 23). Intressant upptäckte vi också en signifikant minskning av de totala CREB-nivåerna i ΔFosB-möss, vilket föreslår en ytterligare minskad kapacitet för dopaminsignaltransduktion som kan vara sekundär till återkoppling som härrör från en förlängd minskning av pCREB (24). BDNF-uttryck regleras av pCREB, höjs med D1-aktivering och är en viktig medlare av belöningsrelaterad neuroplasticitet i NAc (25, 26). Följaktligen detekterade vi en signifikant minskning av BDNF-protein i NAc hos ΔFosB-möss.
Alla medellånga nervceller i NAc uttrycker DARPP-32 (27). Dess många nedströms effektorer gör det till en viktig aktör i belöningsbanor (28), och det har blivit involverat i narkotikamissbruk och i andra sjukdomar som involverar dopaminsystemet inklusive affektiva sjukdomar och schizofreni (27, 29). Vi upptäckte djupa basala reduktioner i DARPP-32-uttryck i NAc av ΔFosB-möss. DARPP-32-uttryck regleras av BDNF och därför kan det reducerade uttrycket vara direkt relaterat till reduktionerna i BDNF-nivåer som detekteras i ΔFosB-möss (27, 29, 30). Även moderata förändringar i fosforyleringstillståndet för DARPP-32 kan leda till avsevärda förändringar av intracellulär signalering inom NAc (27). Tidigare studier har rapporterat ingen förändring av DARPP-32-protein i ΔFosB-möss efter en 12-wk-borttagning från doxycyklin när en bredare striatal bedömning utfördes (31), vilket tyder på att effekterna av ΔFosB på DARPP-32 kan vara tids- och regionsspecifika.
Vi antydde att de dramatiska minskningarna av index av dopamin-signalering i NAc av ΔFosB-möss troligen involverade förändringar i VTA-dopaminprojektionsneuronerna, även om ΔFosB inte överuttrycks inom dessa neuroner. Därför undersökte vi uttryck av dopaminrelaterade gener i VTA, inklusive tyrosinhydroxylas och dopamintransportören. Nivåer av tyrosinhydroxylas och dopamintransportör är positivt korrelerade med dopaminutgång. Det fanns en trend för ΔFosB-möss att uppvisa reducerat tyrosinhydroxylas och en signifikant minskning av dopamintransportören, i enlighet med dysreguleringen av dopamin-signalering i NAc. Eftersom dessa basala reduktioner av dopaminrelaterade gener i VTA av ΔFosB-mössa förmodligen återspeglar förändrad återkoppling från NAc under långvarig FFBB-överuttryck, undersökte vi uttryck av BDNF-receptorn, TrkB, som en möjlig mekanism för NAc-återkoppling till VTA (32). På liknande sätt som tyrosinhydroxylas- och dopamintransportör visade TrkB-uttryck också en trend att reduceras basalt i ΔFosB-möss som inte når betydelse när de korrigeras för multipla jämförelser. BDNF-TrkB-komplexet kan retrograderas transporteras och verkar inom VTA för att påverka lokalt genuttryck och främja celltillväxt och underhåll (33). Vidare kan BDNF-aktivering av presynaptisk TrkB inom NAc direkt stimulera dopamin-neurotransmission (32), som stöder en underliggande minskning av dopamin-signaleringen i dessa möss.
Dynorfinaktivering av K-opioidreceptorer reglerar dopamin-signalering och är en annan mekanism där NAc ger återkoppling till VTA (34). Vi fann att k-opioidreceptoruttryck i VTA visade en trend som skulle reduceras i ΔFosB-möss. Eftersom ΔFosB-överuttryck har visat sig minska dimorfinuttrycket i NAc (20), har FFBB-mus sannolikt en kraftig minskning av netto-VTA-k-opioidaktivering. Även om dynorfinsignalering normalt utövar en hämmande effekt på dopaminneuroner (35) uppvisar råttor som visar ökad självadministrering av missbrukande läkemedel minskade nivåer av dynorfin i NAc, vilket pekar på en roll för basalt reducerad dynorfinsignalering för att förbättra belöningskänsligheten (36 37). Dysregulering av dynorfin-k-opioidsystemet har kopplats till förvärvet och uthålligheten av drogmissbruk, vilket stöder en kritisk balans mellan opioid-signalering vid normalisering av dopaminvägar (38).
Baserat på den förmånliga kapaciteten hos en energität HF-diet antydde vi att en dysregulering i dopamin- och opioidbelöningssignaler i ΔFosB-möss skulle predisponera dessa möss för förbättrade belöningssvar på en sådan diet, vilket normaliserar belöningssystemet via aktivering av hypotalamusen -VTA-NAc krets. Under sex veckors dietexponering observerades inga skillnader i matintag mellan ΔFosB och kontrollmöss, vilket tyder på att förändringarna i biokemiska och molekylära markörer av belöningssignaler i ΔFosB-möss inte berodde på skillnader i kalorier som konsumeras. Som förväntat dämpades basala skillnader i pCREB, totala CREB-, BDNF-, DARPP-32- och K-opioidreceptornivåer mellan ΔFosB och kontrollmöss, sannolikt på grund av ökad dopaminutgång i ΔFosB-möss på HF (29, 39-41) .
Undersökning av både tyrosinhydroxylas och dopamintransportören i VTA avslöjade överraskande motsatta svar på ΔFosB och kontrollmöss efter HF. Kontrollmöss uppvisade en minskning av tyrosinhydroxylas och dopamintransportörsuttryck, medan ΔFosB-möss visade ökat uttryck av båda dessa dopaminrelaterade gener. Intressant förändras tyrosinhydroxylasuttrycket i VTA genom kronisk kokain eller metamfetaminadministration (42-44), vilket tyder på att ΔFosB-möss kan finna den naturliga belöningen för HF mer framträdande än kontrollmöss.
För att undersöka hur potentiell hypotalamisk inmatning till VTA kan omdirigera signaler som reflekterar energibalans, undersöktes också leptinreceptorns och orexinreceptorns 1-expressions. Cirkulerande leptinnivåer ökas av HF, och leptin kan i sin tur agera vid VTA för att ändra dopamin signaleringen (18, 45). VTA-leptinreceptoruttryck minskades på liknande sätt med HF i både FFB och kontrollmöss, i linje med liknande viktökning och dietintag medan den var på HF. Högt fett ökade också uttrycket av orexinreceptorn-1 i VTA hos både FFB och kontrollmöss. Orexin aktiverar dopaminneuroner i VTA, främjar VTA-plasticitet och ökar dopaminnivåerna i NAc (46-48). Hög fet diet har visat sig öka orexinuttrycket hos möss, enligt våra observationer (49, 50). Sålunda kan ökat uttryck av orexinreceptorn såväl som förändringar i leptinsignalering i VTA kunna främja kostbelöning i både ΔFosB och kontrollmöss, vilket stöder en dissociation mellan vägar som omdirigerar energibalanssignaler och de som är bundna direkt till belöning.
För att undersöka de stress-provokerande effekterna av belöningsavdrag, undersöktes möss i ett öppen-fälttest 24-timmar efter avlägsnande av HF. ΔFosB-möss var känsligare för de akuta effekterna av föredragen dietuttag, vilket uppvisade ökad upphetsningsaktivitet och fekal boli-produktion i den nya öppna arenan jämfört med alla andra kontroll- och dietgrupper. ΔFosB-möss visade också ett intressant beteendemönster i detta test som tyder på belöning och stresskänslighet, med HF-kosten som i första hand minskar fekal boli-produktion i förhållande till chow, och tillbakadragandet ökar igen detta ångestrelaterade svar. Denna observerade ökning i öppenfältaktivitet korrelerade inte med förändringar i orexinuttryck, vilket föreslår en relation till stressinducerad upphetsning som inte bara är en effekt av förändringar i orexinförmedlad signalering. Sammantaget stöder dessa data vår hypotes att ΔFosB-möss skulle vara känsligare för de akuta effekterna av föredragen dietuttag på grund av deras ökade belönings känslighet.
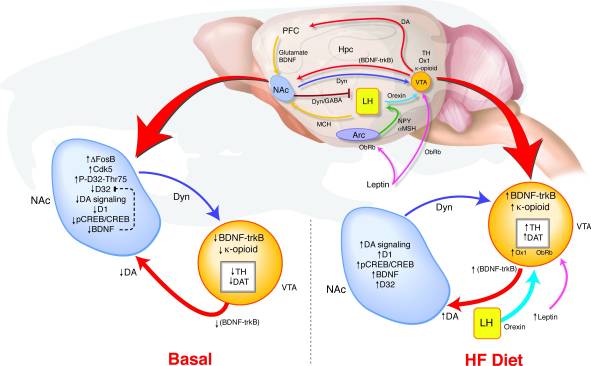
Hur leder långsiktig överuttryck av ΔFosB i NAc till sådana förändringar i beteende och belöningssignaler? Vi har föreslagit en modell av VTA-sammanfallsdetektering där förändrad återkoppling från NAc- och hypotalamusreläerna signalerar om belöningsstatus för att bestämma regleringen av dopamin-systemet som kan stödja en länk mellan belöningsvägdysregulering och en predisposition till fetma (Fig. 8). Vid exponering av HF, överensstämmer flera ingångar som återspeglar både energibalans och belöningsstatus på VTA. Ökningar i leptin- och orexinsignaler samt förändrad feedback från NAc till lateral hypotalamus kan påverka hur dessa orexigena signaler svarar mot HF i ΔFosB-mössen (17, 18, 45, 47, 51-53). Höga fettdietinducerade höjningar i BDNF kan ge belöningsrespons till VTA, ytterligare främja förändringar i dopaminrelaterat genuttryck.
Figur 8
Hög fetthalt (HF) diet normaliserar dysregulerad belöningssignalering i ΔFosB-möss
Dessa resultat avgränsar molekylmarkörer av belöningsförebyggande känslighet och indikerar att långvarig dysregulering av dopaminsystemet kan predisponera en individ för missbruk och fetma. Vidare ger dessa data ett viktigt steg mot att identifiera potentiella nya terapeutiska mål vid behandling och förebyggande av fetma och andra störningar som kan centrera på belöningssystemet. I framtiden är det viktigt att undersöka hur detta system svarar mot borttagning av HF-kosten, samt att undersöka eventuella könsskillnader i känslighet för belöning och hög fetthaltsexponering.
Extramaterial
Supp. metoder
Klicka här för att visa. (61K, doc)
Erkännanden
Författarna vill tacka Cathy Steffen för hjälp med djuruppfödning och överföring. Detta arbete stöddes av ett bidrag från University of Pennsylvania Diabetes Center (DK019525) och genom bidrag från National Institute of Mental Health (R01 MH51399 och P50 MH66172) och National Institute on Drug Abuse (R01 DA07359).
fotnoter
Finansiella upplysningar: Alla författare förklarar att de inte har några biomedicinska ekonomiska intressen eller potentiella intressekonflikter.
Referensprojekt
1. Wadden TA, Berkowitz RI, Womble LG, Sarwer DB, Phelan S, Cato RK, Hesson LA, Osei SY, Kaplan R, Stunkard AJ. Randomiserad prövning av livsstilsmodifiering och farmakoterapi mot fetma. N Engl J Med. 2005; 353 (20): 2111-20 [PubMed].
2. Blendy JA, Strasser A, Walters CL, Perkins KA, Patterson F, Berkowitz R, Lerman C. Nedsatt nikotinbelöning i fetma: korsjämförelse i människa och mus. Psykofarmakologi (Berl) 2005
3. Franken IH, Muris P. Individuella skillnader i belöningssensitivitet är relaterade till matbehov och relativ kroppsvikt hos friska kvinnor. Aptit. 2005; 45 (2): 198-201 [PubMed].
4. Kelley AE, Berridge KC. Neurovetenskap av naturliga belöningar: relevans för beroendeframkallande droger. J Neurosci. 2002; 22 (9): 3306-11 [PubMed].
5. Cagniard B, Balsam PD, Brunner D, Zhuang X. Möss med kroniskt förhöjd dopamin uppvisar ökad motivation, men inte lärande, för en matbelöning. Neuropsychopharmacology. 2006; 31 (7): 1362-70 [PubMed].
6. Liang NC, Hajnal A, Norgren R. Sham matar majsolja ökar accumbens dopamin i råttan. Am J Physiol Regulator Integr Comp Physiol. 2006; 291 (5): R1236-9 [PubMed].
7. Mendoza J, Angeles-Castellanos M, Escobar C. Entrainment av en smaklig måltid inducerar matförväntande aktivitet och c-Fos uttryck i belöningsrelaterade områden i hjärnan. Neuroscience. 2005; 133 (1): 293-303 [PubMed].
8. Schroeder BE, Binzak JM, Kelley AE. En vanlig profil av prefrontal kortikal aktivering efter exponering för nikotin- eller chokladrelaterade kontextuella signaler. Neuroscience. 2001; 105 (3): 535-45 [PubMed].
9. Nestler EJ, Barrot M, Self DW. DeltaFosB: en hållbar molekylärbrytare för missbruk. Proc Natl Acad Sci USA A. 2001; 98 (20): 11042-6. [PMC gratisartikel] [PubMed]
10. Teegarden SL, Bale TL. Minskningar i kosttillskott ger ökad känslighet och risk för återfall av kost. Biolpsykiatri. 2007; 61 (9): 1021-9 [PubMed].
11. Olausson P, Jentsch JD, Tronson N, Nestler EJ, Taylor JR. dFosB i Nucleus Accumbens reglerar matförstärkt instrumentalt beteende och motivation. Journal of Neuroscience. 2006; 26 (36): 9196-9204 [PubMed].
12. Chen J, Kelz MB, Zeng G, Sakai N, Steffen C, Shockett PE, Picciotto MR, Duman RS, Nestler EJ. Transgena djur med inducerande, riktade genuttryck i hjärnan. Mol Pharmacol. 1998; 54 (3): 495-503 [PubMed].
13. Kelz MB, Chen J, Carlezon WA, Jr, Whisler K, Gilden L, Beckmann AM, Steffen C, Zhang YJ, Marotti L, Själv DW, Tkatch T, Baranauskas G, Surmeier DJ, Neve RL, Duman RS, Picciotto MR, Nestler EJ. Uttryck av transkriptionsfaktorn deltaFosB i hjärnan styr känsligheten för kokain. Natur. 1999; 401 (6750): 272-6 [PubMed].
14. Bale TL, Dorsa DM. Sexskillnader i och effekter av östrogen på oxytocinreceptorns messenger-ribonukleinsyrauttryck i den ventromediala hypotalamusen. Endokrinologi. 1995; 136 (1): 27-32 [PubMed].
15. Avena NM, Long KA, Hoebel BG. Sockerberoende råttor visar ökad respons på socker efter avhållande: Bevis på en sockerberoende effekt. Physiol Behav. 2005; 84 (3): 359-62 [PubMed].
16. Kommer MJ, Franzblau EB, Kelley AE. Nucleus accumbens mu-opioider reglerar intag av en fet diet genom aktivering av ett distribuerat hjärnanät. J Neurosci. 2003; 23 (7): 2882-8 [PubMed].
17. Zheng H, Patterson LM, Berthoud HR. Orexinsignalering i det ventrala tegmentala området krävs för hög fetthalt, som induceras av opioidstimulering av kärnans accumbens. J Neurosci. 2007; 27 (41): 11075-82 [PubMed].
18. Hommel JD, Trinko R, Sears RM, Georgescu D, Liu ZW, Gao XB, Thurmon JJ, Marinelli M, DiLeone RJ. Leptinreceptorsignalering i dopaminneuroner i midhjärnan reglerar utfodring. Nervcell. 2006; 51 (6): 801-10 [PubMed].
19. Colby CR, Whisler K, Steffen C, Nestler EJ, Self DW. Striatal celltypsspecifik överuttryck av DeltaFosB ökar incitamentet för kokain. J Neurosci. 2003; 23 (6): 2488-93 [PubMed].
20. Zachariou V, Bolanos CA, Selley DE, Theobald D, Cassidy MP, Kelz MB, Shaw-Lutchman T, Berton O, Sim-Selley LJ, Dileone RJ, Kumar A, Nestler EJ. En viktig roll för DeltaFosB i kärnan accumbens i morfin åtgärder. Nat Neurosci. 2006; 9 (2): 205-11 [PubMed].
21. Lee KW, Kim Y, Kim AM, Helmin K, Nairn AC, Greengard P. Kokaininducerad dendritisk ryggradssbildning i D1- och D2-dopaminreceptorinnehållande mellanspinniga neuroner i nukleinsymboler. Proc Natl Acad Sci USA A. 2006; 103 (9): 3399-404. [PMC gratisartikel] [PubMed]
22. Blendy JA, Maldonado R. Genetisk analys av narkotikamissbruk: rollen av cAMP-responselementbindande protein. J Mol Med. 1998; 76 (2): 104-10 [PubMed].
23. Nestler EJ. Molecular mechanisms of drug addiction. Neuro. 2004; 47 1: 24-32. [PubMed]
24. Tanis KQ, Duman RS, Newton SS. CREB Bindning och aktivitet i hjärnan: Regional specificitet och induktion genom elektrokonvulsiv beslag. Biolpsykiatri. 2007
25. Kumar A, Choi KH, Renthal W, Tsankova NM, Theobald DE, Truong HT, Russo SJ, Laplant Q, Sasaki TS, Whistler KN, Neve RL, Self DW, Nestler EJ. Chromatin remodeling är en nyckelmekanism som ligger bakom kokaininducerad plasticitet i striatum. Nervcell. 2005; 48 (2): 303-14 [PubMed].
26. Graham DL, Edwards S, Bachtell RK, Dileone RJ, Rios M, Self DW. Dynamisk BDNF-aktivitet i kärnan accumbens med kokainanvändning ökar självadministration och återfall. Nat Neurosci. 2007; 10 (8): 1029-37 [PubMed].
27. Svenningsson P, Nairn AC, Greengard P. DARPP-32 medierar åtgärderna av flera missbruksmissbruk. Aaps J. 2005; 7 (2): E353-60. [PMC gratisartikel] [PubMed]
28. Palmer AA, Verbitsky M, Suresh R, Kamens HM, Reed CL, Li N, Burkhart-Kasch S, McKinnon CS, Belknap JK, Gilliam TC, Phillips TJ. Genuttrycksskillnader hos möss som valts avvikande för metamfetaminkänslighet. Mammgenom. 2005; 16 (5): 291-305 [PubMed].
29. Bogush A, Pedrini S, Pelta-Heller J, Chan T, Yang Q, Mao Z, Sluzas E, Gieringer T, Ehrlich ME. AKT och CDK5 / p35 medierar hjärnavledad neurotrof faktorinduktion av DARPP-32 i medelstora snygga neuroner in vitro. J Biol Chem. 2007; 282 (10): 7352-9 [PubMed].
30. Benavides DR, Bibb JA. Rollen av Cdk5 i drogmissbruk och plasticitet. Ann NY Acad Sci. 2004; 1025:. 335-44 [PubMed]
31. Bibb JA, Chen J, Taylor JR, Svenningsson P, Nishi A, Snyder GL, Yan Z, Sagawa ZK, Ouimet CC, Nairn AC, Nestler EJ, Greengard P. Effekter av kronisk exponering för kokain regleras av neuronproteinet Cdk5. Natur. 2001; 410 (6826): 376-80 [PubMed].
32. Blochl A, Sirrenberg C. Neurotropiner stimulerar frisättningen av dopamin från råttmemencefaliska neuroner via Trk- och p75Lntr-receptorer. J Biol Chem. 1996; 271 (35): 21100-7 [PubMed].
33. Berton O, McClung CA, Dileone RJ, Krishnan V, Renthal W, Russo SJ, Graham D, Tsankova NM, Bolanos CA, Rios M, Monteggia LM, Self DW, Nestler EJ. BDNF: s viktig roll i den mesolimbiska dopaminvägen i social nederlagsspänning. Vetenskap. 2006; 311 (5762): 864-8 [PubMed].
34. Nestler EJ, Carlezon WA., Jr Den mesolimbiska dopaminbelöningskretsen i depression. Biolpsykiatri. 2006; 59 (12): 1151-9 [PubMed].
35. Ford CP, Beckstead MJ, Williams JT. Kappa opioidinhibering av somatodendritiska dopaminhämmande postsynaptiska strömmar. J Neurophysiol. 2007; 97 (1): 883-91 [PubMed].
36. Nylander I, Vlaskovska M, Terenius L. Hjärndynorfin- och enkefalinsystem i Fischer- och Lewis-råttor: effekter av morfintolerans och uttag. Brain Res. 1995; 683 (1): 25-35 [PubMed].
37. Nylander I, Hyytia P, Forsander O, Terenius L. Skillnader mellan alkoholföreträdande (AA) och alkoholavvikande (ANA) råttor i prodynorfin- och proenkefalinsystemen. Alkoholklin Exp Exp. 1994; 18 (5): 1272-9 [PubMed].
38. Kreek MJ. Kokain, dopamin och det endogena opioidsystemet. J Addict Dis. 1996; 15 (4): 73-96 [PubMed].
39. Carlezon WA, Jr, Duman RS, Nestler EJ. CREBs många ansikten. Trender Neurosci. 2005; 28 (8): 436-45 [PubMed].
40. Dudman JT, Eaton ME, Rajadhyaksha A, Macias W, Taher M, Barczak A, Kameyama K, Huganir R, Konradi C. Dopamin D1-receptorer medierar CREB-fosforylering via fosforylering av NMDA-receptorn vid Ser897-NR1. J Neurochem. 2003; 87 (4): 922-34 [PubMed].
41. Själv DW. Reglering av läkemedelsbehandling och -sökande beteenden genom neuroadaptations i mesolimbic dopaminsystemet. Neuro. 2004; 47 1: 242-55. [PubMed]
42. Beitner-Johnson D, Nestler EJ. Morfin och kokain utövar vanliga kroniska verkningar på tyrosinhydroxylas i dopaminerge hjärnbelöningsregioner. J Neurochem. 1991; 57 (1): 344-7 [PubMed].
43. Lu L, Grimm JW, Shaham Y, Hope BT. Molecular neuroadaptations i accumbens och ventral tegmental area under de första 90 dagarna av tvungen abstinens från kokain selfadministration hos råttor. J Neurochem. 2003; 85 (6): 1604-13 [PubMed].
44. Shepard JD, Chuang DT, Shaham Y, Morales M. Effekt av metamfetamin-självadministrering på tyrosinhydroxylas- och dopamintransportörnivåer i råttens mesolimbiska och nigrostriatala dopaminvägar. Psykofarmakologi (Berl) 2006; 185 (4): 505-13. [PubMed]
45. Fulton S, Pissios P, Manchon RP, Stiles L, Frank L, Pothos EN, Maratos-Flier E, Flier JS. Leptinreglering av mesoaccumbens dopaminvägen. Nervcell. 2006; 51 (6): 811-22 [PubMed].
46. Narita M, Nagumo Y, Miyatake M, Ikegami D, Kurahashi K, Suzuki T. Inverkan av proteinkinas C i den orexininducerade höjningen av extracellulära dopaminnivåer och dess givande effekt. Eur J Neurosci. 2007; 25 (5): 1537-45 [PubMed].
47. Narita M, Nagumo Y, Hashimoto S, Khotib J, Miyatake M, Sakurai T, Yanagisawa M, Nakamachi T, Shioda S, Suzuki T. Direkt involvering av orexinerga system vid aktivering av mesolimbisk dopaminväg och relaterat beteende inducerat av morfin. J Neurosci. 2006; 26 (2): 398-405 [PubMed].
48. Borgland SL, Taha SA, Sarti F, Fields HL, Bonci A. Orexin A i VTA är avgörande för induktion av synaptisk plasticitet och beteendets sensibilisering mot kokain. Nervcell. 2006; 49 (4): 589-601 [PubMed].
49. Park ES, Yi SJ, Kim JS, Lee HS, Lee IS, Seong JK, Jin HK, Yoon YS. Förändringar i orexin-A- och neuropeptid Y-uttryck i hypotalamus hos de fasta och högfettiga dietmatade råttorna. J Vet Sci. 2004; 5 (4): 295-302 [PubMed].
50. Wortley KE, Chang GQ, Davydova Z, Leibowitz SF. Peptider som reglerar matintag: Örexin-genuttryck ökas under tillstånd av hypertriglyceridemi. Am J Physiol Regulator Integr Comp Physiol. 2003; 284 (6): R1454-65 [PubMed].
51. Zheng H, Corkern M, Stoyanova I, Patterson LM, Tian R, Berthoud HR. Peptider som reglerar matintag: appetit-inducerande accumbens manipulation aktiverar hypotalamiska orexin neuroner och hämmar POMC neuroner. Am J Physiol Regulator Integr Comp Physiol. 2003; 284 (6): R1436-44 [PubMed].
52. Baldo BA, Gual-Bonilla L, Sijapati K, Daniel RA, Landry CF, Kelley AE. Aktivering av en subpopulation av orexin / hypokretinhaltiga hypotalamiska neuroner genom GABAA-receptor-medierad inhibering av kärnans accumbens skal, men inte genom exponering för en ny miljö. Eur J Neurosci. 2004; 19 (2): 376-86 [PubMed].
53. Harris GC, Wimmer M, Aston-Jones G. En roll för laterala hypotalamiska orexinneuroner i belöningssökande. Natur. 2005; 437 (7058): 556-9 [PubMed].