Abstrakt
De för närvarande rekommenderade första linjebehandlingarna av erektil dysfunktion (ED), fosfodiesteras-typ 5-hämmare (PDE5i), till exempel sildenafil, är effektiva hos många patienter med ED av vaskulärt ursprung, men denna terapi är otillräcklig i ungefär 30-40% av män med ED där det också finns en neuronal affektion. Det krävs nya metoder för att behandla tillståndet. Vi granskar möjligheten att modulera de dopaminergiska vägarna för att förbättra erektil funktion. dopamin D1 (D1 , D5 ) - och D2 (D2 -D4 receptorer i det paraventrikulära området, det mediala pre-optiska området, ryggmärgen och i erektil vävnad är involverade i erektion, och flera agonister utvecklade för behandling av Parkinsons sjukdom är associerade med ökad libido. Ett terapeutiskt fönster för behandling av ED hittades genom sublingual administration av generalen dopamin receptoragonist apomorfin, men det misslyckades främst på grund av mindre effekt på erektil funktion jämfört med PDE5i. För att undvika de dosbegränsande biverkningarna förmedlade av D2 receptorer, illamående och emes, dopamin D4 receptoragonister utvecklades och de inducerar erektion i gnagare, men dessa läkemedel infördes aldrig kliniskt. P-laktamashämmaren klavulansyra ökar dopamin och serotonin och befanns öka sexuell upphetsning och erektioner, men dosresponskurvan är klockformad. Bupropion har selektivitet för hämning av dopamin återupptagande transporter och kan användas för att lindra sexuell symptom orsakade av andra antidepressiva läkemedel, vilket ger ett intressant sätt att behandla ED. Sammanfattningsvis ger modulering av de dopaminerga vägarna en möjlighet att förbättra behandlingen av ED.
- PMID: 27541930
- DOI: 10.1111 / bcpt.12653
Erektion är en hemodynamisk händelse där vasodilatation av intrakavernösa och helikärartärer följs av ökat arteriellt blodinflöde till corpora cavernosa. Erektion involverar olika centrala och perifera neurala och / eller humorala mekanismer 1. Centrala neurotransmittorer och neuropeptider kan antingen underlätta, till exempel dopamin (DA), eller hämma (t.ex. opioidpeptider) penil erektion genom att verka i flera hjärnområden. Serotonin kan utöva både underlättande och hämmande effekter, beroende på den berörda receptortypen 2.
Perifera neurotransmittorer frisatta från sympatiska (noradrenalin, ATP) och parasympatiska (acetylkolin, kväveoxid, vasoaktiv tarmpeptid) nerver som kommer in i corpora cavernosa, corpus spongiosum och glans penis reglerar blodflödet under erektion och detumescens 1, 3, 4. Vid metaboliskt syndrom och diabetes kan neuropati liksom en obalans mellan perifera kontraktila och avslappnande faktorer i erektil vävnad bidra till erektil dysfunktion (ED) 5.
Nuvarande riktlinjer rekommenderar fosfodiesteras-typ 5-hämmare (PDE5i), sildenafil, vardenafil, tadalafil och avanafil, som den första linjebehandlingen av ED; ungefär 30 – 40% av män med ED svarar emellertid inte på PDE5-hämmare terapi 6, 7. Patienter som lider av neurologisk skada, diabetes mellitus eller svår vaskulär sjukdom kan vara resistenta mot PDE5-hämmare 8. Förutom dessa sjukdomar, har mediciner av centrala nervsystemet (CNS), som antidepressiva medel, antipsykotika och ångestdämpare också en negativ inverkan på erektil funktion 5. Antidepressiva medel, såsom selektiva serotoninåterupptagshämmare (SSRI) och venlafaxin, kan påverka den manliga sexuella funktionen (önskan / upphetsning - spänning - orgasm). Andra antidepressiva medel, som bupropion, nefazodon och mirtazapin, påverkar också sexuell funktion, även om förekomsten av sexuell dysfunktion är lägre jämfört med SSRI 9. Förutom humörsjukdomar används antidepressiva medel också för att behandla neuropatisk smärta; därför påverkar sexuell dysfunktion inducerad av antidepressiva en större befolkning. I vissa kliniska studier korrigerade sildenafil ED inducerad av antidepressiva läkemedel; på grund av ett ökande antal icke-svarande på PDE5-hämmare finns det emellertid ett behov av nya metoder för behandling av ED. En metod skulle vara att rikta in sig inte bara på de perifera vägarna utan också på de centrala vägarna som är viktiga för erektil funktion. Som nämnts är en serie neurotransmittorer involverade i erektil funktion både på centrala och perifera nivåer och en serie av de senaste recensionerna har behandlat förordningen i detalj 1, 2 och kliniska studier relaterade till sexuell dysfunktion och monoaminer 10. En omfattande översyn som täcker några av de senaste läkemedlen under utveckling för ED kan också rekommenderas 11. För behandling av Parkinsons sjukdom utvecklades flera läkemedel med dopaminerg effekt, och ett av dessa läkemedel, den allmänna dopaminreceptoragonisten, apomorfin, befanns inducera erektion 12-15. Därför är fokus för den nuvarande MiniReview att överväga möjligheten att modulera de dopaminergiska vägarna för att förbättra erektil funktion.
Dopaminergiska vägar involverade i erektil funktion
Centrala vägar
De centrala vägarna som är involverade i kontrollen av erektil funktion inkluderar flera hjärnområden såsom det mediala preoptiska området (MPOA), den paraventrikulära kärnan (PVN) i hypothalamus, det ventrale tegmentala området, hippocampus, amygdala, bäddkärnan i stria terminalis, nucleus accumbens, medulla oblongata och ryggmärgen 2, där PVN för hypothalamus och det ventrale tegmentområdet är särskilt viktigt 2, 15. En serie neurotransmittorer är involverade i den centrala regleringen av erektion och de underlättar erektil funktion (dopamin, kväveoxid, glutamat, acetylkolin, oxytocin, hexarelinpeptid, ACTH, MSH och pro-VGF), hämmar erektil funktion (t.ex. noradrenalin, enkefaliner, GABA och endocannabinoider) eller i fall av serotonin både underlättar och hämmar erektil funktion 2. Dopamin är den huvudsakliga neurotransmitteren i CNS och underlättar sexuell motivation, copulation och genital reflexer 1, 16. Dopamin, som anses vara av betydelse för erektil funktion, är lokaliserat i MPOA och PVN för hypotalamus och nucleus accumbens. Dessa tre områden får dopaminerg innervation från det incertohypothalamic systemet 17. I PVN leder dopamin till aktivering av oxytocinerga neuroner antagligen genom att öka intracellulärt kalcium följt av aktivering av neuronal kväveoxidsyntas (nNOS). Kväveoxid genom en cyklisk GMP-oberoende väg tros troligen nitrosylering leda till aktiveringen av de oxytocinerga neuronerna (fig. 1). Kväveoxid bildas genom nNOS och kastrering och även exogent testosteron, nedåt och uppreglerar uttrycket av nNOS i PVN 2.
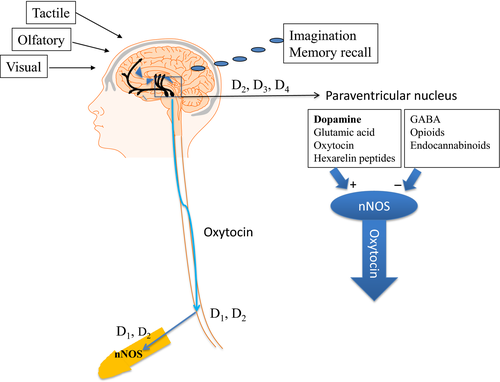
Figur 1
Vidare har dopaminerga nervceller identifierats som rör sig från caudal hypothalamus för att innervera de autonoma och somatiska kärnorna i lumbosakrala ryggmärgen 18, 19. Således kan dopamin förväntas delta i regleringen av både de autonoma och somatiska komponenterna i penreflexerna.
De PVN-oxytocinergiska neuronerna projicerar till neurohypofysen och andra hjärnområden, men också till medulla oblongata och ryggmärgen, där det leder till aktivering av de pro-erektila lumbo-sakrala parasympatiska nervcellerna som inverterar könsorganen.
Spinalvägar
Tydligen är en spinal dopaminergisk väg också av betydelse för erektil funktion. Fibrer som är immunreaktiva för dopamin finns i den thoracolumbar sympatiska kedjan och även i den lumbosakrala parasympatiska kärnan 20, 21. Dessutom en stark dopamin D2 receptoruttryck hittades i de lumbosakrala parasympatiska nervcellerna 22. Ytterligare stöd för en dopaminergisk väg på ryggradnivå kommer från iakttagelserna att hos råttor med ryggmärgsskador vid det torakala T8-segmentet kan den dopaminerga agonisten apomorfin som infunderas systemiskt inducera erektion hos råttor med en mekanism antagoniserad av dopamin D2 receptorantagonist (haloperidol, sulpirid) och underlättas av en dopamin D1 receptorantagonist (SCH23390) 23. Dessa observationer stöds också av observationerna att intratekal administrering av apomorfin inducerar spontana erektil respons 24.
Perifera vägar
Penil erektion initieras genom hämning av de sympatiska nerverna och aktivering av parasympatiska bäckenervar vilket leder till penilartärutvidgning och avslappning av de erektila glatta muskelcellerna i corpora cavernosa. Detta möjliggör blodfyllning av cavernösa sinusoider och begränsning av det venösa utflödet, med infångning av trycksatt blod i corpora cavernosa. Frigörande av kväveoxid från de parasympatiska nerverna spelar en viktig roll för avslappningen, och ökningen av blodinflöde till penis under erektionen stimulerar också endotelcellskiktet att frigöra kväveoxid och andra endotel-beroende vasodilatorer som bidrar till att upprätthålla erektion 25-27.
Till skillnad från rollen som dopamin i CNS är rollen som dopamin i den perifera erektila vävnaden mindre tydlig. Infusion av dopamin inducerar erektion hos katter 28och en antagonist av dopamin D1 receptorer, SCH23390, hämmar markant ökningen av intrakavernosalt tryck inducerat genom att stimulera den kavernösa nerven hos råttor 29. Dopamin D1 och D2 receptorer uttrycks i erektil vävnad från råttor och människor 30, 31och plåsterklämma av isolerade glatta muskelceller från corpus cavernosum antydde att dopamin och dopaminerga agonister inducerar avslappning genom öppnande av kalciumaktiverade kaliumkanaler med stor ledning 32. Det finns bevis för uttrycket av dopamintransportören i endotelcellerna i systemiska artärer 33, 34, men detta har fortfarande inte undersökts i endotelceller i erektil vävnad. Trots att dopamin kan bildas i sympatiska nervterminaler återstår källan till dopamin i erektil vävnad att klargöras, och även om dopaminen involverad i erektion härrör från endotelet eller andra strukturer i erektilvävnaden.
Sammanfattningsvis är dopaminergiska vägar i CNS och i den lumbosakrala delen av ryggmärgen involverade i erektil funktion, och i erektilvävnad finns det troligtvis också en dopaminerg väg. Detta antyder att modulering av de dopaminerga vägarna kan rikta sig till alla tre nivåer eller att hydrofila läkemedel som endast är inriktade på de perifera dopaminerge vägarna kan försökas.
Farmakologisk modulering av de dopaminergiska vägarna för att förbättra erektil funktion
Dopaminreceptoragonister
Det första läkemedlet med dopaminerg effekt som visade sig inducera erektion var den allmänna dopaminerga receptoragonisten, apomorfin 12och de flesta bevis relaterade till pro-erektil effekter har erhållits för dopaminerga receptoragonister. Det finns fem huvudtyper av dopaminreceptorer D1-D5 grupperad som D1-Lik (D1, D5) och D2-Lik (D2, D3 och D4) receptorer. Bindande affiniteter beskrivs för dopaminreceptoragonisterna i tabellen 1även om detta inte nödvändigtvis motsvarar de funktionella effekterna av läkemedlen på respektive receptorer. Vissa av läkemedlen är endast partiella agonister vid receptorerna vilket innebär att höga koncentrationer kan motverka den endogena liganddopamin. Dessutom har homo- och heterodimerer av dopaminreceptorer beskrivits, och det kan också förändra både affinitet och effekt hos respektive agonister 35.
| D1 GaS cAMP Ca, Ca2+↑ | D2 Gi/Go cAMP ↓, K+↑ | D3 Gi/Go cAMP ↓, K+↑ | D4 Gi/Go cAMP ↓, K+↑ | D5 GaS cAMP ↑ | |
|---|---|---|---|---|---|
| dopamin | 4.3-5.2 | 4.7-7.2 | 6.4-7.3 | 7.6 | 6.6 |
| apomorfin | 5.3-6.2 | 7.6 (PA) | 6.1-7.6 | 8.4 (PA) | 6.4 – 7.8 (PA) |
| Bromokriptin | 6.2 (PA) | 7.3 | 7.1 (PA) | - | 6.3 (PA) |
| fenoldopam | 6.5-7.9 | - | - | 6.5 | - |
| Kabergolin | 6.7 | 9.0 – 9.2 (PA) | 9.1 | 7.3 (PA) | 7.7 |
| pergolid | 5.9-6.5 | 7.5-7.6 | 8.3 | 7.2 | 6.0-7.5 |
| ropinirol | - | 8.1 | 7.7 | - | - |
| rotigotin | 5.6 | 10.2 | 8.4 | 7.3 | 6.0 |
| lisurid | 7.2 | 9.2-9.5 | 9.3 (PA) | 8.3 | - |
| kinpirol | - | 4.9-7.7 | 6.4-8.0 | 7.5 | - |
| Quinelorane | - | 5.5-5.7 | 7.2-7.4 | - | - |
| PD168,077 | - | - | - | 8.8 (PA) | - |
| ABT 724 | - | <5 | - | 7.2 (PA) | - |
| ABT 670 | - | <5 | - | 5.8 (PA) | - |
- Tabellen har konstruerats baserat på informationen om bindning till humana dopaminreceptorer tillgängliga i databasen: www.guidetopharmacology.org ägs av International Union of Pharmacology (IUPHAR) och British Pharmacological Society, där referenser som ger de ursprungliga mätningarna också kan nås. När ett intervall ges reflekterar det bindning till subpopulationer av receptorundertypen. När det gäller ABT 724, Ki värden kommer från det ursprungliga verket 57. Vissa av agonisterna har karakteriserats vara partiella agonister (PA) på receptorerna. G-proteinerna och signaltransduktionsvägarna täcker endast de klassiska vägarna. För en detaljerad beskrivning, se text 35.
Dopaminreceptorer anses signalera genom G-proteinberoende cellulära vägar, där D1-Liknande receptorer (D1 och D5) par till GαS protein och vid aktivering stimulerar adenylatcyklas och ökar cyklisk AMP, medan D2-Liknande receptorer (D2, D3 och D4) par till Gαi/ Ga0 proteiner och hämmar adenylatcyklas vilket leder till reducerade cykliska AMP-nivåer 35, 36. Men nyligen dopamin D1Det har också visat sig att liknande receptorer kopplas till ökningar i intracellulärt kalcium, antagligen genom Gαq följt av aktivering av fosfolipas C och frisättning av intracellulärt kalcium med inositoltrifosfat (IP)3) 35, och det kan förklara dopamin D1 receptorinducerad ökning av kalcium- och kväveoxidbildning (fig. 1). Också D2-Liknande receptorer och / eller heterodimerer av dopaminreceptorerna har beskrivits för att koppla till andra signaltransduktionsvägar både genom Gpy och arrestin 35. På grund av partisk agonism hos några av agonisterna kan därför de funktionella effekterna av agonister med uppenbarligen samma bindningsaffinitet skilja sig avsevärt.
apomorfin
Det finns en omfattande litteratur om apomorfin och sexuell funktion 1, 37. I korthet är apomorfin en allmän dopaminreceptoragonist med rapporterad receptorbindningsaffinitet (Ki) för dopaminreceptorer enligt följande: D1-Liknande [D1 (101 nM), D5 (10 nM)] och D2-Liknande [D2 (32 nM), D3 (26 nM) och D4 (2.6 nM)] 38 (tabell 1). I den supraoptiska kärnan (SON), MPOA och PVN för hypotalamus uttrycker oxytocinerga neuroner D2, D3 och D4 receptorer och apomorfin föreslogs att inducera erektion genom aktivering av D2–Liknande receptorer i PVN 39. Aktivering av spinal dopamin D2 receptorer kan också spela en roll i den pro-erektila effekten av apomorfin som nämnts ovan 23. Matsumoto et al. 40 fann att i isolerad erektilvävnad från råttor verkar apomorfininducerad relaxation involvera dopamin D1 och D2 receptorer, men författarna drog slutsatsen att "vid relevanta systemiska doser av apomorfin är perifera effekter av föreningen osannolikt att bidra till dess pro-erektila effekter hos råttor". Därför stöder den bindande profilen och studierna av erektil funktion huvudsakligen ett engagemang av central D2-Liknande receptorer i den pro-erektila effekten av apomorfin.
Apomorfin utvecklades för behandling av Parkinsons sjukdom, men en stor nackdel är induktion av illamående och kräkningar. Genom sublingual administrering av apomorfin hittades emellertid ett acceptabelt terapeutiskt fönster som möjliggjorde induktion av erektion och sänkning av incidensen av biverkningar (gäspningar, illamående, kräkningar, yrsel, dimsyn, diafores, blekhet, mild hypotoni och bradykardi) observerad av intranasal administrering av apomorfin 41. I en fas III-studie av effekten av apomorfin på ED med måttlig till svår dysfunktion hos 74% av männen inträffade apomorfininducerade erektioner 10–25 min. efter administrering. Dessutom ledde apomorfin i denna studie till erektion lämplig för samlag hos 54.4% kontra 33.8% i placebogruppen 42. I en observations kohortstudie efter marknadsföring av 11,185-män som presenterades med ED i allmän praxis var dock den främsta orsaken till att stoppa behandlingen med apomorfin att läkemedlet var ineffektivt i 64.7% av patienterna 43.
Som nämnts har apomorfin en serie potentiella biverkningar. Den vanligaste biverkningen av den sublinguala formuleringen av apomorfin i studien efter marknadsföring var huvudvärk 43och liknande hypotoni och gäspningar är denna effekt förmodligen förutsägbar av effekten på dopaminreceptorer. Apomorfin har emellertid också visats i låga koncentrationer för att aktivera övergående receptorpotential ankyrin 1 (TRPA1) -kanaler involverade i smärtkänsla, inflammation och illamående 44, vilket antyder att bindning utanför målet bidrar till biverkningarna av apomorfin.
Selektiv dopamin D1 receptoragonister och erektil funktion
I de första studierna av effekten av apomorfin-mikroinjicerad i PVN blockerades den pro-erektila effekten både av dopamin D1 receptorantagonist, SCH 23390, och dopamin D2 receptorantagonister, haloperidol och (-) - sulpirid 12. Fenoldopam är ett bensazepinderivat och en selektiv partiell agonist främst vid dopamin D1 receptorer (tabell 1och har ingen signifikant affinitet för dopamin D2 receptorer, men binder med måttlig affinitet till a2adrenoceptorer. Det är registrerat som ett antihypertensivt läkemedel främst för behandling av hypertensiv kris och / eller perifer kärlsjukdom. Systemisk infusion av fenoldopam-dos potentiellt ökade ökningarna i intrakavernosaltrycket (ett mått på erektil funktion) som framkallas genom submaximal elektrisk stimulering av den distala delen av den cavernösa nerven i anestetiserade råttor 45. Även in vitro studier visade att kväveoxid deltog i relaxationer av corpus cavernosum inducerat av fenoldopam och en annan dopamin D1 receptorselektiv agonist, A ‐ 68930 31, 45, in vivo den pro-erektila effekten av fenoldopam varade i närvaro av en NOS-hämmare, vilket tyder på att det finns en direkt pro-erektil effekt av fenoldopam. Dessa fynd måste emellertid bekräftas av andra studier, och det vore också intressant att klargöra om lokal administration eller systemisk administration av fenoldopam i intakt medvetna djur och / eller människor leder till erektion.
Selektiv dopamin D2 och D3 receptoragonister och erektil funktion
Liknar apomorfin, dopamin D2/D3 agonister, bromokriptin och kineloran, inducerar spontana erektioner och ökar antalet erektilhändelser hos råttor 46-48, troligen genom aktivering av oxytocinerga nervceller i PVN hos råttor 47. Dopamin D2 och D3 receptorer har 50% homologi i struktur, och det har visat sig svårt att få föreningar selektiva för dopamin D3, i motsats till D2receptorer 49. Dopamin D2 receptorer har varit målet för behandling av rörelsestörningar relaterade till Parkinsons sjukdom med dopamin D2 agonister, medan modulering av dopamin D3 receptorer är av intresse för behandling av Parkinsons sjukdom, drogberoende och schizofreni 49, 50. Flera av dopaminagonisterna, till exempel bromokriptin, cabergolin, pergolid, ropinirol och rotigotin, som används för behandling av denna sjukdom har dopamin D2 receptoragonisteffekter (tabell 1), och de kan också associeras med ökad libido (hypersexualitet). Långvarig erektion (> 4 timmar) definierad som priapism hos människa har beskrivits i fallrapporter för kabergolin och rotigotin 51, 52 och är förödande för erektil funktion. Förutom effekt på dopamin D2 receptorer, cabergolin och rotigotin binder båda till och motverkar a1–Adrenoceptorer och antagonism av α1–Adrenoceptorer är ofta orsak till priapism 53.
Antalet studier som undersöker effekten av dopamin D2 och D3 agonister för behandling av sexuell dysfunktion är begränsade. I en öppen studie där 13 patienter rapporterade sexuell dysfunktion efter att de började med antidepressiv behandling visade sexuell funktion, mätt med Arizona Sexual Experience Scale och Clinical Global Impression of Improvement scales, en signifikant effekt på båda skalorna 3 veckor efter behandlingsstart. med ropinirol 54. Doserna av ropinirol (3–4 mg / dag) i den senare studien var markant lägre än de doser (20-25 mg / dag) som beskrivits för att orsaka hypersexualitet och sexuella behov hos patienter med Parkinsons sjukdom 10, 54. Därför är potentialen för behandling av ED av blandat ursprung av selektiva agonister för dopamin D2 eller D3 receptorer återstår att utforska, även om effekterna på potentiellt allvarliga biverkningar som beteende och blodtryck bör beaktas. Dessutom skulle det vara relevant att genomföra randomiserade, dubbelblinda studier med låga doser av dessa agonister för behandling av antidepressiva inducerade sexuell dysfunktion.
Selektiv dopamin D4 receptoragonister och erektil funktion
En selektiv dopamin D4 receptoragonist, PD168077, visade sig inducera erektion hos råttor när mikroinjicerad i PVN 47, 55, 56. Genom färgning för Fos i oxytocinerga nervceller i PVN kunde PD168077, i motsats till quineloran, emellertid inte påvisas aktivera dessa neuroner. Dessutom var effekten av PD168077 kontextberoende; till exempel observerades effekten i närvaro av mottagliga honråttor och kan involvera dopamin D4 receptoraktivering av det magnocellulära oxytocinsystemet 47.
Apomorfin har hög affinitet för dopamin D4 receptorer, men den binder också till dopamin D2 receptorer med hög affinitet (tabell 1). För att undvika dosbegränsande biverkningar förmedlade av D2 receptorer, till exempel illamående och emes, dopamin D4 receptoragonister, ABT 724 och ABT 670, utvecklades för behandling av ED. Hos fritt rörliga råttor mättes ökningar i intracavernosal tryck och visade att ABT 724 administrerat subkutant dos-beroende ökade incidensen och storleken på spontana erektioner, och dessa svar var större och av längre varaktighet i närvaro av en PDE5i, sildenafil 57. Injektion i illrar, som en preklinisk modell för illamående och emes, avslöjade att i motsats till en selektiv dopamin D2 receptoragonist, PNU ‐ 95666E, ABT 724 i ganska höga doser hade inte dessa effekter 57. En annan dopamin D4 receptoragonist, ABT 670, med bättre oral biotillgänglighet utvecklades, men det har markant mindre affinitet till dopamin D4 receptorer jämfört med ABT 724 (tabell 1, 58). Vid subkutan administrering var förekomsten av ABT 670-inducerade penistektioner mindre än observerats med samma dos av apomorfin 58. Dessa data överensstämmer med observationerna att ABT 724 och ABT 670 är mindre potent och har mindre effekt jämfört med apomorfin, förmodligen förklaras också av observationerna att de är partiella agonister vid dopamin D4 receptorer 57, 58. Utvecklingen av dessa dopamin D4 agonister, ABT 724 och ABT 670, nådde respektive fas I- och fas II-studier. Trots tydligen mindre biverkningar med ABT 724 och ABT 670 jämfört med apomorfin var därför styrkan och effekten lägre. Här också upptäckten att effekten på erektil funktion av dopamin D4 receptorer är kontextberoende kan spela en roll för resultatet.
Selektiv dopamin D5 receptoragonister och erektil funktion
Information om effekten av dopamin D5 receptoragonister på sexuell funktion är begränsade. Flera studier har utförts för att identifiera uttrycksområdena för dopamin D5 receptorer. Dopamin D5 receptorn uttrycks i hypotalamus och den parafascikulära kärnan i talamus i hjärnan hos råttan och människan. De olika uttrycksområdena för dopamin D5 receptorer kontra andra dopaminreceptorer antyder att dopamin D5 receptorer spelar en roll som regulator och integrator av dopaminerg funktion 59. Dopamin D5 receptorer uttrycks också i andra hjärnområden, till exempel substantia nigra-pars compacta, striatum, cerebral cortex, nucleus accumbens och luktknölen 60. En ny rapport visade att knockout av dopamin D5 receptorer minskar den sexuella mottagligheten hos kvinnliga möss och hos män påverkar de givande effekterna av pre-ejaculatory penom intromission 61. Minskning av sexuellt intresse, ED och utlösningsproblem finns hos patienter med antipsykotika 62. Därför en dopamin D5 receptoragonist kan vara ett komplement för att förbättra sexuell disposition och troligtvis libido hos dessa patienter.
Sammanfattningsvis är agoniststimulering av dopaminreceptorer ett sätt framåt för att uppnå pro-erektila effekter, och både centrala och perifera dopaminreceptorer är potentiella mål för behandlingen av ED. Det verkar som om de erektila effekterna är beroende av aktiveringen av dopamin D2, D3, D4 receptorer i CNS och i periferin huvudsakligen beroende av dopamin D1 receptoraktivering i corpus cavernosum (fig. 1). Även om apomorfin verkade som ett lovande läkemedel för behandling av ED, representerar det den första generationen. Kravet för nästa generation är att läkemedelskandidaterna har åtminstone samma effekt vid exempelvis D3/D4 receptorer och samtidigt undvika biverkningarna av apomorfin.
Dopaminreceptorantagonister och erektil funktion
Antipsykotika och erektil funktion
De flesta antipsykotiska läkemedel binder till och motverkar effekten av dopamin vid dopamin D2 receptorer, till exempel haloperidol. Därför är äldre antipsykotiska läkemedel ofta förknippade med minskad erektion och anorgasmi hos 30 – 60% av patienterna, medan nyare antipsykotika verkar ha lägre förekomst av sexuell dysfunktion 5, 62. Bland de nyare antipsykotika verkar risperidon ha den högsta frekvensen av sexuell dysfunktion, medan det inte finns tillräcklig information om aripiprazol och ziprasidon. En pilotstudie som bytte behandling från atypiska antipsykotika, risperidon, amisulpride och olanzapin till aripiprazol förbättrade uppenbarligen den sexuella prestationen hos en liten patientpopulation 63, men detta måste bekräftas av studier med större antal patienter.
Det är svårt att skilja sjukdomen från läkemedelseffekten och att få tillförlitlig information från patienter med psykotisk sjukdom. Således påverkar den sexuella dysfunktionen som är associerad med den antipsykotiska behandlingen inte bara erektil funktion, utan minskar också libido, orsakar retrograd utlösning och minskar sexuell upphetsning och sexuell tillfredsställelse. En ny Cochrane-granskning undersökte möjligheterna till intervention mot sexuell dysfunktion hos patienter i behandling med antipsykotika och föreslog att byte till olanzapin kan förbättra sexuell funktion både hos män och kvinnor. 64. Dessa resultat baserades dock på en liten öppen etikettest, och en annan möjlighet är att behandla patienterna med schizofreni och ED med sildenafil, men återigen är bevisen gles 64.
Buspiron
Buspirone är ett ängslöst läkemedel med mindre sexuell funktion jämfört med SSRI och kan till och med vända den sexuella dysfunktionen i samband med SSRI-behandling 65, 66. Buspirone är en partiell agonist på 5 ‐ hydroxytryptamin typ 1A (5 ‐ HT1A receptorer), men både buspiron och de viktigaste 5 ‐ och 6 ‐ hydroxylmetaboliterna binder till dopamin D3 och D4 receptorer med affiniteter jämförbara med bindningen till 5-HT1A receptorer, och de fungerar som antagonister vid båda dopamin D3 och D4 receptorer 67. Aktivering av 5 ‐ HT1A receptorer av agonister, till exempel 8 – OH ‐ DPAT, hämmar penile erektion hos råttor, medan antagonister för denna receptor förstärker den akuta pro-erektila effekten av subkutant administrerad apomorfin och fluoxetin 68. Därför desto mindre påverkan av erektil funktion observeras med buspiron kontra SSRI kan antagligen tillskrivas buspiron som fungerar som antagonist på 5 ‐ HT1A receptorer, men ytterligare studier kommer att krävas för att fullt ut förstå mekanismen som ligger bakom effekten av buspiron kontra SSRI om erektil funktion.
Läkemedel som ökar det synaptiska dopamininnehållet
Det synaptiska dopamininnehållet kan ökas antingen genom ökad frisättning av dopamin, genom hämning av dopaminåterupptagningstransportören (DAT) eller genom att blockera nedbrytningen av dopamin genom hämning av katekol-O‐Metyltransferas (COMT) eller monoaminoxidas (MAO) typ B-hämmare.
Frisättning av dopamin
Amantadin
Det antivirala läkemedlet amantadin stimulerar frisättningen av dopamin från nervterminalerna och hämmar återupptag av dopamin i den presynaptiska neuronen. Dessutom är det en svag antagonist vid N-metyl-d-Aspartat (NMDA) receptorer. Trots en lång halveringstid på 10–15 timmar hos människa anses effekterna vara kortlivade eftersom det finns utveckling av tolerans mot läkemedlet. I flera fallrapporter där män och kvinnor var i behandling med antidepressiva medel, till exempel fluoxetin och paroxetin, har det rapporterats att tillsats av behandling med amantadin reverserade den sexuella dysfunktionen (anorgasm, ED) 10, 69. Emellertid kommer randomiserade studier att behövas för att utvärdera huruvida amantadin i själva verket är användbart för att vända sexuell dysfunktion hos patienter som behandlas med antidepressiva medel.
Amfetamin och metamfetamin
Oral metamfetamin används för behandling av hyperaktivitetsstörningar i uppmärksamhetsunderskott och också som fritidsläkemedel. Amfetamin har rapporterats väcka sexuellt beteende 70. Amfetamin är förknippat med ökad frisättning av dopamin, men också ökad frisättning av noradrenalin från sympatiska nerver, vilket kommer att leda till sammandragning av penisartärer och corpus cavernosum 71. Därför leder metamfetamin missbruk och / eller kronisk användning ofta till ED, en effekt som också kan reproduceras hos råttor 72. PDE5i, till exempel tadalafil, förbättrar erektilfunktion hos råttor kroniskt behandlade med metamfetamin 72, och detta kan förklara rekreationsanvändningen som kombinerar metamfetamin / amfetamin med intaget av en PDE5i 73, 74.
Clavulansyra
Clavulansyra är en beta-laktamashämmare och används ofta i kombination med penicillin för att förhindra nedbrytning av penicillinet, till exempel amoxicillin, av bakteriell beta-laktamas. Clavulansyra är oralt aktiv och stabil och cirka 25% når cerebrospinalvätskan hos människor. Testning av icke-mänskliga primater med klavulansyra visade sig öka den sexuella upphetsningen 75, och därför testades läkemedlet hos hanråttor som exponerades för honråttor som fördes in i sexuellt beteendeströss genom injektion av 50 μg östradiolbensoat och antalet intromissioner och utlösningar mättes 76. Eliminationshalveringstiden för klavulansyra är cirka 1 timme 77, men endast mindre akut pro-sexuell aktivitet observerades vid den högsta administrerade dosen. Efter 7 dagars behandling ökade dock klavulansyra både antalet utlösningar och intromissioner, medan SSRI, paroxetin, minskade sexuell aktivitet 76. Uppenbarligen binds clavulansyra inte till en serie klassiska neurotransmitterreceptorer 75, men i odlade neuronala cellinjer (PC12- och SH ‐ SY5Y-celler) ökade stimulering med en relativt hög klavulansyrakoncentration (100 μM) frisättningen av dopamin, troligen genom bindning till två proteiner av betydelse för neurosekretion och vesikeltransport 78. De förväntade cerebrospinalkoncentrationerna av klavulansyra med ångestdämpande och erektil effekter ligger i intervallet 1–10 pM 75. Att denna mekanism kunde spela en roll stöds ytterligare av observationerna att en dopamin D2 receptorantagonist motverkar den pro-erektila effekten av klavulansyra hos råttor 79. I den senare studien jämfördes effekten av klavulansyra administrerad genom intraperitoneal injektion med apomorfin, och medan apomorfin inducerade koncentrationsberoende ökningar av antalet spontana erektioner, var koncentrationssvarskurvan för klavulansyra klockformad med maximal effekt vid 1 mg / kg och minskar sedan med högre doser 80. Författarna föreslog att utöver ökande dopaminfrisättning kan klavulansyra också öka frisättningen av serotonin som verkar vid 5-HT2C receptorer, eftersom mianserin också antagoniserade den pro-erektila effekten av klavulansyra. En fas II-studie planerades för att undersöka effekten av clavulanic hos patienter, men den avbröts 11. Det återstår att lösa en serie problem för klavulansyra inklusive de mål som är involverade i den pro-erektila effekten och en förklaring till den klockformade dos-svarskurvan för klavulansyra på erektil funktion.
Hämning av transportören för återupptag av dopamin
Kokain
Beroendeframkallande läkemedel inklusive kokain anses normalt förbättra dopamin inom den mesotelencefala belönings- / förstärkningscirkeln i förhjärnan, främst i nucleus accumbens 81, men andra vägar observerade av magnetisk resonansbild inklusive subcallosal cortex caudate, putamen, basal förhjärna, thalamus, insula, hippocampus, parahippocampal gyrus, cingulat, temporala cortices, parietal cortex, extra-striatal cortices och pons spelar också en viktig roll i kokainmissbruk 82. Dessutom spelar farmakokinetiken och snabb penetration till CNS en viktig roll för missbruk av kokain 83. Kokain hämmar de pre-synaptiska transportörerna för noradrenalin (NET), dopamin (DAT) och serotonin (SERT), vilket ökar de synaptiska koncentrationerna av noradrenalin, dopamin och serotonin. Kokain kan öka sexuell upphetsning och leda till erektion av penis 84, men kronisk användning av kokain är associerad med ED hos människor 85, D1/D5 antagonister som SCH39166 (ecopipam) kan dämpa de euforiska effekterna av kokain 86. Centralt administrerat kokain hämmar uppenbarligen erektion av penis hos råttor via noradrenerg neurotransmission, vilket aktiverar α-adrenoceptorer i hippocampus 87. På perifer nivå visade sig kokaininducerad endotelial dysfunktion med ökad bildning av endotelin-1 och reducerad kväveoxid och vasokonstriktion bidra till kokaininducerad ED 85. Dessa fynd visar ett bra samband mellan normal erektil funktion av hjärnaktiverade områden och hjärnaktiverade områden med kokain, vilket antyder att läkemedel för att förbättra erektil funktion med påverkan på monoamintransportörerna bör ha selektivitet för dopamintransportören. Dessutom bör ett läkemedel utan ett snabbt påbörjande av hämningen av återupptag av dopamin syfta till att undvika missbruk som observerats för kokain.
bupropion
Antidepressiva agerar i varierande grad på monoamintransportörerna. Selektiviteten är hög för hämning av SERT av SSRI, till exempel fluoxetin, och dessa läkemedel är ofta associerade med sexuell dysfunktion. Depression i sig gör det svårt att skilja effekten av sjukdom från läkemedlets tillsatseffekt. Humörstörningar kan leda till bristande intresse och känslomässigt tillbakadragande från sexpartnern. Antidepressiva kan ha många effekter på sexuell funktion inklusive minskad sexuell lust, erektionssvårigheter och orgasmproblem. SSRI och venlafaxin kan påverka alla steg i den manliga sexuella responscykeln (lust / upphetsning - spänning – orgasm). Som sammanfattat baserat på femton randomiserade studier har bupropion, nefazodon och mirtazapin lägre frekvenser av sexuell dysfunktion än SSRI: er 9, 88och bupropion kan användas för att lindra sexuella symtom orsakade av andra antidepressiva läkemedel 89, 90. Bupropion är hittills den enda antidepressiva med viss selektivitet för DAT över NET och SERT med Ki värden (nM) för respektive 526, 52,600 och 9100 för de tre transportörerna. Infusion av bupropion i MPOA hos råttor ökade dopamin mätt genom mikrodialys och framkallade erektioner hos penna hos råttor 91, men en ganska hög koncentration (10 mM) av bupropion måste appliceras för att observera effekten 91 vilket antyder att MPOA inte är den primära platsen där bupropion verkar eller att läkemedlet under akut infusion aktiverar andra anti-erektilvägar. Akut systemisk administrering av bupropion reducerade faktiskt penilexektioner hos råttor, medan bupropionbehandling i 14 dagar (kronisk behandling) inte var associerad med förändringar i penilexektioner hos råttor, vilket var i kontrast till behandling med fluoxetin eller desipramin, en hämmare av främst NET 92. Dessa fynd antyder att inte bara en uppreglering av dopamin i den synaptiska klyftan troligen är tillräcklig för att förklara en pro-erektil effekt. Förändringar i dopamininnehåll är förknippade med förändrat dopaminreceptoruttryck 35, 93 och kan förklara skillnader i de akuta och kroniska effekterna på erektil funktion hos centralt verkande hämmare av monoamintransportörer.
Fördelning av dopamin
Selegilin
Selegiline är en selektiv, irreversibel hämmare av MAO B och används ensam eller i kombination med levodopa vid behandling av Parkinsons sjukdom. Hämningen av MAO B kommer att fördröja nedbrytningen och förlänga dopaminens verkan. Selegilin genomgår metabolism till amfetamin och metamfetamin, vilket också kan bidra till de farmakologiska effekterna på erektilfunktionen som beskrivs ovan för amfetamin och metamfetamin. Selegiline förstärker effekten av dopamin i PVN hos råttor 94. Därför applicerades selegilin eller vehikel under 3 veckor för behandling av sexuell dysfunktion hos patienter i antipsykotisk behandling i placebokontrollerad crossover-studie. Förutom minskning av prolaktin inducerat av selegilin fanns det ingen skillnad i sexuell funktion jämfört med placebobehandlingsperioden 95.
katekolO-Metyltransferasinhibitorer
COMT-hämmare entakapon och tolcapon används som ett komplement till levodopa för försämring av dosen i slutet av Parkinsons sjukdom och de ökar levodopatillgängligheten i hjärnan. Endast tolkapon tränger in i hjärnan och ökar dopamin i pre-frontal cortex och ventral hippocampus, men denna effekt är mer uttalad hos kvinnor jämfört med hanråttor 96. Det är emellertid oklart om hämning av perifert COMT, som också ökar noradrenalin, kommer att motverka den centrala effekten av ökande dopamin på sexuell funktion, och detta återstår att klargöra.
Modulering av dopaminergiska vägar och utlösning
När man överväger läkemedel för behandling av ED är effekten på utlösning också mycket relevant. Fysiologi och farmakologi för utlösning har nyligen granskats omfattande 97, 98, och här är bara en kort beskrivning av rollen för de dopaminergiska vägarna vid utlösning. Den incertohypothalamic vägen som inkluderar MPOA verkar vara involverad i kontrollen av utlösningsresponsen. I båda fallen inducerar ökningar i extracellulära dopaminnivåer i MPOA och injektion av apomorfin i MPOA förkortning av ejakulationslatenstiden med ökat antal utlösningar och kopulationshastighet hos hanråttor 97. Dopamin D3 receptorn verkar spela en viktig roll, som D2/D3 receptoragonist 7 ‐ hydroxy‐N,Ndi-n‐Propyl ‐ 2 ‐ aminotetralin (7 ‐ OH ‐ DPAT) förbättrar ejakulatoriskt beteende, medan blockad av dopamin D3 receptorer med mycket selektiva antagonister förlänger ejakulationslatens och den eldfasta perioden efter ejakulation 99. Därför D3 receptorantagonister har också föreslagits för behandling av för tidig utlösning 97även om 7 ‐ OH ‐ DPAT hade visat en delvis återhämtning i utlösningsreflexer i en modell av ryggmärgsskada 100. Polymorfism med ökat antal upprepningar av DAT1-transportergenen har föreslagits vara kopplat till mänsklig för tidig utlösning 101medan det är mindre tydligt om en hämmare av DAT, bupropion, i terapeutiska koncentrationer påverkar utlösning. Dapoxetin och off-label SSRI är effektiva och säkra för behandling av för tidig utlösning, medan det återstår att undersöka hos människor om det skulle ha en gynnsam effekt av dopamin D3 receptorantagonister. De vägar som är involverade i utlösning förstås fortfarande ofullständigt 98och med tanke på läkemedel som specifikt förändrar de dopaminergiska vägarna för behandling av ED, skulle det vara relevant att undersöka också effekten på utlösning i hälsa och sjukdomar för att säkerställa den allmänna sexuella funktionen.
Modulering av dopaminergiska vägar och omöjliga behov hos patienter med erektil dysfunktion
Trots att PDE5-hämmare är effektiva läkemedel finns det fortfarande stora populationer av patienter där denna behandling är otillräcklig eller kan optimeras inklusive patienter med ED som lider av diabetes, metaboliskt syndrom, neurodegenerativ sjukdom och patienter som har genomgått en radikal prostatektomi som påverkar cavernös nerver. I det följande har vi fokuserat på diabetes och neurodegenerativ sjukdom där vi tycker att läkemedel som modulerar de dopaminergiska vägarna kommer att vara av intresse. Många av övervägandena beträffande metaboliskt syndrom liknar diabetes, medan vi finner nervskador i samband med radikal prostatektomi eller bäckenoperation kräver andra tillvägagångssätt och detta har tagits upp någon annanstans 102.
Diabetes och erektil funktion
Diabetes är förknippat med en markant högre risk för ED än i den allmänna befolkningen 103-105. I kliniker som behandlar ED är förekomsten av diabetes som komorbiditet 20 – 25% 106. Intensiv glykemisk kontroll minskar förekomsten av ED 10 år senare hos unga män med typ 1-diabetes 107. Det finns emellertid brist på effekt av PDE5-hämmare hos 50% av patienterna som lider av diabetes och ED 8, 108-110. Dessa observationer antyder att utöver affektion av den perifera vävnaden som är involverad i erektion, påverkar diabetes också den komplexa växelverkan mellan sensoriska och autonoma nerver involverade i erektion.
Affektionen av erektilvävnad och perifera parasympatiska nerver vid diabetes är väl beskrivet. I korthet har endotelcelldysfunktion, dysfunktion i glatt muskel och autonom neuropati beskrivits hos diabetiska råttor och i isolerad vävnad från diabetiker. 111, 112 (se Ref. 5). Dessutom är hypogonadism vanligare hos patienter med diabetes och ED jämfört med icke-diabetiker med ED. På grund av bristande effekt av PDE5-hämmare har tillskott med testosteron och även läkemedel som riktar sig till Rho-kinasvägen undersökts och testats hos patienter med ED och diabetes 113-115.
Diabetesens påverkan av centrala vägar involverade i erektil funktion är mindre väl beskrivna. Emellertid är prevalensen av ED hos patienter med diabetisk neuropati nära 100% 116. Hos råttor med spontan utveckling av diabetes hittades BB / WOR-råtta, både centrala och perifera neuropatier, involverad i den sexuella dysfunktionen. 117. Minskning i mikrovaskulärt flöde har föreslagits att spela en roll för utvecklingen av perifer neuropati associerad med ED 118. Andra mekaniker verkar också spela en roll. I streptozotocin-inducerade diabetiska råttor av typ 1, undersöktes NMDA-inducerad erektion genom direkt injektion i PVN 119. NMDA stimulerar samma oxytocinergiska vägar som dopamin, och det fanns ED och reducerat uttryck av neuronal NOS i PVN 119. Författarna fann att både träning och behandling med angiotensin II typ 1 (AT1) receptorantagonister förbättrar erektil funktion i den streptozocininducerade diabetiska råttmodellen 120, 121, men effekten av dopaminerge läkemedel på erektil funktion återstår att undersökas i djurmodeller med diabetes.
Det finns bevis för att diabetes påverkar de centrala dopaminerga vägarna och leder till sjukdom. Risken för Parkinsons sjukdom var ~ 40% högre bland patienter med diabetes än bland patienter utan diabetes 122och insulinresistens i hjärnan i hjärnspecifik knockout av insulinreceptorn inducerar ökade nivåer av monoaminoxidas typ B, ökad dopaminomsättning och minskad frisättning av dopamin 123. Hos möss med hög fettsinducerad diabetes finns det en förlust av dopaminerga nervceller 124. Dessa resultat tyder på att affektion av dopaminerge vägar i diabetes också kan spela en roll i ED. Den centralt verkande dopaminerga agonisten, apomorfin, inducerade emellertid endast effekten jämförbar med placebo hos 130-patienter med diabetes och ED, och den typiska respondern var ung och med god glykemisk kontroll 125. Ytterligare studier kommer att krävas för att förstå om modulering av de dopaminergiska vägarna inte bara i centrala utan också på perifer nivå kan återställa erektil funktion vid diabetes.
Neurodegenerativ sjukdom och erektil dysfunktion
Effekterna av neurodegenerativa sjukdomar, Parkinsons sjukdom och Alzheimers sjukdom, på sexuell dysfunktion och rekommenderad behandling har nyligen granskats av andra. 126. Sexuell dysfunktion är vanligt hos patienter med dessa störningar, och ED anses vara en av de mest störande associerade funktionsnedsättningarna 127. PDE5i och apomorfin är effektiva hos de flesta patienter med Parkinsons sjukdom och ED 42även om högre doser än den som rekommenderas av apomorfin kommer att krävas 127. Som nämnts i förhållande till de olika dopaminerga läkemedlen i avsnitten ovan måste läkemedelsinducerad hypersexualitet också hanteras för att ge en optimal behandling med dopaminerga läkemedel vid Parkinsons sjukdom.
Slutsatser och perspektiv
Vi har fokuserat på modulering av den dopaminerga vägen för behandling av ED. En serie dopaminerga agonister påverkar erektil funktion i gnagare med central aktivering av dopamin D2–Liknande receptorer och huvudsakligen av D1-Liknande receptorer i erektilvävnad. Det terapeutiska fönstret för den allmänna dopaminagonisten apomorfin är smalt och verkar huvudsakligen på centrala dopaminreceptorer. Därför befanns apomorfin misslyckas hos patienter med ED och diabetes och var mindre effektiva jämfört med PDE5-hämmare. Föreliggande MiniReview av litteraturen föreslår att modulering av de dopaminerge vägarna ger en möjlighet att förbättra behandlingen av ED. Detta kan emellertid kräva ett nytt tillvägagångssätt som riktar sig till den dopaminergiska vägen vid flera nivåer av penreflexbågen. Vidare skulle ytterligare test av dopaminerga läkemedel i djurmodeller för diabetes, metaboliskt syndrom och / eller neurodegenerativ sjukdom vara relevant.
Tack
Ulf Simonsen är en del av MEMBRANES, Aarhus University, medan Simon Comerma ‐ Steffensen fick stöd av ett doktorandbidrag från Aarhus University.
Intressekonflikter
Författarna förklarar ingen intressekonflikt.
- 1Andersson KE. Mekanismer för erektion av penis och grund för farmakologisk behandling av erektil dysfunktion. Pharmacol Rev 2011;63: 811-59.
- 2Melis MR, Argiolas A. Central kontroll av erektionen av penis: en återbesök av oxytocins roll och dess interaktion med dopamin och glutaminsyra hos hanråttor. Neurosci Biobehav Rev 2011;35: 939-55.
- 3Giuliano F, Bernabe J, Jardin A, Rousseau JP. Det sympatiska nervsystemets antierektila roll hos råttor. J Urol 1993;150: 519-24.
- 4Dail WG, Barba V, Leyba L, Galindo R. Neural och endotelial kväveoxidsyntasaktivitet i erektil vävnad hos råtta. Cell Tissue Res 1995;282: 109-16.
- 5Gratzke C, Angulo J, Chitaley K, Dai YT, Kim NN, Paick JS et al. Anatomi, fysiologi och patofysiologi av erektil dysfunktion. J Sex Med 2010;7: 445-75.
- 6Goldstein I, Jones LA, Belkoff LH, Karlin GS, Bowden CH, Peterson CA et al. Avanafil för behandling av erektil dysfunktion: en multicenter, randomiserad, dubbelblind studie på män med diabetes mellitus. Mayo Clin Proc 2012;87: 843-52.
- 7Porst H, Burnett A, Brock G, Ghanem H, Giuliano F, Glina S et al. SOP-konservativ (medicinsk och mekanisk) behandling av erektil dysfunktion. J Sex Med 2013;10: 130-71.
- 8Nehra A, Jackson G, Miner M, Billups KL, Burnett AL, Buvat J et al. Princeton III-konsensusrekommendationerna för hantering av erektil dysfunktion och hjärt-kärlsjukdom. Mayo Clin Proc 2012;87: 766-78.
- 9Taylor MJ, Rudkin L, Hawton K. Strategier för att hantera antidepressiva inducerade sexuell dysfunktion: systematisk granskning av randomiserade kontrollerade studier. J Påverka Disord 2005;88: 241-54.
- 10Moll JL, Brown CS. Användning av farmakologiska monoaminer för behandling av sexuell dysfunktion: bevis i litteraturen. J Sex Med 2011;8: 956-70.
- 11Peak TC, Yafi FA, Sangkum P, Hellstrom WJ. Emerging mediciner för behandling av erektil dysfunktion. Expert Opin Emerg Drugs 2015;20: 263-75.
- 12Melis MR, Argiolas A, Gessa GL. Apomorfininducerad erektion och gäspning: verkningsplats i hjärnan. Brain Res 1987;415: 98-104.
- 13Argiolas A, Hedlund H. Farmakologin och klinisk farmakokinetik för apomorfin SL. BJU Int 2001;88(Suppl 3): 18-21.
- 14Argiolas A, Melis MR, Mauri A, Gessa GL. Paraventrikulär nukleusskada förhindrar gäspning och erektion av penis inducerad av apomorfin och oxytocin men inte av ACTH hos råttor. Brain Res 1987;421: 349-52.
- 15Chen KK, Chan JY, Chang LS. Dopaminerg neurotransmission vid den paraventrikulära kärnan i hypothalamus i central reglering av peniminektion hos råttan. J Urol 1999;162: 237-42.
- 16Hull EM, Muschamp JW, Sato S. Dopamin och serotonin: påverkan på manligt sexuellt beteende. Physiol Behav 2004;83: 291-307.
- 17Bjorklund A, Lindvall O, Nobin A. Bevis på ett incerto-hypothalamic dopamin-neuronsystem hos råtta. Brain Res 1975;89: 29-42.
- 18Skagerberg G, Lindvall O. Organisering av diencefaliska dopaminneuroner som projicerar till ryggmärgen i råttan. Brain Res 1985;342: 340-51.
- 19Skagerberg G, Bjorklund A, Lindvall O, Schmidt RH. Ursprung och avslutning av diencephalo-spinal dopaminsystemet hos råtta. Brain Res Bull 1982;9: 237-44.
- 20Ridet JL, Sandillon F, Rajaofetra N, Geffard M, Privat A. Råttens spinala dopaminergiska system: mikroskopisk ljus- och elektronstudie med antiserum mot dopamin, med särskild tonvikt på synaptisk incidens. Brain Res 1992;598: 233-41.
- 21Holstege JC, Van DH, Buijs RM, Goedknegt H, Gosens T, Bongers CM. Fördelning av dopaminimmunreaktivitet i rått-, katt- och apa ryggmärgen. J Comp Neurol 1996;376: 631-52.
- 22Van DH, Dijk J, Voom P, Holstege JC. Lokalisering av dopamin D2-receptor i ryggradsmärg identifierad med immuncytokemi och in situ hybridisering. Eur J Neurosci 1996;8: 621-8.
- 23Giuliano F, Allard J. Dopamin och manlig sexuell funktion. Eur Urol 2001;40: 601-8.
- 24Giuliano F, Allard J, Rampin O, Droupy S, Benoit G, Alexandre L et al. Spinal proerektil effekt av apomorfin i den bedövade råtta. Int J Impot Res 2001;13: 110-5.
- 25Hurt KJ, Musicki B, Palese MA, Crone JK, Becker RE, Moriarity JL et al. Akt-beroende fosforylering av endotel kväveoxidsyntas medierar erektion av penis. Proc Natl Acad Sci USA 2002;99: 4061-6.
- 26Simonsen U, Garcia ‐ Sacristan A, Prieto D. Penil artärer och erektion. J Vasc Res 2002;39: 283-303.
- 27Schjorring O, Kun A, Flyvbjerg A, Kirkeby HJ, Jensen JB, Simonsen U. Flödet framkallade vasodilatation avstoppas i penilarterior från Zucker-diabetiska fettråttor. J Sex Med 2012;9: 1789-800.
- 28Lue TF, Tanagho EA. Fysiologi för erektion och farmakologisk hantering av impotens. J Urol 1987;137: 829-36.
- 29El ‐ Din MM, Senbel AM, Daabees TT, Sharabi FM. Perifer modulering av dopaminerga receptorer påverkar erektil respons hos råttor. Basic Clin Pharmacol Toxicol 2007;100: 225-32.
- 30Hyun JS, Bivalacqua TJ, Baig MR, Yang DY, Leungwattanakij S, Abdel ‐ Mageed A et al. Lokalisering av perifera dopamin-D1- och D2-receptorer i råtta corpus cavernosum. BJU Int 2002;90: 105-12.
- 31d'Emmanuele di Villa Bianca R, Sorrentino R, Roviezzo F, Imbimbo C, Palmieri A, De Dominicis G et al. Perifer relaxantaktivitet av apomorfin och av en D1-selektiv receptoragonist på humant corpus cavernosum-remsor. Int J Impot Res 2005;17: 127-33.
- 32Han DH, Chae MR, Så jag, Park JK, Lee SW. Effekterna av dopaminreceptoragonister på BK Ca-kanaler och signaltransduktionsmekanism i corpus cavernosal glatta muskelceller. Int J Impot Res 2008;20: 53-9.
- 33Mignini F, Traini E, Tomassoni D, Amenta F. Dopaminplasmamembrantransportör (DAT) i råttthymus och mjälte: en immunokemisk och immunohistokemisk studie. Auton Autacoid Pharmacol 2006;26: 183-9.
- 34Pfeil U, Kuncova J, Bruggmann D, Paddenberg R, Rafiq A, Henrich M et al. Intrinsic vaskulär dopamin - en nyckelmodulator för hypoxi-inducerad vasodilatation i splanchnic kärl. J Physiol 2014;592: 1745-56.
- 35Beaulieu JM, Espinoza S, Gainetdinov RR. Dopaminreceptorer - IUPHAR Review 13. Br J Pharmacol 2015;172: 1-23.
- 36Kebabian JW. Flera klasser av dopaminreceptorer i däggdjurens centrala nervsystem: inblandning av dopaminkänslig adenylylcyklas. Life Sci 1978;23: 479-83.
- 37Heaton JP. Viktiga problem från de kliniska studierna av apomorfin SL. World J Urol 2001;19: 25-31.
- 38Hsieh GC, Hollingsworth PR, Martino B, Chang R, Terranova MA, O'Neill AB et al. Centrala mekanismer som reglerar penile erektion hos medvetna råttor: de dopaminerge systemen relaterade till den proerektila effekten av apomorfin. J Pharmacol Exp Ther 2004;308: 330-8.
- 39Baskerville TA, Douglas AJ. Interaktioner mellan dopamin och oxytocin vid kontroll av sexuellt beteende. Prog Brain Res 2008;170: 277-90.
- 40Matsumoto K, Yoshida M, Andersson KE, Hedlund P. Effekter in vitro och in vivo av apomorfin i råttkorpus cavernosum. Br J Pharmacol 2005;146: 259-67.
- 41Heaton JP, Morales A, Adams MA, Johnston B, el Rashidy R. Återhämtning av erektil funktion genom oral administrering av apomorfin. Urologi 1995;45: 200-6.
- 42Heaton JP, Altwein JE. Apomorfins SL roll i behandlingen av erektil dysfunktion hos män. BJU Int 2001;88(Suppl 3): 36-8.
- 43Maclennan KM, Boshier A, Wilton LV, Shakir SA. Undersökning av säkerheten och användningen av apomorfin som föreskrivs i allmän praxis i England som behandling för erektil dysfunktion. BJU Int 2006;98: 125-31.
- 44Schulze A, Oehler B, Urban N, Schaefer M, Hill K. Apomorfin är en bimodal modulator av TRPA1-kanaler. Mol Pharmacol 2013;83: 542-51.
- 45Senbel AM. Interaktion mellan kväveoxid och dopaminerg överföring vid perifer kontroll av peniminektion. Fundam Clin Pharmacol 2011;25: 63-71.
- 46Sharifzadeh M, Dehpour AR, Samini M, Hassan ‐ Mazandarani H, Samadian T, Asghari GR. Förändringar av bromokriptininducerad penistektion med kronisk litium hos råttor. J Psychopharmacol 1996;10: 157-61.
- 47Baskerville TA, Allard J, Wayman C, Douglas AJ. Dopamin-oxytocin-interaktioner vid penning erektion. Eur J Neurosci 2009;30: 2151-64.
- 48Radosavljevic M, Pajovic B, Radunovic M, Radojevic N, Bjelogrlic B. Påverkan av dihydroergotoxin, bromokriptin och ergotamin på erektion med penil hos Wistar-råttor. J Androl 2012;33: 866-71.
- 49Le FB, Collo G, Rabiner EA, Boileau I, Merlo PE, Sokoloff P. Dopamin D3-receptorligander för läkemedelsberoende: uppdatering av de senaste resultaten. Prog Brain Res 2014;211: 255-75.
- 50Sokoloff P, Diaz J, Le FB, Guillin O, Leriche L, Bezard E et al. Dopamin D3-receptorn: ett terapeutiskt mål för behandling av neuropsykiatriska störningar. CNS Neurol Disord Drug Mål 2006;5: 25-43.
- 51De La Peña Zarzuelo E, Hernández Cañas V, Llorente AC. [Priapism sekundär till behandling på grund av cabergoline: den första beskrivningen av denna förening]. Actas Urol Esp 2010;34: 487-8.
- 52Cannas A, Meloni M, Mascia MM, Solla P, Orofino G, Farris R et al. Priapism och hypersexualitet förknippat med rotigotin hos en äldre parkinsonpatient: en fallrapport. Clin Neuropharmacol 2016;39: 162-3.
- 53Spagnul SJ, Cabral PH, Verndl DO, Glina S. Adrenerga alfa-blockerare: en sällsynt och förbises orsak till priapism. Int J Impot Res 2011;23: 95-8.
- 54Worthington JJ III, Simon NM, Korbly NB, Perlis RH, Pollack MH. Ropinirol för antidepressiva inducerad sexuell dysfunktion. Int Clin Psychopharmacol 2002;17: 307-10.
- 55Melis MR, Succu S, Sanna F, Melis T, Mascia MS, Enguehard ‐ Gueiffier C et al. PIP3EA och PD ‐ 168077, två selektiva dopamin D4-receptoragonister, inducerar penilexektion hos hanråttor: plats och verkningsmekanism i hjärnan. Eur J Neurosci 2006;24: 2021-30.
- 56Melis MR, Succu S, Mascia MS, Argiolas A. PD ‐ 168077, en selektiv dopamin D4-receptoragonist, inducerar penilexektion när den injiceras i den paraventrikulära kärnan hos hanråttor. Neurosci Lett 2005;379: 59-62.
- 57Brioni JD, Moreland RB, Cowart M, Hsieh GC, Stewart AO, Hedlund P et al. Aktivering av dopamin D4-receptorer genom ABT ‐ 724 inducerar peniminektion hos råttor. Proc Natl Acad Sci USA 2004;101: 6758-63.
- 58Patel MV, Kolasa T, Mortell K, Matulenko MA, Hakeem AA, Rohde JJ et al. Upptäckt av 3 ‐ metyl‐N- (1 ‐ oxy ‐ 3 ′, 4 ′, 5 ′, 6′ ‐ tetrahydro ‐ 2′H‐ [2,4′ ‐ bipyridine] ‐1′ ‐ ylmetyl) benzam ide (ABT ‐ 670), en oralt biotillgänglig dopamin för behandling av erektil dysfunktion. J Med Chem 2006;49: 7450-65.
- 59Meador ‐ Woodruff JH, Mansour A, Grandy DK, Damask SP, Civelli O, Watson SJ Jr. Distribution av D5 dopaminreceptor mRNA i råttahjärnan. Neurosci Lett 1992;145: 209-12.
- 60Khan ZU, Gutierrez A, Martin R, Penafiel A, Rivera A, de la Calle A. Dopamin D5-receptorer från råtta och mänsklig hjärna. Neuroscience 2000;100: 689-99.
- 61Kudwa AE, Dominguez ‐ Salazar E, Cabrera DM, Sibley DR, Rissman EF. Dopamin D5-receptor modulerar manligt och kvinnligt sexuella beteende hos möss. Psychopharmacology 2005;180: 206-14.
- 62Young SL, Taylor M, Lawrie SM. "Först skada inte". En systematisk översyn av förekomsten och hanteringen av antipsykotiska biverkningar. J Psychopharmacol 2015;29: 353-62.
- 63Jeong HG, Lee MS, Lee HY, Ko YH, Han C, Joe SH. Förändringar i sexuell funktion och hormoner efter gonadalaxel efter byte till aripiprazol hos manliga schizofrenipatienter: en prospektiv pilotstudie. Int Clin Psychopharmacol 2012;27: 177-83.
- 64Schmidt HM, Hagen M, Kriston L, Soares ‐ Weiser K, Maayan N, Berner MM. Hantering av sexuell dysfunktion på grund av antipsykotisk läkemedelsbehandling. Cochrane Database Syst Rev 2012;11: CD003546.
- 65Landen M, Eriksson E, Agren H, Fahlen T. Effekt av buspiron på sexuell dysfunktion hos deprimerade patienter som behandlas med selektiva serotoninåterupptagshämmare. J Clin Psychopharmacol 1999;19: 268-71.
- 66Landen M, Bjorling G, Agren H, Fahlen T. En randomiserad, dubbelblind, placebokontrollerad studie av buspiron i kombination med en SSRI hos patienter med behandling-eldfast depression. J Clin Psychiatry 1998;59: 664-8.
- 67Bergman J, Roof RA, Furman CA, Conroy JL, Mello NK, Sibley DR et al. Modifiering av självadministrering av kokain med buspiron (buspar (R)): potentiell involvering av D3 och D4 dopaminreceptorer. Int J Neuropsychopharmacol 2013;16: 445-58.
- 68Protais P, Windsor M, Mocaer E, Comoy E. Post-synaptisk 5 ‐ HT1A-receptorinvolvering i gäspningar och erektioner inducerade av apomorfin, fysostigmin och mCPP hos råttor. Psychopharmacology 1995;120: 376-83.
- 69Balogh S, Hendricks SE, Kang J. Behandling av fluoxetininducerad anorgasmia med amantadin. J Clin Psychiatry 1992;53: 212-3.
- 70Angrist B, Gershon S. Kliniska effekter av amfetamin och L ‐ DOPA på sexualitet och aggression. Compr Psykiatri 1976;17: 715-22.
- 71Rothman RB, Baumann MH, Dersch CM, Romero DV, Rice KC, Carroll FI et al. Amfetamin-typstimulanter av centrala nervsystemet frisätter noradrenalin mer kraftfullt än de frisätter dopamin och serotonin. Synapsen 2001;39: 32-41.
- 72Tar MT, Martinez LR, Nosanchuk JD, Davies KP. Effekten av metamfetamin på en djurmodell av erektil funktion. andrologi 2014;2: 531-6.
- 73Mansergh G, Shouse RL, Marks G, Guzman R, Rader M, Buchbinder S et al. Användning av metamfetamin och sildenafil (Viagra) är kopplade till oskyddade mottagande respektive infogande analsex i ett prov av män som har sex med män. Sex Transm Infect 2006;82: 131-4.
- 74Prestage G, Jin F, Kippax S, Zablotska I, Imrie J, Grulich A. Användning av olagliga droger och mediciner med erektil dysfunktion och efterföljande HIV-infektion bland homosexuella män i Sydney, Australien. J Sex Med 2009;6: 2311-20.
- 75Kim DJ, King JA, Zuccarelli L, Ferris CF, Koppel GA, Snowdon CT et al. Clavulansyra: en konkurrenskraftig hämmare av beta-laktamaser med ny ångestdämpande aktivitet och minimala biverkningar. Pharmacol Biochem Behav 2009;93: 112-20.
- 76Chan JS, Kim DJ, Ahn CH, Oosting RS, Olivier B. Clavulansyra stimulerar sexuellt beteende hos hanråttor. Eur J Pharmacol 2009;609: 69-73.
- 77Nakagawa H, Yamada M, Tokiyoshi K, Miyawaki Y, Kanayama T. [Penetration av kaliumklavulanat / ticarcillinnatrium i cerebrospinalvätska hos neurokirurgiska patienter]. Jpn J Antibiot 1994;47: 93-101.
- 78Kost GC, Selvaraj S, Lee YB, Kim DJ, Ahn CH, Singh BB. Clavulansyra ökar frisättningen av dopamin i nervceller genom en mekanism som involverar förbättrad vesikelhandel. Neurosci Lett 2011;504: 170-5.
- 79Sanna F, Succu S, Hubner H, Gmeiner P, Argiolas A, Melis MR. Dopamin D2-liknande receptoragonister inducerar penilexektion hos hanråttor: differentiell roll för D2, D3 och D4-receptorer i paraventrikulär kärna i hypotalamus. Behav Brain Res 2011;225: 169-76.
- 80Sanna F, Melis MR, Angioni L, Argiolas A. Clavulansyra inducerar erektion och gäspning hos hanråttor: jämförelse med apomorfin. Pharmacol Biochem Behav 2013;103: 750-5.
- 81Robinson TE, Berridge KC. Den neurala grunden för läkemedelsbegär: en incitament-sensibiliseringsteori för missbruk. Brain Res Brain Res Rev 1993;18: 247-91.
- 82Breiter HC, Gollub RL, Weisskoff RM, Kennedy DN, Makris N, Berke JD et al. Akuta effekter av kokain på människans hjärnaktivitet och känslor. Neuron 1997;19: 591-611.
- 83Chow HS, Chen Z, Matsuura GT. Direkt transport av kokain från näshålan till hjärnan efter intranasal kokainadministrering hos råttor. J Pharm Sci 1999;88: 754-8.
- 84Cregler LL, Mark H. Medicinska komplikationer av kokainmissbruk. N Engl J Med 1986;315: 1495-500.
- 85Kendirci M, Pradhan L, Trost L, Gur S, Chandra S, Agrawal KC et al. Perifera mekanismer för erektil dysfunktion i en råttmodell för kronisk kokainanvändning. Eur Urol 2007;52: 555-63.
- 86Romach MK, Lim P, Kampman K, Kaplan HL, Somer GR, Poole S et al. Dämpning av euforiska effekter av kokain med dopaminen D1 / D5-antagonist-ekopipam (SCH 39166). Arch Gen Psychiatry 1999;56: 1101-6.
- 87Chang AY, Chan JY, Chan SH. Hippocampal noradrenerg neurotransmission vid samtidig EEG-desynkronisering och hämning av erektionen inducerad av kokain hos råtta. Br J Pharmacol 2000;130: 1553-60.
- 88Coleman CC, King BR, Bolden ‐ Watson C, Book MJ, Segraves RT, Richard N et al. En placebokontrollerad jämförelse av effekterna på sexuell funktion av bupropion fördröjd frisättning och fluoxetin. Clin Ther 2001;23: 1040-58.
- 89Gitlin MJ, Suri R, Altshuler L, Zuckerbrow ‐ Miller J, Fairbanks L. Bupropion-fördröjd frisättning som behandling för SSRI-inducerade sexuella biverkningar. J Sex äktenskaplig ter 2002;28: 131-8.
- 90Taylor MJ, Rudkin L, Bullemor ‐ Day P, Lubin J, Chukwujekwu C, Hawton K. Strategier för att hantera sexuell dysfunktion inducerad av antidepressiva läkemedel. Cochrane Database Syst Rev 2013;5: CD003382.
- 91Adachi H, Sato Y, Kato R, Hisasue S, Suzuki K, Masumori N et al. Direkt bevis på underlättande verkningar av dopamin i det mediala preoptiska området vid reflexiva och icke-kontaktade erektioner hos hanråttor. J Urol 2003;169: 386-9.
- 92Sukoff Rizzo SJ, Schechter LE, Rosenzweig ‐ Lipson S. En ny metod för att förutsäga antidepressiva inducerad sexuell dysfunktion hos råttor. Psychopharmacology 2008;195: 459-67.
- 93Beaulieu JM, Gainetdinov RR. Fysiologi, signalering och farmakologi av dopaminreceptorer. Pharmacol Rev 2011;63: 182-217.
- 94Allard J, Bernabe J, Derdinger F, Alexandre L, McKenna K, Giuliano F. Selegilin förbättrar erektil aktivitet inducerad genom dopamininjektion i den paraventrikulära kärnan i hypotalamus hos anestesierade råttor. Int J Impot Res 2002;14: 518-22.
- 95Kodesh A, Weizman A, Aizenberg D, Hermesh H, Gelkopf M, Zemishlany Z. Selegilin vid behandling av sexuell dysfunktion hos schizofrenipatienter som upprätthålls på neuroleptika: en pilotstudie. Clin Neuropharmacol 2003;26: 193-5.
- 96Laatikainen LM, Sharp T, Harrison PJ, Tunbridge EM. Sexuellt dimorfa effekter av katekol-OHämning av metyltransferas (COMT) på dopaminmetabolismen i flera hjärnregioner. PLoS ONE 2013;8: e61839.
- 97Giuliano F, Clement P. Farmakologi för behandling av för tidig utlösning. Pharmacol Rev 2012;64: 621-44.
- 98Clement P, Giuliano F. Fysiologi och farmakologi för utlösning. Basic Clin Pharmacol Toxicol 2015; doi: 10.1111 / bcpt.12546.
- 99Clement P, Pozzato C, Heidbreder C, Alexandre L, Giuliano F, Melotto S. Försening av utlösning inducerad av SB ‐ 277011, en selektiv dopamin D3-receptorantagonist, hos råttan. J Sex Med 2009;6: 980-8.
- 100Kozyrev N, Staudt MD, Brown A, Coolen LM. Kronisk kontusion ryggmärgsskada försämrar utlösningsreflexer hos hanråttor: partiell återhämtning genom systemiska infusioner av dopamin D3 receptoragonist 7OHDPAT. J Neurotrauma 2016;33: 943-53.
- 101Safarinejad MR. Förhållandet mellan för tidig utlösning och genetiska polymorfismer av dopamintransportgenen (SLC6A3). BJU Int 2011;108: 292-6.
- 102El ‐ Sakka AI. Vilken är den aktuella rollen för intrakavernosal injektion i hanteringen av erektil dysfunktion? Int J Impot Res 2016;28: 88-95.
- 103Feldman HA, Goldstein I, Hatzichristou DG, Krane RJ, McKinlay JB. Impotens och dess medicinska och psykosociala samband: resultat från Massachusetts Male Aging Study. J Urol 1994;151: 54-61.
- 104Johannes CB, Araujo AB, Feldman HA, Derby CA, Kleinman KP, McKinlay JB. Förekomst av erektil dysfunktion hos män 40 till 69 år: longitudinella resultat från Massachusetts manliga åldringsstudie. J Urol 2000;163: 460-3.
- 105Martin ‐ Morales A, Sanchez ‐ Cruz JJ, Saenz de Tejada I, Rodriguez ‐ Vela L, Jimenez ‐ Cruz JF, Burgos ‐ Rodriguez R. Prevalens och oberoende riskfaktorer för erektil dysfunktion i Spanien: resultat av Epidemiologia de la Disfuncion Erectil Masculina-studie. J Urol 2001;166: 569-74.
- 106Sairam K, Kulinskaya E, Boustead GB, Hanbury DC, McNicholas TA. Prevalens av odiagnostiserad diabetes mellitus vid manlig erektil dysfunktion. BJU Int 2001;88: 68-71.
- 107Wessells H, Penson DF, Cleary P, Rutledge BN, Lachin JM, McVary KT et al. Effekt av intensiv glykemisk terapi på erektil funktion hos män med typ 1-diabetes. J Urol 2011;185: 1828-34.
- 108Behrend L, Vibe ‐ Petersen J, Perrild H. Sildenafil vid behandling av erektil dysfunktion hos män med diabetes: efterfrågan, effekt och patienttillfredsställelse. Int J Impot Res 2005;17: 264-9.
- 109Israilov S, Shmuely J, Niv E, Engelstein D, Livne P, Boniel J. Utvärdering av ett progressivt behandlingsprogram för erektil dysfunktion hos patienter med diabetes mellitus. Int J Impot Res 2005;17: 431-6.
- 110Porst H, Gacci M, Buttner H, Henneges C, Boess F. Tadalafil en gång dagligen hos män med erektil dysfunktion: en integrerad analys av data erhållna från 1913-patienter från sex randomiserade, dubbelblinda, placebokontrollerade, kliniska studier. Eur Urol 2014;65: 455-64.
- 111Saenz de Tejada I, Goldstein I, Azadzoi K, Krane RJ, Cohen RA. Nedsatt neurogen och endotel-medierad avslappning av glatt muskel från penis från diabetiker med impotens. N Engl J Med 1989;320: 1025-30.
- 112Xie D, Odronic SI, Wu F, Pippen A, Donatucci CF, Annex BH. Musmodell av erektil dysfunktion på grund av dietinducerad diabetes mellitus. Urologi 2007;70: 196-201.
- 113Sopko NA, Hannan JL, Bivalacqua TJ. Förstå och rikta in sig på Rho-kinasvägen vid erektil dysfunktion. Nat Rev Urol 2014;11: 622-8.
- 114Corona G, Mannucci E, Petrone L, Ricca V, Balercia G, Mansani R et al. Förening av hypogonadism och typ II-diabetes hos män på en poliklinik för erektil dysfunktion. Int J Impot Res 2006;18: 190-7.
- 115Gur S, Peak TC, Kadowitz PJ, Sikka SC, Hellstrom WJ. Granskning av erektil dysfunktion i diabetiska djurmodeller. Curr Diabetes Rev 2014;10: 61-73.
- 116Matfin G, Jawa A, Fonseca VA. Erektil dysfunktion: samband med det metaboliska syndromet. Curr Diab Rep 2005;5: 64-9.
- 117McVary KT, Rathnau CH, McKenna KE. Sexuell dysfunktion i diabetisk BB / WOR-råtta: en roll som central neuropati. Am J Physiol 1997;272: R259-67.
- 118Cellek S, Cameron NE, Cotter MA, Muneer A. Patofysiologi för erektil dysfunktion hos diabetiker: potentiellt bidrag från vasa nervorum och avancerade slutprodukter av glykation. Int J Impot Res 2013;25: 1-6.
- 119Zheng H, Bidasee KR, Mayhan WG, Patel KP. Brist på central kväveoxid utlöser erektil dysfunktion vid diabetes. Am J Physiol Regul Integr Comp Physiol 2007;292: R1158-64.
- 120Zheng H, Liu X, Patel KP. Centralt förmedlad erektil dysfunktion hos råttor med typ 1-diabetes: roll av angiotensin II och superoxid. J Sex Med 2013;10: 2165-76.
- 121Zheng H, Mayhan WG, Patel KP. Träning förbättrar de defekta centralt medierade erektilresponserna hos råttor med typ I-diabetes. J Sex Med 2011;8: 3086-97.
- 122Xu Q, Park Y, Huang X, Hollenbeck A, Blair A, Schatzkin A et al. Diabetes och risk för Parkinsons sjukdom. Diabetes Care 2011;34: 910-5.
- 123Kleinridders A, Cai W, Cappellucci L, Ghazarian A, Collins WR, Vienberg SG et al. Insulinresistens i hjärnan förändrar dopaminomsättningen och orsakar beteendestörningar. Proc Natl Acad Sci USA 2015;112: 3463-8.
- 124Khang R, Park C, Shin JH. Dysregulering av parkin i substantia nigra hos db / db och dieter med fetthalt. Neuroscience 2015;294: 182-92.
- 125Gontero P, D'Antonio R, Pretti G, Fontana F, Panella M, Kocjancic E et al. Klinisk effekt av apomorfin SL vid erektil dysfunktion hos diabetiker. Int J Impot Res 2005;17: 80-5.
- 126Bronner G, Aharon ‐ Peretz J, Hassin ‐ Baer S. Sexualitet hos patienter med Parkinsons sjukdom, Alzheimers sjukdom och andra demenssjukdomar. Handb Clin Neurol 2015;130: 297-323.
- 127Bronner G, Vodusek DB. Hantering av sexuell dysfunktion vid Parkinsons sjukdom. Ther Adv Neurol Disord 2011;4: 375-83.