จิตเวช Biol 2008 Dec 1; 64 (11): 941-50 Epub 2008 Jul 26
Teegarden SL, Nestler EJ, Bale TL
แหล่ง
ภาควิชาชีววิทยาสัตว์มหาวิทยาลัยเพนซิลเวเนียฟิลาเดลเฟีย PA 19104-6046 สหรัฐอเมริกา
นามธรรม
พื้นหลัง:
ความไวต่อการให้รางวัลได้รับการมีส่วนร่วมเป็นปัจจัยโน้มถ่วงสำหรับพฤติกรรมที่เกี่ยวข้องกับยาเสพติดเช่นเดียวกับการกินมากเกินไป อย่างไรก็ตามกลไกพื้นฐานที่เอื้อต่อการให้รางวัลความไวไม่เป็นที่รู้จัก เราตั้งสมมติฐานว่าความผิดปกติในการส่งสัญญาณโดปามีนอาจเป็นสาเหตุพื้นฐานของความไวของรางวัลที่มีความคิดริเริ่มสูงขึ้นโดยสิ่งเร้าที่ให้รางวัลสามารถทำหน้าที่ทำให้ระบบเป็นปกติ
วิธีการ:
เราใช้แบบจำลองทางพันธุกรรมของเมาส์เพื่อเพิ่มความไวของรางวัลเดลต้าฟอสบีที่แสดงออกมากเกินไปเพื่อตรวจสอบการเปลี่ยนแปลงทางเดินของรางวัลเพื่อตอบสนองต่ออาหารไขมันสูงที่น่ารับประทาน เครื่องหมายของการให้รางวัลสัญญาณในหนูเหล่านี้ถูกตรวจสอบทั้งพื้นฐานและหลังจาก 6 สัปดาห์ของการสัมผัสอาหารที่น่ากิน หนูถูกตรวจสอบในการทดสอบพฤติกรรมหลังจากการอดอาหารไขมันสูงเพื่อประเมินความเสี่ยงของแบบจำลองนี้เพื่อกำจัดสิ่งเร้าที่คุ้มค่า
ผล:
ผลลัพธ์ของเราแสดงให้เห็นถึงการเปลี่ยนแปลงการกระตุ้นการเปิดใช้งานเส้นทางที่มีการเปลี่ยนแปลงตามวงจรนิวเคลียส accumbens-hypothalamic-ventral tegmental ซึ่งเป็นผลมาจากการแสดงออกของ Delta FosB ที่มากเกินไปในนิวเคลียส accumbens และภูมิภาคที่เกิดใหม่. ระดับการตอบสนองของโปรตีนฟอสโฟรีเลตไซโคล adenosine monophosphate (ค่าย) โปรตีน (pCREB) neurotrophic factor ที่ได้จากสมอง (BDNF) และโดปามีนและไซโคลอะดีโนซีนโมโนโฟสเฟตควบคุมฟอสโฟโปรตีนที่มีมวลโมเลกุลของ 32 kDa (DARPP-32) ในนิวเคลียส accumbens ลดลงในหนู Delta FosB แนะนำการลดลงของสัญญาณโดปามีน หกสัปดาห์ของการได้รับอาหารที่มีไขมันสูงทำให้ความแตกต่างเหล่านี้ดีขึ้นอย่างสมบูรณ์เปิดเผยความสามารถที่มีคุณค่าของอาหารอร่อย หนู Delta FosB ยังแสดงให้เห็นการเพิ่มขึ้นอย่างมีนัยสำคัญในกิจกรรมของหัวรถจักรและการตอบสนองที่เกี่ยวข้องกับความวิตกกังวลชั่วโมง 24 หลังจากการถอนไขมันสูง
สรุป
ผลลัพธ์เหล่านี้สร้างความอ่อนไหวพื้นฐานต่อการเปลี่ยนแปลงของรางวัลที่เกี่ยวข้องกับ dysregulation ของ Delta FosB และการส่งสัญญาณโดปามีนที่สามารถทำให้เป็นมาตรฐานด้วยอาหารที่อร่อยและอาจเป็นฟีโนไทป์ที่เริ่มต้นในบางรูปแบบของโรคอ้วน.
บทนำ
แม้เราจะมีความรู้เพิ่มขึ้นเกี่ยวกับระบบประสาทที่ควบคุมความอยากอาหารและความอิ่มแปล้ แต่อัตราโรคอ้วนยังคงเพิ่มขึ้นในสหรัฐอเมริกา การรักษาด้วยยาในปัจจุบันมีประสิทธิภาพ จำกัด และการปรับเปลี่ยนพฤติกรรมต้องทนทุกข์ทรมานจากการปฏิบัติตามในระยะยาวน้อยที่สุด (1) การบริโภคอาหารที่มีแคลอรี่หนาแน่นและน่ากินมีการเชื่อมโยงกับการเปลี่ยนแปลงของความเครียดและให้รางวัลแก่เส้นทางในสมองแนะนำว่าคุณสมบัติที่มีคุณค่าของอาหารดังกล่าวอาจแทนที่สัญญาณสมดุลพลังงาน (2-4) อาหารที่มีไขมันสูงทำหน้าที่เป็นรางวัลตามธรรมชาติเปิดใช้งานศูนย์รับรางวัลสมองในลักษณะที่คล้ายคลึงกับยาเสพติดและถูกนำมาใช้ในกระบวนทัศน์การบริหารจัดการด้วยตนเอง (5-8) ดังนั้นจึงเป็นไปได้ว่าพฤติกรรมและแรงจูงใจในการกินมากเกินไปและการใช้ยาในทางที่ผิดแบ่งปันกลไกพื้นฐานร่วมกันซึ่งอาจเปิดช่องทางใหม่ในการรักษาทั้งสองเงื่อนไข
ในการศึกษาความสัมพันธ์ระหว่างอาหารอร่อยกับวิถีทางที่ควบคุมการให้รางวัลและความเครียดในสมอง ก่อนหน้านี้เราได้ระบุเครื่องหมายโมเลกุลและชีวเคมีของรางวัลที่ลดลงและความเครียดที่เพิ่มขึ้นหลังจากการถอนออกจากอาหารไขมันสูง (HF) ที่น่าพึงพอใจ คล้ายกับยาเสพติดในทางที่ผิดการสัมผัสกับอาหารที่อร่อยในการศึกษาของเราส่งผลให้ระดับการถอดรหัสปัจจัยΔFosBเพิ่มขึ้นในนิวเคลียส accumbens (NAc) โครงสร้างสมองรางวัลกลาง (9, 10). หนูที่แสดงออกอย่างชัดเจนเกินจริงΔFosBแสดงเครื่องมือตอบสนองที่เพิ่มขึ้นสำหรับรางวัลอาหาร (11) ทำให้พวกเขาเป็นเครื่องมือที่มีค่าสำหรับการตรวจสอบบทบาทของความไวของรางวัลและการควบคุมระยะยาวของระบบการให้รางวัลในการตอบสนองระดับโมเลกุลและชีวเคมี
ในการศึกษาครั้งนี้เราใช้หนูΔFosBที่มีการแสดงออกมากเกินไปเพื่อตรวจสอบการเปลี่ยนแปลงระยะยาวในเครื่องหมายของรางวัลในบริเวณที่มีระบบประสาทส่วนปลาย (VTA) ของ NAc-hypothalamus – ventral tegmental (VTA) เพื่อตอบสนองต่ออาหาร HF ที่น่าพอใจ จากการศึกษาก่อนหน้านี้ในหนูที่ไวต่อการให้รางวัลเราตั้งสมมติฐานว่าการเปลี่ยนแปลงที่เกิดจาก sensitivityFosB ในความไวของรางวัลเกี่ยวข้องกับการควบคุม dysregulation ในการส่งสัญญาณโดปามีนซึ่งเป็นผลมาจากข้อเสนอแนะของ NAc ต่อ VTA นอกจากนี้เราตั้งสมมติฐานว่าการได้รับรางวัลตามธรรมชาติของอาหารที่มีพลังงานหนาแน่นจะทำให้ระบบ dopaminergic เป็นปกติในหนูเหล่านี้ส่งผลให้เกิดการตอบสนองต่อความเครียดจากการถอนออกจากอาหาร HF นี้. ลักษณะพิเศษของการใช้อาหารอร่อยเป็นสารที่คุ้มค่าช่วยให้เราสามารถรวมอินพุต hypothalamic เพื่อให้รางวัลวงจรในฟีโนไทป์ที่อาจทำนายของประชากรมักจะชอบโรคอ้วนทนต่อการรักษา ในการตรวจสอบสมมติฐานนี้เราได้ศึกษาเครื่องหมายของสารสื่อประสาทโดปามีนรวมถึง pCREB, BDNF และ DARPP-32 ใน NAc และไทโรซีนไฮดรอกซีเลสและโดปามีนใน VTA หลังจากได้รับ HF นอกจากนี้เรายังตรวจสอบเครื่องหมายเฉพาะของสมดุลพลังงานที่ทราบว่ามีอิทธิพลต่อโดปามีนเอาท์พุทรวมถึง leptin และตัวรับ orexin ในการแสดงออก VTA และ orexin ภายใน hypothalamus ด้านข้าง
วัสดุและวิธีการ
สัตว์
หนู bitransgenic หนูที่ชักนำให้เกิดการแสดงออกอย่างรุนแรงΔFosBในเซลล์ประสาทแบบบวก dynorphin ใน NAc และหลังศูนย์ striatum (Kelz et al., 1999) ถูกสร้างขึ้นบนพื้นหลังแบบผสม (ICR: C57Bl6 / SJL) ที่มหาวิทยาลัยเท็กซัสตะวันตกเฉียงใต้ ทดสอบที่มหาวิทยาลัยเพนซิลเวเนีย หนูทุกตัวได้รับการบำรุงรักษาที่ doxycycline (100 μg / ml ในน้ำดื่ม) จนกระทั่งมาถึงที่มหาวิทยาลัยเพนซิลเวเนีย เพื่อกระตุ้นให้เกิดการแสดงออกมากเกินไป doxycycline จะถูกลบออก (n = 23) (12) หนูควบคุม (n = 26) รับยาต่อไป หนูได้รับมอบหมายให้กลุ่มอาหารแปดสัปดาห์หลังจากการกำจัดของ doxycyline ซึ่งการแสดงออกเวลาได้แสดงให้เห็นถึงระดับสูงสุด (13) หนูถูกเก็บรักษาไว้ใน 12: 12 รอบแสงมืด (ไฟบน 0700) พร้อมอาหารและน้ำที่มีให้ฟรี การศึกษาทั้งหมดดำเนินการตามระเบียบวิธีการทดลองที่ได้รับอนุมัติจากคณะกรรมการการดูแลและการใช้สัตว์แห่งมหาวิทยาลัยเพนซิลเวเนียและขั้นตอนทั้งหมดได้ดำเนินการตามแนวทางของสถาบัน
การได้รับสารอาหาร
หนูถูกเก็บไว้ในโรงเรือน (n = 16) หรือวางไว้บน HF (n = 16-17) เป็นเวลาหกสัปดาห์ Chow House (Purina Lab Diet, St. Louis, MO) มี 4.00 kcal / g ซึ่งประกอบด้วยโปรตีน 28%, 12% ไขมัน, และคาร์โบไฮเดรต 60% อาหาร HF (Research Diets, New Brunswick, NJ) มี 4.73 kcal / g ซึ่งประกอบด้วยโปรตีน 20%, 45% ไขมัน, และคาร์โบไฮเดรต 35%
ชีวเคมีและการแสดงออกของยีน
วิเคราะห์หนูหลังจากได้รับอาหารเป็นเวลาหกสัปดาห์ สมองถูกถอดออกจากกะโหลกศีรษะและแช่แข็งทั้งบนน้ำแข็งแห้งหรือ NAc ผ่า (ประมาณ 0.5 - 1.75 mm จาก bregma ที่ระดับความลึก 3.5 - 5.5 mm) และแช่แข็งในไนโตรเจนเหลว เนื้อเยื่อถูกเก็บไว้ที่ -80 ° C จนกระทั่งทำการตรวจวัด
การวิเคราะห์ทางชีวเคมี
วิธีการสำหรับการทำลายแบบตะวันตกนั้นได้อธิบายไว้ในวัสดุเสริม แอนติบอดีที่ใช้คือ: Cdk5, CREB และ BDNF (1: 500, เทคโนโลยีชีวภาพของ Santa Cruz, Santa Cruz, CA) และ phospho-CREB (pCREB) (Ser 133), 1: 500: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX: XNUMX
ตัวรับอัตโนมัต
วิธีการโดยละเอียดสำหรับการถ่ายภาพอัตโนมัติมีการอธิบายไว้ในวัสดุเสริม แกนด์ที่ใช้คือ 2 nM H3 - SCH 23390 และ 5 nM H3 - spiperone (PerkinElmer, Boston, MA)
การผสมข้ามสายพันธุ์ในแหล่งกำเนิด
การประมวลผลของเนื้อเยื่อและการผสมพันธุ์ดำเนินการตามที่อธิบายไว้ก่อนหน้า (14) โพรบ DARPP-32 ได้รับการจัดเตรียมโดย P. Greengard (Rockefeller University) และโพรบ orexin ของ J. Elmquist (ศูนย์การแพทย์มหาวิทยาลัยเท็กซัสตะวันตกเฉียงใต้) สไลด์ที่ประเมินสำหรับ DARPP-32 ถูกใส่ลงในฟิล์มเป็นเวลา 3 วันและสไลด์ที่ประเมินสำหรับ Orexin จะถูกนำไปติดฟิล์มเป็นเวลา 4 วัน ปริมาณของภาพภาพยนตร์ได้ดำเนินการตามที่อธิบายไว้ก่อนหน้า (10)
QRT-PCR
RNA ถูกแยกออกจาก VTA และการแสดงออกของแต่ละยีนที่ประเมินโดยใช้ชุดตรวจสอบการแสดงออกของยีนของ TaqMan (Applied Biosystems, ฟอสเตอร์ซิตี, แคลิฟอร์เนีย) วิธีการอย่างละเอียดและการวิเคราะห์ทางสถิติอาจพบได้ในวัสดุเสริม
การวิเคราะห์พฤติกรรม
เพื่อตรวจสอบผลกระทบของการให้รางวัลความไวต่อการเปลี่ยนแปลงพฤติกรรมที่เกิดจากอาหารกลุ่มย่อยของหนูถูกถอนออกจาก HF หลังจากการสัมผัสเป็นเวลาสี่สัปดาห์และกลับไปที่บ้านเชา (n = 9 control, n = 8 ΔFosB) ยี่สิบสี่ชั่วโมงหลังจากการถอนตัวหนูได้สัมผัสกับการทดสอบแบบเปิดตามความต้องการในการอดอาหาร (10) สั้น ๆ วางเมาส์ไว้ที่กึ่งกลางของอุปกรณ์เปิดโล่งและตรวจสอบเป็นเวลาห้านาที วัดค่า cross cross line, fecal boli, เวลาที่อยู่ตรงกลางและ crosses เข้าสู่ศูนย์กลาง
สถิติ
ข้อมูลทั้งหมดยกเว้น Western blots ได้รับการวิเคราะห์โดยใช้ two-way ANOVA ตามด้วยการทดสอบ PLSD ของ Fisher ด้วยการรักษา doxycycline (การแสดงออกของΔFosB) และสภาพอาหารเป็นตัวแปรอิสระ สำหรับการวิเคราะห์ RT-PCR ค่า P ที่ลดลงถูกนำมาใช้เพื่อแก้ไขการเปรียบเทียบหลายรายการภายในกลุ่มของยีนที่เกี่ยวข้อง (ดูข้อมูลเพิ่มเติม) Western blots ได้รับการวิเคราะห์โดยใช้ t-test ของนักเรียนที่มีการรักษา doxycycline เป็นตัวแปรอิสระโดยเปรียบเทียบความหนาแน่นของแสงภายใน blot เดียวกัน ข้อมูลทั้งหมดแสดงเป็นค่าเฉลี่ย± SEM
ผลสอบ
ความแตกต่างทางชีวเคมีพื้นฐาน
เพื่ออธิบายเส้นทางของโมเลกุลที่รองรับความไวในการให้รางวัลที่เพิ่มขึ้นในหนูที่แสดงออกมากเกินไปΔFosBระดับของโมเลกุลสัญญาณสำคัญหลายตัวได้รับการตรวจสอบใน NAc มีแนวโน้มที่ระดับ Cdk5 ที่เพิ่มขึ้นใน NAc ของหนูΔFosBเมื่อเทียบกับสัตว์ควบคุมครอกที่รักษาด้วย doxycycline (F = 5.1, P = 0.08; รูปที่ 1A) Δหนู FosB แสดงระดับ pCREB ที่ลดลงอย่างมีนัยสำคัญ (F = 7.4, P <0.05; รูปที่ 1B) รวมทั้งระดับ CREB ทั้งหมด (F = 5.4, P = 0.05; รูปที่ 1C) พบการลดลงอย่างมีนัยสำคัญของ BDNF ใน NAc ของหนูΔFosB (F = 10.6, P <0.05; รูปที่ 1D)
รูป 1
หนูแสดงอาการเกินจริงΔFosBแสดงเครื่องหมายทางชีวเคมีของการส่งสัญญาณโดปามีนที่ลดลงใน NAc
การรับประทานอาหารและน้ำหนักตัวในอาหารที่มีไขมันสูง
ต่อไปเราจะตรวจสอบผลของอาหาร HF ที่ให้ผลตอบแทนตามธรรมชาติต่อการเปลี่ยนแปลงโมเลกุลสัญญาณในหนูที่แสดงออกมากเกินไปΔFosB ไม่พบความแตกต่างระหว่างหนูΔFosBและการควบคุมปริมาณอาหารในบ้านหรือ HF อย่างไรก็ตามปริมาณแคลอรี่โดยรวมลดลงโดยรวมกับน้ำหนักตัวเมื่อสัมผัสกับ HF ที่จำเพาะต่อหนูΔFosB (F = 11.2, P <0.01; รูปที่ 2A) เมื่อสิ้นสุดหกสัปดาห์ของการได้รับอาหารหนูที่ได้รับ HF จะมีน้ำหนักมากกว่าหนูที่ได้รับอาหาร Chow อย่างมีนัยสำคัญ (F = 17.2, P <0.001) และหนูΔFosBมีน้ำหนักโดยรวมน้อยกว่าการควบคุม (F = 5.6, P <0.05; 2B) ผลกระทบนี้มีความเฉพาะเจาะจงกับความแตกต่างระหว่างกลุ่มที่รับประทานอาหารเชา (P <0.05)
รูป 2
expressFosB หนูที่มีการแสดงออกมากเกินไปไม่พบความแตกต่างในการรับประทานอาหารในอาหารที่มีไขมันสูง (HF)
ความแตกต่างทางชีวเคมีในอาหารที่มีไขมันสูง
เพื่อตรวจสอบความแตกต่างพื้นฐานในการส่งสัญญาณ NAc อาจเปลี่ยนแปลงโดยการรับประทานอาหาร HF โปรตีนที่ส่งสัญญาณการศึกษาเดียวกันที่พื้นฐานที่ถูกตรวจสอบในสัตว์ที่ได้รับ HF หกสัปดาห์ ไม่มีความแตกต่างอย่างมีนัยสำคัญในระดับ Cdk5 (รูปที่ 3A) ระดับของ pCREB และ CREB รวมนั้นไม่แตกต่างกันหลังจากผ่านไปหกสัปดาห์ของ HF (รูปที่ 3B, C) ระดับของ BDNF นั้นเพิ่มขึ้นอย่างมีนัยสำคัญในหนูΔFosBหลังจากการสัมผัส HF เป็นเวลาหกสัปดาห์ (F = 6.5, P = 0.05; รูปที่ 3D)
รูป 3
อาหารไขมันสูง (HF) ความแตกต่างของสัญญาณ ameliorated สังเกตใน NAc ของΔFosBหนู overexpressing
Dopamine autoradiography ตัวรับ
เราใช้อัตชีวประวัติของตัวรับเพื่อประเมินว่าการเปลี่ยนแปลงที่เกิดจากΔFosBในการส่งสัญญาณโดปามีนใน NAc เกี่ยวข้องกับการเปลี่ยนแปลงในการแสดงออกของตัวรับโดปามีนหรือไม่ (รูปที่ 4A) อาหารที่มีไขมันสูงดูเหมือนจะเพิ่มความหนาแน่นของการจับตัวรับ D1 dopamine เล็กน้อย (P = 0.14) และความแตกต่างนี้มีมากกว่าในหนู FosB (รูปที่ 4B) นอกจากนี้ยังมีแนวโน้มการเพิ่มขึ้นของพื้นที่จับ D1 ตาม HF (P = 0.06) และการทดสอบหลังการทดสอบพบว่าสิ่งนี้มีนัยสำคัญในหนูΔFosB (P <0.05; รูปที่ 4C) ตรงกันข้ามกับตัวรับ D1 ไม่มีการเปลี่ยนแปลงของ D2 receptor binding density (control chow = 97.6 ± 6.9, control HF = 101.1 ± 8.2, ΔFosB chow = 91.6 ± 1.0, ΔFosB HF = 94.8 ± 9.5) หรือพื้นที่ผูกพัน (ควบคุม chow = 47.3 ± 3.4, ควบคุม HF = 53.8 ± 6.0, ΔFosB chow = 51.9 ± 3.7, ΔFosB HF = 49.0 ± 3.3) ใน NAc ถูกสังเกต
รูป 4
อาหารไขมันสูง (HF) นำไปสู่การเปลี่ยนแปลงใน D1 dopamine receptor binding และการแสดงออกของ DARPP-32 ในนิวเคลียส accumbens (NAc) ของΔFosBหนูที่แสดงออกมากเกินไป
DARPP-32 นิพจน์ใน NAc
การผสมพันธุ์ในแหล่งกำเนิดถูกใช้เพื่อกำหนดระดับการแสดงออกของ DARPP-32 ใน NAc (รูปที่ 4D) อาหารที่มีไขมันสูงเพิ่มการแสดงออกของ DARPP-32 อย่างมีนัยสำคัญในบริเวณสมองนี้ (F = 5.1, P <0.05) และมีปฏิสัมพันธ์อย่างมีนัยสำคัญระหว่างการรับประทานอาหารและการแสดงออกของΔFosB (F = 8.9, P <0.05) โดยหนูΔFosBแสดงค่าที่มากกว่า การเปลี่ยนแปลงที่เกิดจากอาหาร (รูปที่ 4E) ความแตกต่างพื้นฐานในการแสดงออกของ DARPP-32 ระหว่างหนูควบคุมและΔFosBถูกเปิดเผยโดยการทดสอบหลังการทำงาน (P <0.01) รวมทั้งการแสดงออกของ DARPP-32 ที่เพิ่มขึ้นอย่างมีนัยสำคัญในหนูΔFosBบน HF (P <0.01)
การแสดงออกของยีนใน VTA
QRT-PCR ถูกใช้เพื่อประเมินการเปลี่ยนแปลงของการแสดงออกของยีนใน VTA โดยกำหนดเป้าหมายไปที่ยีนหลักหลายตัวที่เกี่ยวข้องก่อนหน้านี้ในการควบคุมการให้รางวัล ตัวอย่างทั้งหมดถูกปรับให้เป็นβ-actin เพื่อให้แน่ใจว่าการแสดงออกของβ-actin ไม่ได้ถูกเปลี่ยนแปลงโดยการรักษาจึงมีการเรียกใช้การทดสอบแยกต่างหากเพื่อเปรียบเทียบβ-actin กับการควบคุมภายในครั้งที่สอง GAPDH ไม่มีความแตกต่างอย่างมีนัยสำคัญในการแสดงออกของβ-actin (ค่าΔCT, β-actin - GAPDH: ควบคุม chow = 2.29 ± 0.21, ควบคุม HF = 2.01 ± 0.04, ΔFosB chow = 2.32 ± 0.49, ΔFosB HF = 2.37 ± 0.10)
มีการสังเกตแนวโน้มของปฏิสัมพันธ์ระหว่างการแสดงออกของΔFosBและการรักษาอาหารสำหรับการแสดงออกของไทโรซีนไฮดรอกซิเลส (F = 3.6, P <0.06; รูปที่ 5A) หกสัปดาห์ของการสัมผัส HF ดูเหมือนว่าจะลดการแสดงออกของไทโรซีนไฮดรอกซิเลสในหนูควบคุมและเพิ่มการแสดงออกในหนูΔFosB พบปฏิสัมพันธ์ที่สำคัญระหว่างการแสดงออกของΔFosBและการได้รับอาหารสำหรับการแสดงออกของผู้ขนส่งโดปามีน (F = 6.7, P <0.03; รูปที่ 5B) คล้ายกับไทโรซีนไฮดรอกซิเลสการสัมผัสกับ HF ช่วยลดการแสดงออกของตัวขนย้ายโดปามีนในหนูควบคุมและการแสดงออกที่เพิ่มขึ้นอย่างมีนัยสำคัญในหนู PFosB (P <0.05) ความแตกต่างพื้นฐานในการแสดงออกของโดปามีนตัวขนส่งระหว่างหนูควบคุมและΔFosBไม่ถึงนัยสำคัญ (P = 0.16) แต่หลังจาก 6 สัปดาห์ของ HF หนูΔFosBแสดงระดับของตัวขนส่งโดพามีนที่เพิ่มขึ้นอย่างมีนัยสำคัญเมื่อเทียบกับตัวควบคุม (P <0.05)
รูป 5
การได้รับอาหารไขมันสูง (HF) และการแสดงออกของ BFosB ทำให้เกิดการเปลี่ยนแปลงในการแสดงออกของโมเลกุลสำคัญจำนวนหนึ่งใน VTA
มีแนวโน้มที่บ่งชี้ถึงผลของการแสดงออกของΔFosBที่เพิ่มขึ้นเพื่อลดระดับ TrkB ใน VTA (F = 5.7, P <0.04; รูปที่ 5C) แม้ว่าจะไม่มีผลกระทบหลักในการแสดงออกของตัวรับκ-opioid แต่ก็มีแนวโน้มที่จะลดการแสดงออกในหนูΔFosB (P = 0.08; รูปที่ 5D) การแสดงออกของตัวรับเลปตินยังถูกกำหนดใน VTA พบผลอย่างมีนัยสำคัญของการได้รับอาหาร (F = 6.1, P <0.03) โดย HF ช่วยลดระดับของตัวรับเลปตินใน VTA ได้อย่างมีนัยสำคัญทั้งในΔFosBและหนูควบคุม (รูปที่ 5E) นอกจากนี้ยังตรวจสอบการแสดงออกของตัวรับ orexin 1 ใน VTA มีผลอย่างมากของอาหารต่อการแสดงออกของตัวรับ orexin (F = 9.0, P <0.02) โดยหนูที่สัมผัสกับ HF จะแสดงระดับที่สูงขึ้นใน VTA (รูปที่ 5F) นอกจากนี้ยังมีแนวโน้มที่หนูΔFosBจะแสดงระดับที่สูงขึ้นโดยรวมของตัวรับ orexin 1 ในบริเวณสมองนี้ (P <0.05)
การแสดงออกของ Orexin ในมลรัฐด้านข้าง
เราวัดระดับของ orexin ใน hypothalamus ด้านข้างซึ่งเป็นจุดกำเนิดของการปกคลุมด้วยเส้นของ orexinergic ของ VTA โดยการผสมพันธุ์ในแหล่งกำเนิด (รูปที่ 6A) มีปฏิสัมพันธ์อย่างมีนัยสำคัญระหว่างการแสดงออกของΔFosBและการได้รับอาหารต่อการแสดงออกของ orexin (F = 9.1, P <0.01) โดย HF เพิ่มระดับ orexin ในหนูควบคุมอย่างมีนัยสำคัญ (P <0.05) และการแสดงออกที่ลดลงในหนูΔFosB (รูปที่ 6B) แม้ว่าจะไม่มีความแตกต่างอย่างมีนัยสำคัญในการแสดงออกของ orexin ในสถานะพื้นฐานหลังจาก 6 wks ของ HF หนูΔFosBแสดงระดับของ orexin ลดลงอย่างมีนัยสำคัญเมื่อเทียบกับการควบคุม (P <0.05)
รูป 6
อาหารที่มีไขมันสูง (HF) มีผลต่อการแสดงออกของ orexin ในการควบคุม (Ctrl) และΔFosBที่หนูแสดงออกมากเกินไป
Beการวิเคราะห์ผู้ช่วยให้รอด
เพื่อประเมินการเปลี่ยนแปลงในการปลุกเร้าอารมณ์และอารมณ์อันเนื่องมาจากการเปลี่ยนแปลงของอาหารหนูได้รับการทดสอบแบบเปิดสนาม 24 ชม. หลังการถอนอาหาร HF (10) การข้ามเส้นทั้งหมดซึ่งได้คะแนนเป็นตัววัดความเร้าอารมณ์ได้รับผลกระทบอย่างมีนัยสำคัญจากการแสดงออกของΔFosB (F = 6.6, P <0.05) และอาหาร (F = 4.6, P <0.05; รูปที่ 7A) Δหนู FosB มีความกระตือรือร้นในสภาพแวดล้อมแบบใหม่มากกว่าหนู contrils และการทดสอบหลังการทดลองแสดงให้เห็นว่าหนูที่ถูกถอนออกจาก HF มีความกระตือรือร้นมากกว่าหนูที่สัมผัสกับ chow (P <0.05) Fecal boli ถูกนับเป็นพฤติกรรมที่คล้ายกับความวิตกกังวล (10) มีผลกระทบหลักของการแสดงออกของΔFosB (F = 10.2, P <0.01) โดยที่หนูที่แสดงออกมากเกินไปΔFosBจะผลิตอุจจาระออกมามากขึ้นในสภาพแวดล้อมใหม่โดยเฉพาะอย่างยิ่งในกลุ่มถอนการเลี้ยงสุนัขและ HF (รูปที่ 7B) หนูΔFosBที่ได้รับอาหาร HF จะสร้างอุจจาระได้น้อยกว่าหนูที่ได้รับการบำรุงด้วย chow และหนูที่ถูกถอนออกไป 24 ชม. ก่อนการทดสอบ หนูควบคุมไม่ได้รับผลกระทบจากอาหาร ไม่มีผลกระทบอย่างมีนัยสำคัญของการแสดงออกของΔFosBหรือการรับประทานอาหารตามเวลาที่ใช้ในบริเวณกลางทุ่งโล่ง (ควบคุม chow = 14.5 ± 3.1 วินาทีควบคุม HF = 18.0 ± 3.2 วินาทีควบคุม W / D = 15.4 ± 1.9 วินาทีΔFosB chow = 16.9 ± 2.4 วินาที, ΔFosB HF = 13.1 ± 3.9 วินาที, ΔFosB W / D = 19.8 ± 2.6 วินาที)
รูป 7
หนูที่แสดงออกว่าΔFosBมีความไวต่อผลของการถอนอาหารที่มีไขมันสูง (HF)
การสนทนา
ในการรักษาโรคอ้วนมีความจำเป็นอย่างยิ่งในการระบุปัจจัยที่มีอิทธิพลต่อความอ่อนแอต่อการกินมากเกินไปและการเพิ่มน้ำหนัก เส้นทางการให้รางวัลของสมองมีบทบาทสำคัญในการสร้างแรงจูงใจและตอบสนองต่ออาหารอร่อยและการเปลี่ยนแปลงอาหาร (6, 10, 15, 16) เนื่องจากสัญญาณ orexigenic และ anorexigenic สามารถส่งผลโดยตรงต่อการส่งสัญญาณรางวัลผ่านวงจร hypothalamus-VTA-NAc การอธิบายของยีนที่ตอบสนองต่ออาหารที่อุดมด้วยพลังงานภายในศูนย์ให้รางวัลอาจให้เป้าหมายการรักษาแบบใหม่ในการรักษาโรคอ้วน (17, 18) ดังนั้นเราจึงตรวจสอบเครื่องหมายทางชีวเคมีและโมเลกุลของรางวัลและการส่งสัญญาณสมดุลพลังงานตามวงจร hypothalamus-VTA-NAc เพื่อตอบสนองต่ออาหาร HF ในหนู inFosB overexpressing เป็นแบบจำลองของความไวที่เพิ่มขึ้นต่อการเปลี่ยนแปลงในรางวัล (13, 19, 20) และความไวของพฤติกรรมหลังจากการอดอาหาร เราตั้งสมมติฐานว่าฐานการส่งสัญญาณโดปามีนในหนูหนูΔFosBจะถูกทำให้เป็นมาตรฐานโดยผลที่ได้รับจากอาหารที่มี HF ซึ่งครอบคลุมการแยกสัญญาณสมดุลพลังงานและระบบโดปามีน
ในการตรวจสอบเครื่องหมายที่บ่งบอกถึงความผิดปกติในการส่งสัญญาณโดปามีนใน NAc เราตรวจสอบระดับตัวรับ D1 และเอฟเฟกต์ปลายน้ำ แม้ว่าจะไม่มีความแตกต่างอย่างมีนัยสำคัญในการรวมตัวรับ D1 มีแนวโน้มที่การสัมผัส HF จะเพิ่มพื้นที่การจับในหนูΔFosB. สิ่งนี้น่าสนใจเมื่อการเหนี่ยวนำของΔFosBจากยาและผลตอบแทนตามธรรมชาตินั้นดูเหมือนจะมีอิทธิพลเหนือเซลล์ย่อยแบบไดโนฟินในเชิงบวกของเซลล์ประสาทส่วนกลางที่มีหนามปานกลางซึ่งส่วนใหญ่แสดงตัวรับ D1 (9, 21) ระดับของการส่งสัญญาณเป้าหมายโดพามีนดาวน์สตรีม pCREB ลดลงอย่างมีนัยสำคัญในหนู osFosB สนับสนุนการลดการกระตุ้นการรับ D1 ในพื้นที่สมองนี้ (22, 23) ที่น่าสนใจคือเรายังตรวจพบการลดลงอย่างมีนัยสำคัญของระดับ CREB ทั้งหมดในหนูΔFosBซึ่งเป็นการแนะนำความสามารถที่ลดลงสำหรับการส่งสัญญาณโดปามีนซึ่งอาจเป็นรองจากการตอบรับซึ่งเป็นผลมาจาก pCREB (24) ลดลงเป็นเวลานาน การแสดงออกของ BDNF นั้นควบคุมโดย pCREB ซึ่งเพิ่มขึ้นด้วยการเปิดใช้งาน D1 และเป็นผู้ไกล่เกลี่ยที่สำคัญของระบบประสาทที่เกี่ยวข้องกับการให้รางวัลใน NAc (25, 26) ดังนั้นเราตรวจพบการลดลงอย่างมีนัยสำคัญของโปรตีน BDNF ใน NAc ของΔFosBหนู
เซลล์ประสาทหนามขนาดกลางทั้งหมดใน NAc express DARPP-32 (27) เอฟเฟ็กต์ดาวน์สตรีมจำนวนมากทำให้มันกลายเป็นผู้เล่นที่สำคัญในเส้นทางการให้รางวัล (28) และมันเกี่ยวข้องกับการติดยาเสพติดและความผิดปกติอื่น ๆ ที่เกี่ยวข้องกับระบบโดปามีนรวมถึงโรคอารมณ์แปรปรวนและโรคจิตเภท (27, 29) เราตรวจพบการลดลงของฐานที่ลึกซึ้งในการแสดงออก DARPP-32 ใน NAc ของΔFosBหนู นิพจน์ DARPP-32 ถูกควบคุมโดย BDNF และดังนั้นการแสดงออกที่ลดลงอาจเกี่ยวข้องโดยตรงกับการลดลงของระดับ BDNF ที่ตรวจพบในหนูΔFosB (27, 29, 30) แม้การเปลี่ยนแปลงระดับปานกลางในสถานะฟอสโฟรีเลชั่นของ DARPP-32 สามารถนำไปสู่การเปลี่ยนแปลงที่สำคัญในการส่งสัญญาณภายในเซลล์ภายใน NAc (27) การศึกษาก่อนหน้านี้ได้รายงานว่าไม่มีการเปลี่ยนแปลงโปรตีน DARPP-32 ในหนูΔFosBหลังจากการกำจัด 12-wk จาก doxycycline เมื่อมีการประเมินในเชิงกว้างมากขึ้น (31) แนะนำว่าผลของΔFosBใน DARPP-32 อาจเป็นเวลาและภูมิภาคเฉพาะ
เราตั้งสมมติฐานว่าการลดลงอย่างมากของดัชนีโดปามีนใน NAc ของหนูΔFosBน่าจะเกี่ยวข้องกับการเปลี่ยนแปลงในเซลล์ประสาทฉายโดปามีนของ VTA แม้ว่าΔFosBจะไม่แสดงออกมากเกินไปภายในเซลล์ประสาทเหล่านี้. ดังนั้นเราจึงตรวจสอบการแสดงออกของยีนที่เกี่ยวข้องกับโดปามีนใน VTA รวมถึงไทโรซีนไฮดรอกซีเลสและการขนส่งโดพามีน ระดับของไทโรซีนไฮดรอกซีเลสและโดปามีนมีความสัมพันธ์เชิงบวกกับการส่งออกโดพามีน มีแนวโน้มสำหรับหนูΔFosBที่จะแสดงไทโรซีนไฮดรอกไซเลสที่ลดลงและการลดลงอย่างมีนัยสำคัญในการขนส่งโดพามีน, เพื่อให้สอดคล้องกับ dysregulation ของการส่งสัญญาณโดปามีนใน NAc. เนื่องจากการลดลงของฐานเหล่านี้ในยีนที่เกี่ยวข้องกับโดปามีนใน VTA ของหนูΔFosBอาจสะท้อนการตอบรับที่เปลี่ยนแปลงจาก NAc ในระยะยาว expressFosBเราตรวจสอบการแสดงออกของตัวรับ BDNF TrkB ซึ่งเป็นกลไกที่เป็นไปได้ของข้อเสนอแนะ NAc กับ VTA (32) การแสดงออกของ TrkB ก็คล้ายกับไทโรซีนไฮดรอกซีเลสและโดปามีนการแสดงออกของ TrkB ก็แสดงให้เห็นแนวโน้มที่จะลดลงอย่างเห็นได้ชัดในหนูΔFosBที่ไม่ได้มีนัยสำคัญเมื่อแก้ไขเพื่อเปรียบเทียบหลายอย่าง คอมเพล็กซ์ BDNF-TrkB สามารถขนส่งย้อนหลังและกระทำภายใน VTA เพื่อส่งผลกระทบต่อการแสดงออกของยีนในท้องถิ่นและส่งเสริมการเติบโตและการบำรุงรักษาเซลล์ (33) นอกจากนี้การเปิดใช้งาน BDNF ของ presynaptic TrkB ภายใน NAc สามารถกระตุ้นสารสื่อประสาทโดปามีน (32) โดยตรงสนับสนุนการลดลงของสัญญาณโดปามีนในหนูเหล่านี้
การเปิดใช้งาน Dynorphin ของตัวรับ op-opioid ควบคุมการส่งสัญญาณโดปามีนและเป็นอีกกลไกหนึ่งที่ NAc ให้ข้อเสนอแนะต่อ VTA (34) เราพบว่าการแสดงออกของตัวรับ op-opioid ใน VTA แสดงให้เห็นแนวโน้มที่จะลดลงในหนูΔFosB เนื่องจากการแสดงออกของΔFosBมีการแสดงออกเพื่อลดการแสดงออกของ dynorphin ใน NAc (20) หนูΔFosBน่าจะมีการลดลงอย่างมากใน VTA สุทธิκ-การเปิดใช้งาน opioid แม้ว่าการส่งสัญญาณ dynorphin ตามปกติจะมีผลยับยั้งเซลล์ประสาทโดปามีน (35) แต่หนูที่แสดงการบริหารยาเสพติดด้วยตนเองที่เพิ่มขึ้นจะแสดงระดับของ dynorphin ใน NAc ลดลงซึ่งชี้ให้เห็นถึงบทบาทในการส่งสัญญาณ dynorphin ที่ลดลงพื้นฐานในการเพิ่มความไวต่อรางวัล (36 , 37) Dysregulation ของระบบ dynorphin - κ-opioid ได้รับการเชื่อมโยงกับการได้มาและการคงอยู่ของการใช้ยาในทางที่ผิดซึ่งสนับสนุนความสมดุลที่สำคัญของการส่งสัญญาณ opioid ในการทำให้วิถีโดปามีนเป็นปกติ (38)
จากความสามารถในการให้รางวัลของอาหาร HF ที่มีพลังงานหนาแน่นเราตั้งสมมติฐานว่าการส่งสัญญาณ dopamine และ opioid ใน dyspulation ในสัญญาณ mFosB mice จะทำให้หนูเหล่านี้มีความโน้มเอียงที่จะตอบสนองต่อการให้อาหารดังกล่าว - วงจร VTA-NAc. ในช่วงหกสัปดาห์ที่ผ่านมาการรับประทานอาหารไม่มีความแตกต่างในการรับประทานอาหารระหว่างΔFosBและหนูควบคุมพบว่าการเปลี่ยนแปลงที่พบในตัวบ่งชี้ทางชีวเคมีและโมเลกุลของสัญญาณการให้รางวัลในหนูΔFosBไม่ได้เกิดจากความแตกต่างของแคลอรี่ที่บริโภค ตามที่คาดไว้ความแตกต่างพื้นฐานที่ตรวจพบใน pCREB, CREB ทั้งหมด, BDNF, DARPP-32, และκ-opioid ระดับตัวรับระหว่างΔFosBและหนูควบคุมถูกลดทอนลงเนื่องจากการเพิ่มขึ้นของโดปามีนในหนูΔFosBบน HF (29, 39NUMXUMUMUM) .
การตรวจสอบทั้งไทโรซีนไฮดรอกซิเลสและตัวขนส่งโดปามีนใน VTA เปิดเผยการตอบสนองของฝ่ายตรงข้ามที่น่าประหลาดใจของ controlFosB และหนูควบคุมที่ติดตาม HF. หนูควบคุมพบว่าการแสดงออกของไทโรซีนไฮดรอกซีเลสและโดปามีนลดลงในขณะที่หนูΔFosBแสดงการแสดงออกที่เพิ่มขึ้นของยีนที่เกี่ยวข้องกับโดพามีนทั้งสองนี้ ที่น่าสนใจคือการแสดงออกของไทโรซีนไฮดรอกซีเลสจะเปลี่ยนไปใน VTA ด้วยโคเคนเรื้อรังหรือการบริหารแอมเฟตตามิน (42-44) แนะนำว่าหนูΔFosBอาจได้รับผลธรรมชาติของ HF มากกว่าหนูควบคุม
เพื่อที่จะตรวจสอบว่าสัญญาณ hypothalamic input ที่อาจเกิดขึ้นกับ VTA นั้นอาจเป็นสัญญาณถ่ายทอดที่สะท้อนความสมดุลของพลังงานการแสดงออกของตัวรับ leptin และตัวรับ orexin-1 ก็ถูกตรวจสอบเช่นกัน ระดับเลปตินหมุนเวียนเพิ่มขึ้นโดย HF และเลพตินสามารถทำหน้าที่ที่ VTA เพื่อเปลี่ยนการส่งสัญญาณโดปามีน (18, 45) การแสดงออกของตัวรับเลปติน VTA ลดลงเช่นเดียวกันโดย HF ทั้งในΔFosBและหนูควบคุมในการรักษาด้วยการเพิ่มน้ำหนักและการบริโภคอาหารที่คล้ายกันในขณะที่ใน HF ไขมันสูงยังเพิ่มการแสดงออกของตัวรับ orexin-1 ใน VTA ของทั้งΔFosBและหนูควบคุม Orexin เปิดใช้งานเซลล์ประสาทโดปามีนใน VTA ส่งเสริมพลาสติก VTA และเพิ่มระดับโดปามีนใน NAc (46-48) อาหารที่มีไขมันสูงได้รับการแสดงเพื่อเพิ่มการแสดงออก orexin ในหนูตามการสังเกตของเรา (49, 50) ดังนั้นการแสดงออกที่เพิ่มขึ้นของตัวรับ orexin เช่นเดียวกับการเปลี่ยนแปลงในการส่งสัญญาณเลปตินใน VTA สามารถส่งเสริมรางวัลอาหารทั้งในΔFosBและหนูควบคุมสนับสนุนการแยกตัวระหว่างเส้นทางถ่ายทอดสัญญาณสมดุลพลังงานและที่เชื่อมโยงโดยตรงกับรางวัล
ในการตรวจสอบผลกระทบที่เกิดจากความเครียดของการถอนรางวัลหนูถูกตรวจสอบในการทดสอบภาคสนาม 24 ชม. หลังจากการกำจัด HF หนูΔFosBมีความไวต่อผลกระทบรุนแรงของการถอนอาหารที่ต้องการแสดงกิจกรรมกระตุ้นที่เพิ่มขึ้นและการผลิตอุจจาระในเวทีเปิดใหม่เมื่อเทียบกับกลุ่มควบคุมและกลุ่มควบคุมอื่น ๆ Δหนู FosB ยังแสดงให้เห็นถึงรูปแบบพฤติกรรมที่น่าสนใจในการทดสอบนี้เพื่อชี้แนะการให้รางวัลและความไวต่อความเครียดโดยอาหาร HF เริ่มลดการผลิตอุจจาระ boli เมื่อเทียบกับ Chow และการถอนเพิ่มการตอบสนองที่เกี่ยวข้องกับความวิตกกังวลนี้อีกครั้ง สิ่งที่เพิ่มขึ้นที่สังเกตได้ในกิจกรรมเปิดโล่งไม่สัมพันธ์กับการเปลี่ยนแปลงในการแสดงออกของ orexin การแนะนำความสัมพันธ์กับการเร้าอารมณ์ที่เกิดจากความเครียดซึ่งไม่ได้เป็นเพียงผลของการเปลี่ยนแปลงในการส่งสัญญาณ orexin-mediated โดยรวมแล้วข้อมูลเหล่านี้สนับสนุนสมมุติฐานของเราว่าΔFosBหนูจะไวต่อผลกระทบเฉียบพลันของการอดอาหารที่ต้องการเนื่องจากความไวของรางวัลที่เพิ่มขึ้น.
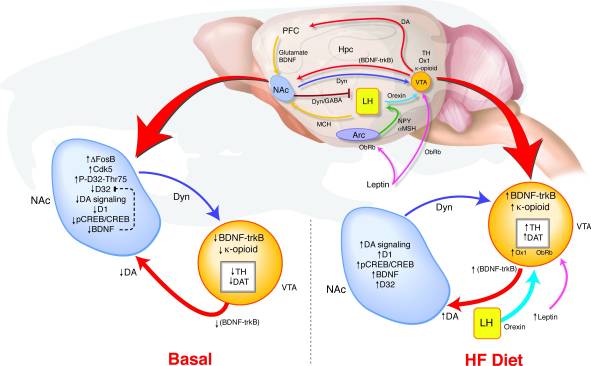
การแสดงออกในระยะยาวของΔFosBใน NAc นำไปสู่การเปลี่ยนแปลงพฤติกรรมและการส่งสัญญาณรางวัลอย่างไร? เราได้เสนอรูปแบบของการตรวจจับพ้อง VTA ซึ่งการเปลี่ยนแปลงข้อเสนอแนะจาก NAc และ hypothalamus ถ่ายทอดสัญญาณเกี่ยวกับสถานะของรางวัลเพื่อกำหนดกฎระเบียบของระบบโดปามีนที่อาจสนับสนุนการเชื่อมโยงระหว่าง dysregulation ทางเดินของรางวัลและความบกพร่องต่อโรคอ้วน (รูปที่ 8) ในระหว่างการสัมผัส HF อินพุตหลายรายการจะสะท้อนถึงทั้งความสมดุลของพลังงานและสถานะการรวมกันบน VTA การเพิ่มสัญญาณ leptin และ orexin เช่นเดียวกับการตอบรับที่เปลี่ยนแปลงจาก NAc ไปเป็น hypothalamus ด้านข้างอาจส่งผลกระทบต่อสัญญาณ orexigenic เหล่านี้ตอบสนองต่อ HF ในหนูΔFosB (17, 18, 45, 47, 51, 53, XNUMX-XNUMX) การยกระดับอาหารที่มีไขมันสูงใน BDNF อาจให้ผลตอบรับตอบแทนแก่ VTA ส่งเสริมการเปลี่ยนแปลงในการแสดงออกของยีนที่เกี่ยวข้องกับโดปามีน
รูป 8
อาหารที่มีไขมันสูง (HF) ทำให้การส่งสัญญาณแบบไร้การควบคุมเป็นปกติในหนูΔFosB
ผลลัพธ์เหล่านี้วิเคราะห์ตัวบ่งชี้ระดับโมเลกุลของความไวในการให้รางวัลและบ่งชี้ว่าการควบคุมความผิดปกติในระยะยาวของระบบโดปามีนอาจทำให้บุคคลติดยาเสพติดและโรคอ้วนได้ นอกจากนี้ข้อมูลเหล่านี้ยังเป็นก้าวสำคัญในการระบุเป้าหมายการรักษาใหม่ที่อาจเกิดขึ้นในการรักษาและป้องกันโรคอ้วนและความผิดปกติอื่น ๆ ที่อาจมุ่งเน้นไปที่ระบบการให้รางวัล ในอนาคตมันเป็นสิ่งสำคัญที่จะตรวจสอบว่าระบบนี้ตอบสนองต่อการกำจัดของอาหาร HF เช่นเดียวกับการตรวจสอบความแตกต่างทางเพศใด ๆ ในความไวต่อการให้รางวัลและการสัมผัสอาหารไขมันสูง
วัสดุเสริม
ภาคผนวก วิธีการ
คลิกที่นี่เพื่อดู (61K, doc)
กิตติกรรมประกาศ
ผู้เขียนต้องการขอบคุณ Cathy Steffen สำหรับความช่วยเหลือในการผสมพันธุ์สัตว์และการถ่ายโอน งานนี้ได้รับการสนับสนุนโดยทุนสนับสนุนจากศูนย์โรคเบาหวานแห่งมหาวิทยาลัยเพนซิลเวเนีย (DK019525) และได้รับทุนสนับสนุนจากสถาบันสุขภาพจิตแห่งชาติ (R01 MH51399 และ P50 MH66172) และสถาบันยาเสพติดแห่งชาติ (R01 DA07359)
เชิงอรรถ
การเปิดเผยข้อมูลทางการเงิน: ผู้เขียนทั้งหมดประกาศว่าพวกเขาไม่มีผลประโยชน์ทางการเงินทางชีวการแพทย์หรือความขัดแย้งทางผลประโยชน์ที่อาจเกิดขึ้น
อ้างอิง
1 Wadden TA, Berkowitz RI, Womble LG, Sarwer DB, Phelan S, Cato RK, Hesson LA, Osei SY, Kaplan R, Stunkard AJ การทดลองแบบสุ่มของการปรับเปลี่ยนวิถีชีวิตและการรักษาด้วยยาสำหรับโรคอ้วน N Engl J Med 2005; 353 (20): 2111 20-[PubMed].
2 Blendy JA, Strasser A, Walters CL, Perkins KA, Patterson F, Berkowitz R, Lerman C. ลดนิโคตินในโรคอ้วน: เปรียบเทียบระหว่างมนุษย์และเมาส์ Psychopharmacology (Berl) 2005
3 Franken IH, Muris P. ความแตกต่างของแต่ละบุคคลในเรื่องความไวของรางวัลเกี่ยวข้องกับความอยากอาหารและน้ำหนักตัวที่สัมพันธ์กันในผู้หญิงที่มีสุขภาพดี ความกระหาย. 2005; 45 (2): 198 201-[PubMed].
4 ตวัด AE, Berridge KC ประสาทวิทยาศาสตร์ของรางวัลตามธรรมชาติ: ความเกี่ยวข้องกับยาเสพติด J Neurosci 2002; 22 (9): 3306 11-[PubMed].
5 Cagniard B, Balsam PD, Brunner D, Zhuang X. หนูที่มีโดปามีนที่ยกระดับเรื้อรังแสดงแรงจูงใจที่เพิ่มขึ้น แต่ไม่ได้เรียนรู้เพื่อเป็นรางวัลอาหาร Neuropsychopharmacology 2006; 31 (7): 1362 70-[PubMed].
6 เหลียงอร์ทแคโรไลนา, Hajnal A, Norgren R. Sham ที่ให้น้ำมันข้าวโพดเพิ่มโดปามีนในหนู Am J Physiol Regul Integr Comp Physiol 2006; 291 (5): R1236-9 [PubMed].
7 Mendoza J, Angeles-Castellanos M, Escobar C. อาหารที่น่ารับประทานทำให้เกิดกิจกรรมที่คาดการณ์ไว้และการแสดงออกของ c-Fos ในพื้นที่ที่เกี่ยวข้องกับการให้รางวัลของสมอง ประสาท 2005; 133 (1): 293 303-[PubMed].
8 ชโรเดอร์ พ.ศ. , Binzak JM, Kelley AE รายละเอียดทั่วไปของการเปิดใช้งานเยื่อหุ้มสมอง prefrontal หลังจากสัมผัสกับตัวชี้นำบริบทนิโคตินหรือช็อคโกแลตที่เกี่ยวข้อง ประสาท 2001; 105 (3): 535 45-[PubMed].
9 Nestler EJ, Barrot M, DW เอง DeltaFosB: สวิตช์โมเลกุลที่ยั่งยืนสำหรับการติดยาเสพติด Proc Natl Acad Sci US A. 2001; 98 (20): 11042 – 6 [PMC บทความฟรี] [PubMed]
10 Teegarden SL, Bale TL การลดความชอบในการบริโภคอาหารทำให้อารมณ์และความเสี่ยงต่อการกำเริบของอาหารลดลง จิตเวช Biol 2007; 61 (9): 1021 9-[PubMed].
11 Olausson P, Jentsch JD, Tronson N, Nestler EJ, Taylor JR dFosB ในนิวเคลียส Accumbens ควบคุมพฤติกรรมการใช้เครื่องมือและแรงจูงใจในการเสริมอาหาร วารสารประสาทวิทยาศาสตร์ 2006; 26 (36): 9196 9204-[PubMed].
12 เฉิน J, Kelz MB, เซงจี, ซาไกเอ็น, สเตฟเฟนซี, Shockett PE, Picciotto MR, Duman RS, Nestler EJ สัตว์ดัดแปลงพันธุกรรมที่มีการเหนี่ยวนำการแสดงออกของยีนเป้าหมายในสมอง Mol Pharmacol 1998; 54 (3): 495 503-[PubMed].
13 Kelz MB, Chen J, Carlezon WA, Jr, Whisler K, Gilden L, Beckmann AM, Steffen C, Zhang YJ, Marotti L, DW ตนเอง, Tkatch T, Baranauskas G, Surmeier DJ, Neve RL, Duman RS, Picciotto MR, Nestler EJ การแสดงออกของปัจจัยการถอดรหัส deltaFosB ในสมองควบคุมความไวต่อโคเคน ธรรมชาติ. 1999; 401 (6750): 272 6-[PubMed].
14 Bale TL, Dorsa DM ความแตกต่างระหว่างเพศและผลของฮอร์โมนเอสโตรเจนต่อการแสดงออกของกรดอะมิโนรับซิโตนิกซินในนิวทาลัมมัส การศึกษาเกี่ยวกับต่อมไร้ท่อ 1995; 136 (1): 27 32-[PubMed].
15 Avena NM, ลองกอง, Hoebel BG หนูที่ขึ้นกับน้ำตาลแสดงการตอบสนองที่ดีขึ้นสำหรับน้ำตาลหลังเลิกบุหรี่: หลักฐานของผลการกีดกันน้ำตาล Behiol Behav 2005; 84 (3): 359 62-[PubMed].
16 จะ MJ, Franzblau EB, Kelley AE นิวเคลียส accumbens mu-opioids ควบคุมปริมาณของอาหารไขมันสูงผ่านการเปิดใช้งานของเครือข่ายสมองกระจาย J Neurosci 2003; 23 (7): 2882 8-[PubMed].
17 Zheng H, Patterson LM, Berthoud HR การส่งสัญญาณ Orexin ในพื้นที่หน้าท้องเป็นสิ่งจำเป็นสำหรับความอยากอาหารไขมันสูงที่เกิดจากการกระตุ้น opioid ของนิวเคลียส accumbens J Neurosci 2007; 27 (41): 11075 82-[PubMed].
18 Hommel JD, Trinko R, เซียร์ RM, Georgescu D, Liu ZW, Gao XB, Thurmon JJ, Marinelli M, DiLeone RJ Leptin รับสัญญาณในเซลล์ประสาทโดปามีนในสมองส่วนกลางควบคุมการให้อาหาร เซลล์ประสาท 2006; 51 (6): 801 10-[PubMed].
19 Colby CR, Whisler K, Steffen C, Nestler EJ, DW ตัวเอง การแสดงออกเฉพาะของเซลล์มากเกินไปของ DeltaFosB ช่วยเพิ่มแรงจูงใจสำหรับโคเคน J Neurosci 2003; 23 (6): 2488 93-[PubMed].
20 Zachariou V, Bolanos CA, Selley DE, Theobald D, Cassidy MP, Kelz MB, Shaw-Lutchman T, Berton O, Sim-Selley LJ, Dileone RJ, Kumar A, Nestler EJ มีบทบาทสำคัญสำหรับ DeltaFosB ในนิวเคลียส accumbens ในการกระทำมอร์ฟีน Nat Neurosci 2006; 9 (2): 205 11-[PubMed].
21 Lee KW, Kim Y, Kim AM, Helmin K, Nairn AC, Greengard P. การก่อตัวของ dendritic กระดูกสันหลังโคเคนที่เกิดจากโคเคนใน D1 และ D2 ตัวรับโดปามีนที่มีโดพามีนปานกลางในนิวเคลียส accumbens Proc Natl Acad Sci US A. 2006; 103 (9): 3399 – 404 [PMC บทความฟรี] [PubMed]
22 Blendy JA, Maldonado R. การวิเคราะห์ทางพันธุกรรมของการติดยาเสพติด: บทบาทของโปรตีนตอบสนองค่ายองค์ประกอบผูกพันโปรตีน J Mol Med 1998; 76 (2): 104 10-[PubMed].
23 Nestler EJ กลไกระดับโมเลกุลของการติดยา Neuropharmacology 2004; 47 1: 24 – 32 [PubMed]
24 Tanis KQ, Duman RS, Newton SS การผูกมัดของ CREB และกิจกรรมในสมอง: ความจำเพาะและการเหนี่ยวนำในระดับภูมิภาคโดยการชักด้วยไฟฟ้า จิตเวช Biol 2007
25 Kumar A, Choi KH, Renthal W, Tsankova NM, Theobald DE, Truong HT, Russo SJ, Laplant Q, Sasaki TS, Whistler KN, Neve RL, DW ตัวเอง, Nestler EJ Chromatin remodeling เป็นกลไกสำคัญที่แสดงถึงความเป็นพลาสติกที่เกิดจากโคเคนใน striatum เซลล์ประสาท 2005; 48 (2): 303 14-[PubMed].
26 เกรแฮม DL, Edwards S, Bachtell RK, Dileone RJ, Rios M, DW ตนเอง กิจกรรม BDNF แบบไดนามิกในนิวเคลียส accumbens ด้วยการใช้โคเคนเพิ่มการบริหารตนเองและการกำเริบของโรค Nat Neurosci 2007; 10 (8): 1029 37-[PubMed].
27 Svenningsson P, Nairn AC, Greengard P. DARPP-32 ไกล่เกลี่ยการกระทำของยาเสพติดหลายรายการในทางที่ผิด Aaps J. 2005; 7 (2): E353 – 60 [PMC บทความฟรี] [PubMed]
28 พาลเมอร์ AA, Verbitsky M, Suresh R, Kamens HM, Reed CL, Li N, Burkhart-Kasch S, McKinnon CS, Belknap JK, Gilliam TC, Phillips TJ ความแตกต่างในการแสดงออกของยีนในหนูที่ถูกเลือกแตกต่างกันไปสำหรับความไวของแอมเฟตตามิน Mamm Genome 2005; 16 (5): 291 305-[PubMed].
29 Bogush A, Pedrini S, Pelta-Heller J, Chan T, Yang Q, Mao Z, Sluzas E, Gieringer T, Ehrlich ME AKT และ CDK5 / p35 ไกล่เกลี่ยการเหนี่ยวนำปัจจัยทางประสาทที่ได้มาจากสมองของ DARPP-32 ในเซลล์ประสาทแบบหนามขนาดกลางในหลอดทดลอง J Biol Chem 2007; 282 (10): 7352 9-[PubMed].
30 Benavides DR, Bibb JA บทบาทของ Cdk5 ในการใช้ยาและพลาสติก Ann NY Acad Sci 2004; 1025:. 335 44-[PubMed]
31 Bibb JA, Chen J, Taylor JR, Svenningsson P, Nishi A, Snyder GL, Yan Z, Sagawa ZK, Ouimet CC, Nairn AC, Nestler EJ, Greengard P. ผลกระทบของการสัมผัสโคเคนแบบเรื้อรังกับโปรตีนโคเคน Cdk5 ธรรมชาติ. 2001; 410 (6826): 376 80-[PubMed].
32 Blochl A, Sirrenberg C. Neurotrophins กระตุ้นการหลั่งโดปามีนจากเซลล์ประสาทหนู mesencephalic ผ่านตัวรับสัญญาณ Trk และ p75Lntr J Biol Chem 1996; 271 (35): 21100 7-[PubMed].
33 Berton O, McClung CA, Dileone RJ, Krishnan V, Renthal W, รุสโซ SJ, เกรแฮม D, Tsankova NM, Bolanos CA, Rios M, Monteggia LM, DW ตนเอง, Nestler EJ บทบาทสำคัญของ BDNF ในเส้นทางโดปามีน mesolimbic ในความเครียดจากการพ่ายแพ้ทางสังคม วิทยาศาสตร์. 2006; 311 (5762): 864 8-[PubMed].
34 Nestler EJ, Carlezon WA., Jr วงจรรางวัลโดปามีน mesolimbic ในภาวะซึมเศร้า จิตเวช Biol 2006; 59 (12): 1151 9-[PubMed].
35 Ford CP, Beckstead MJ, Williams JT การยับยั้ง Kappa opioid ของการยับยั้งโดปามีน somatodendritic J Neurophysiol 2007; 97 (1): 883 91-[PubMed].
36 Nylander I, Vlaskovska M, Terenius L. ระบบสมองและสมองในหนู Fischer และ Enkephalin ของ Fischer และ Lewis: ผลของการทนและการถอนมอร์ฟีน ความต้านทานของสมอง 1995; 683 (1): 25 35-[PubMed].
37 Nylander I, Hyytia P, Forsander O, Terenius L. ความแตกต่างระหว่างการใช้แอลกอฮอล์ (AA) และการหลีกเลี่ยงแอลกอฮอล์ (ANA) ในหนูในระบบ prodynorphin และ proenkephalin แอลกอฮอล์ Clin ประสบการณ์ Res 1994; 18 (5): 1272 9-[PubMed].
38 Kreek MJ โคเคนโดปามีนและระบบ opioid จากภายนอก J Addict Dis 1996; 15 (4): 73 96-[PubMed].
39 Carlezon WA, Jr, Duman RS, Nestler EJ ใบหน้าจำนวนมากของ CREB เทรนด์ Neurosci 2005; 28 (8): 436 45-[PubMed].
40 Dudman JT, Eaton ME, Rajadhyaksha A, Macias W, Taher M, Barczak A, Kameyama K, Huganir R, Konradi C. ผู้รับ Dopamine D1 ไกล่เกลี่ย CREB phosphorylation ผ่านตัวรับ NMDA ที่ Ser897-NRXUMXNNXXXX J Neurochem 1; 2003 (87): 4 922-[PubMed].
41 DW ตนเอง ระเบียบของการใช้ยาและพฤติกรรมการมองหาโดย neuroadaptations ในระบบโดปามีน mesolimbic Neuropharmacology 2004; 47 1: 242 – 55 [PubMed]
42 Beitner-Johnson D, Nestler EJ มอร์ฟีนและโคเคนออกฤทธิ์เรื้อรังที่พบบ่อยในไทโรซีนไฮดรอกซีเลสในพื้นที่ที่ได้รับรางวัลโดปามีนสมอง J Neurochem 1991; 57 (1): 344 7-[PubMed].
43 Lu L, Grimm JW, Shaham Y, Hope BT การปรับระบบประสาทในระดับโมเลกุลในบริเวณที่มีอาการท้องร่วงและหน้าท้องในช่วงวัน 90 แรกของการงดเว้นจากการโคเคนด้วยตนเองในหนู J Neurochem 2003; 85 (6): 1604 13-[PubMed].
44 Shepard JD, Chuang DT, Shaham Y, Morales M. ผลของการจัดการด้วยตนเองของ methamphetamine ต่อไทโรซีนไฮดรอกซีเลสและโดพามีนในระดับ transporter dopamine ใน mesolimbic และ nigrostriatal ของหนู Psychopharmacology (Berl) 2006; 185 (4): 505 – 13 [PubMed]
45 Fulton S, Pissios P, Manchon RP, Stiles L, Frank L, Pothos EN, Maratos-Flier E, Flier JS ระเบียบ Leptin ของ mesoaccumbens dopamine pathway เซลล์ประสาท 2006; 51 (6): 811 22-[PubMed].
46 Narita M, Nagumo Y, Miyatake M, Ikegami D, Kurahashi K, Suzuki T. ความหมายของโปรตีน kinase C ในระดับโดปามีนที่เพิ่มขึ้นจาก orexin และผลของการให้รางวัล Eur J Neurosci 2007; 25 (5): 1537 45-[PubMed].
47 Narita M, Nagumo Y, Hashimoto S, Khotib J, Miyatake M, Sakurai T, Yanagisawa M, Nakamachi T, Shioda S, Suzuki T. การมีส่วนร่วมโดยตรงของระบบ orexinergic ในการเปิดใช้งานของโดปามีน mesolimbic dopamine และพฤติกรรมที่เกี่ยวข้องที่เกิดจากมอร์ฟีน J Neurosci 2006; 26 (2): 398 405-[PubMed].
48 Borgland SL, Taha SA, Sarti F, ทุ่ง HL, Bonci A. Orexin A ใน VTA เป็นสิ่งสำคัญสำหรับการเหนี่ยวนำของพลาสติก synaptic และความไวต่อพฤติกรรมกับโคเคน เซลล์ประสาท 2006; 49 (4): 589 601-[PubMed].
49 Park ES, Yi SJ, Kim JS, Lee HS, Lee IS, Seong JK, Jin HK, Yoon YS การเปลี่ยนแปลงในการแสดงออกของ orexin-A และ neuropeptide Y ใน hypothalamus ของการอดอาหารและไขมันสูงที่เลี้ยงหนู J Vet Sci 2004; 5 (4): 295 302-[PubMed].
50 Wortley KE, Chang GQ, Davydova Z, Leibowitz SF เปปไทด์ที่ควบคุมการบริโภคอาหาร: การแสดงออกของยีน orexin เพิ่มขึ้นในระหว่างภาวะไขมันในเลือดสูง Am J Physiol Regul Integr Comp Physiol 2003; 284 (6): R1454-65 [PubMed].
51 Zheng H, Corkern M, Stoyanova I, Patterson LM, Tian R, Berthoud HR เปปไทด์ที่ควบคุมการรับประทานอาหาร: การกระตุ้นความอยากอาหาร - กระตุ้นการทำงานของเซลล์ประสาทเปิดใช้งาน hypothalamic orexin และยับยั้ง POMC เซลล์ประสาท Am J Physiol Regul Integr Comp Physiol 2003; 284 (6): R1436-44 [PubMed].
52 Baldo BA, Gual-Bonilla L, Sijapati K, Daniel RA, Landry CF, Kelley AE การเปิดใช้งานของประชากร subexulation ของเซลล์ประสาท hypothalamic ที่มี orexin / hypocretin โดย GABAA ยับยั้งการรับผู้รับไกล่เกลี่ยของนิวเคลียสเปลือก accumbens แต่ไม่ได้สัมผัสกับสภาพแวดล้อมที่แปลกใหม่ Eur J Neurosci 2004; 19 (2): 376 86-[PubMed].
53 Harris GC, Wimmer M, Aston-Jones G. บทบาทของเซลล์ประสาท hypothalamic orexin ด้านข้างในการแสวงหารางวัล ธรรมชาติ. 2005; 437 (7058): 556 9-[PubMed].