Коментари: Овај преглед су направили шеф НИДА, Нора Волков и њен тим. Нема сумње да хемијске овисности и овисности о понашању дијеле исте или сличне механизме и неуронске склопове. Ово има смисла јер хемијске овисности отимају неуронска кола за спајање, секс и јело. Пошто секс испушта двоструко више допамина од једења ваше омиљене хране, а порно корисник може задржати допамин повишен сатима, лудо је рећи да порнографија не може постојати.
Цурр Топ Бехав Неуросци. КСНУМКС Оцт КСНУМКС.
Волков НД, Ванг ГЈ, Фовлер ЈС, Томаси Д, Балер Р.
извор
Национални институт за злоупотребу дрога, КСНУМКС Екецутиве Боулевард КСНУМКС, соба КСНУМКС, Бетхесда, МД, КСНУМКС, САД, [емаил заштићен].
Апстрактан
И овисност о дрогама и гојазност могу се дефинирати као поремећаји у којима вриједност наглашености једне врсте награде (лијекови и храна) постају ненормално повећана у односу на, и на штету других. Овај модел је у складу са чињеницом да и лекови и храна имају снажне појачавајуће ефекте - делимично посредоване повећањем допамина у лимбичном систему - који би, под одређеним околностима или код рањивих појединаца, могли да надвладају хомеостатске механизме контроле мозга. Такве паралеле су изазвале значајан интерес за разумевање заједничких рањивости и путања између зависности и гојазности. Сада, открића слике у мозгу су почела да откривају заједничке карактеристике између ова два стања и да разграниче неке од преклапајућих можданих кругова чије дисфункције могу да објасне стереотипне и повезане поремећаје у понашању код људи. ТОви резултати указују да и гојазни и овисни појединци пате од поремећаја у допаминергичким путевима који регулишу неуронске системе повезане не само са награђиваном осјетљивошћу и мотивационом мотивацијом, већ и са условљавањем (памћење / учење), контролом импулса (инхибиција понашања), стресна реактивност и интероцептивна свест. Овде, ми интегрирамо налазе претежно изведене из позитронске емисијске томографије која бацају светло на улогу допамина у зависности од дроге и у гојазности, и предлажу ажурирани модел рада који би помогао у идентификацији стратегија лечења које могу имати користи од оба ова стања.
1 позадина
2 Улога допамина у акутној награди за дроге и храну
3 Излагање ДА у одговору на дроге и условљене знакове у зависности
4 Утицај дисфункције у инхибиторној контроли
5 Укључивање мотивационих кругова
6 Учешће интероцептивног круга
7 Цирцуитри оф Аверсион
8 Патолошка награда за лекове и храну: ажурирани модел рада
1 позадина
Допамин (ДА) се сматра кључним за ефекте награђивања природних и дрога. Међутим, његова улога у губитку контроле и компулзивном понашању које је повезано са зависношћу и гојазношћу су много мање јасне. ПЕТ студије су одиграле кључну улогу у карактеризацији улоге система мозга ДА у зависности (поред своје улоге у награди за лекове) и код гојазности. Заиста, лекови злоупотребе (укључујући алкохол) се конзумирају од стране људи или се сами примењују од стране лабораторијских животиња јер су инхерентно корисни, ефекат који је посредован њиховим својствима повећања ДА у мезолимбичком систему (Висе). 2009). Хупркос томе, у случају зависности, сликовне студије су откриле да поремећај утиче не само на круг награђивања ДА, већ и на друге путеве ДА који су укључени у модулацију кондиционих / навика, мотивацију и извршне функције (инхибиторна контрола, атрибуција истакнутости и одлука - стварање), и да дефицити ДА могу такође да учествују у појачаној реактивности стреса и ометању интероцептивне свести у вези са зависношћу. Претклиничке и клиничке студије су такође откриле друге неуротрансмитере (и неуропептиде) који играју важну улогу у наградама и зависности од дроге (тј. канабиноиди, опиоиди) и блиско су укључени у неуропластичне промјене које прате поновну употребу дрога (тј. глутамат, опиоиди, ГАБА, фактор отпуштања кортикотропина). Глутаматергични систем је посебно истакнут у овом погледу, јер посредује у прекидима у дугорочном појачавању и дугорочној депресији која је уочена у животињским моделима хроничне примене лекова. (Тхомас ет ал. 2008). Рецензије које се односе на ове додатне системе могу се наћи на другим мјестима (Каливас 2009; Кооб 1992).
Будући да лекови активирају исте системе награђивања који наглашавају награђивање хране, није потпуно неочекивано да су, у принципу, студије слике мозга подржале идеју да су оштећења у ДА-модулираним круговима такође укључена у патолошка, компулзивна понашања у исхрани.. Знакови хране, попут знакова дроге, повећавају екстрацелуларни ДА и потичу мотивацију да се укључе у понашања која су неопходна за набавку и јело хране, пружајући доказе за укључивање ДА не само у награду за храну, већ иу не-хедонистичку мотивацију својства хране (тј. калоријски захтјеви) и смањење инхибиторне контроле у компулзивном преједању (Авена ет ал. 2008; Волков ет ал. КСНУМКСа).
Овде разматрамо налазе из студија слика које се посебно фокусирају на преклапања у можданим круговима који су поремећени у гојазности и зависности од дроге. Међутим, ваља имати на уму да је регулација понашања уношења хране много сложенија од регулације уноса дроге. Ово последње је претежно посредовано ефектом награђивања лекова, док је први модулиран не само његовим ефектима награђивања (хедонским факторима), већ и вишеструким периферним и централним факторима који утичу на потребе нутријента у телу неопходне за преживљавање (хомеостатски фактори). Интересантно је да постоји све више доказа да хомеостатски фактори (нпр. Инсулин, лептин, грелин) модулирају унос хране делимично повећавајући или смањујући осетљивост кругова награђивања мозга на стимулансе хране (Волков ет ал. КСНУМКСа).
2 Улога допамина у акутној награди за дроге и храну
Било директно или индиректно, сви лекови који изазивају заразу показују способност повећања ДА у нуцлеус аццумбенс (НАц) преко специфичних интеракција са различитим молекуларним циљевима (Нестлер) 2004) (Шипак. 1). Чини се да је мезолимбички ДА пут [ДА ћелије у вентралном тегменталном подручју (ВТА) који пролази у НАц] пресудан за награду за лекове (Висе) 2009). Међутим, као што је ниже описано, други путеви ДА [мезостриатални (ДА ћелије у супстанцији нигра које се шире у дорзални стриатум) и мезокортикални (ДА ћелије у ВТА које се шире у фронтални кортекс)] такође доприносе награди и зависности од дроге (Висе) 2009). Све у свему, чини се да су ефекти награђивања и кондиционирања лијекова претежно вођени фазним отпуштањем ДА ћелија, што доводи до великих и пролазних повећања ДА. Насупрот томе, низводне промјене у извршној функцији које се јављају у зависности повезане су са промјенама у тоничком испаљивању ДА ћелија и резултирају нижим, али стабилнијим ДА нивоима 2000; Ванат ет ал. 2009). Ово, пак, указује на ДКСНУМКС рецепторе (ДКСНУМКСР), који су ДА рецептори ниског афинитета који стимулишу цикличну АМП сигнализацију, као што су укључени у акутну награду за лекове, као и за кондиционирање, пошто су они повезани са високим концентрацијама ДА да стимулише ДКСНУМКСР. Насупрот томе, ДКСНУМКСРс, који инхибирају цикличну АМП сигнализацију, стимулишу се и фазним и тоничким ДА. Треба приметити да, услед недостатка специфичних радиотражера за ПЕТ имиџе ДА рецептора типова ДКСНУМКС, ДКСНУМКС, ДКСНУМКС и ДКСНУМКС, већина студија о ефектима дрога злоупотребе и зависности у људском мозгу је фокусирана на ДКСНУМКСР.
Сл. КСНУМКС Лијекови злоупотребе дјелују на награде и помоћне кругове кроз различите механизме, међутим, сви они доводе до сличних допаминергичких ефеката у ВТА и НАц. Према томе, стимуланси директно појачавају акумбални ДА, док опијати то чине тако што смањују инхибиторни тон ГАБАергичних интернеурона на ДА сигнализацији, било у ВТА, било у НАц. Док су механизми других дрога злоупотребе мање јасни, постоје докази који упућују на то да никотин може активирати ВТА ДА директно преко никотинског ацетилхолинског рецептора (нАЦхР) на тим неуронима и индиректно преко стимулације његових рецептора на терминалима глутаматергичних живаца који инервишу ДА ћелије. Чини се да алкохол инхибира ГАБАергичне терминале у ВТА, што доводи до дисинхибиције ДА неурона у ВТА. Канабиноиди делују, између осталог, кроз активацију ЦБКСНУМКС рецептора на глутаматергичким и ГАБАергичким нервним терминалима у НАц, и на самим НАц неуронима. Фенциклидин (ПЦП) може дјеловати инхибирањем постсинаптичких НМДА глутамат рецептора у НАц. Поред тога, постоје неки докази који указују на то да никотин и алкохол такође могу да интерагују са ендогеним опиоидним и канабиноидним путевима (нису приказани). ППТ / ЛДТ, понтине тегментум / латерал дорсал тегментум. Прештампано са дозволом Нестлер (2005)
Код људи, ПЕТ студије су показале да неколико лекова [стимуланси (Древетс ет ал. 2001; Волков ет ал. КСНУМКСб), никотин (Броди ет ал. 2009), алкохол (Боилеау ет ал. 2003и марихуане (Боссонг ет ал. 2009)] повећање ДА у дорзалном и вентралном стриатуму (где се налази НАц). Ове студије користе предности неколико радиотерапија, као што су [11Ц] рацлоприд, који се везује за ДКСНУМКСР, али само када они нису обавезујући ендогени ДА (незаузети), што у основним условима одговара КСНУМКС-КСНУМКС% стриаталне ДКСНУМКСР (Аби-Даргхам ет ал. 1998). Дакле, поређење [11Везивање Ц] рацлоприда након плацеба и након примене лека може да нам помогне да проценимо смањење расположивости ДКСНУМКСР изазване леком (или друге стимулансе који могу повећати ДА). Ово се смањује у [11Ц] рацлоприд везивање је пропорционално повећању ДА (Бреиер ет ал. 1997). Ове студије су показале да су повећане ДА у стриатуму изазване леком пропорционалне интензитету субјективног искуства еуфорије или “високог” [види преглед (Волков ет ал. КСНУМКСа)] (Шипак. 2).
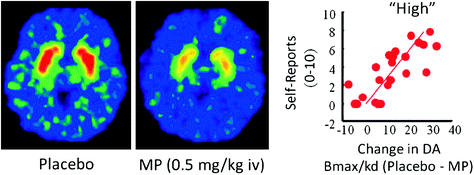
Сл. КСНУМКС Ефекти интравенског метилфенидата (МП) у везивању рацлоприда и однос између повећања стриаталног ДА изазваног МП у стриатуму и самопроцене „високог“. Измењено из Волков ет ал. (КСНУМКСб)
ПЕТ студије су такође откриле јасну, директну везу између фармакокинетичког профила лека (тј. Брзине којом улази и излази из мозга) и његових појачавајућих ефеката. Конкретно, што брже лек достигне вршне нивое у мозгу, то је интензитет „висок“ (Волков ет ал. КСНУМКСа). На пример, за еквивалентни ниво кокаина који допире до мозга (процењен преко ПЕТ-а), када је кокаин брзо ушао у мозак (пушење или ив администрација), изазвао је интензивније „високо“ него када је ушао спорије (фркнуо) (Волков ет ал. 2000). Ово је у складу са претклиничким студијама које показују сличну корелацију између фармакокинетичког профила лека и његових појачавајућих особина (Балстер и Сцхустер). 1973). ИРазумно је претпоставити да таква нагла и велика повећања ДА, која су изазвана дрогама злоупотребе, могу опонашати брзо и велико повећање ДА које је резултат фазног ДА паљења које су повезане, у мозгу, са обрадом информација о наградама и истакнутости (Сцхултз 2010). Оваква повећања ДА узрокована лековима у НАц могу бити неопходна за овисност, али чињеница да се оне јављају и код особа које нису овисне, указује на то да су оне недовољне да објасне импулсивну и компулзивну употребу дрога карактеристичну за овисност.
Сада постоје докази да су упоредиви допаминергички одговори повезани са наградом за храну и да су ти механизми такодје вјероватно играли улогу у прекомјерној потрошњи хране и гојазности. Добро је познато да одређене намирнице, посебно оне које су богате шећером и масти, снажно награђују (Леноир ет ал. 2007). Висококалорична храна може промовисати преједање (једење које је одвојено од енергетских потреба) и потакнути научене везе између стимулуса и награде (кондиционирање). У еволуционом смислу, ово својство укусних намирница је имало предност у срединама у којима су извори хране били оскудни и / или непоуздани, јер је осигурало да се храна једе када је доступна, омогућавајући да се енергија ускладишти у телу (као маст) за будућу употребу . Нажалост, у друштвима као што је наша, гдје је храна обилна и стално доступна, ова адаптација је постала одговорност.
Неколико неуротрансмитера, укључујући ДА, канабиноиде, опиоиде и серотонин, као и хормоне и неуропептиде укључене у хомеостатску регулацију уноса хране, као што су инсулин, орексин, лептин и грелин, укључени су у награђивање ефеката хране (Аткинсон) 2008; Цасон ет ал. 2010; Цота ет ал. 2006). Од њих, ДА је највише истражена и најбоље је окарактерисана. Експерименти на глодавцима су показали да се, након првог излагања награди за храну, отпуштање ДА неурона у ВТА повећава са резултирајућим повећањем ДА ослобађања у НАц (Норгрен ет ал. 2006). Слично, код здравих, нормалних људи, ингестија укусне хране показала се да ослобађа ДА у дорзалном стриатуму пропорционално оцјенама угодности оброка (Смалл ет ал. 2003) (Шипак. 3). Међутим, и као што се види у истраживањима са овисницима о дрогама, повећање узроковано храном узроковано само стриатом, не може објаснити разлику између нормалног уноса хране и прекомјерне компулзивне потрошње хране, јер се оне јављају и код здравих особа које не једу прекомјерно. Према томе, као што је случај са зависношћу, адаптације низводно ће вјероватно бити укључене у губитак контроле над уносом хране.
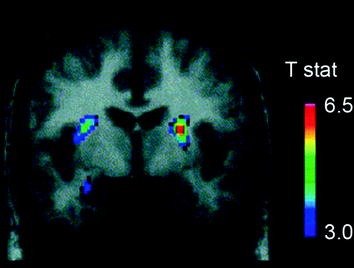
Сл. КСНУМКС Ослобађање допамина изазвано храњењем. Коронална секција из Т-мапе статистички значајних смањења у [11Ц] потенцијал везивања рацлоприда (БП) након храњења. Трака боја представља т статистичке вредности. (Преписано са дозволом Смалл ет ал. 2003)
3 Излагање ДА у одговору на дроге и условљене знакове у зависности
Улога ДА у појачавању је сложенија него само кодирање за награду пер се (хедонско задовољство); на пример, подстицаји који подстичу брзо и велико повећање ДА такође изазивају условљене реакције и изазивају мотивацију мотивације за њихову набавку (Овессон-Вхите ет ал. 2009). Ово је важно зато што, кроз процес условљавања, неутрални подражаји који су повезани са појачивачем (било да је то природни или ојачивач дроге) стичу способност да повећају ДА у стриатуму (укључујући НАц) у очекивању награде, и тиме изазивају снажна мотивација за тражење лека (Овессон-Вхите ет ал. 2009). Међутим, раздвајање механизама награђивања и кондиционирања у процесу овисности о дрогама је изазовније него за потрошњу хране, јер лијекови злоупотребе, кроз њихове фармаколошке ефекте, директно активирају ДА неуроне (тј. Никотин) или повећавају ослобађање ДА (тј. Амфетамина).
Студије снимања мозга које су упоређивале повећање ДА изазвано стимулансом метилфенидатом (МП) или амфетамином (АМПХ) код субјеката зависних од кокаина у односу на контролу, показало је значајно слабљење МП или АМПХ-индукованог повећања ДА у стриатуму (КСНУМКС% ниже код детоксификованих злостављача и КСНУМКС% у активним злостављачима) и нижим само-извештајима о ефектима награђивања лека у односу на контроле које не злоупотребљавају лекове (Мартинез ет ал. 2007; Волков ет ал. 1997) (Шипак. 4). Ово је било изненађујуће, јер су МП и АМПХ фармаколошки слични кокаину и метамфетамину, а злостављачи дрога не могу да их разликују када се дају интравенозно. Пошто су уочена значајна смањења у повећању ДА изазваног леком, да ли су злостављачи кокаина детоксифицирани или не, то указује да стање повлачења није фактор који збуњује (Волков ет ал. КСНУМКСб). Ови и сродни резултати (Волков ет ал. КСНУМКСа) су у складу са хипотезом да хедонични одговор постаје мањкав код појединаца који су овисни о дрогама, и даље јача мишљење да акутни фармаколошки ефекти повећања ДА-а у НАц-у не могу сами по себи објаснити повећану мотивацију да их конзумирају.
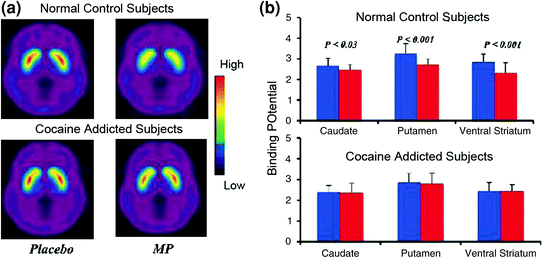
Сл. КСНУМКС Промене ДА изазване ив МП у контролама и код активних субјеката зависних од кокаина. Просечне невидљивог бидинг потенцијала (БПНД) слике [11Ц] рацлоприд у активних субјеката зависних од кокаина (н = КСНУМКС) и код контрола (н = КСНУМКС) тестираних након плацеба и након ив МП. б Доступност ДКСНУМКСР (БПНД) у каудату, путамену и вентралном стриатуму након плацеба (плава) и након МП (црвена) у контролама и код субјеката зависних од кокаина. МП је смањио ДКСНУМКСР у контролама, али не и код субјеката зависних од кокаина. Имајте на уму да злостављачи кокаина показују и смањење основног стријалног ДКСНУМКСР расположења (плацебо мјера) и смањење ослобађања ДА када се даје ив МП (мерено као смањење доступности ДКСНУМКСР од основне линије). Иако се може довести у питање степен до којег је ниска доступност стрикалног ДКСНУМКСР у субјекту овисном о кокаину ограничава могућност откривања даљњих смањења од МП, чињеница да субјекти овисни о кокаину показују смањење доступности ДКСНУМКСР када су изложени кокаинским знаковима указује да атенуирани ефекти МП на [11Повезивање Ц] рацлоприда одражава смањено ослобађање ДА. Штампано уз дозволу (Волков ет ал. 1997; Ванг ет ал. 2010)
Одговор ВТА ДА неурона на награђивање стимулуса се мења са поновљеном изложеношћу.
Док ДА ћелије пале након првог излагања новој награди, поновљено излагање ДА узрокује да неурони престану да пуцају на потрошњу награде и умјесто тога пале када су изложени стимулусима који предвиђају награду (Сцхултз ет ал. 1997). Ово је вјероватно подлога улоге ДА у учењу и кондиционирању. Заиста, фазна природна сигнализација ДА може изазвати неуроадаптације у помоћним круговима који се односе на формирање навике и условљавање понашања. ТХезе промене су углавном индуковане ДКСНУМКСР сигнализацијом и синаптичким променама у НМДА и АМПА рецепторима модулираним глутаматом. (Лусцхер и Маленка 2011; Звеифел ет ал. 2009). Регрутовање ових кругова је значајно у прогресији болести, јер условљени одговори који су уследили помажу да се објасни интензивна жеља за дрогом (жудња) и компулзивна употреба која се јавља када су субјекти који су овисни изложени лековима. Ова хипотеза је конзистентна са независним запажањима (Волков ет ал. КСНУМКСб; Вонг ет ал. 2006) који показују моћ изложености кокаину повезаном са повећањем нивоа ДА у дорзалном стриатуму и изазивају истовремени пораст субјективног искуства жудње за детоксикованим овисницима о кокаину (сл. 5). Пошто дорзални стриатум игра улогу у учењу навике (Белин ет ал. 2009; Иин ет ал. 2004), асоцијација ће вероватно одражавати јачање навика како хроничност зависности напредује. Ово сугерише да би основни поремећај зависности могао бити повезан са ДА изазваним условљеним реакцијама које доводе до навика које воде до интензивне жудње и компулзивне конзумације дрога. Занимљиво, код активног коришћења субјеката зависних од кокаина, чини се да су повећања ДА изазвана условљеним знаковима чак и већа од оних произведених самим стимулативним леком, као што је процењено у две одвојене групе субјеката (Волков ет ал. КСНУМКСб, КСНУМКСб), сугерирајући да условљени одговори могу довести до сигнализације ДА која одржава мотивацију за узимање лијека чак и када се чини да су његови фармаколошки ефекти смањени. Према томе, иако лекови могу иницијално да изазову осећај непосредне награде кроз ослобађање ДА у вентралном стриатуму, уз вишеструку употребу, и како се навика развија, чини се да постоји прелазак са лека на условљени стимуланс. Према студијама на лабораторијским животињама, глутаматергичне пројекције из префронталног кортекса и из амигдале у ВТА / СН и НАц посредују ове условљене реакције (Каливас). 2009). На овај начин, само предвиђање награде може на крају постати награда која мотивише понашање неопходно за конзумирање дроге (или хране).
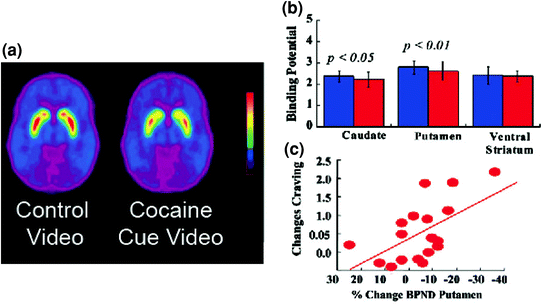
Сл. КСНУМКС Промене ДА изазване условљеним знаковима код активних субјеката зависних од кокаина. Просечни невидљиви потенцијал везивања (БПНД) слика [КСНУМКСЦ] рацлоприда код субјеката зависних од кокаина (н = КСНУМКС) тестираних приликом гледања неутралног видеа (призорима природе) и приликом гледања видео кокаинских знакова (субјекти који дају кокаин). б Доступност ДКСНУМКСР (БПНД) у каудату, путамену и вентралном стриатуму за неутрални видео (плави) и видео кокаински знак (црвени). Кокаински знакови су смањили ДКСНУМКСР у каудату и путамену. • Корелације између промена у ДКСНУМКСР (које одражавају повећања ДА) и самопроцене о кокаинској жудњи изазваној видео кокаинским знаковима. Измењено од реф. (Волков ет ал. КСНУМКСб)
IНажалост, овај тип функционалног "прекидача" је такође пријављен за природне појачиваче, који ће вероватно изазвати еквивалентни и постепени помак у повећању ДА, од вентралних до више дорзалних региона стриатума током транзиције од новог стимулуса који је инхерентно награђивања од оних повезаних знакова који то предвиђају. Ова транзиција се преноси преко ДА сигнализације, која изгледа да кодира “грешку предвиђања награде” (Сцхултз 2010). Опсежни глутаматергични аференти за ДА неуроне из региона који су укључени у процесирање сензорних (инсула или примарни густаторни кортекс), хомеостатика (хипоталамус), награда (НАц), емоционалне (амигдала и хипокампус) и мултимодалне (орбитофронтални кортекс за атрибуцију истакнутости) , модулирати своју активност као одговор на награде и условљене знакове (Геислер и Висе) 2008). Конкретније, пројекције из амигдале и орбитофронталног кортекса (ОФЦ) у ДА неуроне и НАц су укључене у условљене реакције на храну (Петровицх) 2010). Штавише, студије снимања су показале да када се од испитаника који нису гојазни од мушкараца тражи да инхибирају своју жељу за храном, док су изложени знаковима хране, показали су смањену метаболичку активност у амигдали и ОФЦ (као иу хипокампусу), инсули и стриатуму, и да је смањење ОФЦ било повезано са смањењем жудње за храном (Ванг ет ал. 2009). Слична инхибиција метаболичке активности у ОФЦ (и такође у НАц) је примијећена код овисника о кокаину када су замољени да инхибирају жудњу за дрогом након излагања кокаину (Волков ет ал. КСНУМКСб).
Ипак, појава тако снажно условљених жудњи, које се за храну јављају и код здравих појединаца који се не прејецају, не би била тако разарајућа ако не би била повезана са све већим дефицитима у способности мозга да инхибирају маладаптивно понашање.
4 Утицај дисфункције у инхибиторној контроли
Способност да се инхибирају препотентни одговори је дужан да допринесе способности појединца да избегне укључивање у неприкладно понашање, као што је узимање дроге или конзумирање прошлости тачке ситости и на тај начин повећава његову / њену рањивост на зависност (или гојазност) (Волков и Фовлер) 2000; Волков ет ал. КСНУМКСа).
ПЕТ студије су откриле значајна смањења у доступности ДКСНУМКСР у стриатуму субјеката који су овисници, а који трају мјесецима након продужене детоксикације [прегледано у (Волков ет ал. КСНУМКСа)]. Слично томе, претклиничке студије на приматима глодаваца и не-људи су показале да су поновљене изложености лековима повезане са смањењем стриалног нивоа ДКСНУМКСР (Надер ет ал. 2006; Тханос ет ал. 2007; Волков ет ал. 2001). У стриатуму, ДКСНУМКСР посредује сигнализацију у стриатном индиректном путу који модулира префронталне регионе; и показано је да његова регулација смањује сензибилизацију на ефекте лекова у животињским моделима (Фергусон ет ал. 2011). Код људи зависних од дрога, смањење стриаталног ДКСНУМКСР-а повезано је са смањеном активношћу префронталних региона, што се види из смањења почетног метаболизма глукозе (маркер функције мозга) код ОФЦ, предњег цингуларног гируса (АЦЦ) и дорсолатералног префронталног кортекса (ДЛПФЦ) ) (Волков ет ал. 2001, 1993, 2007) (Шипак. 6). Будући да су ОФЦ, АЦЦ и ДЛПФЦ укључени у атрибуцију истакнутости, инхибиторну контролу / регулацију емоција, односно доношење одлука, претпостављено је да би њихова неправилна регулација помоћу ДКСНУМКСР-посредоване ДА сигнализације код зависних субјеката могла бити основа повећане мотивационе вриједности лијекова у њиховом понашању и губитка контроле над уносом дроге (Волков и Фовлер) 2000). Поред тога, зато што су оштећења у ОФЦ-у и АЦЦ-у повезана са компулзивним понашањем и импулзивношћу (Финеберг ет ал. 2009), Поремећена модулација ових региона од стране ДА може допринети компулзивном и импулзивном уносу лекова који се види у зависности (Голдстеин и Волков) 2002). Заиста, код злостављача метамфетамина, ниски стриатални ДКСНУМКСР је био повезан са импулсивношћу (Лее ет ал. 2009), а такође је предвиђала компулзивно давање кокаина код глодара (Еверитт ет ал. 2008). Могући је и обрнути сценарио, у којем почетна рањивост за употребу дрога постоји у префронталним регионима, и при чему се поновна употреба дроге додатно смањује у стриаталном ДКСНУМКСР. Заиста, студија рађена код испитаника који, упркос високом ризику од алкохолизма (позитивна породична историја алкохолизма) нису били алкохоличари, открила је вишу него нормалну стриаталну ДКСНУМКСР доступност која је била повезана са нормалним метаболизмом у ОФЦ, АЦЦ и ДЛПФЦ (Волков) ет ал. КСНУМКСа). Ово сугерише да је код ових субјеката са ризиком од алкохолизма, нормална префронтална функција била повезана са појачаном стриатном ДКСНУМКСР сигнализацијом, што их је пак могло заштитити од злоупотребе алкохола.
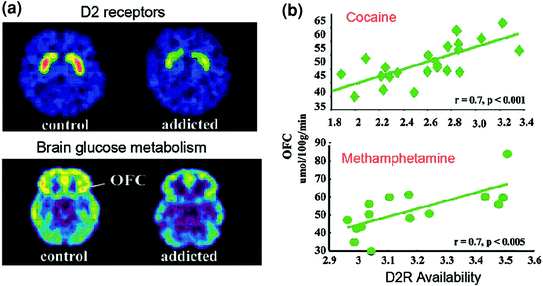
Сл. КСНУМКС Корелације између стриатне доступности ДКСНУМКСР и метаболизма у префронталним регионима мозга. аксијалне слике мозга за контролу и за субјекат овисан о кокаину за основне слике доступности ДКСНУМКСР у стриатуму (добијено са [11Ц] рацлоприда) и метаболизма глукозе у мозгу у ОФЦ (добијено са [18ФДГ). б Корелације између стрикалног ДКСНУМКСР и метаболизма у ОФЦ код субјеката зависних од кокаина и метамфетамина. Штампано из Волков ет ал. (КСНУМКСа) Ауторско право (КСНУМКС), са дозволом Елсевиера
Предвидљиво, докази о дисрегулацији у контролним круговима такође су нађени код гојазних појединаца. Оба претклиничка и клиничка испитивања пружила су доказе смањене стриатне ДКСНУМКСР сигнализације, која је, као што је горе наведено, повезана са наградом (НАц), али и са успостављањем навика и рутина (дорсал стриатум) у обеситуи (Геигер ет ал. 2009; Ванг ет ал. 2001). Важно је да је смањена доступност стрикалног ДКСНУМКСР повезана са принудним уносом хране код гојазних глодара (Јохнсон и Кенни) 2010и са смањеном метаболичком активношћу у ОФЦ и АЦЦ код гојазних људи (Волков ет ал. КСНУМКСб) (Шипак. 7а – ц). Имајући у виду да дисфункција у ОФЦ и АЦЦ доводи до компулзивности [види преглед (Финеберг ет ал. 2009)], то може бити дио механизма којим се сигнализацијом ДКСНУМКСР ниске стриатије олакшава хиперфагија (Давис ет ал. 2009). Поред тога, пошто је смањење сигнала повезаног са ДКСНУМКСР такође вероватно смањило осетљивост на друге природне награде, овај дефицит код гојазних појединаца такође може допринети компензаторној преједању (Геигер ет ал. 2008).
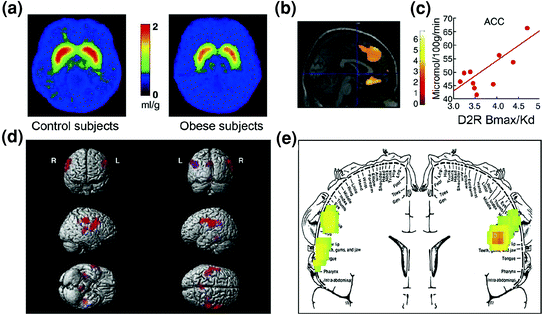
Сл. КСНУМКС Хиперфагија може настати као резултат компензације ослабљеног круга награђивања (обрађеног преко допамин регулисаних кортикостриаталних кругова) у комбинацији са повећаном осетљивошћу на укус (хедонистичка својства хране која се делимично обрађује кроз соматосензорни кортекс).. просечне слике за доступност ДА Д2 рецептора (Д2Р) код контрола (н = 10) и код болесника са гојазним субјектима (н = 10). б Резултати (Статистичко параметарско мапирање) СПМ који идентификује подручја у мозгу где је Д2Р био повезан са метаболизмом глукозе, они су укључивали медијални ОФЦ, АЦЦ и дорсолатерални ПФЦ (регион није приказан). ц Регресиони нагиб између стриаталног Д2Р и метаболичке активности у АЦЦ код гојазних испитаника. д Тродимензионално приказане СПМ слике које приказују подручја са већим метаболизмом код гојазних него код мршавих испитаника (П <0.003, неисправљено). е СПМ резултати кодирани бојом приказани у короналној равни са суперпонираним дијаграмом соматосензорног хомункула. Резултати (з вредност) су представљени коришћењем дугине скале где је црвена> жута> зелена. У поређењу са мршавим испитаницима, гојазни испитаници су имали виши основни метаболизам у соматосензорним областима где су заступљена уста, усне и језик и који су укључени у прераду укуса хране. Измењено, уз дозволу, Волков ет ал. (КСНУМКСа) (а – ц) и Ванг ет ал. (2002) (д, е)
Ова хипотеза је конзистентна са претклиничким доказима који показују да смањена активност ДА у ВТА доводи до драматичног повећања потрошње хране високе масноће (Стоецкел ет ал. 2008). Слично томе, у поређењу са појединцима са нормалном тежином, гојазни појединци који су били изложени сликама високе калоријске хране (подражаји на које су условљени) показали су повећану нервну активацију у регионима који су део круга награђивања и мотивације (НАц, дорзални стриатум, ОФЦ). , АЦЦ, амигдала, хипокампус и инсула) (Киллгоре и Иургелун-Тодд) 2005). Насупрот томе, у контролама нормалне тежине, активација АЦЦ-а и ОФЦ-а (региони који су укључени у атрибуцију истакнутости који се пројектују у НАц) током представљања висококалоричне хране је негативно корелирана са њиховим индексом телесне масе (БМИ) ( Стице ет ал. КСНУМКСб). Ово указује на динамичку интеракцију између количине поједене хране (која се делимично одражава у БМИ) и реактивности региона награђивања на висококалоричну храну (која се одражава у активацији ОФЦ и АЦЦ) код особа са нормалном тежином, што се губи у гојазност.
Изненађујуће, гојазни појединци показали су мање активације кругова награђивања од стварне потрошње хране (што се назива конзумацијска награда за храну) него мршави појединци, док су показали већу активацију соматосензорних кортикалних региона који обрађују укус када су очекивали конзумацију (Стице ет ал. КСНУМКСб). Ово последње посматрање одговарало је регионима у којима је претходна студија показала повећану активност код гојазних испитаника који су тестирани на основном нивоу (не стимулација) (Ванг ет ал. 2002) (Шипак. 7д, е). Повећана активност региона која процесира укус може довести до тога да гојазни субјекти преферирају храну у односу на друге природне појачиваче, док смањена активација допаминергичких циљева стварном потрошњом хране може довести до прекомерне потрошње као средства за компензацију слабог ДКСНУМКСР-посредованог сигнализирања (Стице ет ал. КСНУМКСа). Ово смањено одговарање круга награђивања на потрошњу хране код гојазних субјеката подсећа на смањење повећања ДА изазвано употребом лекова код зависних појединаца у поређењу са не-овисним субјектима.
Префронтални кортекс (ПФЦ) игра кључну улогу у извршној функцији, укључујући инхибиторну контролу (Миллер и Цохен). 2001). Ови процеси су модулирани са ДКСНУМКСР и ДКСНУМКСР (вероватно и ДКСНУМКСР) и према томе, смањена активност у ПФЦ, како у зависности, тако иу гојазности, вероватно доприноси лошој контроли и високој принудној способности. Доступност ДКСНУМКСР-а ниже од нормалне у стриатуму претилих појединаца, што је повезано са смањеном активношћу у ПФЦ и АЦЦ (Волков ет ал. КСНУМКСб) стога ће вјероватно допринијети њиховој мањкавој контроли над уносом хране. Заиста, негативна корелација између БМИ и стриаталног ДКСНУМКСР пријављена је код гојазних (Ванг ет ал. 2001и прекомерне тежине (Халтиа ет ал. КСНУМКСа) појединци то подржавају. Боље разумевање механизама који доводе до нарушене функције ПФЦ-а у гојазности (или зависности) може олакшати развој стратегија за побољшање, или можда чак преокретање, специфичних оштећења у кључним когнитивним доменима. На пример, одлагање кашњења, које представља тенденцију девалвирања награде као функције временског одлагања његове испоруке, једно је од најобимније истражених когнитивних операција у односу на поремећаје повезане са импулзивношћу и компулзивношћу. Дисконтирање кашњења је највише исцрпно истражено код особа које злоупотребљавају дроге које показују претерану склоност ка малим, али непосредним нагодбама (Бицкел ет ал. 2007). Међутим, неколико студија које су обављене са гојазним појединцима такође су откриле доказе о преференцијама за високе, непосредне награде, упркос повећаним шансама да се претрпе већи губици у будућности (Броган ет ал. 2010; Веллер ет ал. 2008). И недавно, друга студија је пронашла позитивну корелацију између БМИ и хиперболичног дисконтовања, при чему су будуће негативне исплате дисконтоване мање од будућих позитивних исплата (Икеда ет ал. 2010). Занимљиво, чини се да дисконтовање одлагања зависи од функције вентралног стриатума (Грегориос-Пиппас ет ал. 2009и ПФЦ, укључујући латерални ОФЦ (Бјорк ет ал. 2009), и осетљив је на манипулације ДА (Пине ет ал. 2010). Конкретно, повећање сигнализације ДА (са Л ДОПА третманом) повећало је импулсивност и временску дисконтовање.
5 Укључивање мотивационих кругова
Допаминергичка сигнализација такођер модулира мотивацију. Бихевиоралне особине, као што су снага, упорност и улагање континуираног напора ка постизању циља, подложни су модулацији ДА која дјелује кроз неколико циљних регија, укључујући НАц, АЦЦ, ОФЦ, ДЛПФЦ, амигдалу, дорзални стриатум и вентрални палидум (Саламоне ет ал. 2007). Дисрегулисано ДА сигнализирање повезано је са појачаном мотивацијом за набавку лијекова, што је знак зависности, због чега појединци овисници о дрогама често се упуштају у екстремна понашања за добивање дроге, чак и када изазивају озбиљне и штетне посљедице (Волков и Ли 2005). Зато што узимање дроге постаје главни мотивациони погон у овисности о дрогама (Волков ет ал. 2003), овисници се побуђују и мотивишу процесом добијања дроге, али имају тенденцију да постану повучени и апатични када су изложени активностима које нису повезане са дрогом. Ова промена је проучена упоређивањем узорака активације мозга који се јављају са излагањем условљеним знаковима са онима који се јављају у одсуству таквих знакова. Насупрот смањењу префронталне активности пријављеног код детоксификованих овисника о кокаину, када нису стимулисани лијековима или лијековима [види преглед (Волков ет ал. КСНУМКСа)], ови префронтални региони постају активни када се злостављачи кокаина изложе стимулусима који изазивају жељу (или лекови или знаци) (Грант ет ал. 1996; Волков ет ал. КСНУМКСа; Ванг ет ал. 1999). Овај резултат подсјећа на запажање да су злостављачи кокаина, који су проучавани убрзо након епизоде бочења кокаина, показали повећање метаболичке активности у ОФЦ и АЦЦ (такође дорзални стриатум) који је био повезан са жудњом (Волков ет ал. 1991).
Штавише, када се упореде одговори на ив МП између кокаин-овисних и не-овисних појединаца, први је одговорио појачаним метаболизмом у вентралном АЦЦ-у и медијалном ОФЦ-у (ефект повезан са жудњом), док је други показао супротан одговор, наиме смањен метаболизам у овим регионима (Волков ет ал. 2005). Ово сугерише да активација ових префронталних региона са излагањем леку може бити специфична за зависност и повезана са повећаном жељом за леком. Поред тога, студија која је потакла субјекте овисне о кокаину да намјерно инхибирају жудњу када је изложена лијековима показала је да су испитаници који су били успјешни у инхибирању жудње показали смањени метаболизам у медијалном ОФЦ-у (који обрађује мотивацијску вриједност појачивача) и НАц (који предвиђају) награда) (Волков ет ал. КСНУМКСб). Ови налази даље потврђују учешће ОФЦ-а, АЦЦ-а и стриатума у појачаној мотивацији за добијање лека виђеног у зависности.
Предвидљиво, ОФЦ је такође био уплетен у приписивање вредности истакнутости храни (Грабенхорст ет ал. 2008; Роллс и МцЦабе 2007), помажући да се процени његова очекивана пријатност и укусност као функција контекста. ПЕТ студије са ФДГ за мерење метаболизма глукозе у мозгу код особа са нормалном тежином показале су да изложеност храни повећава метаболичку активност у ОФЦ-у, што је ефекат повезан са перцепцијом глади и жељом за храном (Ванг ет ал. 2004). Побољшана активација ОФЦ-а стимулацијом хране ће вјероватно одражавати допаминергичне ефекте низводно и учествовати у укључивању ДА у погон за потрошњу хране. ОФЦ игра улогу у учењу асоцијација на појачање стимулација и кондиционирању (Цок ет ал. 2005; Галлагхер ет ал. 1999), подржава условљено храњење (Веингартен 1983), и вероватно доприноси преједању без обзира на сигнале глади (Огден и Вардле 1990). Заиста, дисфункција ОФЦ је повезана са преједањем (Мацхадо и Бацхевалиер 2007).
Упркос неким недоследностима међу истраживањима, подаци о можданим снимцима такође подржавају идеју да структурне и функционалне промене у регионима мозга које су укључене у извршну функцију (укључујући инхибиторну контролу) могу бити повезане са високим БМИ у иначе здравих особа. На примјер, МРИ студија проведена код старијих жена, користећи морфометрију засновану на вокселу, пронашла је негативну корелацију између БМИ и волумена сиве твари (укључујући фронталне регије), која је у ОФЦ-у била повезана с оштећеном извршном функцијом (Валтхер и сар. 2010). Користећи ПЕТ за мерење метаболизма глукозе у мозгу код здравих контрола, пријавили смо негативну корелацију између БМИ и метаболичке активности у ДЛПФЦ, ОФЦ и АЦЦ. У овој студији, метаболичка активност у префронталним регионима је предвидела учинак испитаника у тестовима извршне функције (Волков ет ал. КСНУМКСц). Слично томе, спектроскопска студија нуклеарне магнетне резонанције (НМР) у контролним испитивањима здравих средњих година и старијих особа показала је да је БМИ негативно повезан са нивоима Н-ацетил-аспартата (маркер неуронског интегритета) у фронталном кортексу и АЦЦ (Газдзински и сар. 2008; Волков ет ал. КСНУМКСц).
Студије снимања мозга које су упоређивале гојазне и витке појединце такође су показале мању густину сиве твари у фронталним регионима (фронтални оперцулум и средњи фронтални гирус) и пост-централни гирус и путамен (Паннацциулли ет ал. 2006). Друга студија, међутим, није пронашла разлике у количини сиве твари између гојазних и витких субјеката, забиљежена је позитивна корелација између волумена бијеле твари у базалним структурама мозга и омјера струка и кука, тренд који је дјеломично преокренут дијетама (Халтиа ет ал. КСНУМКСб). Интересантно је да су кортикалне области, као ДПФЦ и ОФЦ које су укључене у инхибиторну контролу, такође активиране у успешним дијетама као одговор на потрошњу оброка (ДелПариги ет ал. 2007), сугеришући потенцијални циљ за понављање обуке у лечењу гојазности (и такође у зависности).
6 Учешће интероцептивног круга
Неуроимагинг студије су откриле да средња инсула игра кључну улогу у жудњи за храном, кокаином и цигаретама. (Бонсон ет ал. 2002; Пелцхат ет ал. 2004; Ванг ет ал. 2007). Важност инсуле је истакнута у студији која је показала да су пушачи са оштећењем у овом региону (али не и контролни пушачи који су претрпели екстра-инсуларне лезије) били у стању да престану да пуше и без доживљавања жудње или релапса (Накви ет ал . 2007). Инсула, посебно њене предње области, реципрочно је повезана са неколико лимбичких региона (нпр. Вентромедијалним префронталним кортексом, амигдалом и трбушним стриатумом) и изгледа да има интероцептивну функцију, интегрише аутономну и висцералну информацију са емоцијама и мотивацијом, чиме обезбеђује свесност ових нагона (Накви и Бецхара 2009). Штавише, студије можданих лезија указују да су вентромедијални ПФЦ и инсула неопходне компоненте дистрибуираних кола које подржавају емоционално доношење одлука (Цларк ет ал. 2008). У складу са овом хипотезом, сликовне студије константно показују диференцијално активирање инсуле током жудње (Броди ет ал. 2009; Гоудриаан ет ал. 2010; Накви и Бецхара 2009; Ванг ет ал. 1999). Сходно томе, реактивност овог региона мозга је предложена да служи као биомаркер за помоћ у предвиђању рецидива (Јанес ет ал. 2010).
Инсула је такодје и примарно подруцје окуса, које уцествује у многим аспектима понашања у исхрани, као што је укус. Поред тога, рострална инсула (повезана са примарним кортексом укуса) даје информацију ОФЦ-у која утиче на њену мултимодалну репрезентацију пријатности или награђене вредности улазне хране (Роллс). 2008). Због укључености инсуле у интероцептивни осећај тела, у емоционалну свест (Цраиг 2003) иу мотивацији и емоцијама (Роллс 2008), може се очекивати допринос инсуларног оштећења гојазности. Заиста, желучана дистензија доводи до активације постериорне инсуле, која ће вероватно одражавати њену улогу у свесности телесних стања (у овом случају пунине) (Ванг ет ал. 2008). Штавише, код мршавих, али не код гојазних испитаника, желучана дистензија је резултирала активацијом амигдале и деактивацијом предње инсуле (Томаси и сар. 2009). Недостатак одговора на амигдалу код гојазних испитаника може одражавати отупјену интероцептивну свијест о тјелесним стањима повезаним са ситости (пуни желудац). Иако је модулација инсуларне активности ДА била слабо истражена, препознато је да је ДА укључен у одговоре на дегустацију укусних намирница које су посредоване кроз инсулу (Хајнал и Норгрен) 2005). Људске слике су показале да дегустација укусних намирница активира подручја инсуле и средњег мозга (ДелПариги ет ал. 2005; Франк ет ал. 2008). Међутим, сигнализација ДА може такође бити неопходна за детектовање садржаја калорија у храни. На пример, када су жене нормалне тежине пробале заслађивач са калоријама (сахароза), и инсула и допаминергична средња зона су се активирали, док је дегустација сладила без калорија (сукралоза) активирала само инсулу (Франк ет ал. 2008). Гојазни субјекти показују већу инсуларну активацију од нормалних контрола када дегустирају течни оброк који се састоји од шећера и масти (ДелПариги ет ал. 2005). Насупрот томе, субјекти који су се опоравили од анорексије нервозе показују мању активацију у инсули када пробају сахарозу и нема повезаности осећања пријатности са инсуларном активацијом као што је уочено у нормалним контролама (Вагнер ет ал. 2008). Када се комбинују, ови резултати чине вјероватним да дисрегулација инсуле као одговор на подражаје укуса може бити укључена у ослабљену контролу различитих навика понашања.
7 Цирцуитри оф Аверсион
Као што је раније поменуто, тренинг (кондиционирање) на знак који предвиђа награду доводи до допаминергичких ћелија које се пале као одговор на предвиђање награде, а не на саму награду. С друге стране, и конзистентно са овом логиком, примећено је да ће допаминергичне ћелије испалити мање него нормално ако се очекивана награда не материјализује (Сцхултз ет ал. 1997). Кумулативни докази (Цхристопх ет ал. 1986; Лисоправски ет ал. 1980; Матсумото и Хикосака 2007; Нисхикава ет ал. 1986) указује на хабенулу као један од региона који контролише смањење испуштања допаминергичних ћелија у ВТА, што може да прати неуспех да се добије очекивана награда (Кимура ет ал. 2007). Дакле, повећана осетљивост хабенула, као резултат хроничне изложености леку, може да подстакне већу реактивност на лекове. Заиста, активација хабенуле, код субјеката зависних од кокаина, била је повезана са понављањем понашања до узимања лека након излагања (Бровн ет ал. 2011; Зханг ет ал. 2005). У случају никотина, изгледа да никотински рецептори αКСНУМКС-а у хабенули модулирају аверзивне одговоре на велике дозе никотина (Фовлер ет ал. 2011); и αКСНУМКС и αКСНУМКС рецептори у хабенули су укључени у повлачење никотина (Салас ет ал. 2009). Због супротног одговора хабенула на онај ДА неурона да награђују (деактивирају) и његову активацију након излагања аверзивним стимулусима, овде се односи на сигнализацију хабенула као оне која преноси "антиревард" улаз.
Чини се да хабенула игра сличну улогу у погледу награђивања хране. Високо укусна дијета са храном може изазвати гојазност код пацова, са повећањем тежине која је у корелацији са повећањем везивања μ-опиоидног пептида у базолатералној и басомедијалној амигдали. Занимљиво је да је медијска хабенула показала значајно веће везивање μ-опиоидног пептида (за приближно КСНУМКС%) након излагања укусној храни код пацова који су добијали на тежини (они који су конзумирали више хране), али не и код оних који нису (Смитх ет ал. 2002). Ово сугерише да хабенула може бити укључен у преједање у условима доступности укусне хране. Штавише, неурони у ростромедијалном тегменталном језгру, који добијају главни унос из латералне хабенуле, пројектују на ВТА ДА неуроне и активирају се након ускраћивања хране (Јхоу ет ал. 2009). Ови налази су у складу са улогом хабенула у посредовању одговора на аверзивне стимулансе или стања као што су они који се јављају током дијете или повлачења дроге.
Учешће хабенула као антиревард средишта у емоционалним мрежама је у складу са претходним теоријским моделима зависности који постулирају сензибилисане анти-наградне одговоре (посредоване повећаном осетљивошћу амигдале и повећаном сигнализацијом код фактора ослобађања кортикотропина) као узимање дроге у зависности од зависности (Кооб и Ле Моал 2008). Слични антирегардни одговори могу такође допринети прекомерној потрошњи хране у гојазности.
8 Патолошка награда за лекове и храну: ажурирани модел рада
Tспособност да се одупре пориву да се користи лек или поједе крај ситости захтева исправно функционисање неуронских кругова укључених у контролу одозго према доле да би се супротставила условљеним одговорима који предвиђају награду од узимања хране / лека и жеље да се унесе храна / лек. Овде смо истакли шест од ових кругова: награда / истакнутост, кондиционирање / навике, инхибиторна контрола / извршна функција, мотивација / погон, интероцепција и избегавање аверзије / реактивност на стрес (сл. 8). На основу приказаних сликовних података, претпостављамо да је несклад између очекивања за ефекте дроге / хране (условљени одговори) и отупљених неурофизиолошких ефеката који одржавају узимање дрога или прекомерно конзумирање хране у покушају да се постигне очекивана награда. Такође, било да су тестирани током раних или дугих периода апстиненције / дијете, овисници / гојазни испитаници показују нижи ДКСНУМКСР у стриатуму (укључујући НАц), који су повезани са смањењем основне активности у фронталним регионима мозга који су укључени у атрибуцију истакнутости (орбитофронтални кортекс) и инхибиторни контроле (АЦЦ и ДЛПФЦ), чији поремећај доводи до компулзивности и импулзивности. Фу суштини, појављују се и докази о улози интероцептивних и одбојних кола у системским неравнотежама које доводе до принудне конзумације било дроге или хране.
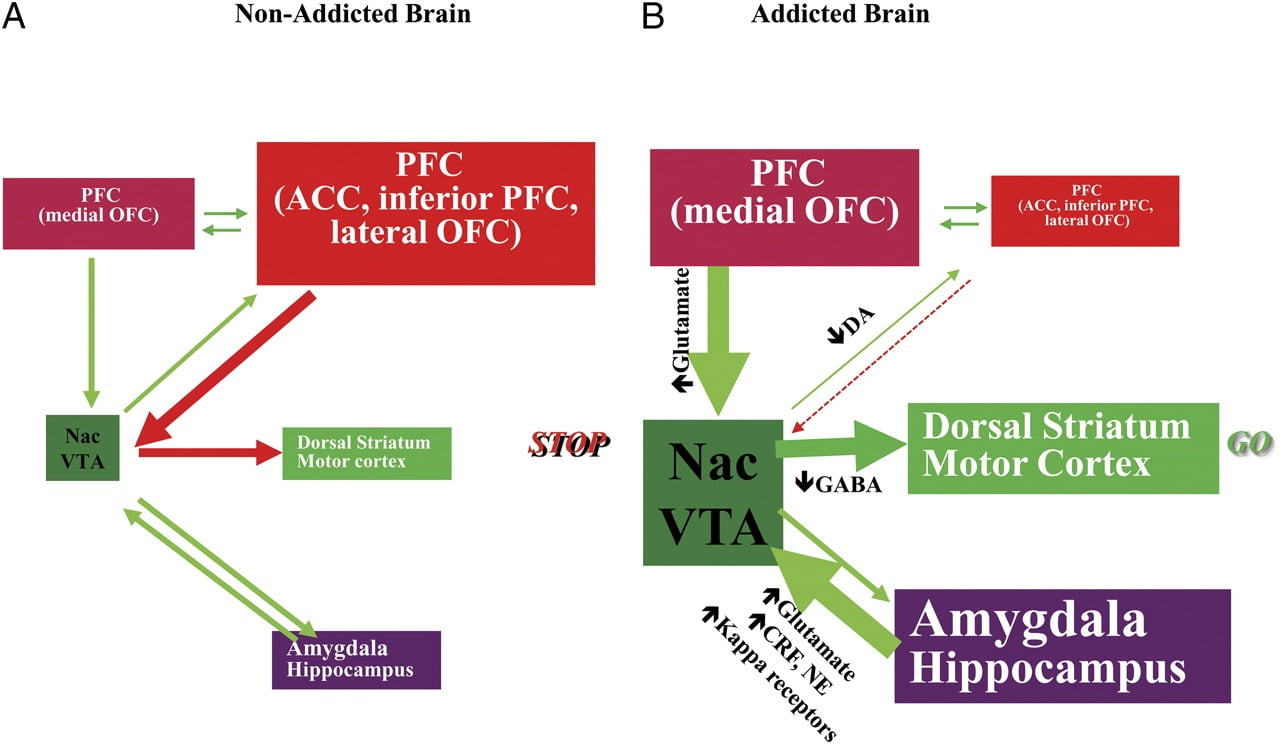
Сл. КСНУМКС Модел који предлаже мрежу интерактивних кругова, поремећаја који доприносе сложеном скупу стереотипних понашања која су у основи овисности о дрогама и хроничној преједању: награда (нуцлеус аццумбенс, ВТА, и вентрал паллидум), кондиционирање / памћење (амигдала, медијалан ОФЦ за атрибуцију истакнутости, хипокампус и дорзални стриатум за навике), извршна контрола (ДЛПФЦ, АЦЦ, доњи фронтални кортекс и латерални ОФЦ), мотивација / погон (медијски ОФЦ за атрибуцију истакнутости, вентрални АЦЦ, ВТА, СН, дорзални стриатум и моторни кортекс). Нац, нуцлеус аццумбенс, интероцепција (Инсула и АЦЦ), и аверзија / избегавање (Хабенула). Када су ови кругови уравнотежени, то резултира правилном инхибицијском контролом и доношењем одлука. б Током зависности, када повећана вредност очекивања лека у наградним, мотивационим и меморијским круговима превазилази контролни круг, фаворизујући позитивну повратну петљу иницирану потрошњом лека и продужену појачаном активацијом мотивације / нагона и меморијска кола. Ови кругови такође комуницирају са круговима који су укључени у регулацију расположења, укључујући реактивност на стрес (која укључује амигдалу, хипоталамус, хабенулу) и интероцепцију (која укључује инсулу и АЦЦ и доприноси свести о жудњи). Неколико неуротрансмитера је укључено у ове неуроадаптације, укључујући глутамат, ГАБА, норепинефрин, фактор ослобађања кортикотропина и опиоидне рецепторе. ЦРФ, фактор ослобађања кортикотропина; НЕ, норепинефрин. Измењено уз дозволу Волков ет ал. (КСНУМКСб)
Као посљедица секвенцијалног поремећаја у овим круговима, појединци могу искусити КСНУМКС) повећану мотивацијску вриједност лијека / хране (секундарно у односу на научене асоцијације кроз кондиционирање и навике) на штету других појачивача (секундарни према смањеној осјетљивости круга награђивања) ), КСНУМКС) ослабљена способност да инхибира намјерне (циљно усмјерене) акције изазване снажном жељом да се узме лијек / храна (секундарна до оштећене извршне функције) која доводи до принудног узимања дроге / хране и КСНУМКС) појачана реактивност на стрес и аверзивно избегавање које доводи до импулсивног узимања дроге да би избегло аверзивно стање.
Овај модел предлаже вишеструки терапијски приступ овисности који је дизајниран да смањи појачавајуће особине лијека / хране, поново успостави / побољша награђивана својства природних појачивача, инхибира условљене научене асоцијације, побољша мотивацију за активности које нису повезане са дрогом / храном, смањује реактивност стреса побољшавају расположење и јачају инхибиторну контролу опште намене.
priznanja
Аутори желе да се захвале подршци НИААА интрамуралног програма Националног института за здравље.
Референце