Научни извјештаји запремина 9, Број артикла: 16918 (2019)
Апстрактан
Прекомјерна конзумација сахарозе изазива жудњу попут овисности која може бити основа епидемије претилости. Опиоиди и допамин посредују корисне ефекте злоупотребе дрога и природне награде од стимулуса попут хране која се прија. Истражили смо ефекте сахарозе помоћу ПЕТ снимања са [11Ц] карфентанил (агонист µ-опиоидних рецептора) и [11Ц] раклоприд (антагонист рецептора допамина Д2 / 3) у седам женских мини-прасика под анестезијом. Затим смо мини-свињама дали приступ раствору сахарозе током једног сата током 12 дана узастопно и обавили снимање поново 24 сата након коначног приступа сахарози. На мањем узорку од пет минипирића, урадили смо додатни [11Ц] ПЕТ карфентанил сесије након прве изложености сахарози. Израчунали смо потенцијале везивања који се тичу воксела (БП)ND) користећи мозак као регију неисплативог везивања, анализирао је разлике са статистичким непараметарским мапирањем и урадио регионалну анализу. Након 12 дана приступа сахарози, БПND оба трагача су се значајно смањила у стриатуму, језгри акунди, таламусу, амигдали, цингулатском кортексу и префронталном кортексу, у складу са доњом регулацијом густине рецептора. Након једног излагања сахарози, открили смо смањено везивање [11Ц] карфентанил у нуклеусним језграма и цингулат кортекса, у складу са ослобађањем опиоида. Нижа доступност опиоидних и допаминских рецептора може објаснити потенцијал зависности који је повезан са уносом сахарозе.
увод
Пет одсто светске популације је клинички претило1. Као одлика метаболичког синдрома, гојазност је повезана са дијабетесом типа 2, кардиоваскуларним болестима, респираторним проблемима и ризиком од депресије и евентуалне деменције2. Повећана потрошња енергетски густе хране повећала је физиолошку разлику између хомеостатске глади која прати недостатак хране и хедонске глади или „жудње“ која се јавља у недостатку ускраћености3,4. Како хомеостатска регулација сама по себи не може објаснити тренутни пораст гојазности, обавезно је тестирати утицај на мождане механизме награђивања и задовољства зависних својстава високо пријатне хране.
Конзумирање сахарозе повезано је са гојазношћу, а сахароза се све више сматра зависном супстанцом5. Нека се открића подударају са овом тврдњом због потешкоћа у одвајању конзумације хране која се не прија на хедонске реакције на храну, те у одређивању зависног састојка у прерађеној храни, као и због различитих механизама помоћу којих храна мијења мождану струју природним путевима6. Ипак, у специфичним контекстима, унос сахарозе потиче награду и жудњу, упоредиву по величини са оним који изазивају лекови зависности, који доводе до прекомерне конзумације и евентуалне гојазности.6,7.
Глад је повезан са „жељом“ која је уско повезана са ефектима допаминергичке неуротрансмисије у бројним околностима награђивања8, али остаје нејасно како се деловање допамина (ДА) модулира као одговор на компулзивно једење. Конзумирање укусне хране повезано је са „вољењем“, посредованим пре свега ендогеним опиоидним системом, посебно µ-опиоидним рецепторима (µОР)9,10, што може промовисати превелику потрошњу када се дерегулише. У овом извештају тестирамо тврдњу да сахароза доводи до ослобађања опиоида и допамина који смањују доступност µОР и ДА Д2 / 3 рецептора. Доступност је индекс броја незаузетих рецептора који су доступни за везивање пратилаца и у принципу не прави разлику између попуњености лиганда и густине рецептора11.
Почетак компулзивног једења зависи од више фактора, а каузалне студије код људи покрећу етичка питања. Стога се већина студија фокусира на понашање код храњења код пацова12. Иако штакори имају „слатки зуб“, њихови хомеостатички механизми важни за дебљање, метаболизам и врсту накупљања масти значајно се разликују од оних код људи. Мини гиг из Готтингена је велика свеобухватна животиња са добро развијеним гиренцефалним мозгом, која се може сликати у довољној резолуцији. Добро дефинисани субкортикални и префронтални кортикални региони13 омогућавају директнији превод на функцију људског мозга. Овде за тестирање користимо сликање позитронско-емисијске томографије (ПЕТ) ин виво доступност µОР и ДА Д2 / 3 у моделу мини-свиња субкроничне изложености сахарози. У мањем узорку, истражили смо непосредне ефекте на попуњеност µОР након првог излагања сахарози. Коначно, тестирали смо однос између промена расположивости рецептора за два трагача.
Резултати
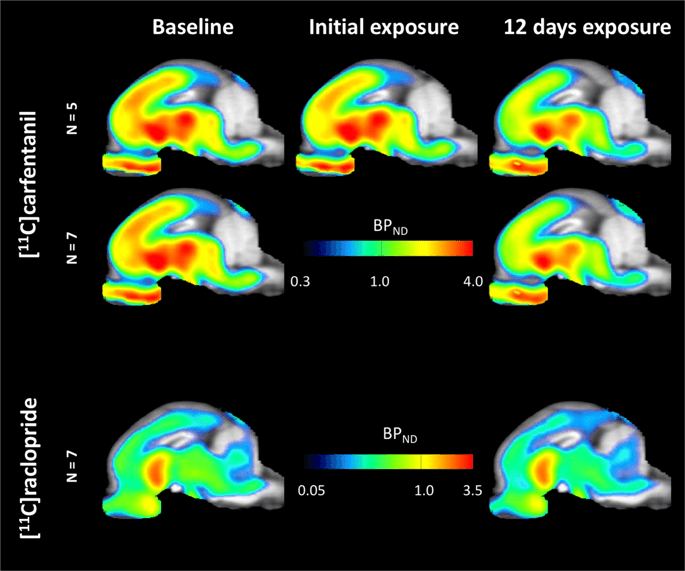
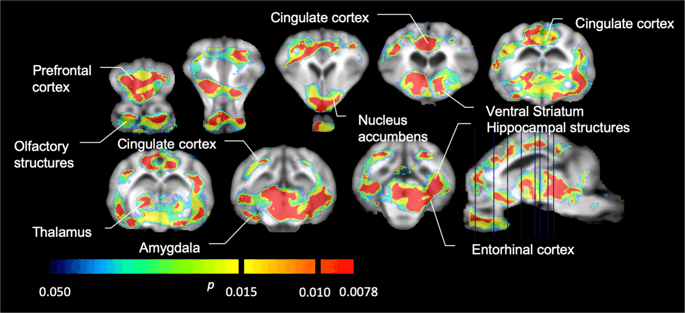
Просечне параметричке мапе од [11Ц] карфентанил и [11Ц] потенцијал везања раклоприда (БП)ND) приказани су на Сл. 1. Анализирати промјене које су се догодиле након прве изложености сахарози у пет минипирића у односу на почетну вриједност и један дан након 12th приступ сахарози у седам минипири у поређењу са основном линијом, користили смо теорију пермутације и нерегионално ограничену анализу целог мозга, преферирани метод за узорке ове величине14.
Просечан потенцијал који се не може заменити на вокселе (БП)ND) мапе наложене на МРИ слике у сагиталном погледу. Подаци су представљени за [11Ц] карфентанил БПND од 5 мини-свиња снимљених на почетној линији, након почетне изложености сахарози и након 12 дана излагања сахарози (горњи ред). [11Ц] карфентанил БПND од свих 7 мини-свиња снимљених у почетној линији и након 12 дана приступа сахарози, представљени су у средњем реду. [11Ц] рацлоприд БПND од свих 7 мини-свиња снимљених на почетној линији и након 12 дана приступа сахарози, приказани су у доњем реду. Имајте на уму да је скала боја експоненцијална за истицање [11Ц] рацлоприд БПND у екстрастријаталним регионима.
Почетна изложеност сахарози
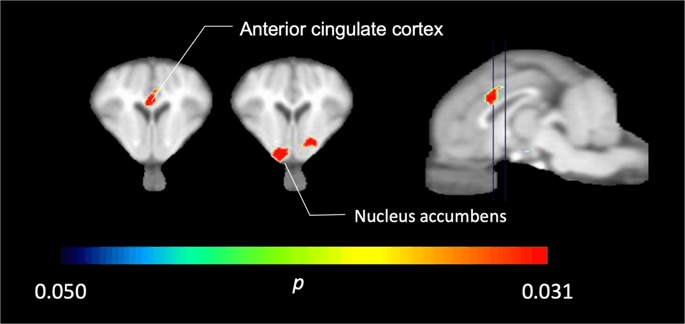
У пет мини-свиња снимљених са [11Ц] карфентанил на почетку и одмах након прве изложености сахарози, открили смо значајно смањено везивање пратилаца у кортексу предњег цингулата и нуклеусу као одговор на сахарозу, приказано у боји на Сл. 2, што указује на п <0.05. Открили смо чак 14% смањеног везивања трагова у обе области у поређењу са основном линијом.
Значајна смањења у [11Ц] карфентанил БПND после првог излагања води сахарози у поређењу са почетном вриједности (н = 5). Само воксели са значајним (p Смањења <0.05) приказана су као обојена подручја пројектована на Т1 пондерисане резове магнетне резонанце на нивоу предњег цингулативног кортекса (лево) и нуцлеус аццумбенс (средина) из стереотаксичног атласа минипиг мозга. Имајте на уму да је максимални ниво значајности који се може постићи са 5 животиња износи 2-КСНУМКС ≈ 0.031 (види траку са бојама). Подаци су представљени на короналним пресецима мозга свиње на нивоима наведеним на сагиталној слици (десно).
12 дана приступа сахарози
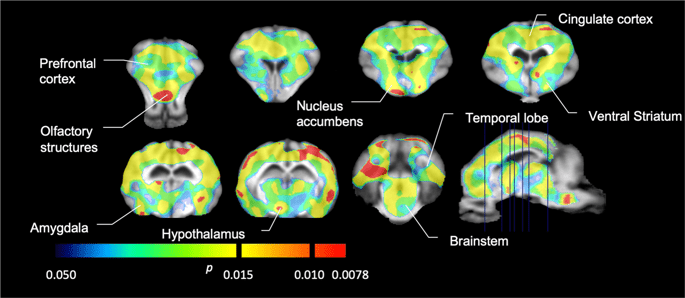
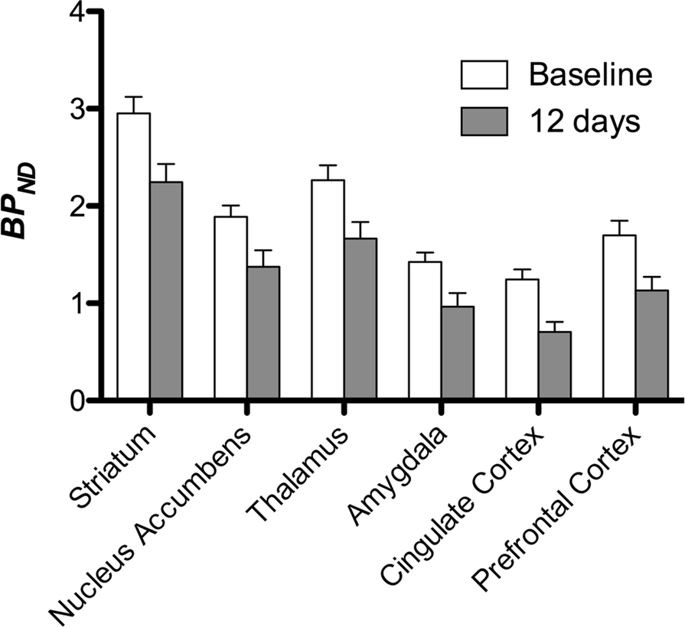
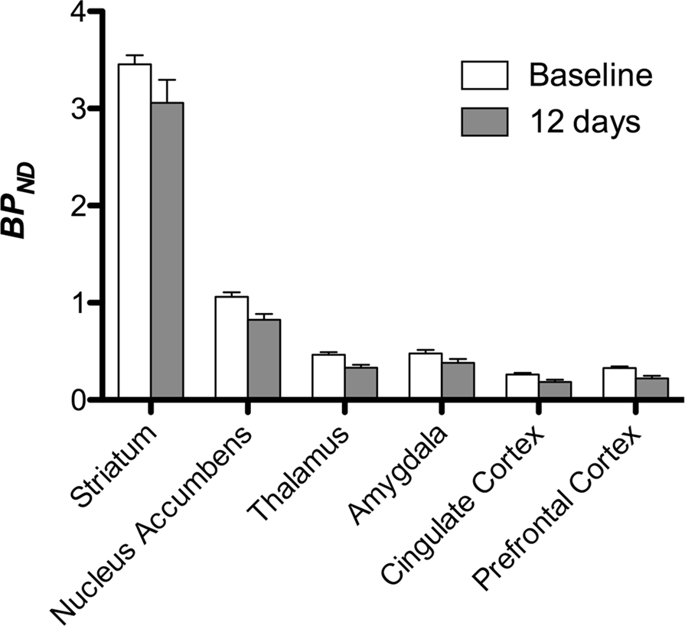
Затим смо извршили анализу седам мини-свиња снимљених са [11Ц] карфентанил на почетку и након 12 дана приступа сахарози и утврђено је значајно смањено везивање пратилаца у животињама изложеним сахарози у поређењу са почетном вриједности. Најизраженије регије су приказане црвеном бојом на Сл. 3 (п <0.01) и укључују делове олфакторних структура, нуцлеус аццумбенс / вентрал стриатум и темпорални кортекс / режањ, праћени областима приказаним жутом бојом (п <0.015) која су обухватала делове префронталног кортекса, цингуларног кортекса, амигдале и можданог стабла . Да би се добио БПND вриједности и процијенили промене, извршили смо регионалну анализу и добили средње вриједности у свакој регији на почетку и након потрошње сахарозе (Сл. 4).
Значајна смањења у [11Ц] потенцијал везања карфентанила (БП)ND) између основне вриједности и након 12 дана излагања води сахарозе (н = 7). Вокелс са значајним (p Смањења <0.05) приказана су као обојена подручја која се пројектују на Т1 пондерисани МРИ резови из стереотаксичног атласа мозга минипиг. Подаци су представљени на короналним деловима мозга на нивоима назначеним на сагиталној слици (доле десно). Имајте на уму да је максимални ниво значајности који се може постићи са 7 животиња 2-КСНУМКС ≈ 0.0078 (види траку са бојама).
Користили смо [11Ц] раклоприд као трагач за ДА Д2 / 3 рецепторе у стријаталним и екстрастријаталним регијама мозга код минипирића на почетку и након 12 дана приступа сахарози (Сл. 1). Открили смо смањено везивање трагача код животиња изложених сахарози, у поређењу са основним нивоом са највећим ефектима (п <0.01) на префронталном кортексу, нуцлеус аццумбенс / вентрал стриатум, цингулате цортек, амигдала, таламус, месенцепхалон, хипокампална подручја и олфакторна подручја (Шипак. 5). Подаци из регионалне анализе приказани су на Сл. 6.
Значајна смањења у [11Ц] потенцијал везања раклоприда (БП)ND) између основне вриједности и након 12 дана излагања води сахарозе (н = 7). Вокелс са значајним (p Смањења <0.05) приказана су као обојена подручја која се пројектују на Т1 пондерисани МРИ резови из стереотаксичног атласа мозга минипиг. Подаци су представљени на короналним пресецима свињског мозга на нивоима назначеним на сагиталној слици (доле десно). Имајте на уму да је максимални ниво значајности који се може постићи са 7 животиња 2-КСНУМКС ≈ 0.0078 (види траку са бојама).
Корелације између [11Ц] рацлоприд и11Ц] карфентанил податке
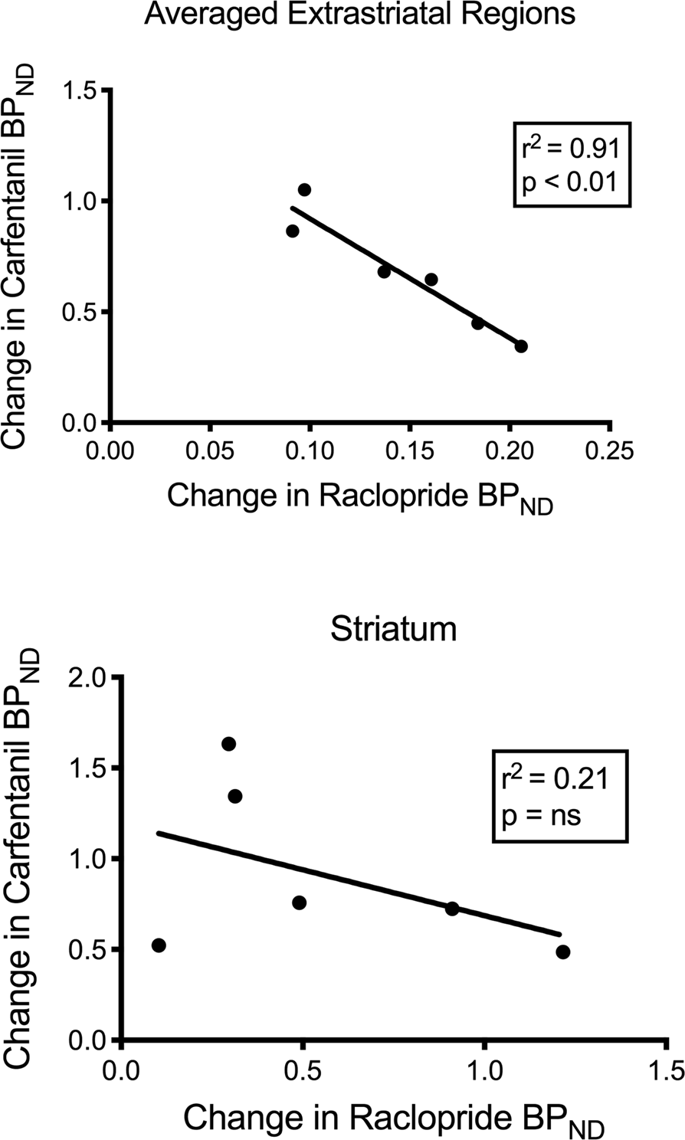
Тестирали смо потенцијалну повезаност између [11Ц] рацлоприд и11Ц] карфентанил вредности БПND у стријаталним и нестријалним регионима у минипигама у почетној фази и након 12 дана уноса сахарозе, без примећења асоцијација. Затим смо тестирали да ли је пад везања пратилаца корелиран, и упоређивали смо промене БПND за [11Ц] раклоприд са променама БПND за [11Ц] карфентанил само у минипасема које имају нижи крвни удиоND оба трагача након уноса сахарозе (н = 6). Пронашли смо значајне негативне корелације у просечном екстрастријалу (р2 = 0.91, п <0.01), али не и у стриаталним регионима (сл. 7).
Корелације између пре минус минус одбитка од [11Ц] рацлоприд и11Ц] потенцијали за везивање карфентанила (БП)ND) код минипирића са смањеним везивањем пратилаца након уноса сахарозе (н = 6). Приказани су подаци из просечних екстрастријаталних региона (врх) и стриатум (дно). Коефицијент одређивања (р2) и п вриједности су приказане за сваки граф.
Дискусија
Утврдили смо ефекте опетованог повременог приступа сахарозе на неуротрансмисију опиоида и ДА у мозгу сисара. Лонгитудинал ин виво ПЕТ снимање µОР и ДА Д2 / 3 рецептора показало је смањену доступност рецептора у читавом кругу награђивања, укључујући језгро језгра, префронтални кортекс и кору предњег цингулата. Резултати јасно показују да сахароза утиче на механизме награђивања на сличан начин као и злоупотреба дрога.
Познато је да унос сахарозе као пријатне супстанце ослобађа ДА и изазива зависност код глодара15, са сахарозом се показало да је још пријатнија од кокаина код глодара у одређеним контекстима. Тако глодари интензивно раде на добијању сахарозе од кокаина, чак и ако нема недостатка хране5. Међутим, ефекти сахарозе су регулисани и хомеостатским системом и хедонским наградним круговима16,17 који могу посредовати у разлици између нутритивних и хедонских аспеката деловања сахарозе18. Одлучили смо се за сат времена дневно како бисмо промовисали „бингинг“, јер су претходне студије на пацовима откриле већи унос током првог сата дневног приступа у повременом распореду15,19. Студије понашања уноса хране често циљају животиње са ограниченом храном, али дизајн не мора нужно одражавати исте неуронске механизме који су активни у претилости. Свиње у овој студији нису биле ограничене храном и биле су храњене уобичајеним количинама своје уобичајене исхране, осим приступа сахарози.
Опиоидни рецептори (ОР) су широко експримирани у мозгу, тачније у структурама за које се зна да модулирају процесе једења и награђивања20. Показало се да су ОР важне у користима кокаина који награђују и понављају21,22,23,24. Промене у везивању такође су повезане са хомеостатским реакцијама на јело и ужитком повезаним са укусном храном25. Конкретно, „вољење“ хране повезано је са ендогеним опиоидним системом, посебно µОР9,10 у љусци језгре језгре и вентралном палидуму26. Инфузија агониста µОР-а у различите делове нуклеусног језгра и вентрални палидум снажно појачава „симпатично“ понашање, укључујући избочење језика и лизање шапе, након повећаног пријатног уноса хране27,28,29. Даљњи докази за опиоидну сигнализацију у обради хедонске регулације потичу од антагониста µОР-а који смањују потрошњу укусног хлеба у оба по вољи- животиње са ограниченом исхраном и храном, али са ограниченим ефектом на унос стандардних пелета који се не могу пријати30,31. У људи, антагонисти µОР-а смањују краткотрајни унос хране и смањују пријатност хране која се прија32,33,34. Опиоидна сигнализација у базолатералној амигдали такође доприноси храни „која жели“ модулацијом тражења награде и подстицајне вредности хране35.
Са [11Ц] карфентанилом, добили смо слике везивања пратилаца које је осетљиво и на ниво µОР и на ослобађање ендогених опиоида од мозга36,37. Открили смо тренутни губитак доступности µОР у областима нуклеуса нуклеуса и предњем цингулату кортекса, специфичним деловима мозга наградног пута, након почетне конзумације сахарозе од пет минипирића, што је у складу са ослобађањем ендогеног опиоида. Претходне студије су показале да храна која се може слагати може довести до осећаја угоде38 стимулишући ослобађање опиоида. Након 12 дана приступа сахарози, приметили смо смањен [11Ц] везивање карфентанила, које има неколико могућих објашњења39 укључујући ендогено ослобађање опиоида и везивање за μОР, интернализација µОР као резултат повећаног везања опиоида и повећану активацију рецептора ДА Д2 / 3 што доводи до хетеролошке десензибилизације µОР40.
У прилог садашњим налазима, [11Ц] карфентанил студије пацијената са булимијом41гојазност42,43,44и поремећај једења45, показују смањену доступност рецептора. Међутим, ово су хронична стања док су минипири примали сахарозу само 12 дана. У студији акутног понашања храњења код здравих мушкараца, храњење је довело до снажног и широко распрострањеног ендогеног церебралног ослобађања опиоида, како у присуству тако и у одсуству хедоније, што сугерише да отпуштање опиоида одражава метаболичке и хомеостатске, као и хедонске реакције25. Ова студија, заједно са другом која је сликала пацијенте после течног оброка са укусом чоколаде44, директно је релевантан за акутно испитивање пет минипирића после прве изложености сахарози, али се разликује од студије субкроничне изложености сахарози током 12 дана, где смањена доступност рецептора вероватније одражава поновљену прекомерну стимулацију и истовремено сурегулацију µОР.
Префронтални кортекс важан је у одлучивању и приписивању вредности предметима, те стога µОР у префронталном кортексу може бити одговоран за измењену процену храњивости хране, која може повећати потенцијал зависности од хране. Открили смо смањено везивање у префронталном кортексу, у складу са претходним студијама које показују да исхрана са високим удјелом масти смањује ниво мОРНА µОР у префронталном кортексу46 и да инфузија ђОР агониста у префронталном кортексу повећава унос слатке хране47. Међутим, поново се поставља питање да ли је исхрана са високим удјелом масти хроничније стање које вероватније посредује доњу регулацију рецептора, у поређењу са краћим временским дизајном храњења сахарозом, сугерирајући продужено ослобађање ендогених опиоида који избацује трацер карфентанил везан на µОР , чак и након 12 дана сахарозе.
ДА је био умешан у награде и од дроге и од понашања. Откривено је да хронична употреба кокаина инхибира ДА сигнализацију48. Ниво рецептора ДА Д1 и Д2 / 3 је измењен никотином у мозгу свиње49и код примата који нису људи са анамнезом злоупотребе кокаина50, у складу са смањењем регулације Д2 / 3 рецептора у мозгу овисника о људском кокаину51,52. Што се тиче злоупотребе лекова, показало се да сахароза појачава ДА Д1 рецепторе19 и повећати ДА издање53, појачавајући улогу ДА у „жељи“ у односу на укусну храну. Претходне ПЕТ студије су показале смањење расположивости рецептора ДА Д2 / 3 у стријали код морбидне гојазности у односу на просечну тежину54,55, сличне величине као смањење пацијената зависника од дрога56и код животиња са моделима гојазности57. У истраживањима на глодарима, оборење Д2 / 3 рецептора у стриатуму промовише развој компулзивног тражења хране код пацова који имају приступ укусној храни57.
Наша запажања о смањеној доступности Д2 / 3 рецептора за свиње могу указивати на повећане нивое ДА као одговор на потицајну моћ повезаност са уносом сахарозе, јер се ДА ослобађа као део жеље за злоупотребом дрога и других пријатних активности52,58,59,60. Пошто су свиње анестезиране током сликања и нису примиле сахарозу у року од 24 сата, смањени Д2 / 3 БПND вероватније одражава смањење броја рецептора као одговор на продужено повећање отпуштања ДА у сваком од 12 дана приступа сахарози. Смањење може повисити прагове награде за мозак, повезане са смањеном регулацијом стријаталних ДА Д2 рецептора. Ово може објаснити повећану осетљивост на дроге злоупотребе уочене у претходним студијама пацова који су преједли сахарозу, што је довело до унакрсне преосетљивости на кокаин, хиперактивности након амфетамина у малим дозама, повећаног уноса алкохола када су се суздржавали од сахарозе и толеранције на аналгетске ефекте опијата6.
Претходна студија гојазности у минијатурди из Готтингена утврдила је смањени церебрални проток крви у језгри језгре, вентрално тегментално подручје (ВТА) и префронтални кортекс, са једном фотонском емисијском рачунарском томографијом (СПЕЦТ) мозга61. У складу са овим налазима, приметили смо смањено везање ДА Д2 / 3 у вентрофоребраин регији које садржи нуклеус аццумбенс и у префронталном кортексу. Изванћелијски ниво ДА се повећава троструко у језгри језгра након уноса сахарозе у слободно покретних пацова који су подвргнути микродиализи62. Код животиња које зависе од сахарозе, поновљени унос сахарозе може довести до ослобађања ДА из љуске језгре језгре63. Животиње које су храњене ограниченом исхраном са ограниченим приступом сахарози имале су ниже везивање рецептора ДА Д2 у шкољци језгре језгре и дорзални стриатум64. Ограничена дијета са високим удјелом масти и сахарозе може довести до продужене регулације мРНА рецептора Д1 и Д2 у језгри језгре65. Студија микродијализе о ефектима укусне хране открила је повећано ослобађање ДА у нуклеусним језграма и префронталном кортексу када се храна још увек сматра новом; Једном када су се пацови навикли на нову храну, повећано ослобађање је пригушено у нуклеусним језграма, али не у префронталном кортексу66. Различита осетљивост на хабитуацију и условљавање активности у две регије може да објасни веће повећање примећено у префронталном кортексу него у нуклеусним прилозима минипириша изложених истој укусној супстанци која је изгубила новост после дванаест дана. Међутим, како нисмо сликали минипиг са [11Ц] раклоприд после прве примене сахарозе, ово објашњење је спекулативно.
Префронтални кортекс модулира извршну функцију, доношење одлука и самоконтролу67. Нефункционални ДА-ов пренос у префронталном кортексу умањује модулацију обраде награда, што сугерише оштећену извршну функцију и вештине доношења одлука код гојазних појединаца68,69. Штавише, људско испитивање ПЕТ корелирало је смањени метаболизам фронталне коре и смањено стријатално везивање Д2 у претилости70. Овде налазимо смањену доступност Д2 / 3 рецептора у префронталном кортексу, укључујући орбитофронтални корте свиња изложених режиму сахарозе.
Допаминергички неурони ВТА шаљу пројекције у хипокампус и амигдалу, где подржавају навика попут понашања71 и посредују кодирање и проналажење кондиционирања на леку72,73 и храну храну74,75. Снимање људског мозга показало је активацију хипокамела као одговор на жељу за храном и дегустацију76. У складу са нашим налазима о смањеној доступности Д2 / 3 рецептора хипокампа и амигдалара као одговор на сахарозу, мапирање људског мозга са [18Ф] фаллиприд је показао отпуштање ДА изазваног кокаином у амигдали и хипокампусу77. У мозгу глодара, излагање кокаину изазивало је ослобађање ДА у амигдали78и промене нивоа амигдале ДА утицале су на понашање које тражи кокаин79.
У истраживању гојазних појединаца, веза између раздвојености Д2 / 3 и μОР, за које се зна да постоје у стријаталним регионима мршавих јединки, поремећена је у вентралном стриатуму80. Упоредили смо вредности БПND два тражила за тестирање да ли су подаци репродуковали овај ефекат. За разлику од мршавих људи, садашњи мозак свиња није имао повезаност између вредности БПND два трагача, на почетку или након излагања сахарози. Затим смо тестирали да ли ће животиње са највећим падом везивања тракалског раклоприда такође имати највеће опадање везивања трацер карфентанила, али уместо тога пронашли смо негативну повезаност у просечним екстрастријаталним регионима, сугеришући да животиње са највећом променом потенцијала везивања Трацер-раклоприд је имао најмању промену потенцијала везивања трацер карфентанила. Инверзни однос измена указује да су ефекти уноса сахарозе на расположивост одговарајућих рецептора регулисани у супротним смеровима. Познато је да прекомерно конзумирање укусне хране или лекова може да се покрене жељом или вољењем, или обоје60,81. Могуће је да величина жеља вођених допамином негира величину допадљивости коју изазивају опиоиди, или обрнуто. Недавни докази указују на улоге ГАБА-еA рецептори у ВТА и холинергички терминали у стриатуму и евентуално кортекси који делују као прекидачи између механизама опиоидног деловања зависних од допамина и независних допамина82,83 што може објаснити реципроцитет ефеката допамина и опиоида у екстрактриаталним регионима свиња који су овде одређени.
Недостатак ПЕТ-а, такође код релативно великих животиња, је ограничена просторна резолуција томографије која утиче на резултате малих регија мозга који су укључени у понашање повезано са храном. Међутим, и поред ове забринутости, [11Ц] раклопридно везивање раније је забележено и у стријаталном и екстрастријаталном региону84,85,86,87. Употреба [11Ц] раклоприд за обележавање исте врсте рецептора не изазива забринутост због потенцијалних разлика у афинитету које могу утицати на употребу одвојених трагача за исте рецепторе у различитим регионима. Недавне студије укључују записе о екстрастријаталном везивању [11Ц] раклоприд. Алакуртти сар. пронађена је добра репродуктивност мера везивања стријаталног раклоприда у стриатуму, са само добром до умереном обновљивошћу у кортексу85. У каснијој студији, Свенссон сар. разговарали о неколико питања која утичу на употребу [11Ц] раклоприд као маркер екстрастриаталних Д2 / 3 рецептора у истраживању здравих људи, укључујући слабу репродуктивност кортекса и ограничен пад екстрастријаталног везивања у фронталном кортексу као одговор на средство за блокирање Д2 / 388. Поређења тестова-поновног тестирања открила су варијабилности од 4–7% у стриатуму и 13–59% у кортикалним регионима, али време између прегледа износило је 20 дана, за разлику од информативнијих 1-2 дана већине студија. Бројни фактори из живота тих субјеката можда су имали времена да утичу на налазе. Заиста, овде показујемо да је само додавање конзумације сахарозе у јутарњу рутину током 12 дана могло утицати на мере везивања добијене две недеље касније. Остали фактори као што су играње видео игара, куповина, улазак у нове романтичне везе и сексуална активност, употреба дрога или промена исхране и вежбања могу утицати на екстрастријаталне нивое допамина са потенцијалом за велике варијације сетова података. Тренутна студија у мини-свињама увела је добро контролисан сет с тим да је једина варијабла одсуство или присуство сахарозе у исхрани. У том контексту, подаци од седам животиња имали су довољно малу варијабилност у релевантним екстрастријаталним регионима да идентификују статистички значајно смањење везања као одговора на сахарозу.
Ограничење тренутне студије је употреба анестетика који су потребни да се осигура непокретност током ин виво снимање животиња. Ефекти специфичних анестетика и њихове интеракције са лековима или друге интервенције могу да ометају везивање радиолиганда89,90. Кетамин је анти-глутаматергички лек са брзим антидепресивима у субанестетичким дозама91,92,93, који не смањују стријатално [11Ц] везивање раклоприда код људи94. Ипак, откривено је да С-кетамин смањује везујући распон рецептора допамина Д2 / 3 у стриатуму свесних примата који нису човечан95. Изофлуран је уобичајени анестетик у животињском ПЕТ-у. У претходним студијама открили смо стријатално нагомилавање [11Ц] СЦХ23390, радиолиганд рецептора допамина Д1 ће бити значајно већи код минипири анестезираних исофлураном, а не пропофолом, што сугерише подложност допаминергичкој неуротрансмисији на ефекте анестезије96. У тренутној студији, све мини-свиње су сликане на обе временске тачке под претплатом кетамина и анестезијом изофлурана, чиме су поређења важеће.
Zakljucak
Прекомерна конзумација хране која се може окусити може узроковати и постати последица зависности која има директне последице по здравље због гојазности. Тестирали смо тврдњу да опиоиди и допамин посредују награде, важне за опстанак и злоупотребу дрога. Мини-свиње са испрекиданим приступом раствору сахарозе 12 узастопних дана показале су смањену доступност допамина Д2 / 3 и µ-опиоидних рецептора у стријаталним и екстрастријаталним регијама мозга, имплицирајући да храна са високом концентрацијом сахарозе утиче на структуру награђивања мозга на начине сличне онима примећенима код зависних лекова се конзумирају. Почетна појединачна изложеност сахарози била је конзистентна са ослобађањем опиоида у регионима мозга који су награђивани. Промјене расположивости опиоида и допамина објашњавају зависни потенцијал сахарозе коју трошимо у вишку.
Материјал и метод
Животињска етика
Ову студију је одобрила и регулирала Данска инспекција за експерименте на животињама и сви експерименти су изведени у складу са директивом 2010/63 / ЕУ Европског парламента и Савета о заштити животиња које се користе у научне сврхе и смерницама АРРИВЕ. Користили смо седам женки мини гиг Готтинген (Еллегаард, Далмосе, Данска). Минипигијеви су били храњени пелетом (6 дЛ, 2 пута дневно, Специјалне услуге прехране, Архус, Данска) са доступном водом из славине по вољи. Температура околине је била 20–22 ° Ц, релативна влажност ваздуха 50–55%, а ваздух се мењао осам пута сваког сата.
Испрекидана потрошња сахарозе
Снимили смо седам минипипа са [11Ц] рацлоприд и11Ц] карфентанил на почетку, и поново један дан након 12 узастопних дана излагања сахарозној води. Излагање сахарози састојало се од једног сата приступа сахарози (сахароза, Дансуккер, Копенхаген, Данска) (500 грама сахарозе у 2 литре воде), током 12-дневног периода. Забележена је количина уноса сахарозе и све мини-свиње су дневно конзумирале 2 литре. Такође смо снимили пет истих мини-слика са [11Ц] карфентанил, 30 минута након првог приступа сахарози, како би се проучило акутно ослобађање опиоида.
Мини свиње су у просеку добиле 13.6% телесне тежине са 25.4 кг (± 0.73 СЕМ) на почетку до 28.9 кг (± 0.69 СЕМ) након 12-дневног излагања сахарози, што је било значајно веће (једнострани т-тест, п < 0.001) од повећања уочених у узорку контролних мини-свиња добијених у претходним студијама, где су се пондери повећавали у просеку за само 4.9%, током истог развојног периода.
ПЕТ Имагинг мозга
Преко ноћи смо постили свиње са слободним приступом води. Ми смо претходно лечили и анестезирали мини-свиње како је претходно описано97 и смештали их у леђа у ПЕТ / ЦТ уређај (Сиеменс Биограпх 64 Труепоинт ПЕТ). Обавили смо ЦТ са малим дозама пре сваког прикупљања ПЕТ ради анатомске дефиниције и корекције пригушења ПЕТ података о емисији. Интравенски смо давали [11Ц] раклоприд на почетној основи (360 ± 18 МБк, специфична активност 77 ± 76 ГБк / μмол, убризгана маса 0.12 ± 0.08 µг / кг) и након 12 дана сахарозе (374 ± 54 МБк, специфична активност 127 ± 85 ГБк / μмол, убризгана маса 0.06 ± 0.05 µг / кг) и [11Ц] карфентанил на почетној основи (377 ± 43 МБк, специфична активност 311 ± 195 ГБк / μмол, убризгана маса 0.03 ± 0.02 µг / кг) и након 12 дана сахарозе (337 ± 71 МБк, специфична активност 177 ± 157 ГБк / μмол, убризгана маса 0.06 ± 0.08 µг / кг) у ушну вену, у 10 мЛ физиолошког раствора, током првог минута 90-минутног скенирања. Реконструисали смо ПЕТ податке користећи ТруеКс 3Д ОСЕМ (3 итерације, 21 подскуп), матрицу 256 × 256 × 109 и Гауссов филтер 2 мм, користећи временску структуру од 5 × 60, 3 × 300, 4 × 600 , 2 × 900 секунди (укупно 14 кадрова, 90 минута). На почетку и након 12 дана сахарозе, мини-свиње су снимљене са обе трагачице убризганим у размаку од најмање 100 минута, због полуживота [11Ц] ПЕТ трагачи. По завршетку последњег сесија ПЕТ-а, еутаназирали смо мини-свиње под дубоком анестезијом интравенским предозирањем пентобарбитала (100 мг / кг).
Квантитативне анализе и статистике
Извели смо кораке претходне обраде користећи ПМОД 3.7 (ПМОД Тецхнологиес Лтд, Цирих, Швајцарска). Да бисмо дефинисали параметре стереотактичке трансформације из ПЕТ просечних слика, користили смо предлошке за лиганде. На одговарајућу динамичку временску серију ПЕТ применили смо генерисане матрице трансформације и деформациона поља. Генерисали смо параметричне слике [11Ц] потенцијал везања раклоприда (БП)ND) помоћу мултилинеарног референтног ткива методом Ицхисе-а и сарадника98. Направили смо по мери направљену маску мозга која је искључила вермис да би се током времена постигла радиоактивност можданог ткива у подручју занемарљиве густине рецептора ДА Д2 / 3. Генерисали смо параметричне слике [11Ц] карфентанил употребом примене Логан модела референтног ткива99,100 са т * = 30 мин. Студије [11Ц] Везање карфентанила у људском мозгу користило је окципитални кортекс као референтну област36; међутим, код свиње, према кривуљи временске активности, неподношљиво везивање било је ниже у мождану него у окципиталном кортексу, у складу са налазима студије ауторадиографије пацова101. Стога смо изабрали мозак као референтну регију у тренутној студији.
Статистичка анализа
Мапе смо подвргли анализи воксела помоћу статистичког непараметричког мапирања (СнПМ в13.01, http://warwick.ac.uk/snpm) СПМ алатни оквир који користи непараметарску теорију пермутације да би пружио оквир за статистички закључак, приступ за који се показало да добро функционише на малим узорцима због строге контроле лажних позитивних резултата14 и наноси се као што је претходно описано102. Стручњак за неуроанатомију свиња (ДО) упоредио је резултирајуће слике са нивоом значајности од 5% са атлантским атрибутом минијатуре Готтинген високе резолуције103,104 за дефинисање и обележавање региона смањеног ДА Д2 / 3 и µОР БПND од основне до пост-сахарозне кондиције. Затим смо урадили анализу региона од интереса (РОИ) како бисмо извукли БПND вредности специфичних региона за које је утврђено да су занимљиве на основу анализе СнПМ, укључујући стриатум, нуклеус ацумбенс, таламус, амигдала, цингулатни кортекс и префронтални кортекс. Нису изведене додатне статистике за РОИ анализу, јер је за ове регије већ откривено да су значајне користећи СнПМ.
Референце
- 1.
Смитх, С. и Херон, А. Дијабетес и гојазност: епидемије близанаца. Нат Мед 12, КСНУМКС – КСНУМКС, https://doi.org/10.1038/nm0106-75 (КСНУМКС).
- 2.
Флегал, КМ, Царролл, МД, Огден, ЦЛ & Цуртин, ЛР Преваленца и трендови гојазности код одраслих Американаца, 1999–2008. ЈАМА 303, КСНУМКС – КСНУМКС, https://doi.org/10.1001/jama.2009.2014 (КСНУМКС).
- 3.
Давис, Калифорнија сар. Допамин за „желе“ и опиоиди за „укус“: поређење гојазних одраслих са и без преједања. Гојазност (Силвер Спринг) 17, КСНУМКС – КСНУМКС, https://doi.org/10.1038/oby.2009.52 (КСНУМКС).
- 4.
Древновски, А. Гојазност и окружење хране: густина прехрамбене енергије и трошкови исхране. Амерички часопис за превентивну медицину 27, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.amepre.2004.06.011 (КСНУМКС).
- 5.
Леноир, М., Серре, Ф., Цантин, Л. & Ахмед, СХ Интензивна сласт надмашује награду од кокаина. ПЛоС ОНЕ 2, е698, https://doi.org/10.1371/journal.pone.0000698 (КСНУМКС).
- 6.
Ахмед, С., Авена, НМ, Берридге, КЦ, Геархардт, А. и Гуиллем, К. Ин Неурознаност у 21. веку (ед. Пхафф, ДВ) (Спрингер, 2012).
- 7.
Авена, НМ, Голд, ЈА, Кролл, Ц. и Голд, МС Даљи развој у неуробиологији хране и зависности: ажурирање стања науке. Исхрана 28, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.nut.2011.11.002 (КСНУМКС).
- 8.
Леитон, М. Ин Задовољства мозга (ур. Крингелбацх, МЛ & Берридге, КЦ) (Окфорд Университи Пресс, 2010).
- 9.
Натхан, ПЈ & Буллморе, ЕТ Од хедонике укуса до мотивацијског нагона: централни му-опиоидни рецептори и понашање преједања. Инт Ј Неуропсицхопхармацол 12, КСНУМКС – КСНУМКС, https://doi.org/10.1017/S146114570900039X (КСНУМКС).
- КСНУМКС.
Берридге, КЦ Награда за храну: мождани супстрати жеље и допадљивости. Неуросциенце и биобехавиорал ревиевс 20, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Гједде, А., Вонг, ДФ, Роса-Нето, П. & Цумминг, П. Мапирање неурорецептора на делу: о дефинисању и тумачењу везивних потенцијала након 20 година напретка. Инт Рев Неуробиол 63, КСНУМКС – КСНУМКС, https://doi.org/10.1016/S0074-7742(05)63001-2 (КСНУМКС).
- КСНУМКС.
Авена, НМ, Боцарсли, МЕ & Хоебел, БГ Животињски модели преливања шећера и масти: веза са зависношћу од хране и повећаном телесном тежином. Метод Мол Биол 829, КСНУМКС – КСНУМКС, https://doi.org/10.1007/978-1-61779-458-2_23 (КСНУМКС).
- КСНУМКС.
Јелсинг, Ј. сар. Префронтални кортекс у мозгу минијатуре у Готтингену дефинисан критеријумима неуронске пројекције и цитоархитектуром. Браин Рес Булл 70, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.brainresbull.2006.06.009 (КСНУМКС).
- КСНУМКС.
Ницхолс, ТЕ & Холмес, АП Непараметријски тестови пермутације за функционално неуроимагинг: пример са примерима. Хум Браин Мапп 15, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Авена, НМ, Рада, П. & Хоебел, БГ Докази о зависности од шећера: бихевиорални и неурохемијски ефекти повременог, прекомерног уноса шећера. Неуросциенце и биобехавиорал ревиевс 32, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neubiorev.2007.04.019 (КСНУМКС).
- КСНУМКС.
Алонсо-Алонсо, М. сар. Систем награђивања хране: тренутне перспективе и будуће потребе истраживања. Нутр Рев 73, КСНУМКС – КСНУМКС, https://doi.org/10.1093/nutrit/nuv002 (КСНУМКС).
- КСНУМКС.
Фиглевицз, ДП, Беннетт-Јаи, ЈЛ, Киттлесон, С., Сиполс, АЈ & Завосх, А. Самоуправљање сахарозом и активација ЦНС-а код пацова. Ам Ј Пхисиол Регул Интеграл Цомп 300, Р876–884, https://doi.org/10.1152/ajpregu.00655.2010 (КСНУМКС).
- КСНУМКС.
Теллез, ЛА сар. Одвојени кругови кодирају хедонске и храњиве вредности шећера. Натуре неуросциенце 19, КСНУМКС – КСНУМКС, https://doi.org/10.1038/nn.4224 (КСНУМКС).
- КСНУМКС.
Цолантуони, Ц. сар. Превелики унос шећера мења везивање за допамин и му-опиоидне рецепторе у мозгу. Неурорепорт 12, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Перт, ЦБ, Кухар, МЈ и Снидер, СХ Опијатни рецептор: ауторадиографска локализација у мозгу пацова. Проц Натл Ацад Сци УСА 73, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Содерман, АР и Унтервалд, ЕМ Награда за кокаин и хиперактивност пацова: места модулације му опиоидних рецептора. Неуронауке 154, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroscience.2008.04.063 (КСНУМКС).
- КСНУМКС.
Вард, СЈ, Мартин, ТЈ & Робертс, ДЦ Бета-фуналтрексамин утиче на самоуправљање кокаином код пацова који реагују на прогресивни распоред ојачања. Фармакологија, биохемија и понашање 75, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Сцхроедер, ЈА сар. Улога му опиоидних рецептора у активности изазваној кокаином, сензибилизацији и награђивању пацова. Псицхопхармацологи 195, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00213-007-0883-z (КСНУМКС).
- КСНУМКС.
Танг, КСЦ, МцФарланд, К., Цагле, С. и Каливас, ПВ Враћање индуковано кокаином захтева ендогену стимулацију му-опиоидних рецептора у вентралном палидуму. Јоурнал оф неуросциенце: званични дневник Друштва за неуронауку 25, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.0685-05.2005 (КСНУМКС).
- КСНУМКС.
Туулари, ЈЈ сар. Храњење ослобађа ендогене опиоиде у људи. Ј Неуросци 37, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.0976-17.2017 (КСНУМКС).
- КСНУМКС.
Смитх, КС & Берридге, КЦ Опиоидни лимбички круг за награду: интеракција између хедонских жаришта нуклеусног акумбена и вентралног палидума. Ј Неуросци 27, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.4205-06.2007 (КСНУМКС).
- КСНУМКС.
Пецина, С. и Берридге, КЦ Опиоидно место у љусци нуцлеус аццумбенс посредује у јелу и хедонском „наклоности“ храни: мапа заснована на микроињекционим перјаницама Фос. Браин Рес 863, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Зханг, М. и Келлеи, АЕ Унос раствора сахарина, соли и етанола повећава се инфузијом му опиоидног агониста у језгро акуменса. Псицхопхармацологи 159, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00213-001-0932-y (КСНУМКС).
- КСНУМКС.
Зханг, М., Госнелл, БА & Келлеи, АЕ Унос хране са високим садржајем масти селективно се појачава стимулацијом му опиоидних рецептора унутар језгра гомиле. Часопис за фармакологију и експерименталну терапију 285, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Левине, АС, Велдон, ДТ, Граце, М., Цлеари, ЈП & Биллингтон, ЦЈ Налоконе блокира тај део храњења вођен слатким укусом код пацова са ограниченом храном. Ам Ј Пхисиол 268, Р248–252 (1995).
- КСНУМКС.
Гласс, МЈ, Биллингтон, ЦЈ & Левине, АС Опиоиди и унос хране: распоређени функционални неуронски путеви? Неуропептидес 33, КСНУМКС – КСНУМКС, https://doi.org/10.1054/npep.1999.0050 (КСНУМКС).
- КСНУМКС.
Фантино, М., Хосотте, Ј. и Апфелбаум, М. Опиоидни антагонист, налтрексон, смањује склоност сахарози код људи. Ам Ј Пхисиол 251, Р91–96, https://doi.org/10.1152/ajpregu.1986.251.1.R91 (КСНУМКС).
- КСНУМКС.
Арбиси, ПА, Биллингтон, ЦЈ & Левине, АС Ефекат налтрексона на праг детекције укуса и препознавања. апетит 32, КСНУМКС – КСНУМКС, https://doi.org/10.1006/appe.1998.0217 (КСНУМКС).
- КСНУМКС.
Древновски, А., Крахн, ДД, Демитрацк, МА, Наирн, К. & Госнелл, БА Налоконе, блокатор опијата, смањује потрошњу слатке хране са високим уделом масти код гојазних и мршавих ждерача. Ам Ј Цлин Нутр 61, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Вассум, КМ, Остлунд, СБ, Маидмент, НТ и Баллеине, БВ Изразита опиоидна кола одређују укусност и пожељност награђивања догађаја. Проц Натл Ацад Сци УСА 106, КСНУМКС – КСНУМКС, https://doi.org/10.1073/pnas.0905874106 (КСНУМКС).
- КСНУМКС.
Цоласанти, А. сар. Ендогено ослобађање опиоида у систему награђивања људског мозга изазвано акутном администрацијом амфетамина. Биол Псицхиатри 72, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.biopsych.2012.01.027 (КСНУМКС).
- КСНУМКС.
Мицк, ја. сар. Ослобођење ендогеног опиоида изазваног амфетамином у људском мозгу откривено је [11Ц] карфентанил ПЕТ-ом: репликација у независној кохорти. Инт Ј Неуропсицхопхармацол, КСНУМКС – КСНУМКС, https://doi.org/10.1017/S1461145714000704 (КСНУМКС).
- КСНУМКС.
Иеоманс, МР & Граи, РВ Опиоидни пептиди и контрола ингестивног понашања код људи. Неуросциенце и биобехавиорал ревиевс 26, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Спренгер, Т., Бертхеле, А., Платзер, С., Боецкер, Х. & Толле, ТР Од чега научити ин виво опиоидергијско снимање мозга? Еур Ј Паин 9, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.ejpain.2004.07.010 (КСНУМКС).
- КСНУМКС.
Унтервалд, ЕМ & Цунтапаи, М. Допамин-опиоидне интеракције у стриатуму пацова: модулаторна улога допаминских Д1 рецептора у делта опиоидној рецептури посредованој трансдукцији сигнала. Неурофармакологија 39, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Бенцхериф, Б. сар. Регионално везивање му-опиоидног рецептора у изолацијском кортексу је смањено у булимији нервози и обрнуто је повезано са понашањем након поста. Часопис нуклеарне медицине: званично издање, Друштво за нуклеарну медицину 46, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Карлссон, ХК сар. Гојазност је повезана са смањеном доступношћу му-опиоидних, али непромењених Дпам рецептора у мозгу. Ј Неуросци 35, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.4744-14.2015 (КСНУМКС).
- КСНУМКС.
Карлссон, ХК сар. Губитак килограма након баријатријске операције нормализује мождане опиоидне рецепторе код морбидне гојазности. Мол Псицхиатри 21, КСНУМКС – КСНУМКС, https://doi.org/10.1038/mp.2015.153 (КСНУМКС).
- КСНУМКС.
Бургхардт, ПР, Ротхберг, АЕ, Дикхуис, КЕ, Бурант, ЦФ & Зубиета, ЈК Ендогени опиоидни механизми умешани су у гојазност и губитак тежине код људи. Ј Цлин Ендоцринол Метаб 100, КСНУМКС – КСНУМКС, https://doi.org/10.1210/jc.2015-1783 (КСНУМКС).
- КСНУМКС.
Мајури, Ј. сар. Допамин и опиоидна неуротрансмисија у бихејвиоралним зависностима: упоредна ПЕТ студија у патолошком коцкању и преједању. Неуропсицхопхармацологи 42, КСНУМКС – КСНУМКС, https://doi.org/10.1038/npp.2016.265 (КСНУМКС).
- КСНУМКС.
Вучетић, З., Киммел, Ј. и Реиес, ТМ Хронична дијета са високим садржајем масти покреће постнаталну епигенетску регулацију му-опиоидног рецептора у мозгу. Неуропсицхопхармацологи: званична публикација Америчког колеџа за неуропсихопармакологију 36, КСНУМКС – КСНУМКС, https://doi.org/10.1038/npp.2011.4 (КСНУМКС).
- КСНУМКС.
Мена, ЈД, Садегхиан, К. & Балдо, БА Индукција хиперфагије и уноса угљених хидрата стимулацијом му-опиоидних рецептора у ограниченим регионима фронталног кортекса. Јоурнал оф неуросциенце: званични дневник Друштва за неуронауку 31, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.2050-10.2011 (КСНУМКС).
- КСНУМКС.
Парк, К., Волков, НД, Пан, И. & Ду, Ц. Хронични кокаин пригушује допаминску сигнализацију током интоксикације кокаином и дебалансира Д1 у односу на сигнализацију Д2 рецептора. Јоурнал оф неуросциенце: званични дневник Друштва за неуронауку 33, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.1935-13.2013 (КСНУМКС).
- КСНУМКС.
Цумминг, П. сар. Утицај акутног никотина на хемодинамику и везивање [11Ц] раклоприда за допаминске Д2,3 рецепторе у свињском мозгу. НеуроИмаге 19, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Мооре, РЈ, Винсант, СЛ, Надер, МА, Поррино, Љ & Фриедман, ДП Ефекат само-администрације кокаина на допаминске Д2 рецепторе код резус мајмуна. Синапсе 30, 88–96, doi:10.1002/(SICI)1098-2396(199809)30:1<88::AID-SYN11>3.0.CO;2-L (1998).
- КСНУМКС.
Волков, НД сар. Знакови кокаина и допамина у дорзалном стриатуму: механизам жудње за зависношћу од кокаина. Јоурнал оф неуросциенце: званични дневник Друштва за неуронауку 26, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.1544-06.2006 (КСНУМКС).
- КСНУМКС.
Вонг, ДФ сар. Повећана попуњеност допаминских рецептора у људском стриатуму током жудње за кокаином. Неуропсицхопхармацологи 31, КСНУМКС – КСНУМКС, https://doi.org/10.1038/sj.npp.1301194 (КСНУМКС).
- КСНУМКС.
Хајнал, А., Смитх, ГП & Норгрен, Р. Орална стимулација сахарозе повећава акуменс допамин код пацова. Ам Ј Пхисиол Регул Интеграл Цомп 286, Р31–37, https://doi.org/10.1152/ajpregu.00282.2003 (КСНУМКС).
- КСНУМКС.
Волков, НД, Фовлер, ЈС, Ванг, ГЈ, Балер, Р. & Теланг, Ф. Улога слике допамина у злоупотреби дрога и зависности. Неурофармакологија 56(Суппл 1), 3–8, https://doi.org/10.1016/j.neuropharm.2008.05.022 (КСНУМКС).
- КСНУМКС.
Ванг, ГЈ сар. Мозак допамина и гојазност. Ланцета 357, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Ванг, ГЈ, Волков, НД, Тханос, ПК & Фовлер, ЈС Сличност између гојазности и зависности од дрога према процени неурофункционалног снимања: преглед концепта. Часопис за зависне болести 23, КСНУМКС – КСНУМКС, https://doi.org/10.1300/J069v23n03_04 (КСНУМКС).
- КСНУМКС.
Јохнсон, ПМ & Кенни, ПЈ Допамине Д2 рецептори у дисфункцији награђивања сличној зависности и компулзивном исхрани код гојазних пацова. Натуре неуросциенце 13, КСНУМКС – КСНУМКС, https://doi.org/10.1038/nn.2519 (КСНУМКС).
- КСНУМКС.
Берридге, КЦ & Крингелбацх, МЛ Афективна неуронаука задовољства: награда код људи и животиња. Псицхопхармацологи 199, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00213-008-1099-6 (КСНУМКС).
- КСНУМКС.
Берридге, КЦ и Крингелбацх, МЛ Системи задовољства у мозгу. Неурон 86, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuron.2015.02.018 (КСНУМКС).
- КСНУМКС.
Сцхултз, В. Предиктивни сигнал награђивања неурона допамина. Ј Неуропхисиол 80, КСНУМКС – КСНУМКС, https://doi.org/10.1152/jn.1998.80.1.1 (КСНУМКС).
- КСНУМКС.
Вал-Лаиллет, Д., Лаиец, С., Гуерин, С., Меурице, П. & Малберт, ЦХ Промене у активности мозга након гојазности изазване дијетом. Гојазност 19, КСНУМКС – КСНУМКС, https://doi.org/10.1038/oby.2010.292 (КСНУМКС).
- КСНУМКС.
Хајнал, А. и Норгрен, Р. Акумулира механизме допамина у уносу сахарозе. Браин Рес 904, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Рада, П., Авена, НМ & Хоебел, БГ Свакодневно уживање у шећеру у више наврата ослобађа допамин у овојници акумбена. Неуронауке 134, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroscience.2005.04.043 (КСНУМКС).
- КСНУМКС.
Белло, НТ, Луцас, ЛР & Хајнал, А. Поновљени приступ сахарози утиче на густину рецептора допамина Д2 у стриатуму. Неурорепорт 13, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Алсио, Ј. сар. Експресија гена рецептора допамина Д1 се смањује у језгри која се смањује након дуготрајне изложености укусној храни и разликује се у зависности од фенотипа гојазности изазваног исхраном код пацова. Неуронауке 171, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroscience.2010.09.046 (КСНУМКС).
- КСНУМКС.
Бассарео, В. и Ди Цхиара, Г. Диференцијални утицај механизама асоцијативног и неасоцијативног учења на одзив префронталног и акумбалног преноса допамина на подражаје храни код пацова храњених ад либитум. Ј Неуросци 17, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Волков, НД, Ванг, ГЈ, Томаси, Д. и Балер, РД Неуравнотежени неуронски кругови у зависности. Цурр Опин Неуробиол 23, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.conb.2013.01.002 (КСНУМКС).
- КСНУМКС.
Броган, А., Хевеи, Д. и Пигнатти, Р. Анорекиа, булимиа и гојазност: заједнички недостаци у доношењу одлука о задатку коцкања у Иови (ИГТ). Ј Инт Неуропсицхол Соц 16, КСНУМКС – КСНУМКС, https://doi.org/10.1017/S1355617710000354 (КСНУМКС).
- КСНУМКС.
Давис, Ц., Левитан, РД, Муглиа, П., Бевелл, Ц. & Кеннеди, ЈЛ Дефицит одлучивања и преједање: модел ризика за гојазност. Обес Рес 12, КСНУМКС – КСНУМКС, https://doi.org/10.1038/oby.2004.113 (КСНУМКС).
- КСНУМКС.
Волков, НД сар. Низак допамински стријатални Д2 рецептори повезани су са префронталним метаболизмом код претилих субјеката: могући фактори који доприносе. НеуроИмаге 42, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroimage.2008.06.002 (КСНУМКС).
- КСНУМКС.
Лингави, НВ & Баллеине, БВ Централно језгро амигдале комуницира са дорсолатералним стриатумом ради регулисања стицања навика. Ј Неуросци 32, КСНУМКС – КСНУМКС, https://doi.org/10.1523/JNEUROSCI.4806-11.2012 (КСНУМКС).
- КСНУМКС.
Грант, С. сар. Активирање меморијских кола током жељеног кокаина. Проц Натл Ацад Сци УСА 93, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Цхилдресс, АР сар. Лимбичка активација током жудње за кокаином изазваним цуром. Ам Ј Псицхиатри 156, КСНУМКС – КСНУМКС, https://doi.org/10.1176/ajp.156.1.11 (КСНУМКС).
- КСНУМКС.
Махлер, СВ и Берридге, КЦ Шта и када „желети“? Фокусирање подстицајне издвојености на шећер и пол засновано на амигдали. Псицхопхармацологи 221, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00213-011-2588-6 (КСНУМКС).
- КСНУМКС.
Кооб, ГФ & Волков, НД Неуробиологи оф аддицтион: а неуроцирцуитри аналисис. Ланцет Псицхиатри 3, КСНУМКС – КСНУМКС, https://doi.org/10.1016/S2215-0366(16)00104-8 (КСНУМКС).
- КСНУМКС.
Хаасе, Л., Церф-Дуцастел, Б. и Мурпхи, Ц. Активација кортекса као одговор на чисте стимулусе укуса током физиолошких стања глади и ситости. НеуроИмаге 44, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroimage.2008.09.044 (КСНУМКС).
- КСНУМКС.
Фотрос, А. сар. Ослобођење допамина изазваног кокаином у амигдали и хипокампусу: студија фалсприда високе резолуције ПЕТ [(1) (8) Ф] код учесника зависних од кокаина. Неуропсицхопхармацологи 38, КСНУМКС – КСНУМКС, https://doi.org/10.1038/npp.2013.77 (КСНУМКС).
- КСНУМКС.
Веисс, Ф. сар. Контрола понашања које тражи кокаин помоћу стимулисаних дрога код пацова: ефекти на опоравак угашених нивоа допамина који реагују на оперативне и ванћелијске допамине у амигдали и нуклеусу. Проц Натл Ацад Сци УСА 97, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Берглинд, ВЈ, Цасе, ЈМ, Паркер, МП, Фуцхс, РА & Сее, РЕ Дотамин Д1 или Д2 антагонизам рецептора унутар базолатералне амигдале различито мења стицање асоцијација кокаин-цуе неопходних за поновно успостављање тражења кокаина изазваног знаком. Неуронауке 137, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroscience.2005.08.064 (КСНУМКС).
- КСНУМКС.
Туоминен, Л. сар. Аберантна мезолимбичка допамин-опијатна интеракција у гојазности. НеуроИмаге 122, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.neuroimage.2015.08.001 (КСНУМКС).
- КСНУМКС.
Сцхултз, В. Бихевиорални допамински сигнали. Трендс Неуросци 30, КСНУМКС – КСНУМКС, https://doi.org/10.1016/j.tins.2007.03.007 (КСНУМКС).
- КСНУМКС.
Тинг, АКР и ван дер Коои, Д. Неуробиологија опијатске мотивације. Цолд Спринг Харб Перспецт Мед 2, https://doi.org/10.1101/cshperspect.a012096 (КСНУМКС).
- КСНУМКС.
Мамалигас, АА, Цаи, И. & Форд, ЦП Регулација никотинских и опиоидних рецептора путем посредовања стриаталних допаминских Д2 рецептора. Сци Реп 6, КСНУМКС, https://doi.org/10.1038/srep37834 (КСНУМКС).
- КСНУМКС.
Номура, И. сар. Смањивање расположивости рецептора допамина Д2 / 3 везано уз старење мерено са [Ц-11] раклопридом у нестријалним регионима људског мозга: Упоређивање четири поступка. НеуроИмаге 41, Т133 – Т133, https://doi.org/10.1016/j.neuroimage.2008.04.101 (КСНУМКС).
- КСНУМКС.
Алакуртти, К. сар. Дугорочна поузданост тест-поновног тестирања стријаталног и екстрастријаталног везања рецептора допамина Д2 / 3: студија са [(11) Ц] раклопридом и ПЕТ високе резолуције. Ј Цереб Проток крви Метаб 35, КСНУМКС – КСНУМКС, https://doi.org/10.1038/jcbfm.2015.53 (КСНУМКС).
- КСНУМКС.
Пиццини, П., Павесе, Н. & Броокс, ДЈ Ендогено ослобађање допамина након фармаколошких изазова код Паркинсонове болести. Анн Неурол 53, КСНУМКС – КСНУМКС, https://doi.org/10.1002/ana.10526 (КСНУМКС).
- КСНУМКС.
Савамото, Н. сар. Когнитивни дефицит и ослобађање стриато-фронталног допамина код Паркинсонове болести. Мозак 131, КСНУМКС – КСНУМКС, https://doi.org/10.1093/brain/awn054 (КСНУМКС).
- КСНУМКС.
Свенссон, ЈЕ сар. Важност и поузданост екстрастриаталног [(11) Ц] квантификације везивања раклоприда у живом људском мозгу. НеуроИмаге, КСНУМКС, https://doi.org/10.1016/j.neuroimage.2019.116143 (КСНУМКС).
- КСНУМКС.
Тсукада, Х. сар. Анестезија изофлураном појачава инхибиторне ефекте кокаина и ГБР12909 на транспортер допамина: ПЕТ студије у комбинацији са микродиализијом мозга мајмуна. Браин Рес 849, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Хассоун, В. сар. ПЕТ студија везивања [11Ц] раклоприда у стриатуму будне мачке: ефекти анестетика и улога церебралног протока крви. Европски часопис за нуклеарну медицину и молекуларно снимање 30, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00259-002-0904-4 (КСНУМКС).
- КСНУМКС.
Серафини, Г., Ховланд, РХ, Роведи, Ф., Гирарди, П. & Аморе, М. Улога кетамина у депресији резистентној на лечење: систематски преглед. Цурр Неуропхармацол 12, КСНУМКС – КСНУМКС, https://doi.org/10.2174/1570159X12666140619204251 (КСНУМКС).
- КСНУМКС.
Берман, РМ сар. Антидепресивно дејство кетамина код пацијената са депресијом. Биол Псицхиатри 47, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Бровне, ЦА и Луцки, И. Антидепресивни ефекти кетамина: механизми у основи брзо делујућих нових антидепресива. Фронт Пхармацол 4, КСНУМКС, https://doi.org/10.3389/fphar.2013.00161 (КСНУМКС).
- КСНУМКС.
Аалто, С. сар. Кетамин не смањује везивање стријаталних допаминских Д2 рецептора код човека. Псицхопхармацологи 164, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00213-002-1236-6 (КСНУМКС).
- КСНУМКС.
Хасхимото, К., Какиуцхи, Т., Охба, Х., Нисхииама, С. и Тсукада, Х. Смањење везивања допаминских Д2 / 3 рецептора у стриатуму након једнократне примене ескетамина, али не и Р-кетамина: ПЕТ проучавајте код свесних мајмуна. Еур Арцх Псицхиатри Цлин Неуросци 267, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00406-016-0692-7 (КСНУМКС).
- КСНУМКС.
Алструп, АК сар. Утицај анестезије и врста на пријем или везивање радиолиганда ин виво у минибигу Готтингена. БиоМед истраживање међународно 2013, КСНУМКС, https://doi.org/10.1155/2013/808713 (КСНУМКС).
- КСНУМКС.
Лиллетхоруп, ТП сар. Лонгитудинална моноаминергичка ПЕТ слика хроничне инхибиције протеасома код минипири. Сци Реп 8, КСНУМКС, https://doi.org/10.1038/s41598-018-34084-5 (КСНУМКС).
- КСНУМКС.
Ицхисе, М., Тоиама, Х., Иннис, РБ & Царсон, РЕ Стратегије за побољшање процене параметара неурорецептора линеарном регресионом анализом. Ј Цереб Проток крви Метаб 22, КСНУМКС – КСНУМКС, https://doi.org/10.1097/01.WCB.0000038000.34930.4E (КСНУМКС).
- КСНУМКС.
Логан, Ј. сар. Количински запремински расподјели без узорковања крви из графичке анализе ПЕТ података. Ј Цереб Проток крви Метаб 16, КСНУМКС – КСНУМКС, https://doi.org/10.1097/00004647-199609000-00008 (КСНУМКС).
- КСНУМКС.
Ендрес, ЦЈ, Бенцхериф, Б., Хилтон, Ј., Мадар, И. & Фрост, ЈЈ Квантификација можданих му-опиоидних рецептора са [11Ц] карфентанилом: методе референтног ткива. Нуцл Мед Биол 30, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Панксепп, Ј. и Бисхоп, П. Ауторадиографска мапа везивања (3Х) дипренорфина у мозгу пацова: ефекти социјалне интеракције. Браин Рес Булл 7, КСНУМКС – КСНУМКС (КСНУМКС).
- КСНУМКС.
Ландау, АМ сар. Електроконвулзивна стимулација различито утиче на [(11) Ц] МДЛ100,907 везивање за кортикалне и субкортикалне 5ХТ2А рецепторе у свињском мозгу. Ј Псицхопхармацол, КСНУМКС, https://doi.org/10.1177/0269881119836212 (КСНУМКС).
- КСНУМКС.
Бјаркам, ЦР, Глуд, АН, Орловски, Д., Соренсен, ЈЦХ & Паломеро-Галлагхер, Н. Тхе теленцепхалон оф тхе Готтинген минипиг, цитоарцхитецтуре анд кортицал сурфаце анатоми. Браин Струцт Фунцт 222, КСНУМКС – КСНУМКС, https://doi.org/10.1007/s00429-016-1327-5 (КСНУМКС).
- КСНУМКС.
Орловски, Д., Глуд, АН, Паломеро-Галлагхер, Н., Соренсен, ЈЦХ & Бјаркам, ЦР Интернет хистолошки атлас Готтинген мозак мини свиња. Хелиион 5, е01363, https://doi.org/10.1016/j.heliyon.2019.e01363 (КСНУМКС).
Признања
Студију је финансирао Универзитет Аархус „Потпора за развој пројеката за АУ Идеас“ за АМЛ. Захвални смо на техничкој подршци особља ПЕТ центра и Универзитетске болнице Аархус и Универзитетске фарме Аархус на помоћи у лечењу животиња. Захваљујемо се професору Мортену Крингелбацху, професору Јøргену Сцхеел-Кругеру и ванредном професору Арнеу Мøллеру на помоћи у покретању ових студија.
Етичке декларације
Конкурентски интереси
Аутори не објављују никакве супротне интересе.
Додатне информације
Напомена издавача Спрингер Натуре остаје неутралан у погледу надлежности у објављеним мапама и институционалним везама.
Права и дозволе
Опен Аццесс Овај чланак је лиценциран под међународном лиценцом Цреативе Цоммонс Аттрибутион 4.0, која дозвољава употребу, дељење, прилагођавање, дистрибуцију и репродукцију у било којем медијуму или формату, под условом да оригиналним ауторима и изворима дате одговарајуће заслуге, наведите линк до лиценце Цреативе Цоммонс и навести да ли су промене извршене. Слике или други материјали треће стране у овом чланку укључени су у лиценцу Цреативе Цоммонс чланка, осим ако је другачије назначено кредитном линијом за материјал. Ако материјал није укључен у лиценцу Цреативе Цоммонс чланка и ако ваша намера није дозвољена законским прописима или премашује дозвољену употребу, морат ћете добити дозволу директно од власника ауторских права. Да бисте видели копију ове лиценце, посетите http://creativecommons.org/licenses/by/4.0/.