Biol Psychiatry. 2008 Kanûn 1; 64 (11): 941-50. Epub 2008 26 tîrmeh.
Teegarden SL, Nestler EJ, Bale TL.
Kanî
Beşa Biyolojiya Heywanan, Zanîngeha Pennsylvania, Philadelphia, PA 19104-6046, USA.
Abstract
PAŞÎ:
Sosyalîzmê ji bo xelata ku ji bo îşkenceyên narkotîkê ve girêdayî ye û herweha zêdebûna faktoriyek pêşniyazkirinê hate tesbît kirin. Lê belê, mekanîzmayên bingehîn ku piştgiriya hestiyariyê ne diyar e. Em fikir kir ku dakêşandina dopamînê di nîşana nîşana dopamînê de dibe sedema sedemek meziniya bihêziya xelasbûnê ku bi awayekî zordarî xelas dibe ku sîstemê normal bikin.
METHODS:
Me modelek mişkek genetîkî ya bi hesasiyeta xelatê ya zêde, mişka Delta FosB-ya zêde îfade dike, bikar anî, da ku guheztinên rêça xelatê di bersivdayîna parêzek rûn-rûn a xweş de lêkolîn bikin. Nîşaneyên nîşana xelatê di van mişkan de hem bi bingehîn û hem jî piştî 6 hefteyên danasîna parêza xweş hatin lêkolîn kirin. Mişk di ceribandinek behrê de li dû vekişîna parêza rûn-rûn hatin ceribandin da ku qelsiya vê modelê li hember rakirina teşwîqên xelatgir binirxîne.
RESULT:
Encamên me aktîvkirina rêça xelatê ya guhêrbar li ser çerxa qada tegmental ya nucleus accumbens-hîpotalamîk-ventral ku ji ber derbirîna zêde ya Delta FosB-ê di navok û deverên striatal de pêk tê destnîşan dikin.. Asta proteîna girêdanê ya elementa bersivê ya adenosine monophosphate cyclic fosforylated (cAMP) (pCREB), faktora neurotrofî ya ku ji mêj ve tê derxistin (BDNF), û dopamine û adenosine monophosphate cyclic fosphoprotein bi girseyek molekularî 32 kDa (DARPP-32) di nucleus accumbens de di mêşên Delta FosB de kêm bûn, ku nîşana kêmbûna nîşana dopamînê destnîşan dike. Şeş hefte danasîna parêza rûn a zêde van cûdahiyan bi tevahî xweş kir, kapasîteya xelata bihêz a parêzek xweş eşkere kir. Mişkên Delta FosB di heman demê de 24 demjimêran piştî vekişîna rûn zêde zêdebûnek girîng di çalakiya lokomotor û bersivên bi fikar de nîşan dan.
BİXWÎNE
Van encaman hesasiyek bingehîn li ser guhertinên di xelata têkildar de bi nerêkûpêkkirina Delta FosB û nîşana dopamînê re destnîşan dikin ku dikare bi parêzên dilşewat re normalîze bibe û dibe ku di hin celebên qelewbûnê de fenotîpek pêşdaraz be..
Pêşkêş
Tevî zanîna me ya zêde ya pergalên neuralî yên ku xwarin û têrbûnê kontrol dikin, rêjeyên qelewbûnê li Dewletên Yekbûyî zêde dibin. Tedawiyên dermanên heyî xwedan bandorek tixûbdar e, û guheztinên behreyî ji pabendbûna demdirêj a hindiktirîn zirarê dibînin (1). Xwarina xwarinên bi kalorî-dûr, xweş bi guheztinên stresê û rêyên xelatê yên di mêjî de ve girêdayî ye, û destnîşan dike ku taybetmendiyên xelatgir ên van xwarinan dibe ku li ser nîşaneyên hevsengiya enerjiyê derbas bibin (2-4). Xwarinên bi rûn ên zêde wekî xelatên xwezayî tevdigerin, navendên xelata mêjî bi rengekî mîna dermanên destavêtinê çalak dikin, û bi vî rengî di paradîgmayên xwe-rêveberiyê de hatine bikar anîn (5-8). Ji ber vê yekê, îhtîmal e ku behre û motîvasyona ji bo zêdexwarin û karanîna narkotîkê mekanîzmayên bingehîn ên hevpar parve dikin, ku potansiyel rêyên nû yên dermankirinê ji bo her du şertan vedike.
Di lêkolîna têkiliya di navbera xwarinên xweş û rêyên ku xelat û stresê di mêjî de rêkûpêk dikin, me berê nîşankerên molekulî û biyokîmyayî yên kêmbûna xelat û stresê zêde kir piştî vekişîna ji parêzek rûn a delal (HF). Mîna dermanên îstismarkirinê, di lêkolînên me de rûbirûbûna parêzek dilşewat bû sedema zêdebûna asta faktora transkripsiyonê ΔFosB di navokê de (NAc), avahiyek xelata mêjî ya navendî (9, 10). Mişkên ku bi awakî zêde ΔFosB-ê zêde derdixin, ji bo xelatek xwarinê (11) bersiva amûrek zêde nîşan didin, ku wan dike amûrek hêja ji bo vekolîna rola hesasiyeta xelatê û nerêkûpêkkirina dirêj-dirêj a pergala xelatê di bersivên molekulî û biyokîmyayî yên li ser parêzek xweş.
Di lêkolîna heyî de, me mişkên ΔFosB-berbiçav bi kar anîn da ku guheztinên dirêj-dirêj ên nîşangirên xelatê di neurocircuitry devera NAc-hypothalamus-ventral tegmental (VTA) de wekî bersivdana parêzek HF-ya dilşewat lêkolîn bikin. Li ser bingeha lêkolînên berê yên di van mişkên hesas-xelat de, me hîpotez kir ku guheztinên ji hêla ΔFosB-ê ve di hesasiyeta xelatê de nerêkûpêkek di nîşana dopamînê de ye ku ji bertekên NAc ji VTA-yê re vedigire. Digel vê yekê, me hîpotez kir ku danasîna xelatek xwezayî ya parêzek HF-ya enerjîk wê hingê dê pergala dopamînergîk di van mişkan de normal bike, û di encamê de bersivek zêde li hember stresa vekişîna ji vê parêza HF-ê çêdibe.. Aliyê bêhempa yê karanîna parêzek dilşewat wekî maddeyek xelatdar dihêle ku me têkevin navgînên hîpotalamîk ji bo xelatkirina dorpêçê di fenotîpek de ku dibe ku pêşbîniya nifûsa ku ji qelewiya berxwedêr a dermankirinê re pêşbîn dike. Ji bo vekolîna vê hîpotezê, me nîşankerên neurotransmissiona dopamînê, di nav de pCREB, BDNF, û DARPP-32 di NAc û tyrosine hydroxylase û veguhezkarê dopamînê di VTA de, li dû rûdana HF lêkolîn kir. Me di heman demê de nîşankerên taybetî yên balansa enerjiyê ya ku tê zanîn bandorê li hilberîna dopamînê dike, di nav de receptorên leptin û orexin di VTA-yê de û îfadeya orexin di hundurê hîpotalamusa paşîn de jî lêkolîn kir.
Alav û Rêbaz
Animals
Mişkên bitransgenîk ên nêr ên ku di noronên dînorfîn-erênî de di NAc û strîatuma dorsalê de bi awakî zêde ΔFosB-ê zêde îfade dikin (Kelz et al., 1999) li ser bingehek tevlihev (ICR: C57Bl6 / SJL) li Navenda Bijîjkî ya Zanîngeha Teksasê ya Başûr-rojavayî hatine çêkirin û parastin û parastin. li Zanîngeha Pennsylvania ceribandin. Hemî mişk li ser doxycycline (100 μg / ml di ava vexwarinê de) hatin parastin heya ku gihîştin Zanîngeha Pennsylvania. Ji bo ku zêde derbirîn, doxycycline hate rakirin (n = 23) (12). Mişkên kontrolê (n = 26) wergirtina derman berdewam kirin. Mişk heşt hefte piştî rakirina doxycyline di komên parêzê de hatin tayîn kirin ku di wê demê de hate xuyang kirin ku digihîje astên herî zêde (13). Mişk li ser çerxa ronî-tarî ya 12:12 (ronahiya 0700) bi xwarin û ava ku adil tê peyda kirin hatin parastin. Hemî lêkolîn li gorî protokolên ezmûnî yên ku ji hêla Komîteya Lênihêrîn û Bikaranîna Heywanan a Saziyê ya Zanîngeha Pennsylvania ve hatine pejirandin hatine kirin, û hemî prosedurên li gorî rêwerzên sazûmaniyê hatine meşandin.
Pêşkêşkirina xwarinê
Mişk şeş hefte li ser xwarina malê (n=16) hatin parastin an jî li ser HF (n = 16-17) hatin danîn. Xwarina malê (Purina Lab Diet, St. Louis, MO) 4.00 kcal/g heye, ku ji %28 proteîn, %12 rûn, û %60 karbohîdartan pêk tê. Xwarina HF (Research Diets, New Brunswick, NJ) 4.73 kcal/g heye, ku ji %20 proteîn, %45 rûn, û %35 karbohîdartan pêk tê.
Biyokîmya û vegotina genê
Mişk piştî şeş hefteyên parêza parêzê hatin analîz kirin. Mejî ji serjê hatin derxistin û an bi tevahî li ser qeşaya hişk hatin cemidandin an jî NAc hate veqetandin (nêzîkî 0.5 - 1.75 mm ji bregmayê, li kûrahiya 3.5 - 5.5 mm) û di nîtrojena şil de hatin cemidandin. Heya ku were ceribandin di -80°C de tê hilanîn.
Analîzên biyolojîk
Rêbazên ji bo blokên rojavayî di materyalên pêvek de têne diyar kirin. Antîbodên ku hatine bikar anîn ev in: Cdk5, CREB, û BDNF (1:500, Biyoteknolojiya Santa Cruz, Santa Cruz, CA) û fosfo-CREB (pCREB) (Ser 133) (1:500, Teknolojiya Signaling Cell, Danvers, MA).
Autoradiography receptor
Rêbazên hûrgulî yên ji bo otoradiografiyê di materyalên pêvek de têne diyar kirin. Lîgandên ku hatine bikar anîn 2 nM H3 - SCH 23390 û 5 nM H3 - spiperone (PerkinElmer, Boston, MA) bûn.
In situ hybridization
Pêvajoya tîrêjê û hîbrîdîzasyon wekî ku berê hatî destnîşan kirin hate kirin (14). Lêpirsîna DARPP-32 ji hêla P. Greengard (Zanîngeha Rockefeller) ve, û sondaya orexin ji hêla J. Elmquist (Navenda Bijîjkî ya Başûr-rojavayî ya Zanîngeha Texasê) bi dilovanî hate peyda kirin. Slaydên ku ji bo DARPP-32 hatine ceribandin 3 rojan, û slaytên ku ji bo orexin hatine ceribandin 4 rojan hatine kişandin. Pîvankirina wêneyên fîlimê wekî ku berê hatî destnîşan kirin hate kirin (10).
QRT-PCR
RNA ji VTA-yê hate veqetandin û vegotina genên kesane bi karanîna ceribandinên vegotina genê TaqMan (Applied Biosystems, Foster City, CA) hate nirxandin. Rêbazên hûrgulî û analîzên îstatîstîkî dikarin di materyalên pêvek de werin dîtin.
Analîzên Behavioral
Ji bo vekolîna bandorên hesasiyeta xelatê li ser guhertinên behrê yên ji hêla parêzê ve hatî çêkirin, binkeyek mişkan piştî çar hefteyên ragirtinê ji HF hate derxistin û vegerandin xwarina malê (n = 9 kontrol, n = 8 ΔFosB). Bîst û çar saetan piştî vekişînê, mêş li gorî paradîgmaya vekişîna parêza me ya berê hatî weşandin (10) ketin ceribandina qada vekirî. Bi kurtasî, mişk li navenda amûra qada vekirî hate danîn û pênc deqeyan çavdêrî kirin. Tevahiya xaçeyên xetê, bolîya fekal, dema li navendê, û xaçeyên nav navendê hatin pîvandin.
Jimare
Hemî dane ji bilî blokên Western bi karanîna ANOVA-ya du-alî ve hatî analîz kirin û li dûv wê jî testa PLSD ya Fisher bi dermankirina doxycycline (îfadekirina ΔFosB) û rewşa parêzê wekî guhêrbarên serbixwe. Ji bo analîzên RT-PCR, nirxek P-ya kêmkirî hate bikar anîn da ku berhevokên pirjimar di nav komên genên têkildar de rast bikin (li materyalên pêvek binêre). Blotên rojavayî bi karanîna testa t-ya xwendekarek bi dermankirina doxycycline wekî guhêrbarek serbixwe ve hate analîz kirin, û dendikên optîkî yên di heman blotê de berhev kirin. Hemî daneyên wekî navîn ± SEM têne pêşkêş kirin.
results
Cûdahiyên biyolojîk ên bingehîn
Ji bo ronîkirina rêyên molekulî yên ku di binê hesasiyeta xelata zêdekirî de di mêşên bi ΔFosB-zêde derbirrîn de ne, astên çend molekulên nîşana sereke di NAc de hatin lêkolîn kirin. Meylek ji bo zêdekirina astên Cdk5 di NAc mişkên ΔFosB de li gorî heywanên kontrolê yên pîvaz ên ku li ser doxycycline têne parastin (F = 5.1, P = 0.08; Fig. 1A) hebû. Mişkên ΔFosB astên pCREB (F = 7.4, P <0.05; Xiflteya 1B) û her weha astên giştî yên CREB (F = 5.4, P = 0.05; Xiflteya 1C) bi girîngî kêm kirin. Kêmkirinek girîng a BDNF di NAc mêşên ΔFosB de jî hate dîtin (F = 10.6, P <0.05; Wêne 1D).
1
Mişkên ku ΔFosB zêde derdixin nîşankerên biyokîmyayî yên kêmkirina nîşana dopamînê di NAc de nîşan didin.
Xwarin û giraniya laş li ser parêza rûn zêde
Dûv re me bandorên parêzek HF-ê ya xwezayî ya xelatgir li ser guheztinên molekulên îşaretkirinê yên di mişkên ΔFosB-zêde derbirrîn de lêkolîn kir. Di navbera mêşên ΔFosB û kontrolên xwarina xwarinê de li ser mal û HF-ê de cûdahî tune. Lêbelê, kêmbûnek giştî di girtina kaloriyê de ku bi giraniya laş ve hatî normalîzekirin hebû dema ku ji HF-ya ku ji mişkên ΔFosB re taybetî bû (F = 11.2, P <0.01; Xiflteya 2A) re hate rûxandin. Di dawiya şeş hefteyên danasîna parêzê de, mêşên ku HF distînin ji yên di parêza xwarinê de girantir bûn (F = 17.2, P <0.001), û mêşên ΔFosB bi giştî ji kontrolê kêmtir giran bûn (F = 5.6, P <0.05; Fig. 2B). Ev bandor ji bo cûdahiyên di navbera komên li ser parêza xwarinê de taybetî bû (P <0.05).
2
Mişkên ku zêde îfade dikin ΔFosB di xwarina xwarinê de di xwarina xwarinê de an jî di parêza rûn zêde (HF) de cûdahî nîşan nedan.
Cûdahiyên biyokîmyayî yên li ser parêza rûn zêde
Ji bo ku were destnîşankirin ka cûdahiyên bingehîn di nîşana NAc de çawa dibe ku ji hêla parêza HF ve were guheztin, heman proteînên nîşankirinê yên ku di destpêkê de hatine lêkolîn kirin li heywanên ku şeş hefte HF wergirtine hatine lêkolîn kirin. Di asta Cdk5 de cudahiyên girîng tune bûn (Hêjîrê 3A). Asta pCREB û tevahî CREB piştî şeş hefteyên HF êdî ji hev cûda nebû (Wêne. 3B,C). Asta BDNF di mêşên ΔFosB de piştî şeş hefteyên rûdana HF-ê bi girîngî bilind bû (F = 6.5, P = 0.05; Wêne 3D).
3
Xwarina rûn zêde (HF) ciyawaziyên îşaretkirinê çêtir dike ku di NAc mêşên ΔFosB de zêde îfade dikin
Autoradiography receptorê Dopamine
Me otoradiyografya receptor bikar anî da ku binirxînin ka guheztinên ji hêla ΔFosB-ê ve di îşaretkirina dopamînê de di NAc de bi guheztinên di îfadeya wergirên dopamînê de têkildar in (Wêne. 4A). Xuya bû ku parêza rûn a zêde tîrêjiya girêdana receptorê D1 dopamine (P = 0.14) hinekî zêde dike, û ev cûdahî di mişkên ΔFosB de (Hêjî. 4B) mezintir bû. Di heman demê de meylek berbi zêdebûna qada girêdana D1 ya li dû HF (P = 0.06) jî hebû, û ceribandina post-hoc ev yek di mişkên ΔFosB de girîng nîşan da (P <0.05; Fig. 4C). Berevajî receptorên D1, di dendika girêdana receptora D2 de tu guheztinek çênebû (çawa kontrolê = 97.6 ± 6.9, kontrol HF = 101.1 ± 8.2, çîçek ΔFosB = 91.6 ± 1.0, ΔFosB HF = 94.8 ± 9.5 qad. ± 47.3, kontrola HF = 3.4 ± 53.8, ΔFosB chow = 6.0 ± 51.9, ΔFosB HF = 3.7 ± 49.0) di NAc de hatin dîtin.
4
Xwarina rûn a zêde (HF) bû sedema guhertinên di girêdana receptorên dopamine D1 û îfadeya DARPP-32 de di navokê de (NAc) ya mêşên ΔFosB de ku zêde îfade dikin.
Di NAc de îfadeya DARPP-32
Ji bo diyarkirina asta îfadeya DARPP-32 di NAc de hîbrîdîzasyona li cîh hate bikar anîn (Wêne. 4D). Xwarina rûn a zêde li vê devera mêjî bi girîngî îfadeya DARPP-32 zêde kir (F = 5.1, P <0.05), û têkiliyek girîng di navbera parêz û îfadeya ΔFosB de (F = 8.9, P <0.05) hebû, bi mişkên ΔFosB re bêtir nîşan didin. guherîna parêzê (Hêjîra 4E). Cûdahiyek bingehîn di vegotina DARPP-32 de di navbera kontrol û mêşên ΔFosB de bi ceribandina post-hoc (P <0.01), û her weha zêdebûnek girîng a vegotina DARPP-32 di mişkên ΔFosB de li ser HF (P <0.01) hate eşkere kirin.
Di VTA de vegotina genê
QRT-PCR hate bikar anîn da ku guhartinên di vegotina genê de di VTA-yê de binirxîne, çend genên sereke yên ku berê di rêziknameya xelatê de têkildar bûne armanc. Hemî nimûne ji β-actin re normal kirin. Ji bo ku pêbaweriya β-actin ji hêla dermankirinê ve nehatiye guheztin, ceribandinek cûda hate meşandin da ku β-actin bi kontrolek navxweyî ya duyemîn, GAPDH re were berhev kirin. Di vegotina β-actin de cûdahiyên girîng tune bûn (nirxên ΔCT, β-actin - GAPDH: çîçeka kontrolê = 2.29 ± 0.21, kontrol HF = 2.01 ± 0.04, ΔFosB chow = 2.32 ± 0.49, ΔFosB HF = 2.37 ±).
Meylek ji bo têkiliyek di navbera îfadeya ΔFosB û dermankirina parêzê de ji bo vegotina tîrosîn hîdroksîlase hate dîtin (F = 3.6, P <0.06; Wêne 5A). Şeş hefteyên rûbirûbûna HF-ê xuya bû ku di mêşên kontrolê de îfadeya tyrosine hydroxylase kêm dike û di mêşên ΔFosB de îfadeyê zêde dike. Têkiliyek girîng a di navbera îfadeya ΔFosB û rûdana parêzê de ji bo vegotina veguhezkarê dopamînê hate dîtin (F = 6.7, P <0.03; Fig. 5B). Mîna tyrosine hydroxylase, rûdana HF di mêşên kontrolê de îfadeya veguhezkarê dopamine kêm kir û di mişkên ΔFosB de bi girîngî zêde kir (P <0.05). Cûdahiya bingehîn di vegotina veguhezkarê dopamînê de di navbera kontrol û mêşên ΔFosB de negihîşt girîngiyê (P = 0.16), lê piştî 6 hefteyên HF, mişkên ΔFosB astên girîng ên veguhezkarê dopamînê li gorî kontrolê diyar kirin (P <0.05).
5
Ragihandina parêza rûn a zêde (HF) û îfadeya ΔFosB bû sedema guhertinên di vegotina hejmarek molekulên sereke yên di VTA de.
Meylek hebû ku bandorek zêdekirina îfadeya ΔFosB nîşan dide ku asta TrkB di VTA-yê de kêm bike (F = 5.7, P <0.04; Fig. 5C). Her çend bandorên sereke li ser vegotina receptorê κ-opioîd tune bûn, di mişkên ΔFosB de meylek berbi kêmbûna îfadeyê hebû (P = 0.08; Wêne 5D). Di VTA de jî îfadeya receptorê leptin hate destnîşankirin. Bandorek girîng a rûbirûbûna parêzê hate dîtin (F = 6.1, P <0.03), digel ku HF di VTA-yê de hem di ΔFosB û hem jî di mêşên kontrolê de astên receptora leptîn bi girîngî kêm dike (Wêne. 5E). Di VTA de îfadeya receptorê orexin 1 jî hate lêkolîn kirin. Bandorek girîng a parêzê li ser vegotina receptorê oreksîn (F = 9.0, P <0.02) hebû, bi mişkên ku ji HF re rû bi rû mane di VTA-yê de astên bilindtir diyar dikin (Hêl. 5F). Di heman demê de meylek ji bo mêşên ΔFosB jî hebû ku di vê devera mêjî de astên bilindtir ên receptorê orexin 1 diyar bikin (P <0.05).
Di hîpotalamusa paşîn de îfadeya Orexin
Me astên oreksînê di hîpotalamusa paşîn de, eslê venesaziya orexinergîk a VTA, bi hîbrîdîzasyona li cîhê pîva (Hêjî. 6A). Têkiliyek girîng di navbera îfadeya ΔFosB û rûxandina parêzê de li ser îfadeya oreksînê (F = 9.1, P <0.01) hebû, digel ku HF bi girîngî asta oreksînê di mêşên kontrolê de zêde dike (P <0.05) û di mişkên ΔFosB de kêmkirina îfadeyê (Hêjîrê. 6B). Her çend di rewşa bingehîn de di vegotina orexin de cûdahiyên girîng tunebûn, piştî 6 hefteyên HF, mişkên ΔFosB li gorî kontrolê asta orexinê bi girîngî kêm kirin (P <0.05).
6
Xwarina rûn zêde (HF) bandorên cihêreng li ser îfadeya orexin di kontrolê de (Ctrl) û ΔFosB mêşên ku zêde îfade dikin hebû.
BeAnalîzên havioral
Ji bo nirxandina guheztinên di şiyarbûn û hestyariyê de ji ber guheztina parêzê, mêş 24 demjimêran piştî vekişîna parêza HF (10) ji ceribandina qada vekirî re hatin rûxandin. Tevahiya xaçeyên rêzê, yên ku wekî pîvanek hêrsbûnê hatine tomar kirin, bi girîngî bandor li ser îfadeya ΔFosB (F = 6.6, P <0.05) û parêz (F = 4.6, P <0.05; Xiflteya 7A) kirin. Mişkên ΔFosB di hawîrdora nûjen de ji kontrolê çalaktir bûn, û ceribandina post-hoc destnîşan kir ku mêşên ku ji HF-yê hatine derxistin ji yên ku li ber çolê hatine kişandin pir çalaktir bûne (P <0.05). Boli fekal wekî pîvanek behremendiya xemgîniyê hate hesibandin (10). Bandorek sereke ya îfadeya ΔFosB (F = 10.2, P <0.01) hebû, bi mêşên ku ΔFosB-berbiçav zêde dikin di hawîrdora nûjen de, nemaze di komên xwarina malê û vekişîna HF-ê de bêtir bolî çêdikin (Hêjî. 7B). Mişkên ΔFosB yên ku li ser parêza HF-ê têne domandin ji yên ku di xwarinê de têne domandin û yên ku 24 demjimêran berî ceribandinê vekişandin kêmtir bolî fekal çêkirin. Mişkên kontrolê ji parêzê bandor nedibûn. Li ser wextê ku li navenda zeviya vekirî derbas bû bandorek girîng a îfadeya ΔFosB an parêzê tune bû (xwarina kontrolê = 14.5 ± 3.1 saniye, kontrol HF = 18.0 ± 3.2 saniye, kontrol W/D = 15.4 ± 1.9 saniye, xwarina ΔFosB = 16.9 ± 2.4 saniye, ΔFosB HF = 13.1 ± 3.9 sek, ΔFosB W/D = 19.8 ± 2.6 sek).
7
Mişkên ku ΔFosB zêde îfade dikin ji bandorên vekişîna parêza rûn zêde (HF) hesastir bûn.
Nîqaş
Di dermankirina qelewbûnê de, pêdivîyek krîtîk ji bo destnîşankirina faktorên ku bandorê li ser hîskirina zêdexwarinê û zêdebûna giraniyê dikin heye. Rêyên xelata mêjî di motîvasyon û bersivdana xwarinên xweş û guhertinên parêz de rolek girîng dileyzin (6, 10, 15, 16). Ji ber ku îşaretên orexigenic û anorexigenic dikarin rasterast bandorê li nîşana xelatê bikin bi navgînek hîpotalamus-VTA-NAc ve, ronîkirina genên ku di nav navendên xelatê de bersivê didin parêzên dilşewat ên dewlemend ên enerjiyê dikarin di dermankirina qelewbûnê de armancên dermankirinê yên nû peyda bikin (17, 18). Ji ber vê yekê, me nîşankerên biyokîmyayî û molekulî yên nîşana xelat û balansa enerjiyê li ser çerxa hîpotalamus-VTA-NAc di bersiva parêzek HF-ê de di mêşên bi ΔFosB-berbiçav de wekî modelek hestiyariya zêde ya ji bo guhertinên di xelatê de lêkolîn kir (13, 19, 20) , û hestiyariya behrê ya piştî vekişîna parêzê. Me hîpotez kir ku nerêkûpêkkirina bingehîn a nîşankirina dopamînê di mişkên ΔFosB de dê ji hêla bandorên xelatgir ên parêzek HF ve were normalîzekirin, ku di nav hevberdana nîşanên hevsengiya enerjiyê û pergala dopamînê de ye.
Ji bo vekolîna nîşankerên ku di NAc-ê de nîşana nerêkûpêkkirina dopamînê nîşan didin, me astên receptorên D1 û bandorkerên jêrîn lêkolîn kirin. Her çend cûdahiyên girîng di girêdana receptorên D1 de tune bûn, meylek ji bo vegirtina HF hebû ku di mişkên ΔFosB de qada girêdanê zêde bike. Ev balkêş e ji ber ku vegirtina ΔFosB ji hêla derman û xelatên xwezayî ve xuya dike ku di bincûreya dînorfîn-erênî ya neuronên spî yên navîn de ku di serî de receptorên D1 diyar dikin de serdest e. (9, 21). Asta pCREB-a hedefa nîşana dopamînê ya jêrîn bi girîngî di mişkên ΔFosB de kêm bû, piştgirî dide çalakkirina receptorê D1 ya li vê devera mêjî (22, 23). Balkêş e, me di heman demê de kêmbûnek girîng a asta giştî ya CREB di mişkên ΔFosB de jî dît, ku ji bo veguheztina sînyala dopamînê kapasîteya bêtir kêmkirî pêşniyar dike ku dibe ku ji bertekên ku ji kêmbûna demdirêj a pCREB-ê pêk tê duyemîn be (24). Vebijandina BDNF ji hêla pCREB ve tê rêve kirin, bi aktîvkirina D1 ve tê bilind kirin, û navbeynkarek girîng a neuroplastîkbûna xelat-girêdayî ya di NAc de ye (25, 26). Li gorî vê yekê, me di NAc ya mişkên ΔFosB de kêmbûnek girîng a proteîna BDNF dît.
Hemî neuronên spî yên navîn ên di NAc de DARPP-32 (27) diyar dikin. Gelek bandorkerên wê yên jêrîn wê di rêyên xelatê de lîstikvanek girîng e (28), û ew di tiryakê de û di nexweşiyên din ên ku pergala dopamînê di nav wan de tevliheviyên hestyarî û şîzofreniyê ve girêdayî ne ve girêdayî ye. (27, 29). Me di NAc ya mişkên ΔFosB de kêmkirina bingehîn a kûr di îfadeya DARPP-32 de dît. Daxuyaniya DARPP-32 ji hêla BDNF ve tê rêve kirin, û ji ber vê yekê vegotina kêmkirî dibe ku rasterast bi kêmbûna asta BDNF-ê ya ku di mişkên ΔFosB de hatî dîtin ve girêdayî be (27, 29, 30). Tewra guheztinên nerm ên di rewşa fosforîlasyonê ya DARPP-32 de dikare bibe sedema guhertinên girîng di nîşana hundurîn a di nav NAc de (27). Lêkolînên berê ti guhertinek di proteîna DARPP-32 de di mişkên ΔFosB de piştî derxistina 12 hefteyî ji doxycycline rapor nekirine dema ku nirxandinek striatal ya berfirehtir hate kirin (31), pêşniyar dike ku bandorên ΔFosB li ser DARPP-32 dibe ku dem û herêmê taybetî bin.
Me hîpotez kir ku kêmbûna dramatîk di nîşaneyên nîşana dopamînê de di NAc ya mişkên ΔFosB de dibe ku di nav neuronên projekirina dopamînê ya VTA de guhertin çêbibe, her çend ΔFosB di nav van neuronan de zêde nayê eşkere kirin.. Ji ber vê yekê, me îfadeya genên têkildarî dopamine di VTA de, tevî tyrosine hydroxylase û veguhezkarê dopamine lêkolîn kir. Asta tyrosine hydroxylase û veguhezkarê dopamine bi hilberîna dopamine re bi erênî ve girêdayî ye. Ji bo mêşên ΔFosB meylek hebû ku tîrosîn hîdroksîlaza kêmkirî û kêmbûnek girîng a veguhêzkarê dopamînê nîşan bidin, li gorî bêserûberkirina nîşana dopamînê ya di NAc de.. Ji ber ku ev kêmkirinên bingehîn ên di genên têkildarî dopamînê de di VTA-ya mişkên ΔFosB de bi guman bertekên guhezbar ên ji NAc-ê di dema zêdebinavkirina ΔFosB-ya demdirêj de nîşan didin., me îfadeya receptorê BDNF, TrkB, wekî mekanîzmayek mimkun a vegera NAc ya ji VTA re lêkolîn kir (32). Mîna tyrosine hydroxylase û veguhezkarê dopamine, vegotina TrkB di heman demê de meylek ku di mêşên ΔFosB de bi bingehîn kêm dibe destnîşan kir ku dema ku ji bo berhevokên pirjimar têne rast kirin negihîştine girîngiyê. Kompleksa BDNF-TrkB dikare bi paşveguhêz were veguheztin û di nav VTA de tevbigere da ku bandorê li îfadeya genê herêmî bike û mezinbûn û domandina hucreyê pêşve bibe (33). Zêdetir, çalakkirina BDNF ya TrkB ya presynaptîk a di nav NAc de dikare rasterast neurotransmissiona dopamînê teşwîq bike (32), piştgirî bide kêmbûna bingehîn a nîşana dopamînê di van mişkan de.
Aktîvkirina dînorfîn a receptorên κ-opioîd nîşana dopamînê bi rê ve dibe û mekanîzmayek din e ku bi vî rengî NAc ji VTA-yê re bertek peyda dike. (34). Me dît ku îfadeya receptorê κ-opioid di VTA de meylek ku di mişkên ΔFosB de kêm dibe nîşan da. Ji ber ku zêde îfadeya ΔFosB hate destnîşan kirin ku di NAc de îfadeya dînorfînê kêm dike (20), mişkên ΔFosB îhtîmal e ku di net VTA κ- de kêmbûnek kûr hebe.çalakkirina opioîdê. Her çend îşaretkirina dînorfînê bi gelemperî bandorek astengker li ser neuronên dopamînê dike (35), mişkên ku xwerêveberiya zêde ya dermanên destavêtinê nîşan didin asta dînorfînê di NAc-ê de kêm dikin, û destnîşan dikin ku di zêdekirina hesasiyeta xelatê de rola kêmkirina nîşana dînorfînê ya bingehîn (36). , 37). Nerêkûpêkkirina dînorfîn - pergala κ-opioîd bi wergirtin û domandina îstismara narkotîkê ve girêdayî ye, di normalîzekirina rêyên dopamînê de piştgirî dide balansek krîtîk ya nîşana opioîdê. (38).
Li ser bingeha kapasîteya xelatkirinê ya parêzek HF-ê ya enerjîk, me hîpotez kir ku nerêkûpêkek di nîşana xelata dopamîn û opioîdê de di mêşên ΔFosB de dê van mişkan ji bo bersivên xelata zêde yên li ser parêzek wusa pêşde bibe, bi vî rengî pergala xelatê bi aktîvkirina hîpotalamusê normal bike. -VTA-NAc circuit. Di dema rûdana parêza şeş hefte de, ti cûdahiyek di girtina xwarinê de di navbera ΔFosB û mêşên kontrolê de nehat dîtin, û destnîşan kir ku guheztinên ku di nîşangirên biyokîmyayî û molekulî yên nîşana xelatê de di mişkên ΔFosB de hatine dîtin ne ji ber cûdahiyên di kaloriyên ku hatine vexwarin de ne. Wekî ku tê pêşbînîkirin, cûdahiyên bingehîn ên ku di pCREB, tevahî CREB, BDNF, DARPP-32, û astên receptorên κ-opioîd de di navbera ΔFosB û mêşên kontrolê de hatine qewirandin kêm bûne, dibe ku ji ber zêdebûna hilberîna dopamînê di mişkên ΔFosB de li ser HF (29, 39-41) .
Lêkolîna hem tyrosine hydroxylase û hem jî veguhezkarê dopamine di VTA de bersivên dijberî yên ecêb ên ΔFosB û mişkên kontrolê yên li dû HF-ê eşkere kirin.. Mişkên kontrolê kêmbûnek di vegotina veguhezkerê tyrosine hydroxylase û dopamine de nîşan dan, dema ku mêşên ΔFosB zêdebûna van her du genên girêdayî dopamînê nîşan dan. Balkêş e, îfadeya tyrosine hydroxylase di VTA-yê de ji hêla rêveberiya kronîk a kokaîn an methamphetamine ve tê guheztin (42-44), pêşniyar dike ku mişkên ΔFosB dikarin xelata xwezayî ya HF ji mêşên kontrolê girîngtir bibînin.
Ji bo ku were vekolîn ka ketina potansiyel a hîpotalamî ya VTA çawa dibe ku îşaretên ku balansa enerjiyê nîşan didin veguhezîne, îfadeya receptorê leptin û receptorê orexin-1 jî hate lêkolîn kirin. Asta leptin a gerok ji hêla HF ve zêde dibe, û leptin dikare di encamê de li VTA-yê tevbigere ku nîşana dopamînê biguhezîne (18, 45). Vebijandina receptorê leptîn VTA bi heman rengî ji hêla HF ve hem di ΔFosB û hem jî di mêşên kontrolê de kêm bû, li gorî zêdebûna giraniya wekhev û girtina parêzê dema ku li ser HF bû. Di heman demê de rûniya zêde di VTA-ya hem ΔFosB û hem jî mêşên kontrolê de îfadeya orexin receptor-1 zêde kir. Orexin neuronên dopamînê di VTA-yê de çalak dike, plastîkbûna VTA pêşve dike, û asta dopamînê di NAc de zêde dike (46-48). Li gorî çavdêriyên me (49, 50) parêza rûn a zêde hate destnîşan kirin ku di mişkan de îfadeya orexin zêde dike. Bi vî rengî, zêdebûna vegotina receptorê orexin û her weha guhertinên di nîşana leptin de di VTA de dikare xelata parêzê hem di ΔFosB û hem jî di mêşên kontrolê de pêşve bibe, piştgirî bide veqetandinê di navbera riyên ku nîşanên hevsengiya enerjiyê vediguhezînin û yên ku rasterast bi xelatê ve girêdayî ne.
Ji bo vekolîna bandorên stresê yên vekişîna xelatê, mişk 24 demjimêran piştî rakirina HF di ceribandinek zeviyek vekirî de hatin lêkolîn kirin. Mişkên ΔFosB ji bandorên tûj ên vekişîna parêza bijarte hesastir bûn, li qada vekirî ya nû li gorî hemî komên din ên kontrol û parêzê, çalakiya acizbûnê û hilberîna bolî ya fekal zêde nîşan didin. Mişkên ΔFosB di vê ceribandinê de jî şêwazek behremendî ya balkêş nîşan dan ku xelat û hestiyariya stresê nîşan dide, digel ku parêza HF di destpêkê de hilberîna bolî ya fekal li gorî xwarinê kêm dike, û vekişîn dîsa vê bersiva bi fikar zêde dike. Vê zêdebûna dîtbar a çalakiya zeviyê vekirî bi guhertinên di îfadeya orexin re têkildar nebû, têkiliyek bi hestiyariya ji stresê re pêşniyar dike ku ne tenê bandorek guhertinên di nîşana navbeynkariya orexin de ye. Bi tevayî, van daneyan hîpoteza me piştgirî dikin ku mêşên ΔFosB dê ji ber hesasiyeta wan a xelata bilindtir ji bandorên tûj ên vekişîna parêza bijare hesastir bin..
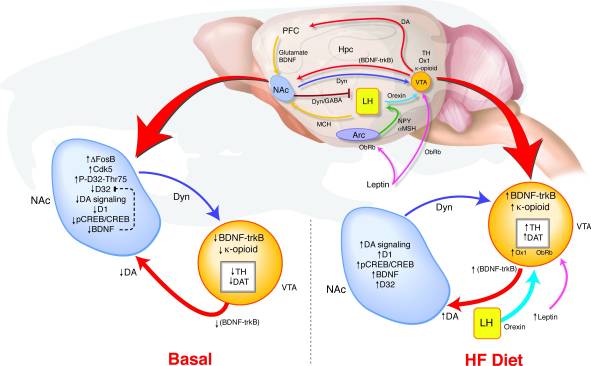
Meriv çawa di NAc-ê de vegotina dirêj-dirêj a ΔFosB dibe sedema guhertinên weha di behre û nîşana xelatê de? Me modelek vedîtina hevedudanî ya VTA-yê pêşniyar kiriye ku tê de bertekên guhezbar ên NAc û hîpotalamusê di derheqê rewşa xelatê de îşaretan radigihîne da ku rêziknameya pergala dopamînê diyar bike ku dibe ku girêdanek di navbera nerêkûpêkkirina riya xelatê û pêşdaraziya qelewbûnê de piştgirî bike (Wêne. 8). Di dema xuyangkirina HF de, gelek têketin ku hem balansa enerjiyê û hem jî rewşa xelatê nîşan didin li ser VTA-yê digihêjin hev. Zêdebûna nîşana leptîn û oreksîn û her weha bertekên guheztin ên ji NAc ber bi hîpotalamusa paşîn ve dibe ku bandor bike ka ev nîşanên orexigenic çawa bersivê didin HF di mişkên ΔFosB de (17, 18, 45, 47, 51-53). Di BDNF-ê de bilindbûna parêza-rûnê ya zêde dibe ku ji VTA-yê re bertekên xelatê peyda bike, û di vegotina genê-girêdayî dopamînê de guheztinan pêşdetir bike.
8
Xwarina rûn a zêde (HF) di mişkên ΔFosB de nîşana xelata nerêkûpêk normal dike
Van encaman nîşangirên molekulî yên hesasiyeta xelatê diyar dikin û destnîşan dikin ku nerêkûpêkkirina demdirêj a pergala dopamînê dibe ku kesek pêşî li tiryakê û qelewbûnê bigire. Zêdetir, van daneyan di dermankirin û pêşîlêgirtina qelewbûn û nexweşiyên din ên ku dibe ku li ser pergala xelatdayînê navend bibin, gavek girîng peyda dikin berbi destnîşankirina armancên dermanker ên nû yên potansiyel. Di pêşerojê de, dê girîng be ku were vekolîn ka ev pergal çawa bersivê dide rakirina parêza HF, û her weha lêkolînkirina cûdahiyên zayendî di hesasiyeta xelat û rûnbûna parêza bilind de.
Pêdivî ye
Supp. Methods
Li vir bibînin li vir bibînin. (61K, doc)
Spasî
Nivîskar dixwazin spasiya Cathy Steffen bikin ji bo arîkariya ji bo çandin û veguheztina heywanan. Ev xebat ji hêla berxek ji Navenda Diyabetê ya Zanîngeha Pennsylvania (DK019525) û ji hêla Enstîtuya Neteweyî ya Tenduristiya Giyanî (R01 MH51399 û P50 MH66172) û Enstîtuya Neteweyî ya li ser Abuse Drug (R01 DA07359) ve hate piştgirî kirin.
Footnotes
Daxuyaniyên darayî: Hemî nivîskaran radigihînin ku ti berjewendîyên darayî yên bijîjkî an nakokiyên berjewendiyê yên potansiyel tune.
Çavkanî
1. Wadden TA, Berkowitz RI, Womble LG, Sarwer DB, Phelan S, Cato RK, Hesson LA, Osei SY, Kaplan R, Stunkard AJ. Ceribandinek rasthatî ya guheztina şêwaza jiyanê û dermankoterapiya ji bo qelewbûnê. N Engl J Med. 2005;353(20):2111–20.[PubMed]
2. Blendy JA, Strasser A, Walters CL, Perkins KA, Patterson F, Berkowitz R, Lerman C. Di qelewbûnê de xelata nîkotînê kêm kirin: di mirov û mişk de hevberhevkirin. Psychopharmacology (Berl) 2005
3. Franken IH, Muris P. Cudahiyên takekesî di hesasiyeta xelatê de bi xwestekên xwarinê û giraniya laşê têkildar di jinên saxlem de têkildar in. Dilbijîn. 2005;45(2):198–201.[PubMed]
4. Kelley AE, Berridge KC. Neurozanistiya xelatên xwezayî: Têkiliya bi dermanên tiryakê re. J Neurosci. 2002;22(9):3306–11.[PubMed]
5. Cagniard B, Balsam PD, Brunner D, Zhuang X. Mişkên bi dopamîna kronîk a bilindkirî ji bo xelata xwarinê motîvasyona zêde nîşan didin, lê fêr nabin. Neuropsychopharmacology. 2006;31(7):1362–70.[PubMed]
6. Liang NC, Hajnal A, Norgren R. Sham xwarina rûnê ceh di nav mişkê de dopamîna accumbens zêde dike. Am J Physiol Regul Integr Comp Physiol. 2006;291(5):R1236–9.[PubMed]
7. Mendoza J, Angeles-Castellanos M, Escobar C. Tevlihevkirina bi xwarinek dilşewat çalakiya pêşbîniya xwarinê û îfadeya c-Fos li deverên mêjî yên têkildar bi xelatan vedihewîne. Neuroscience. 2005;133(1):293–303.[PubMed]
8. Schroeder BE, Binzak JM, Kelley AE. Profîlek hevpar a aktîvkirina kortikê ya prefrontal li dû rûbirûbûna nîkotîn- an çîkolata-girêdayî nîgarên kontekstê. Neuroscience. 2001;105(3):535–45.[PubMed]
9. Nestler EJ, Barrot M, Xwe DW. DeltaFosB: guhêrbarek molekular a domdar ji bo tiryakê. Proc Natl Acad Sci US A. 2001;98(20):11042–6. [Gotara belaş PMC] [PubMed]
10. Teegarden SL, Bale TL. Kêmbûna tercîha parêzê hestyarî û xetera vegerandina parêzê zêde dike. Biol Psychiatry. 2007;61(9):1021–9.[PubMed]
11. Olausson P, Jentsch JD, Tronson N, Nestler EJ, Taylor JR. dFosB di Nucleus Accumbens de Tevger û Motîvasyona Amûra Bi Xwarinê-Pêkûzkirî Rêz dike. Kovara Neuroscience. 2006;26(36):9196–9204.[PubMed]
12. Chen J, Kelz MB, Zeng G, Sakai N, Steffen C, Shockett PE, Picciotto MR, Duman RS, Nestler EJ. Heywanên transjenîk ên ku di mêjî de vegotina genê ya înduksîb û armanckirî ne. Mol Pharmacol. 1998;54(3):495–503.[PubMed]
13. Kelz MB, Chen J, Carlezon WA, Jr, Whisler K, Gilden L, Beckmann AM, Steffen C, Zhang YJ, Marotti L, Xwe DW, Tkatch T, Baranauskas G, Surmeier DJ, Neve RL, Duman RS, Picciotto MR, Nestler EJ. Îfadeya faktora transkripsiyonê deltaFosB di mêjî de hestiyariya ji kokaînê re kontrol dike. Awa. 1999;401(6750):272–6.[PubMed]
14. Bale TL, Dorsa DM. Cûdahiyên zayendî û bandorên estrojenê li ser vegotina asîda ribonukleîk a peyamberê receptorê oksîtocinê di hîpotalamusa ventromedial de. Endokrinolojî. 1995;136(1):27–32.[PubMed]
15. Avena NM, Long KA, Hoebel BG. Mişkên ku bi şekir ve girêdayî ne, piştî bêhnvedanê ji şekir re bersivek zêde nîşan didin: delîlên bandorek kêmbûna şekir. Physiol Behav. 2005;84(3):359–62.[PubMed]
16. Will MJ, Franzblau EB, Kelley AE. Mu-opioîdên Nucleus accumbens bi aktîvkirina torgilokek mêjî ya belavbûyî ve vexwarina parêzek rûn-rûn bi rê ve dibin. J Neurosci. 2003;23(7):2882–8.[PubMed]
17. Zheng H, Patterson LM, Berthoud HR. Nîşana orexinê li qada tegmental a ventral ji bo xwarina rûn a zêde ya ku ji hêla teşwîqkirina opioîdê ya nucleus accumbens ve hatî çêkirin hewce ye. J Neurosci. 2007;27(41):11075–82.[PubMed]
18. Hommel JD, Trinko R, Sears RM, Georgescu D, Liu ZW, Gao XB, Thurmon JJ, Marinelli M, DiLeone RJ. Nîşana receptorê leptîn di neuronên dopamîn ên mêjiyê navîn de xwarinê bi rê ve dibe. Neuron. 2006;51(6):801–10.[PubMed]
19. Colby CR, Whisler K, Steffen C, Nestler EJ, Xwe DW. Zêde îfadekirina celeb-taybetî ya hucreya striatal ya DeltaFosB teşwîqa kokaînê zêde dike. J Neurosci. 2003;23(6):2488–93.[PubMed]
20. Zachariou V, Bolanos CA, Selley DE, Theobald D, Cassidy MP, Kelz MB, Shaw-Lutchman T, Berton O, Sim-Selley LJ, Dileone RJ, Kumar A, Nestler EJ. Rola bingehîn a DeltaFosB di navokê de di çalakiya morfînê de. Nat Neurosci. 2006;9(2):205–11.[PubMed]
21. Lee KW, Kim Y, Kim AM, Helmin K, Nairn AC, Greengard P. Di navokê de di nav nucleus accumbens de di nav D1 û D2 de çêbûna dendrîtîka dendikî ya ku ji hêla kokaîn ve hatî çêkirin de receptorên dopamînê hene. Proc Natl Acad Sci US A. 2006; 103 (9): 3399-404. [Gotara belaş PMC] [PubMed]
22. Blendy JA, Maldonado R. Analîza genetîkî ya tiryakê: rola proteîna girêdana hêmana bersivê ya cAMP. J Mol Med. 1998;76(2):104–10.[PubMed]
23. Nestler EJ. Mekanîzmayên molekular ên narkotîkê. Neuropharmacology. 2004;47 1:24–32.[PubMed]
24. Tanis KQ, Duman RS, Newton SS. Girêdan û Çalakiya CREB di Mejî de: Taybetmendiya Herêmî û Destpêkirina Bi Desthilatdariya Elektrîk. Biol Psychiatry. 2007
25. Kumar A, Choi KH, Renthal W, Tsankova NM, Theobald DE, Truong HT, Russo SJ, Laplant Q, Sasaki TS, Whistler KN, Neve RL, Xwe DW, Nestler EJ. Veavakirina kromatînê mekanîzmayek bingehîn e ku di binavê plastîkiya kokaînê ya di striatumê de ye. Neuron. 2005;48(2):303–14.[PubMed]
26. Graham DL, Edwards S, Bachtell RK, Dileone RJ, Rios M, Xwe DW. Çalakiya dînamîk a BDNF-ê di navokê de bi karanîna kokainê re xwe-rêveberiyê û vegerê zêde dike. Nat Neurosci. 2007;10(8):1029–37.[PubMed]
27. Svenningsson P, Nairn AC, Greengard P. DARPP-32 navbeynkariya kiryarên gelek dermanên îstismarkirinê dike. Aaps J. 2005;7(2):E353–60. [Gotara belaş PMC] [PubMed]
28. Palmer AA, Verbitsky M, Suresh R, Kamens HM, Reed CL, Li N, Burkhart-Kasch S, McKinnon CS, Belknap JK, Gilliam TC, Phillips TJ. Cûdahiyên derbirrîna genê di mişkan de ji bo hesasiyeta metamfetamînê ji hev cuda hatine hilbijartin. Mamm Genome. 2005;16(5):291–305.[PubMed]
29. Bogush A, Pedrini S, Pelta-Heller J, Chan T, Yang Q, Mao Z, Sluzas E, Gieringer T, Ehrlich ME. AKT û CDK5/p35 navbeynkariya faktora neurotrofî ya ji mêjî ya DARPP-32-ê di neuronên spîndî yên navîn de di vitro de dike. J Biol Chem. 2007;282(10):7352–9.[PubMed]
30. Benavides DR, Bibb JA. Rola Cdk5 di narkotîk û plastîkbûnê de. Ann NY Acad Sci. 2004;1025:335–44.[PubMed]
31. Bibb JA, Chen J, Taylor JR, Svenningsson P, Nishi A, Snyder GL, Yan Z, Sagawa ZK, Ouimet CC, Nairn AC, Nestler EJ, Greengard P. Bandorên rûbirûbûna kronîk a kokaînê ji hêla proteîna neuronal ve têne rêve kirin. Cdk5. Awa. 2001;410(6826):376–80.[PubMed]
32. Blochl A, Sirrenberg C. Neurotrofîn bi rêya receptorên Trk û p75Lntr serbestberdana dopamînê ji neuronên mesencefalî yên mişkê teşwîq dikin. J Biol Chem. 1996;271(35):21100–7.[PubMed]
33. Berton O, McClung CA, Dileone RJ, Krishnan V, Renthal W, Russo SJ, Graham D, Tsankova NM, Bolanos CA, Rios M, Monteggia LM, Self DW, Nestler EJ. Rola bingehîn a BDNF di riya dopamîn a mesolimbic de di stresa têkçûna civakî de. Zanist. 2006;311(5762):864–8.[PubMed]
34. Nestler EJ, Carlezon WA., Jr Di depresyonê de çerxa xelata dopamîn a mesolimbic. Biol Psychiatry. 2006;59(12):1151–9.[PubMed]
35. Ford CP, Beckstead MJ, Williams JT. Astengkirina opioîdê Kappa ya herikên postsynaptîk ên astengker ên dopamîn ên somatodendritic. J Neurophysiol. 2007;97(1):883–91.[PubMed]
36. Nylander I, Vlaskovska M, Terenius L. Pergalên dînorfîn û enkephalin ên mêjî di mişkên Fischer û Lewis de: bandorên tolerans û vekişîna morfînê. Brain Res. 1995;683(1):25–35.[PubMed]
37. Nylander I, Hyytia P, Forsander O, Terenius L. Di pergalên prodynorphin û proenkephalin de di navbera mişkên alkol-tercih (AA) û alkol-dûr (ANA) de cûdahiyên. Alkol Clin Exp Res. 1994;18(5):1272–9.[PubMed]
38. Kreek MJ. Kokaîn, dopamîn û pergala opioîdê ya endogenous. J Addict Dis. 1996;15(4):73–96.[PubMed]
39. Carlezon WA, Jr, Duman RS, Nestler EJ. Gelek rûyên CREB. Trends Neurosci. 2005;28(8):436–45.[PubMed]
40. Dudman JT, Eaton ME, Rajadhyaksha A, Macias W, Taher M, Barczak A, Kameyama K, Huganir R, Konradi C. Receptorên Dopamine D1 navbeynkariya fosforîlasyona CREB bi riya fosforîlasyona receptorê NMDA li Ser897-N dikin. J Neurochem. 1;2003(87):4–922.[PubMed]
41. Xwe DW. Rêzkirina tevgerên narkotîkê û lêgerîna narkotîkê ji hêla neuroadaptasyonên di pergala dopamîn a mesolimbic de. Neuropharmacology. 2004;47 1:242–55.[PubMed]
42. Beitner-Johnson D, Nestler EJ. Morfîn û kokaîn li herêmên xelata mêjî yên dopaminergîk li ser tyrosine hydroxylase çalakiyên kronîk ên hevpar dikin. J Neurochem. 1991;57(1):344–7.[PubMed]
43. Lu L, Grimm JW, Shaham Y, Hêvî BT. Neuroadaptasyonên molekulî yên li mêş û devera tegmental a ventral di 90 rojên pêşîn de dûrketina bi zorê ji xwerêveberiya kokaînê di mişkan de. J Neurochem. 2003;85(6):1604–13.[PubMed]
44. Shepard JD, Chuang DT, Shaham Y, Morales M. Bandora xwe-rêveberiya methamphetamine li ser asta tyrosine hydroxylase û veguhastina dopamine di rêyên dopamine yên mesolimbic û nigrostriatal ên rat de. Psychopharmacology (Berl) 2006; 185 (4): 505-13. [PubMed]
45. Fulton S, Pissios P, Manchon RP, Stiles L, Frank L, Pothos EN, Maratos-Flier E, Flier JS. Rêzkirina leptîn a riya dopamînê ya mesoaccumbens. Neuron. 2006;51(6):811–22.[PubMed]
46. Narita M, Nagumo Y, Miyatake M, Ikegami D, Kurahashi K, Suzuki T. Encama proteîna kinase C di bilindbûna orexin-ê de ji asta dopamine derveyî hucreyî û bandora wê ya xelatdar. Eur J Neurosci. 2007;25(5):1537–45.[PubMed]
47. Narita M, Nagumo Y, Hashimoto S, Khotib J, Miyatake M, Sakurai T, Yanagisawa M, Nakamachi T, Shioda S, Suzuki T. Tevlêbûna rasterast a pergalên orexinergîk di çalakkirina riya dopamine mesolimbic û tevgerên têkildar ên ku ji hêla morfîn. J Neurosci. 2006;26(2):398–405.[PubMed]
48. Borgland SL, Taha SA, Sarti F, Fields HL, Bonci A. Orexin A di VTA-yê de ji bo peydakirina plastîkbûna synaptîk û hestiyarbûna behrê ya ji kokaînê re krîtîk e. Neuron. 2006;49(4):589–601.[PubMed]
49. Park ES, Yi SJ, Kim JS, Lee HS, Lee IS, Seong JK, Jin HK, Yoon YS. Guhertinên di îfadeya orexin-A û neuropeptîd Y de di hîpotalamusa mêşên bi rojî û rûn de tê xwarin. J Vet Sci. 2004;5(4):295–302.[PubMed]
50. Wortley KE, Chang GQ, Davydova Z, Leibowitz SF. Peptîdên ku xwarina xwarinê birêkûpêk dikin: di rewşên hîpertrîglîserîdemia de îfadeya genê orexin zêde dibe. Am J Physiol Regul Integr Comp Physiol. 2003;284(6):R1454–65.[PubMed]
51. Zheng H, Corkern M, Stoyanova I, Patterson LM, Tian R, Berthoud HR. Peptîdên ku xwarina xwarinê birêkûpêk dikin: Manîpulasyona accumbens-ê ku şîret çêdike neuronên oreksîn ên hîpotalamî çalak dike û neuronên POMC asteng dike. Am J Physiol Regul Integr Comp Physiol. 2003;284(6):R1436–44.[PubMed]
52. Baldo BA, Gual-Bonilla L, Sijapati K, Daniel RA, Landry CF, Kelley AE. Aktîvkirina binpopulasyonek neuronên hîpotalamîk ên oreksîn / hîpocretin-dihewîne ji hêla astengkirina navbeynkariya receptorê GABAA-yê ya qaça nucleus accumbens ve, lê ne ji hêla hawîrdorek nû ve. Eur J Neurosci. 2004;19(2):376–86.[PubMed]
53. Harris GC, Wimmer M, Aston-Jones G. Di lêgerîna xelatê de rolek ji bo neuronên oreksîna hîpotalamî ya paşîn. Awa. 2005;437(7058):556–9.[PubMed]