ŞƏRHLƏR: Daha sonrakı araşdırmalar DeltaFosB-nin həm dərman, həm də davranış bağımlılığı üçün ümumi molekulyar keçid olduğunu ortaya qoyacaq. Bu, genlərin açıq və ya söndürülməsini təsir edən bir transkripsiya faktorudur. Başqa bir yerdə deyildiyi kimi, asılılıq yaradan dərmanlar yalnız normal mexanizmləri qaçırır. Buna görə davranış asılılıqlarının mövcud ola bilməyəcəyini irəli sürmək axmaqlıqdır.
Proc Natl Acad Sci ABŞ A. 2001 Sentyabr 25; 98 (20): 11042-11046.
doi: 10.1073 / pnas.191352698.
Eric J. Nestler *, Michel Barrot və David W. Self
Texas Psixiatriya və Təməl Sinirbilim Mərkəzi, Texas Southwestern Tibb Mərkəzi Universiteti, 5323 Harry Hines Bulvarı, Dallas, TX 75390-9070
mücərrəd
Narkomaniyanı xarakterizə edən bəzi davranış anormalliklərinin uzunömürlülüyü nüvə geninin ifadə edilməsinin tənzimlənməsinin istismarın narkotik maddələrindən asılılıq halına gətirdiyi prosesdə iştirak edə biləcəyini irəli sürmüşdür. Məndəlilləri nizamlayan transkripsiyanın faktoru ΔFosB, sui-istifadənin dərmanları, beyin fenotipinə qatqı verən nisbətən sabit dəyişikliklər meydana gətirən bir mexanizmi təmsil edir. ΔFosBFos ailəsinin transkripsiya faktorlarının bir üzvü, bir çox növ narkotik istifadəsi təkrarlanan tətbiq edildikdən sonra, nüvə akumbens və dorsal striatumun (asılılıq üçün vacib olan beyin bölgələri) nöronlarının alt hissəsində toplanır. ΔFosB-nin oxşar yığımı kompulsiv qaçışdan sonra baş verir və bu da ΔFosB kompulsiv davranışların bir çox növünə cavab olaraq yığa bilər. Mühüm olaraq, ΔFosB, qeyri-adi sabitliyindən görə nisbətən uzun müddət ərzində nöronlarda davam edir. Buna görə, ΔFosB dərman pozğunluğu dayandırıldıqdan sonra uzun müddət davam edən gen ifadəsində dəyişiklikləri başladan və sonra da davam etdirə biləcək bir molekulyar mexanizmdir. ΔFosB ya da proteinin dominant mənfi bir inhibitoru olan aşındırıcı transgenik siçanlarda edilən tədqiqatlar ΔFosB sui istifadəsinin dərman davranış təsirlərinə və ehtimal ki, artan narkotik axtarış davranışlarına həssaslığa səbəb olduğunu birbaşa sübut edir. Bu iş, ΔFosB'nin, davamlı olaraq narkotik maddələrin reaksiyalarını asılılığa əsaslanan uzun müddətli sinir və davranışçı plastisiyaya kömək edən nisbətən sabit dəyişikliklərə çevrən davamlı "molekulyar keçid" tipi kimi fəaliyyət göstərməsini dəstəkləyir.
Bağımlılıq tədqiqatları, sui-istifadənin dərmanlarının qarışıqlığı xarakterizə edən davranış anormalliyinə səbəb olmaq üçün beynin dəyişdiyini kompleks yolları anlamaq üzərində dayanır. Bu sahədə kritik çətinliklərdən biri, xüsusilə uzun ömürlü olan davranış anormalliklərini hesablamaq üçün beyində nisbətən sabit bir dərmanla bağlı dəyişiklikləri müəyyən etməkdir. Misal üçün, bir insandan asılı olmayaraq, bir neçə ildir davam etmədikdən sonra da relapsa məruz qalma riskini artırır.
Bu davranış anomaliyalarının sabitliyi, ən azından qismən, gen ifadəsində dəyişikliklər vasitəsilə (1-3) vasitəçilik edə biləcək təkliflərə gətirib çıxardı. Bu baxımdan, bir dərman dərmanına təkrar şəkildə məruz qalma dəridə dərmana həssas olan beyində xüsusi sinapslarda ötürülməni dərhal pozur. Belə nüfuzlar nəhayət hüceyrə içi messenger cascades vasitəsilə nüvə, onlar əvvəl ilk başlayacaq və sonra xüsusi genlərin ifadə dəyişikliklər saxlamaq yerləşir siqnalları. Siqnal ötürücülük yollarının gen ifadəsini təsir edən əsas mexanizmi transkripsiyanın, genlərin tənzimləyici bölgələrinə bağlanan və onların transkripsiyasını dəyişən proteinlərin tənzimlənməsidır.
Bağımlılıq tədqiqatlarının bir məqsədi bu səbəbdən, kasıb istismar dərmanlarının tətbiq olunmasından sonra asılılığa gətirib çıxaran beyin bölgələrində dəyişən transkripsiya faktorlarını təyin etmək olmuşdur. Son on ildə (1-6) bu cür bir neçə transkripsiya faktoru müəyyən edilmişdir. Bu araşdırmanın məqsədi ΔFosB adlanan bir xüsusi transkripsiya faktoru üzərindədir.
ΔFosB'yi İstifadənin Narkotiklərlə İndeksi
FosB geninin kodladığı ΔFosB, F-Fos, FosB, Fra1 və Fra2 (7) daxil olan transkripsiyanın fos ailəsinin üzvüdür. Bu Fos ailə zülalları Jun-ailə zülalları (c-Jun, JunB və ya JunD) ilə heterodimerləşdirirlər və onlar AP-1 (aktivator protein-1) transkripsiyası faktoru ilə əlaqəli AP-1 saytlarına (consensus sequence: TGAC / GTCA) bəzi genlərin təşviqçiləri tənzimləmələrini tənzimləməlidir.
Bu Fos ailə zülalları bir çox sui istifadəsinin kəskin şəkildə tətbiqindən sonra (1-8) xüsusi beyin bölgələrində sürətlə və müvəqqəti olaraq indüklənir. Diqqətli bölgələr dərmanlara davranış reaksiyalarının mühüm vasitəçiləri olan, xüsusən onların mükafatlandırıcı və lokomotor aktivləşdirici effektləri (11, 12) olan nüvə adaçayı və dorsal striatumdur. Bu zülal dərman preparatlarının saatları daxilində bazal səviyyələrə qayıdır.
Şəkil 1
ΔFosB-nin tədricən yığılmasını göstərən sxem digər sui-istifadələrə cavab olaraq Fos ailə zülallarının sürətli və müvəqqəti induksiyasına qarşı. (A) Autoradiogram kronik stimullaşmaya qarşı (1 gün təkrarlanan narkotik dərhal sonra) kəskin stimullaşdırılması (bir narkotik dərhal sonra 2-1 saat) bu müxtəlif proteinlərin diferensial induksiya göstərir. Fosb (52-58-kDa izoformları), FosB (46-kDa izoform) və Fra50 və ya Fra33 ( 1 kDa)] nüvəli akumbens və dorsal striatal neyronlarda istifadənin bir dərmanının kəskin şəkildə tətbiqi ilə nəticələnir. Həm də ΔFosB (2-40 kDa) biokimyəvi modifikasiyalı isoformlar əmələ gəlir; Onlar da dərman preparatlarının verilməsindən sonra (aşağı səviyyədə olmasına baxmayaraq) endirilir, lakin uzun müddət ərzində onların sabitliyinə görə beynində davam edirlər. (C) Təkrarlanan (məsələn, gündəlik olaraq iki dəfə) dərman vasitəsinin tətbiqi ilə hər bir kəskin stimulyasiya ΔFosB izoformlarının aşağı səviyyəsini azaldır, bu da hər bir kəskin stimulun yaratdığı ΔFosB göstəricisini əks etdirən üst-üstə düşən xətlərin alt dəsti ilə ifadə edilir. Nəticədə xroniki müalicə kursu zamanı təkrarlanan stimullar ilə ΔFosB-nin ümumi səviyyələrində tədricən artım müşahidə olunur və bu, grafiğin artan addımlı xətti ilə ifadə edilir.
Çox fərqli cavablar sui-istifadənin xroniki tətbiqindən sonra görülür (Şəkil 1). FosB (molekulyar kütlə 35-37 kDa) biokimyəvi modifikasiya edilmiş izoformları təkrarlanan narkotik dərhal sonra eyni beyin bölgələrində toplanır, digər bütün Fos ailə üzvləri isə tolerantlığı göstərirlər (yəni, ilkin narkotik maddələri ilə müqayisədə azalmış indüksiya). ΔFosB'nin bu cür yığımı kokain, morfin, amfetamin, spirt, nikotin və feniksididin üçün müşahidə edilmişdire (11, 14-18). Bu induksiyanın bu beyin bölgələrində (15, 17) yerləşən orta beyin nöronlarının dynorphin / substance P-tərkib alt qrupu üçün seçici olduğuna dair bəzi sübutlar mövcuddur, baxmayaraq bunun müəyyən edilməsi üçün daha çox işə ehtiyac var. 35-37-kDa ΔFosB izoformları bu beyin bölgələrində (1, 19) aktiv və uzunmüddətli AP-20 kompleksi yaratmaq üçün JunD ilə dimerize olunur. Bu ΔFosB izoformları qeyri-adi uzun yarım ömürlər (21) səbəbiylə kronik narkotik dərinliyi ilə yığılır və bu səbəblə dərman tətbiqinin dayandırılmasından ən az bir həftə sonra nöronlarda davam edir. Qeyd edək ki, bu ΔFosB izoformları dərhal erkən genin (fosB) yüksək sabit məhsuludur. ΔFosB izoformlarının sabitliyi yeni bir molekulyar mexanizm təmin edir ki, bununla yanaşı, gen ifadəsində dərmanla bağlı dəyişikliklər narkotikdən çəkilmənin nisbətən uzun müddətinə baxmayaraq davam edə bilər.
Nüvə akumbensi sui istifadəsinin dərman vasitələrinin təsirli təsirlərində kritik bir rol oynasa da, qida, içki, cinsiyyət və sosial qarşılıqlı təsirlər (12, 13) kimi təbii gücləndiricilərə cavab verərək normal fəaliyyət göstərdiyinə inanılır. Nəticədə, bu beyin bölgəsinin digər kompulsiv davranışlarda (məsələn, patoloji aşırma, qumar, məşq və s.) Mümkün rolunda böyük maraq var. Bu səbəblə, ΔFosB'nin kompulsif çalışan bir heyvan modelində tənzimlənib olub-olmadığını araşdırdıq. Həqiqətən, ΔFosB-nin stabil 35-37-kDa izoformları sıxlıqlarda kompulsiv qaçış davranışını göstərən nüvəli akumbenslər içində seçicidir.
Durable ΔFosB Isoforms Biyokimyəvi Kimlik
Yuxarıda qeyd etdiyimiz kimi, sui-istifadənin və ya kompulsif bir dərmanın xroniki tətbiqindən sonra toplanan ΔFosB izoformları 35-37 kDa molekulyar kütləini göstərir. Onlar bir narkotik dərhal sonra (33, 1, 14) bir sürətlə, lakin sürətlə endirimli olan ΔFosB'nin 19-kDa izoformundan fərqləndirilə bilər. Aktual sübutlar 22-kDa izoformunun daha sabit 33-35-kDa məhsullarına (37, 19) çıxmaq üçün dəyişdirilmiş olan proteinin doğma forması olduğunu göstərir. Ancaq qeyri-sabit 21-kDa izoformunu sabit 33-35-kDa izoformlarına çevirən biyokimyəvi modifikasiyanın təbiəti qaranlıq qalmışdır. Fosforilasiyanın məsuliyyətdən (37) məsuliyyəti ola bilər. Məsələn, ΔFosB'nin induksiyası DARPP-11, striatal zənginləşdirilmiş protein (32, 23) olmayan siçanlarda zəiflədilir. DARPP-24, protein fosfataz-32 və protein kinaz A (1, 25) katalitik fəaliyyətini tənzimləyən üçün, bu proteinin stabil ΔFosB izoformlarının normal toplanması üçün tələbi bu sabit məhsulların yaranmasında fosforiliyaya imkan verə bilər.
Davranış plastisitesinde ΔFosB'nin suiistimallığa olan rolu
Narkotik asılılığında ΔFosB rolu anlayışı böyük ölçüdə ΔFosB'nin nüvə adacığına və yetkin heyvanların digər striatal bölgələrinə (27, 28) daxilində selektiv şəkildə tətbiq oluna biləcəyi transgenik siçanların öyrənilməsindən gəldi. Əhəmiyyətli olaraq, bu siçanlar, ΔFosB'yi, narkotik maddələrin proteinə səbəb olacağına inanıldığı dynorphin / substance P-containing orta şişkin neyronları ilə seçicidir. Xroniki narkotik təsirindən sonra heyvanlara bənzəyir olan ΔFosB-overexpressing siçanların davranış fenotipi Cədvəl 1-da öz əksini tapmışdır. Siçanlar kəskin və xroniki idarədən (28) sonra kokainə lokomotor reaksiyaları artırır. Onlar həmçinin kokain və morfinin yerin şişkinlik analizlərində (11, 28) mükəmməl təsirlərinə qarşı həssaslığını göstərirlər və ΔFosB'yi aşmayan littermatesdən daha az dozada kokainin özünü idarə edəcəklər ‡ Bunun əksinə, bu heyvanlar normal vəziyyətdə lokomotor Morris su labirentində (28) kokainə qarşı həssaslaşma və normal məkan öyrənmə. Tbu məlumatlara görə ΔFosB heyvanın kokainə və bəlkə də digər sui-istifadə dərmanlarına həssaslığını artırır və dərmanlara nisbətən uzun müddət həssaslaşma mexanizmini təmsil edə bilər..
 striatum
striatum
| Kəskin və təkrarlanan kokain tətbiqinə cavab olaraq artan lokomotor aktivasiya. |
| Kondisioner yoxlamasında yerlərdə kokain və morfinə cavablandırıcı cavablar artır. |
| Aşağı dozada kokainin özünü idarə etməsinin artması. |
| Kokain üçün mütərəqqi nisbət testlərində artan motivasiya. |
| Spirtə anksiolitik cavabların artması. |
| Artan kompulsiv qaçış davranışı. |
Refs məlumatlarına əsaslanaraq. 28 və 29.† ‡ §¶
Nüvə accumbens-dorsal striatumda ΔFosB tərəfindən vasitəçilik davranışçı plastisitə
IBundan əlavə, ΔFosB-nin təsirləri dərman həssaslığı tənzimlənməsindən kənara çıxa bilər ki, ilkin sübutlar var ki, bu da addiction prosesi ilə bağlı daha kompleks davranışlara gətirib çıxara bilər. ΔFosB ifadə edən siçanlar, mütərəqqi nisbətdə özünüidarə analizlərində özünü idarə edən kokain üçün daha çox iş görürΔFosB heyvanları kokainin motivasiya motivasion xüsusiyyətlərinə həssaslaşdıra bilər və bununla da narkotik maddənin çəkildikdən sonra relapsa meyli olur‡ ΔFosB-ifadə edən siçanlar da spirtin anksiolitik təsirlərinin, § insanlarda artan spirt alışı ilə əlaqəli bir fenotipin göstəricisidir. Birlikdə bu erkən tapıntılar ΔFosB, sui-istifadəyə qarşı həssaslığın artırılmasına əlavə olaraq, narkotik maddələrdən istifadə davranışını təşviq edən davranışlarda keyfiyyət dəyişiklikləri meydana gətirir. Beləliklə, ΔFosB müstəqil dövlətin mühüm aspektlərini başlamağa və sonra da təmin etməyə kömək edən davamlı "molekulyar keçid" kimi fəaliyyət göstərə bilər. Cari tədqiqat zamanı əhəmiyyətli bir sual, ΔFosB səviyyələri normallaşdırıldıqdan sonra (aşağıya baxın) sonra dərman dərmanı dövründə ΔFosB yığılmasının narkotik çıxarılma davranışını uzadılmış çəkiliş dövrlərindən sonra yaradıb-verməməsidir.
Adult nüvəli akumbens və dorsal striatumda selektiv şəkildə ΔFosB'yi seçici olaraq nəzarət edən littermates ilə müqayisədə daha kompulsif qaçış nümayiş etdirir. † Bu müşahidələr bu neyronlar içərisində ΔFosB yığılmasının vərdiş xatirələrinin formalaşmasında və saxlanmasında daha çox ümumi rol oynadığını və kompulsif bu neyronların fəaliyyət göstərdiyi neyron sxemlərin effektivliyini gücləndirərək bəlkə də davranışlar.
ΔFosB, kokainə xroniki məruz qaldıqdan sonra, nüvəsiz acumbens və dorsal striatum xaricində müəyyən beyin bölgələrində birikir. Bunlar arasında məşhurdur bölgələr amigdala və medial prefrontal korteksdir (15). Mövcud tədqiqatların əsas məqsədi bu bölgələrdə ΔFosB induksiyasını addiction fenotipinə aid etməkdir.
Əvvəllər fosB nakavt siçanları üzərində iş bu heyvanların yuxarıda göstərilən ΔFosB-həddindən artıq ifadə edən siçanların tapıntıları ilə uyğun olan kokainin lokomotor təsirlərinə qarşı həssaslaşma inkişaf etdirmədiklərini ortaya çıxardı (22). Bununla birlikdə, fosB mutantları, kokainin kəskin təsirlərinə qarşı həssaslığı artırdı və bu digər tapıntılarla ziddiyyət təşkil etdi. FosB mutantları ilə tapıntıların təfsiri, bu heyvanlarda yalnız ΔFosB deyil, həm də tam uzunluqlu FosB-nin olmaması ilə mürəkkəbdir. Üstəlik mutantlarda beyində və inkişafın ilk mərhələlərində həm zülal var. Həqiqətən, daha yeni iş ΔFosB həddindən artıq eksprese edən siçanların nəticələrini dəstəkləyir: selectFosB dominant mənfi antaqonisti rolunu oynayan c-Jun kəsilmiş bir mutantının induktiv həddindən artıq ekspresiyası, seçici olaraq nüvə akumbensləri və dorsal striatumda kokainin mükafatlandırıcı təsirlərinə həssaslıq azalır. .¶ Bu tapıntılar siçanların qurucu mutasiyalarla nəticələrinin təfsirində istifadə edilməli olan diqqəti vurğulayır və yetkin beyində plastiklik araşdırmalarında induksiya edilə bilən və hüceyrə tipli mutasiyalara sahib siçanların əhəmiyyətini göstərir.
ΔFosB üçün hədəf genləri
Çünki ΔFosB bir transkripsiya faktoru olduğundan, ehtimal ki, protein digər genlərin ifadəsindəki dəyişikliklər nəticəsində davranış plastisitesinə səbəb olur. ΔFosB fosB geninin alternativ birləşməsi ilə yaranır və tam uzunluqlu FosB-də olan C-terminal transaktivasiya sahəsinin bir hissəsi yoxdur. Nəticədə, ΔFosB transkripsiyası repressor (29) kimi fəaliyyət göstərir. Lakin, hüceyrə mədəniyyətində iş göstərmişdir ki, ΔFosB ya təzyiq və ya təzyiq edə bilər AP-1-mediated transkripsiyası istifadə olunan AP-1 saytından asılı olaraq (21, 29-31). Tam uzunluqlu FosB, bəzi promoser fraqmentləri ilə ΔFosB kimi eyni effektlər verir, lakin başqalarına müxtəlif təsirlər göstərir. ΔFosB və FosB-nin müxtəlif tədbirlərindən ibarət olan mexanizmləri anlamaq üçün daha çox iş aparmaq lazımdır.
Qrupumuz, ΔFosB üçün hədəf genlərini təyin etmək üçün iki yanaşma istifadə etdi. Bunlardan biri namizəd gen yanaşmasıdır. Əvvəlcə α-amino-3-hidroksi-5-metil-4-izoksazolepropionik turşu (AMPA) glutamat reseptorlarını, nüvə akumbensində glutamaterjik ötürülmənin vacib rolunu nəzərə alaraq, ehtimal olunan hədəflər kimi qəbul etdik. Bu günə qədər aparılan işlərdən biri, müəyyən bir AMPA glutamat reseptoru alt birliyinin, GluR2'nin, ΔFosB üçün vicdanlı bir hədəf ola biləcəyini göstərmişdir (Şəkil 2). GluR2 ifadəsi, lakin digər AMPA reseptorları alt birləşmələrinin ifadəsi deyil, ΔFosB (28) -nin həddindən artıq ekspresyonu ilə nüvə akumbenslərində artır (lakin dorsal striatumda deyil) və dominant mənfi mutantın ifadəsi kokainin zülalı əmələ gətirmə qabiliyyətini zəiflədir. Bundan əlavə, GluR2 geninin təbliğatçısı, ΔFosB'yi bağlayan bir konsensus AP-1 saytını ehtiva edir (28). Virus-vasitəçiliyi ilə gen ötürülməsindən istifadə edərək nüvəli akumbenslərdə GluR2-nin həddindən artıq ekspresiyası, heyvanın kokainin faydalı təsirlərinə həssaslığını artırır və bununla da ΔFosB ifadə edən siçanlarda görülən fenotipin bir hissəsini təqlid edir (28). GluR2 induksiyası, xroniki kokain tətbiqindən sonra nüvə akumbens nöronlarının AMPA reseptor agonistlərinə azalmış elektrofizyoloji həssaslığını hesaba gətirə bilər (32), çünki GluR2 ehtiva edən AMPA reseptorları ümumi keçiriciliyi azaltmış və Ca2 + keçiriciliyi azaltmışdır. Bu neyronların həyəcan verici girişlərə reaksiya səviyyəsinin azalması daha sonra sui-istifadə dərmanına reaksiyanı artıra bilər. Bununla birlikdə, nüvə akumbenslərindəki dopaminerjik və glutamaterjik siqnalların asılılıq davranışını tənzimləməsinin yolları bilinmir; bunun üçün hələ mövcud olmayan bir sinir dövrü anlayış səviyyəsi lazımdır.
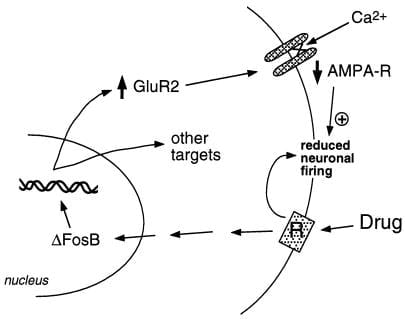
Şəkil 2
AMPA glutamat reseptor alt birliyi, GluR2, ΔFosB üçün nəzərdə tutulmuş bir hədəfdir. GluR2-nin ΔFosB-vasitəçiliyi ilə induksiyanın nüvə akumbens nöronlarının fizioloji reaksiyasını necə dəyişdirə biləcəyi və sui-istifadə dərmanlarına həssas reaksiyalara səbəb ola biləcəyi göstərilir. Bu sxemə görə, sui-istifadə dərmanları, nüvə accumbens nöronlarının inhibisyonu yolu ilə kəskin gücləndirici təsirlərini yaradır. Təkrarlanan məruz qalma ilə, dərmanlar GluR2 daxil olmaqla çoxsaylı hədəf genlərini tənzimləyən ΔFosB əmələ gətirir. Bu, GluR2 alt birliyini ehtiva edən nüvə akumbens nöronlarında AMPA reseptorlarının (AMPA-R) nisbətini artırır ki, bu da ümumi AMPA cərəyanının azalmasına və Ca2 + cərəyanının azalmasına səbəb olur. Bu azalmış həyəcan neyronları dərmanların kəskin inhibitor təsirlərinə və bununla da dərmanların gücləndirici təsirlərinə daha həssas edə bilər..
ΔFosB üçün başqa bir ehtimal hədəf dynorphin kodlayan gendir. Daha əvvəl də qeyd edildiyi kimi, dynorphin, ΔFosB'nin induksiyasını göstərən nüvəli accumbens orta sürünən nöronların. Dynorphin intercellular bir geribildirim loopunda işlədilir: onun buraxılması orta spiny neyronları innervasiya edən dopaminergik nöronları, nucleus accumbenslərində dopaminergik sinir terminalleri üzərində olan opioid reseptorları və ventral tegmental sahədə hüceyrə orqanları və dendritləri (Şəkil 3) (33-35). Bu ideya, bu iki beyin bölgəsinin hər ikisinə tətbiq edilərkən, κ reseptor agonistinin narkotik dərinliyini azaltmaq qabiliyyətinə uyğun gəlir.d (35).
R≥FosB, ΔFosB induksiyası ilə görüldü mükafat mexanizmlərinin artmasına kömək edə biləcək "dynorphin" ifadəsini azaldır. Maraqlıdır ki, başqa bir narkotik tənzimlənən transkripsiyaya səbəb olan faktiki CREB (cAMP reaksiya elementi bağlayıcı protein) (2, 3) əks təsir göstərir: nüvə akumbensində dinorfin ifadəsini incələyir və kokain və morfinin mükəmməl xüsusiyyətlərini azaldır (4).
BCREB-in dərman vasitəsi ilə əmələ gəlməsinin aktivləşdirilməsi dərman preparatından sonra sürətlə yayılır, CREB və ΔFosB tərəfindən dynorphinin qarşılıqlı tənzimlənməsi tənbəl emosional simptomlar və erkən mərhələlərdə azalmış dərman həssaslığı ilə başlayan erkən və gec mərhələlərdə meydana gələn qarşılıqlı davranış dəyişikliklərini izah edə bilər sonrakı zaman nöqtələrində üstünlük təşkil edən dərman vasitələrinin mükafatlandırılması və stimullaşdırıcı motivasiya təsirlərinə qarşı həssaslıq və həssaslıq.
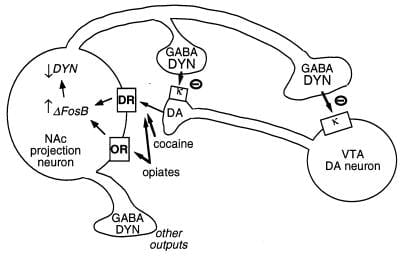
Şəkil 3
Dynorphin, ΔFosB üçün nəzərdə tutulan hədəfdir. Dynorphin (DYN) ifadəsini əks etdirən bir nüvə accumbens (NAc) GABAergic proyeksiya nöronu bir sinir innervating bir ventral tegmental sahəsi (VTA) dopamin (DA) nüvəsidir. Dynorphin bu dövrədə bir geribildirim mexanizminə xidmət edir: NAc neyronlarının terminlərindən sərbəst buraxılan dynorphin, sinir terminalı və OP nöronlarının hüceyrə orqanlarında fəaliyyət göstərən ∞ opioid reseptorlarına təsir göstərir və onların fəaliyyətini maneə törədir. ΔFosB, dynorphin ifadəsini maneə törətməklə, bu geribildirim döngəsini aşağı sala bilər və sui-istifadənin təbii xüsusiyyətlərini artırır. Göstərilməmiş bu sistemdə CREB-in qarşılıqlı təsiridir: CREB dynorphin ifadəsini gücləndirir və bununla da narkotik maddələrin təltif xüsusiyyətlərini azaldır (4). GABA, γ-aminobütirik turşusu; DR, dopamin reseptoru; OR, opioid reseptoru.
ΔFosB üçün hədəf genləri müəyyənləşdirmək üçün istifadə olunan ikinci yanaşma, DNT mikroarray analizini əhatə edir. ΔFosB-nin induksiya edilə bilən həddindən artıq ekspresiyası nüvə akumbensindəki çoxsaylı genlərin ekspresyonunu artırır və ya azaldır (36). İndi bu genlərin hər birini ΔFosB-nin fizioloji hədəfləri kimi təsdiqləmək və onların asılılıq fenotipinə verdiyi töhfəni anlamaq üçün xeyli iş aparılmasına ehtiyac olmasına baxmayaraq, vacib bir hədəf Cdk5 (siklinə bağlı kinaz-5) kimi görünür. Beləliklə, Cdk5 əvvəlcə arrFosB ilə tənzimlənən mikroarayların istifadəsi ilə təyin olundu və daha sonra xroniki kokain tətbiqindən sonra nüvə akumbensləri və dorsal striatumda induksiya edildiyi göstərildi (37). ΔFosB, cdk5 genini genin təbliğatçısı (1) içərisində olan bir AP-36 saytı vasitəsilə aktivləşdirir. Birlikdə, bu məlumatlar, kokainin brainFosB vasitəsilə bu beyin bölgələrində Cdk5 ifadəsini induksiya etdiyi bir sxem dəstəkləyir. Cdk5 induksiyası, protein fosfataz-32 inhibitorundan protein kinaz A inhibitoruna Cdk37 tərəfindən fosforiləşdirildikdən sonra DARPP-1 (5) artan fosforillənmə yolu ilə dopaminerjik siqnalları qismən dəyişdirir.
"Qalıcı" plastisitənin sui-istifadəyə vasitəçilik edilməsində ΔFosB'nin rolu
ΔFosB siqnal nisbətən uzun ömürlü olmasına baxmayaraq, qalıcı deyil. ΔFosB tədricən azalır və 1-2 aydan sonra narkotik maddənin çəkilməsindən sonra beyində aşkar edilə bilməz, baxmayaraq ki, müəyyən davranış anomaliyaları daha uzun müddət ərzində davam edir. Buna görə, ΔFosB, bu yarımdavamlı davranış anormalliklerine vasitəçilik edə bilməyəcək. Bağımlılığı ilə bağlı olduqca sabit davranış dəyişikliyinə səbəb olan molekulyar adaptasiyaları tapmaqda çətinlik, öyrənmə və yaddaş sahəsində qarşılaşdıqları çətinliklərə bənzəyir. Zərif mobil və molekulyar öyrənmə və yaddaş modelləri olmasına baxmayaraq, çox sabit davranış anılarını hesablamaq üçün kifayət qədər uzun ömürlü olan molekulyar və hüceyrəli adaptasiyaları müəyyən etmək mümkün olmayıb. Həqiqətən, ΔFosB, yalnız sui-istifadə dərmanlarına cavab olaraq deyil, digər narahatlıqlara da (lezyonları daxil etmir) reaksiya olaraq, yetkin beyində meydana gəldiyi bilinən ən uzun müddətli bir uyğunlaşmadır. Bu uyğunsuzluğu nəzərə almaq üçün həm asılılıq, həm öyrənmə, həm də yaddaş sahələrində iki təklif inkişaf etmişdir.
Bir ehtimal ki, ΔFosB ya da digər transkripsiya faktları (məsələn, CREB) vasitəsilə vasitəçilik edənlər kimi gen ifadəsində daha çox keçici dəyişikliklər, nöronal morfologiya və sinaptik quruluşda daha uzun müddətli dəyişikliklərə vasitəçilik edə bilər. Misal üçün, Dendritik spinlerin sıxlığının artması (xüsusilə iki başlı sümüklərin artması) müşayiət olunur glutamateriqik sinapsların effektivliyini artırır uzun müddətli potensiasiya (38-40) zamanı hipokampal piramidal nöronlarda və nüvə accumbens (41) orta sünbül neyronları səviyyəsində araşdıran kokainə artan davranış həssaslığına paraleldir. Ən azı 1 aylıq dərmanların çəkilməsinə davam edilsə də, bu cür struktur dəyişikliklərinin davranışda olduqca sabit dəyişikliklər üçün kifayət qədər uzun ömürlü olub-olmaması məlum deyil. Son sübutlar ΔFosB və Cdk5'in induksiyası, nüvəsindəki akumbenslərdə sinaptik strukturda dərmanla bağlı dəyişikliklərin vasitəçisidir (Şəkil 4). Beləliklə, bir Cdk5 inhibitorunun nüvəli akumbensə infuziyası Təkrarlanan kokain pozuntusunun bu bölgədə dendritik bel yoğunluğunu artırma qabiliyyəti. Bu beyində zənginləşdirilmiş Cdk5'in nöral quruluşu və böyüməsini tənzimləyir (baxın: 36 və 37). Nöronal morfologiyada bu dəyişikliklər ΔFosB siqnalının özündən çox ola biləcəyini sübut etməsə də mümkündür.
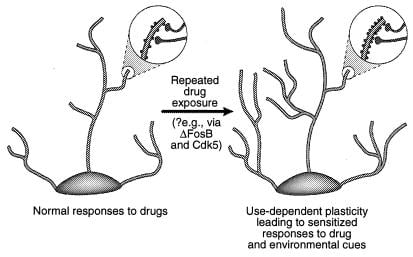
Şəkil 4
Dendritik quruluşun sui-istifadə dərmanları ilə tənzimlənməsi. Nüvə hüceyrələri və prefrontal korteksdə kokain ilə müşahidə edildiyi kimi bir sui-istifadə dərmanına xroniki məruz qaldıqdan sonra bir neyronun dendritik ağacının genişlənməsi göstərilir (41). Böyütmə sahələri aktivləşdirilmiş sinir terminalları ilə birlikdə meydana gəldiyi bildirilən dendritik bellərdə bir artım göstərir. Dendritik bel sıxlığındakı bu artım ΔFosB və bunun nəticəsində Cdk5 induksiyası vasitəsilə vasitəçilik edə bilər (mətnə bax). Bəzi öyrənmə modellərində müşahidə olunanlara bənzər dendritik quruluşdakı bu cür dəyişikliklər (məsələn, uzunmüddətli gücləndirmə), sui-istifadə və ya ətraf mühitin qorunması dərmanlarına qarşı uzun ömürlü həssas cavablara vasitəçilik edə bilər. [Əmlakın icazəsi ilə çoxaldılmışdır. 3 (Müəllif hüquqları 2001, Macmillian Magazines Ltd.)].
Digər bir ehtimal ki, transkripsiya faktoru (məsələn, ΔFosB, CREB) xromati modifikasiyası vasitəsilə gen ifadəsində daha daimi dəyişikliklərə gətirib çıxarırn. Bu və bir çox başqa transkripsiya faktoru genin ətrafında olan histonların (42) müvafiq olaraq asetiliyin və deasetiliyenin təşviq edilməsi nəticəsində hədəf geninin transkripsiyasını aktivləşdirməyə və ya repressiya etməyə inanılır. Histonun bu cür asetiliyin və deasetiliyinin çox tez görülə biləcəyinə baxmayaraq, ΔFosB və ya CREB histonun asetiliyasını idarə edən enzimatik maşında uzunmüddətli uyğunlaşma təmin edə bilər. ΔFosB ya da CREB inkişaf zamanı baş verən gen transkripsiyonundakı qalıcı dəyişikliklərə toxunan kromatinin digər modifikasiyalarını (məsələn, DNT və ya histon metilatı) tənzimləyərək gen ifadəsində daha uzun müddətli dəyişiklikləri təşviq edə bilər (bax: 42 və 43) . Bu ehtimallar spekulyativ qalmasına baxmayaraq, bir sui-istifadəyə (və ya digər bir narahatlığa) keçid uyğunlaşmalarının əsas ömür boyu davranış nəticələrinə gətirib çıxaran bir mexanizm təmin edə bilər.
References
- â † μ
- Nestler EJ,
- Ümid edirəm BT,
- Widnell KL
(1993) Neuron 11: 995-1006.
- â † μ
- Berke JD,
- Hyman SE
(2000) Neuron 25: 515-532.
- â † μ
- Nestler EJ
(2001) Nat Rev Neurosci 2: 119-128.
- â † μ
- Carlezon WA Jr,
- Thome J,
- Olson VG,
- Lane-Ladd SB,
- Brodkin ES,
- Hiroi N,
- Duman RS,
- Neve RL,
- Nestler EJ
(1998) Elm 282: 2272-2275.
- O'Donovan KJ,
- Tourtellotte WG,
- Millbrandt J,
- Baraban JM
(1999) Trends Neurosci 22: 167-173.
- â † μ
- Mackler SA,
- Korutla L,
- Cha XY,
- Koebbe MJ,
- Fournier KM,
- Bowers MS,
- Kalivas PW
(2000) J Neurosci 20: 6210-6217.
- â † μ
- Morgan JI,
- Curran T
(1995) Trends Neurosci 18: 66-67.
- â † μ
- Gənc ST,
- Porrino LJ,
- Iadarola MJ
(1991) Proc Natl Acad Sci ABŞ 88: 1291-1295.
- Graybiel AM,
- Moratalla R,
- Robertson HA
(1990) Proc Natl Acad Sci ABŞ 87: 6912-6916.
- Ümid B,
- Kosofski B,
- Hyman SE,
- Nestler EJ
(1992) Proc Natl Acad Sci ABŞ 89: 5764-5768.
- â † μ
- Kelz MB,
- Nestler EJ
(2000) Curr Opin Neurol 13: 715-720.
- â † μ
- Koob GF,
- Sanna PP,
- Bloom FE
(1998) Neuron 21: 467-476.
- â † μ
- Wise RA
(1998) Drug Alkol Bağlılığı 51: 13-22.
- â † μ
- Ümid edirəm BT,
- Nye HE,
- Kelz MB,
- Self DW,
- Iadarola MJ,
- Nakabeppu Y,
- Duman RS,
- Nestler EJ
(1994) Neuron 13: 1235-1244.
- â † μ
- Nye H,
- Ümid edirəm BT,
- Kelz M,
- Iadarola M,
- Nestler EJ
(1995) J Pharmacol Exp Ther 275: 1671-1680.
- Nye HE,
- Nestler EJ
(1996) Mol Pharmacol 49: 636-645.
- â † μ
- Moratalla R,
- Elibol B,
- Vallejo M,
- Graybiel AM
(1996) Neuron 17: 147-156.
- â † μ
- Pich EM,
- Pagliusi SR,
- Tessari M,
- Talabot-Ayer D,
- Hooft van Huijsduijnen R,
- Chiamulera C
(1997) Elm 275: 83-86.
- â † μ
- Chen JS,
- Nye HE,
- Kelz MB,
- Hiroi N,
- Nakabeppu Y,
- Ümid edirəm BT,
- Nestler EJ
(1995) Mol Pharmacol 48: 880-889.
- â † μ
- Hiroi N,
- Brown J,
- Ye H,
- Saudou F,
- Vaidya VA,
- Duman RS,
- Greenberg ME,
- Nestler EJ
(1998) J Neurosci 18: 6952-6962.
- â † μ
- Chen J,
- Kelz MB,
- Ümid edirəm BT,
- Nakabeppu Y,
- Nestler EJ
(1997) J Neurosci 17: 4933-4941.
- â † μ
- Hiroi N,
- Brown J,
- Haile C,
- Ye H,
- Greenberg ME,
- Nestler EJ
(1997) Proc Natl Acad Sci ABŞ 94: 10397-10402.
- â † μ
- Fienberg AA,
- Hiroi N,
- Mermelstein P,
- Song WJ,
- Snyder GL,
- Nishi A,
- Cheramy A,
- O'Callaghan JP,
- Miller D,
- Cole DG,
- et al.
(1998) Elm 281: 838-842.
- â † μ
- Hiroi N,
- Feinberg A,
- Haile C,
- Greengard P,
- Nestler EJ
(1999) Eur J Neurosci 11: 1114-1118.
- â † μ
- Greengard P,
- Allen PB,
- Nairn AC
(1999) Neuron 23: 435-447.
- â † μ
- Bibb JA,
- Snyder GL,
- Nishi A,
- Yan Z,
- Meijer L,
- Fienberg AA,
- Tsai LH,
- Kwon YT,
- Girault JA,
- Czernik AJ,
- et al.
(1999) Təbiət (London) 402: 669-671.
- â † μ
- Chen JS,
- Kelz MB,
- Zeng GQ,
- Sakai N,
- Steffen C,
- Shockett PE,
- Picciotto M,
- Duman RS,
- Nestler EJ
(1998) Mol Pharmacol 54: 495-503.
- â † μ
- Kelz MB,
- Chen JS,
- Carlezon WA,
- Whisler K,
- Gilden L,
- Beckmann AM,
- Steffen C,
- Zhang YJ,
- Marotti L,
- Self SW,
- et al.
(1999) Təbiət (London) 401: 272-276.
- â † μ
- Dobrazanski P,
- Noguchi T,
- Kovary K,
- Rizzo CA,
- Lazo PS,
- Bravo R
(1991) Mol Cell Biol 11: 5470-5478.
- Nakabeppu Y,
- Nathans D
(1991) Cell 64: 751-759.
- â † μ
- Yen J,
- Wisdom RM,
- Tratner I,
- Verma IM
(1991) Proc Natl Acad Sci ABŞ 88: 5077-5081.
- â † μ
- Ağ FJ,
- Hu XT,
- Zhang XF,
- Wolf ME
(1995) J Pharmacol Exp Ther 273: 445-454.
- â † μ
- Hyman SE
(1996) Neuron 16: 901-904.
- Kreek MJ
(1997) Pharmacol Biochem Behav 57: 551-569.
- â † μ
- Shippenberg TS,
- Rea W.
(1997) Pharmacol Biochem Behav 57: 449-455.
- â † μ
- Chen JS,
- Zhang YJ,
- Kelz MB,
- Steffen C,
- Ang ES,
- Zeng L,
- Nestler EJ
(2000) J Neurosci 20: 8965-8971.
- â † μ
- Bibb JA,
- Chen JS,
- Taylor JR,
- Svenningsson P,
- Nishi A,
- Snyder GL,
- Yan Z,
- Sagawa ZK,
- Nairn AC,
- Nestler EJ,
- et al.
(2001) Təbiət (London) 410: 376-380.
- â † μ
- Luscher C,
- Nicoll RA,
- Malenka RC,
- Muller D
(2000) Nat Neurosci 3: 545-550.
- Malinow R,
- Mainen ZF,
- Hayashi Y
(2000) Curr Opin Neurobiol 10: 352-357.
- â † μ
- Scannevin RH,
- Huganir RL
(2000) Nat Rev Neurosci 1: 133-141.
Robinson, TE & Kolb, B. (1999) (1997) Avro. J. Neurosci.11, 1598-1604.
- â † μ
- Carey M,
- Smale ST
(2000) Eukaryotlarda transkripsiya tənzimlənməsi (Cold Spring Harbor Lab, Press, Plainview, NY).
- â † μ
- Spencer VA,
- Davie JR
(1999) Gen 240: 1-12.
HighWire Press bu məqaləyə istinadən məqalələr yazdı
- Təbii və Narkotik maddələri mükafatlandırılması üçün əsas vasitəçi olaraq {Delta} FosB J. Neurosci. 2013 33 (8) 3434-3442
- Narkotik, Cinayət və Hedonik Allostazın Epigenetiği Müasir Cəza Məhkəməsi 2012 28 (3) 314-328 jurnalı
- mücərrəd
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- mücərrəd
- Tam Mətn (HTML)
- Tam Mətn (PDF)
- Morfin, Dorsal Kök Ganglion Neyronlarından Tükənən F1 hüceyrələrində 1 / 2-dən Extracellular Siqnal-tənzimlənən Kinazlar vasitəsilə 27 Altı Bənzər Transkripsiya Faktoru-11 / J. Pharmacol. Exp. Ther. 2012 342 (1) 41-52
- Bir Gateway Dərmanı üçün Molekulyar Mexanizm: Kokain tərəfindən Nikotin Baş Genə İfadə Edilən Epigenetik dəyişikliklər Sci Transl Med 2011 3 (107) 107ra109
- Təkamülü Sucrose və Kokain Self-Administration və Cue-Induced Drug Mice Midbrain Dopamin Neurons VGLUT2 zərər sonra axtaran J. Neurosci. 2011 31 (35) 12593-12603
- Xroniki aralıq hipoksi, mərkəzi otonom bölgələrdə qan təzyiqi və FosB / {Delta} FosB ifadəsini artırır Am. J. Physiol. Regul. Integr. Comp. Fiziol. 2011 301 (1) R131-R139
- GPR37 / PAEL reseptorunun olmaması striatal Akt və ERK2 fosforiliyi, {Delta} FosB ifadəsini və amfetamin və kokainə şərti yerin üstünlüklərini pozur FASEB J. 2011 25 (6) 2071-2081
- Molekulyar Toleransın Başlanğıc Alkolun Təsirinin və Davamlılığının Arasındaki İlişki Markedly Doğrusal Olmayan J. Neurosci. 2011 31 (7) 2436-2446
- Vivo Bioluminescence Görüntüləmədə Renovasküler Hipertansiyonlu Siçanların Paraventricular Nucleus'unda Redox-Aktivləşdirən Aktivator Protein-1 Aktivləşdirməsi Açar Hipertansiyon 2011 57 (2) 289-297
- {Delta} FosB'nin Striatal Üstünlükü Kronik Levodopa İndüktörlü Sülh hərəkətləri J. Neurosci. 2010 30 (21) 7335-7343
- Böyük Psixik Bozukluklarda Çevresel Etkilerin Epigenetik Aracılığı Şizofr Bull 2009 35 (6) 1045-1056
- Yaşamaqda olan amfetaminin kronik maruz qalmasının spesifik olaraq təyin edilməsi üçün DNT-əsaslı MRI sondası J. Neurosci. 2009 29 (34) 10663-10670
- Kokain-Çıxarılan Sıçanlardaki Dendritik Spin Plastisitesini Değiştirdi J. Neurosci. 2009 29 (9) 2876-2884
- Drosophila-da Aşkarxlama Displeyi AP-3-Dependent İnkişaf Plastisitesinin Regulyatoru olaraq GSK-1 (beta) / shaggy'nin Nöronal Rollərini təyin edir Genetik 2008 180 (4) 2057-2071
- Transkripsiyası MRİ: Yaşayan Brainin Yeni Görünüşü Neuroscientist 2008 14 (5) 503-520
- Orbitofrontal Korteksdə F7B İndüksiyanı Kokain Təşəbbüslü Kognitif Bozukluğa Tolerans J. Neurosci. 2007 27 (39) 10497-10507
- Glial hüceyrə xəttindən yaranan neyrotrofik faktor mutant siçanlarda metamfetamin axtarış davranışının bərpasına davamlı həssaslıq FASEB J. 2007 21 (9) 1994-2004
- Nüvə akumbensindəki {Delta} FosB, Qida ilə təchiz edilmiş instrumental davranış və motivasiyası tənzimləyir J. Neurosci. 2006 26 (36) 9196-9204
- Fosforilasyonla {Delta} FosB Stabilliyinin tənzimlənməsi. J. Neurosci. 2006 26 (19) 5131-5142
- Dopamində Mutan NMDA Reseptorlarının D1 Receptor-Containing Cells-in ifadə edilməsi kokain həssaslığını və kokain seçimini azaldır J. Neurosci. 2005 25 (28) 6651-6657
- D1 Dopamin Reseptorları Aralıq Morfin İdarəsinin Ardından Rat Striatumda {Delta} FosB İndüksiyonunu Modüle Etdi J. Pharmacol. Exp. Ther. 2005 314 (1) 148-154
- Yüksək Könüllü Təkərli Koşulan Fəaliyyət üçün Seçilən Siçanların Nörobiyolojisi Integr. Comp. Biol. 2005 45 (3) 438-455
- Sümük supraoptik nüvədə və laminat terminalı bölgəsində suyun məhrum edilməsinin və c-Fos və FosB boyanmağına səpələnməsinin təsiri Am. J. Physiol. Regul. Integr. Comp. Fiziol. 2005 288 (1) R311-R321
- Osteoblastlarda mexanik stress ilə FosB / {Delta} FosB Geninin transkripsiya indusiyası J Biol Chem 2004 279 (48) 49795-49803
- Kronik Stress Sonrası Mükafatlı Beyin strukturlarında {Delta} FosB'nin İndüksiyonu J. Neurosci. 2004 24 (47) 10594-10602
- Sim1 gen dozası, farelerde artan pəhriz yağına homeostatik qidalanma reaksiyasını modullaşdırır Am. J. Physiol. Endokrinol. Metab. 2004 287 (1) E105-E113
- Hidrostatik təzyiqə cavab olaraq insan optik sinir rəhbəri astrositlərində gen ifadəsinin DNA mikroarray analizi Fiziol. Genomics 2004 17 (2) 157-169
- Superoxid Mərkəzi Sinir Sistemi Aktivləşdirmə və Miyokard İnfarktüsünə səbəb olan ürək çatışmazlığının simptomatikləşməsində iştirak edir Circ. Res. 2004 94 (3) 402-409
- Təkrarlanan dopaminerjik stimullaşdırmaya nöroadaptasiyada adenozin A2A reseptorları: Parkinson xəstəliyində diskineziyaların müalicəsinə təsirləri Nöroloji 2003 61 (90116) S74-81
- Quraqlıqda Fos ilə əlaqəli Proteinlərin Sitoplazmik Versus Nüvə Lokalizasiyası, Rana Esculenta, Testis: Vivo Və Doğrudan In Vitro Bir Gonadotropin-Relizasiya edən Hormon Agonistinin Təsiri Biol. Reprod. 2003 68 (3) 954-960
- Periadolenziyalı siçanlarda güclü Delta FosB kokain və amfetaminə müdaxilənin təkmilləşdirilməsi J. Neurosci. 2002 22 (21) 9155-9159
- Delta FosB təkərlərin qaçışını tənzimləyir J. Neurosci. 2002 22 (18) 8133-8138
- Nucleus accumbens shell-da CREB aktivliyi emosional stimullara davranış reaksiyalarının qapısını nəzarət edir Proc. Natl. Acad. Sci. ABŞ 2002 99 (17) 11435-11440
- Psikogenomik: Anlayış Bağımlılığı üçün Fürsətlər J. Neurosci. 2001 21 (21) 8324-8327
