კომენტარები: ნარკომანიის ეროვნული ინსტიტუტის ხელმძღვანელის, ნორა ვოლკოვისა და მისი გუნდის მიმოხილვა. ამ მიმოხილვაში ჩამოთვლილია 3 ძირითადი ნეირობიოლოგიური დისფუნქცია, რომლებიც მონაწილეობენ ყველა დამოკიდებულებაში. უბრალოდ განაცხადა, რომ ისინი: ა) განცალკევება: dumbamine სიგნალიზაციის შემცირების გამო numbed pleasure response; ბ) სენსიტიზაცია: გაძლიერებული dopamine რეაგირება დამოკიდებულების მინიშნებები, იწვევს ან სტრესი; და გ) ჰიპოფრონალურობა: შესუსტებული თვითკონტროლის სქემები შუბლის ქერქის მოცულობის შემცირებისა და ფუნქციონირების გამო. ტვინის ეს იგივე ცვლილებები გაითვალისწინეს ნარკომანიის ამერიკული საზოგადოების (ASAM) მიერ დამოკიდებულების ახალი განმარტება გამოვიდა აგვისტოში, 2011.
Volkow ND, Wang GJ, Fowler JS, Tomasi D, Telang F, Baler რ Bioessays. 2010 სექცია 32 (9): 748-55.
ეროვნული ინსტიტუტი ნარკოტიკების ბოროტად გამოყენების შესახებ, NIH, Bethesda, MD 20892, აშშ.
აბსტრაქტული
საფუძველზე ტვინის ვიზუალიზაციის შედეგები, ჩვენ წარმოადგინოს მოდელი, რომლის მიხედვითაც დამოკიდებულება ჩნდება როგორც დისბალანსი საინფორმაციო გადამამუშავებელი და ინტეგრაციის სხვადასხვა ტვინის სქემები და ფუნქციები.
დისფუნქციები ასახავს:
a) შემცირდა მდიდარი ჯილდოები,
(ბ) მეხსიერების სქემების მგრძნობელობა ნარკოტიკებისა და ნარკოტიკების მოხმარების მოლოდინებზე, სტრესის რეაქტიულობაზე და ნეგატიურ განწყობაზე,
(გ) და დასუსტებული მართვის წრე.
მიუხედავად იმისა, რომ პირველადი ექსპერიმენტი ნარკოტიკების ბოროტად არის მეტწილად ნებაყოფლობით ქცევას, განაგრძობს ნარკოტიკების გამოყენების საბოლოოდ უარყოფით ნეირონულ სქემები ტვინის, რომლებიც ჩართული თავისუფალი ნება, გარდამტეხი ნარკოტიკების გამოყენების შევიდა ავტომატური compulsive ქცევა. ნეირონების (დოპამინის, გლუტამოტისა და GABA) შორის თანაავტოფოლიზების ნეიროტრანსმიტერული სიგნალების ნარკოტიკული საშუალებების უნარი ცვლის განსხვავებულ ნეირონურ წრეებს, რომლებიც იწყებენ ნარკომანიის ტრაექტორიას სხვადასხვა ეტაპზე. ნარკოტიკების მომატებისას ან ნარკოტიკების ზემოქმედებისას ამ შედეგების გააქტიურება მოტივაციის / დისკის მიკროსქემის შეუძლებელ ჰიპერაქტირებაში, რამაც გამოიწვიოს შეღავათიანი ნარკოტიკების მიღება, რომელიც ახასიათებს დამოკიდებულებას.
შესავალი
უკანასკნელი 25 წლის ნეირომეცნიერების კვლევამ წარმოადგინა მტკიცებულება, რომ დამოკიდებულება არის ტვინის დაავადება, რომელიც უზრუნველყოფს ძლიერ არგუმენტს მედიკამენტების იმავე სტანდარტების დაცვაზე, რომელიც დამოკიდებულია თვითნებურად, როგორც სხვა დაავადებებთან დაკავშირებული ძირითადი საზოგადოებრივი გავლენა, როგორიც არის დიაბეტი. მართლაც, დამოკიდებულების შესწავლა დაიწყო მოვლენების თანმიმდევრობა და გრძელვადიანი sequelae, რომელიც შეიძლება გამოიწვიოს მუდმივი ბოროტად ნარკოტიკული ნივთიერება. ამ კვლევებმა აჩვენა, თუ როგორ განმეორებითი ნარკოტიკების მოხმარება შეუძლია ძირითადი მოლეკულების და ტვინის სქემების მიზანმიმართვა, და საბოლოოდ ჩაშლას უმაღლესი რიგი პროცესები, რომლებიც ემოციებს, შემეცნებას და ქცევას გულისხმობს. ჩვენ ვისწავლეთ, რომ დამოკიდებულება ახასიათებს ტვინის დისფუნქციის გაფართოების ციკლს. გაუფასურება, როგორც წესი, იწყება ტვინის ევოლუციურად უფრო პრიორიტეტულ სფეროებში, რომლებიც აფასებენ ჯილდოს და შემდეგ გადადიან სხვა კომპეტენციებზე, რომლებიც პასუხისმგებელნი არიან უფრო რთული კოგნიტური ფუნქციებისათვის. ამგვარად, ჯილდოს გარდა, ფიზიკურ პირებს შეუძლიათ განიცდიან მძიმე დარღვევები სწავლის (მეხსიერების, კონდიცირების, სავარჯიშო), აღმასრულებელი ფუნქციის (იმპულსი ინჰიბიცია, გადაწყვეტილების მიღება, დაგვიანებული გრაცია), შემეცნებითი ცნობიერების (interoception) და ემოციური (განწყობა და სტრესი რეაქტიულობა) ფუნქციები.
უმეტესად ტვინის გამოთვლითი კვლევების შედეგებიდან გამომდინარე, პოსტოტრონის ემისიის ტომოგრაფია (PET) გამოვიყენეთ საკვანძო ტვინის სქემები, რომლებიც გავლენას ახდენენ ნარკოტიკების ქრონიკული შეურაცხყოფით და შემდგომ თანმიმდევრულ მოდელს წარმოადგენენ, რომლის მიხედვითაც დამოკიდებულება ხდება როგორც დაუბეგრავი ინფორმაციის დამუშავება და ამ წრეებში. ამ თანდათანობით ადაპტირებული (ნევროპლასტიკური) ტვინის პროცესების და ბიოლოგიური და გარემოსდაცვითი მოწყვლადობის ფაქტორების კარგად გაგება, მათი გავლენის გავლენა, კრიტიკულია უფრო ეფექტური პრევენციისა და მკურნალობის მიდგომების შემუშავებაზე დამოკიდებულების შესანარჩუნებლად.
მაღალი, მაგრამ მოკლე, dopamine of bursts საჭიროა დამოკიდებულების
ნარკომანია, უპირველეს ყოვლისა, ტვინის ჯილდო სისტემის დაავადებაა. ეს სისტემა იყენებს ნეიროტრანსმიტერ დოფამინს (DA), როგორც მის მთავარ ვალუტას ინფორმაციის გადასაცემად. ტვინის DA მნიშვნელოვან როლს ასრულებს მარილიანობის შესახებ ინფორმაციის დამუშავებაში [1, 2], რომელიც გულისხმობს მისი უნარის რეგულირებას ან ზეგავლენას [3, 4], ჯილდო მოლოდინი [5], მოტივაცია, ემოციები და სიამოვნების გრძნობები. ტვინის პარკუჭის სტრიატუმში DA– ს დროებითი გამოყოფა აუცილებელი, თუმცა არასაკმარისი მოვლენაა იმ რთულ პროცესებში, რომლებიც იწვევს ჯილდოს შეგრძნებას: DA– ს ზრდა დადებითად უკავშირდება სუბიექტების „მაღალი” ინტენსივობას. პირობითი პასუხები მიიღება მხოლოდ მაშინ, როდესაც DA განმეორებით გამოიყოფა, როგორც ეს მკვეთრი, გარდამავალი, ტალღები, ნარკოტიკების ან ნარკოტიკებთან დაკავშირებული მინიშნებების საპასუხოდ.
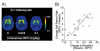
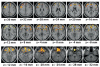
საინტერესოა, რომ პირდაპირ ან არაპირდაპირ, ყველა ნარკოტიკული ნივთიერებები მუშაობს ექსტრემალურად DA- ში გადაჭარბებული, მაგრამ გარდამავალი იზოლაციით,6, 7], კერძოდ, ბირთვულ შრატში განლაგებულ ბირთვში (Nac). ასეთი DA surges ჰგავს, და ზოგიერთ შემთხვევაში მნიშვნელოვნად აღემატება, ფიზიოლოგიური იზრდება გამოიწვია ბუნებრივია სასიამოვნო სტიმული (ჩვეულებრივ მოხსენიებული, როგორც ბუნებრივი reinforcers ან ჯილდოები). როგორც მოსალოდნელი იყო, ადამიანის ტვინის გამოსახულების კვლევა positron ემისიის ტომოგრაფიის (PET) გამოყენებით, ნათლად აჩვენებს, რომ DA იზრდება სხვადასხვა ტიპის ნარკოტიკების საშუალებით (მაგალითად. სტიმულატორები (ნახაზი), [8, 9], ნიკოტინი [10] და ალკოჰოლი [11]) ვენტრალურ შრატში, უკავშირდება ეიფორიის სუბიექტური გამოცდილების (ან მაღალი) ინტოქსიკაციის დროს [12, 13, 14]. მას შემდეგ, რაც PET- ის კვლევები შეიძლება გაკეთდეს ადამიანის სუბიექტებზე, შესაძლებელია ასევე მოახდინოს ნარკოლოგიური ეფექტის სუბიექტური ანგარიშების და დ.ა. უმეტეს კვლევებში აღინიშნა, რომ დ.ა.-ს მიერ გამოვლენილი ნარკოტიკების ექსპოზიციის ზრდა ამფეტამინის, ნიკოტინის, ალკოჰოლური, მეთილფენიდეტის (MPH) მოხსენებებში ასევე აღინიშნება ყველაზე ინტენსიური მაღალი ან ეიფორია (ნახ).
ცხოველთა და ადამიანის კვლევებმა აჩვენა, რომ სიჩქარე, რომლის დროსაც ნარკოტიკების შედის, მოქმედებს და ტოვებს ტვინს (ანუ მისი ფარმაკოკინეტიკური პროფილი) ეფუძნება ფუნდამენტურ როლს მისი განმტკიცების ეფექტების განსაზღვრისას. მართლაც, ყველა ნარკოტიკების ბოროტად, რომლის ტვინის ფარმაკოკინეტიკა იზომება PET (კოკაინი, MPH, methamphetamine და ნიკოტინის) გამოჰყავს იგივე პროფილი, როდესაც ადმინისტრაცია ინტრავენური, ანუ, ადამიანის ტვინში პიკური დონე აღწევს 10 წუთში (ნახაზი) და ამ სწრაფი uptake უკავშირდება "მაღალი" (ნახ). ამ ასოციაციის საფუძველზე, მას შემდეგ, რაც დარწმუნებულია, რომ ნარკოტიკული პრეპარატი შედის ტვინში, როგორც ნელ-ნელა შესაძლებელი უნდა იყოს მისი ეფექტურობის ამაღლების ეფექტური საშუალება, შესაბამისად, მისი ბოროტად გამოყენება. ჩვენ ექსპერიმენტს მივაწოდეთ ექსპერიმენტი ზუსტად ამ ჰიპოთეზის შესამოწმებლად სტიმულატორთან ერთად MPH, რომელიც კოკაინის მსგავსად, DA- ს ზრდის თავის ტრანსპორტის გადატვირთვას საპენსიო ნეირონში (ანუ DA ტრანსპორტირების ბლოკირებით), ამით DA სიგნალის გამაძლიერებელი. მართლაც, ვნახეთ, რომ MPH- ის ინტრავენური შეყვანა ხშირად ეიფორიგენურია, ზეპირად ადმინისტრირებულია MPH, რომელიც ზრდის DA- ს შრატში15], მაგრამ 6- დან 12- მდე ნელა ფარმაკოკინეტიკა, არ არის, როგორც წესი,16, 17]. ამრიგად, ზეპირი MPH - ან ამფეტამინის [18] ამ საკითხზე - მაღალია გამოიწვიოს სავარაუდოდ ასახვა მათი ნელი uptake შევიდა ტვინის [19]. აქედან გამომდინარე, მიზანშეწონილია შესთავაზოს მჭიდრო კორელაციის არსებობა იმ განაკვეთს შორის, რომლის დროსაც ნარკოტიკების ბოროტად შედის ტვინი, რომელიც განსაზღვრავს იმ სიჩქარას, რომლითაც დ.ა. იზრდება ვენტრალური შრატისას და მისი გამაძლიერებელი ეფექტი [20, 21, 22]. სხვა სიტყვებით რომ ვთქვათ, ნარკოტიკების შესამსუბუქებლად ეფექტურობას აქვს ამაღლება დ.ა. რატომ უნდა იყოს ასე?
ნეირონის გათავისუფლების სიდიდისა და ხანგრძლივობის გათვალისწინებით, DA სიგნალს შეუძლია მიიღოს ორი ძირითადი ფორმა: phasic or tonic. Phasic სიგნალიზაცია ხასიათდება მაღალი ამპლიტუდისა და ხანმოკლე პაკეტის გათავისუფლებით, ხოლო ტონიკური სიგნალი აქვს ჩვეულებრივ დაბალ სიჩქარეს და უფრო ხანგრძლივად ან სტაბილურ დროში. განსხვავება მნიშვნელოვანია, რადგან აღმოჩნდება, რომ ფაზური DA სიგნალი აუცილებელია ბოროტად გამოყენებისათვის "პირობითი რეაგირებისთვის", რომელიც წარმოადგენს ერთ-ერთ თავდაპირველ ნევროპათიას, რომელიც აძლიერებს სტიმულს (მათ შორის ნარკოტიკების ჩათვლით). ერთ-ერთი გამორჩეული ასპექტი, რომელიც კონტაქტს ფაზური სიგნალი უკავშირებს არის D2R და გლუტამატის ჩართვა n-მეთილ-d-მჟავას მჟავა (NMDA) რეცეპტორები [23]. მეორეს მხრივ, მატონიზირებელი DA სიგნალი როლს ასრულებს სამუშაო მეხსიერებასა და სხვა აღმასრულებელ პროცესებში. ზოგიერთი ფუნქცია, რომელიც განასხვავებს ამ მეთოდის phasic ტიპის სიგნალს, ის ძირითადად მოქმედებს DA რეცეპტორებთან (DA D1 რეცეპტორები). თუმცა, მიუხედავად იმისა, რომ ჩართული სხვადასხვა მექანიზმების, გაჭიანურებული ნარკოტიკების ექსპოზიცია (და ცვლილებები ტოქსიკური DA სიგნალიზაციის საშუალებით ამ რეცეპტორებით) ასევე იწვევდა ნევროპლასტიკურ ცვლილებებს,25] NMDA- ისა და ალფა-ამინ-ჯუიქს-ჰიდროქსილი- 3- მეთილ- 5- იზოქსაზონ-პროპიონატის (AMPA) გლუტამატის რეცეპტორების მოდიფიცირებით [24].
მტკიცებულება მიუთითებს, რომ მკვეთრი ნარკოტიკების გამოწვეული იზრდება DA mimic phasic DA საკანში სროლის. ეს ხელს უწყობს იმის გამო, რომ ნარკოტიკული ნივთიერების ქრონიკული გამოყენება შეიძლება ისეთი ძლიერ განაპირობებდეს რეაგირებს ნარკოტიკებისადმი, მისი მოლოდინებისა და მისი გამოყენებისას (ხალხის, ნივთები და ადგილები). მიუხედავად იმისა, რომ ამგვარი სწრაფი DA იზრდება ნარკოტიკული საშუალებების მწვავე აძლიერებს, სავარაუდოდ "აუცილებელია" დამოკიდებულების განვითარებისთვის, ისინი აშკარად არ არიან "საკმარისი". განმეორებითი პრეპარატები იწვევს DA ტვინის ფუნქციის ცვლილებას, განვითარება, რადგან ისინი მეორე ნეიროტრანსმიტერის სისტემებში მეორადი ნეიროდეგვაციის შედეგად (მაგალითად გლუტამატი [26] და, შესაძლოა, ასევე γ-aminobutyiric მჟავა (GABA)), რაც, საბოლოო ჯამში, გავლენას ახდენს დამატებითი ტვინის სქემებით DA- ს მიერ. ეს სქემები არის შემდეგი სექციების ფოკუსი.
ქრონიკული ნარკომანია არეგულირებს დოპამინის რეცეპტორებს და დოპამინის წარმოებას: "მაღალია"
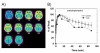
ის ფაქტი, რომ ნარკოტიკების მოხმარება უნდა გახდეს ქრონიკული ხარვეზამდე, ფესვთა ნუსხა არის ნათელი იმის მითითება, რომ დაავადების პროგნოზირება, სოციალურად დაუცველ პირებში, ჯილდოს სისტემის განმეორებითი დარღვევების შესახებ. ეს პროცედურები შეიძლება გამოიწვიოს მრავალი სხვა სქემით (მოტივაცია / დრაივერი, ინჰიბიტორული კონტროლი / აღმასრულებელი ფუნქცია და მეხსიერების / კონდიცირების) ნევროპათიები, რომლებიც ასევე DA [27]. მათ შორის ნეიროპატარაციებს, რომლებიც თანმიმდევრულად იტყობინებიან ნარკოტიკულ ნივთიერებებში, არის D2R (მაღალი შეყვანის) რეცეპტორების დონის მნიშვნელოვანი შემცირება და DA უჯრედების მიერ გამოთავისუფლებული DA ოდენობით [28] (ბ. 3). მნიშვნელოვანია, რომ ეს დეფიციტი უკავშირდება ქვედა რეგიონულ მეტაბოლურ აქტივობას პრეფრონტალური ქერქის (PFC) სფეროებში, რომლებიც სათანადო აღმასრულებელი მუშაობისთვის კრიტიკულია (ანუ წინა cingulate gyrus (CG) და orbitofrontal ქერქის (OFC)) (ნახაზი). ეს დაკვირვება გამოიწვია ჩვენთვის, რომ ეს შეიძლება იყოს ერთ-ერთი მექანიზმი, რომელიც აკავშირებს ნარკოტიკების ინექციურ დარღვევას DA- ში სავალდებულო ნარკოტიკების ადმინისტრირებისა და ნარკოტიკების მოხმარების კონტროლის არარსებობა,29]. ასევე, შედეგად ჰიპოდოპამინერგული მდგომარეობა ახსნის ნარკომანი ადამიანის შემცირებულ მგრძნობელობას ბუნებრივი ჯილდოს მიმართ (მაგ. საკვები, სექსი და ა.შ.) და ნარკოტიკების მოხმარების გახანგრძლივება, როგორც ამ დეფიციტის დროებითი კომპენსაცია30]. ამ ცოდნის მნიშვნელოვანი კორელაციაა ის, რომ ამ დეფიციტის (სტრუქტურული და პრიორიტეტული რეგიონების დონის ზრდისა და დრაიტის გაზრდის გზით) მიღება შეუძლია კლინიკურ სტრატეგიას შესთავაზოს დამოკიდებულების ზემოქმედების გაუმჯობესება [31]. არსებობს თუ არა რაიმე მტკიცებულება, რომ ჰიპოდოფამინერგული მდგომარეობის შეცვლა შეიძლება დადებითი გავლენა იქონიოს ნივთიერებების ბოროტად დაკავშირებულ ქცევებზე? პასუხი კი დიახ. ჩვენი კვლევები გვიჩვენებს, რომ კოკაინის ან ალკოჰოლური და გამოცდილი ვირთაგვების ჯილდოს სისტემაში ღრმა შპრიციანი ძალებით, ჩვენ შეგვიძლია მნიშვნელოვნად შეამციროს კოკაინის თვითმართვალება [31] ან ალკოჰოლი [32], შესაბამისად. უფრო მეტიც, მღრღნელებში, ისევე, როგორც ადამიანის მეტამფეტამინების მკვლელობებში [33], D2R- ის შემცირებული დრეატალური დონე ასევე დაკავშირებულია იმპულსთან, და მღრღნელებში პროგნოზირებს ნარკოტიკულ თვითშეწონასწორებას (იხ. ქვემოთ).
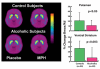
გამოსახულების კვლევებმა ასევე აჩვენა, რომ ადამიანებში დამოკიდებულება უკავშირდება დრაიზის გათავისუფლებას ვენტრალური შრატისა და შრატის სხვა რეგიონებში შემცირებისა და აქტიური და დეტოქსიკადი ნარკოტიკების მომხმარებელთა ნარკოტიკებისადმი სასიამოვნო რეაგირებისას (ბ. 5) [34]. ეს იყო მოულოდნელი დასკვნა, რადგან იგი იყო ჰიპოთეზა, რომ დამოკიდებულების აისახა გაღრმავებული მგრძნობელობა დაჯილდოების (და შესაბამისად dopaminergic) რეაგირება ნარკოტიკების. ნარკოტიკების მომაკვდინებელ მოქმედებებში, DA- ში გათავისუფლება შეიძლება აისახოს ანაზღაურებადი ნეიროფიზიოლოგია ჯილდოს სქემით (ანუ DA- ს ნეირონებს, რომლებიც DA- ს შრატში ათავისუფლებენ) ან, გარდა ამისა, უპირატესობაა პრიორიტეტული (აღმასრულებელი კონტროლი) ან ამაღელდა (ემოციური) გზები (პრიორიტეტული-სასიკვდილო, ამიგდალარდისტალური გლუტამატერგიული გზები). მას შემდეგ, რაც ქრონიკული ნარკოტიკების ბოროტად გამოყენებისას სუფთა დოფამინერგური დისფუნქცია არ იწვევდა ისეთ მახასიათებლებს, რომლებიც დამახასიათებელია ნარკოტიკული ქცევების მახასიათებლებით, როგორიცაა იმპულსური, ბოროტი და რეპრეცედენტი ნარკოტიკების საშუალებით, ძალიან სავარაუდოა, რომ prefrontal regions (როგორც ისევე, როგორც ამიგდალა) აქაც ჩართულია, რადგან მათი დარღვევა საშუალებას მისცემს, ან ამგვარი ქცევის მახასიათებლების გავლენას მოახდენს.
შემცირებული დოპამინის რეცეპტორი (DR2) დონეს უპირატესობას ანიჭებს იმპულსების კონტროლი prefrontal cortex
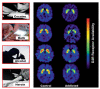
ეს იყო ჰიპოთეზა, რომ impulsive კონტროლი compulsive ნარკოტიკების აღების ქცევას, რომელიც ახასიათებს დამოკიდებულების შეიძლება იყოს ნაწილი ნაწილობრივ კონკრეტული დისფუნქცია თავის შუბლის რეგიონებში [35]. არსებობს მნიშვნელოვანი თანხა მტკიცებულება, რომელიც მხარს უჭერს ამ ცნებას, დაწყებული ცხოველების კვლევებით, რომლებიც შეისწავლიან კავშირი D2R- ს და ქცევის კონტროლს. ექსპერიმენტები ვირთხებით ნათლად აჩვენებს კორელაციას შორის დაბალი D2R და იმპულსური [36], და იმპულსური და ნარკოტიკების თვითმართველობას შორის [37]. მაგრამ რა არის კავშირი? როგორც ზემოთ აღვნიშნეთ, ნარკომანიის დროს, D2R- ის ქვედა ტვინის გლუკოზის მეტაბოლიზმი მნიშვნელოვნად არის დაკავშირებული PFC- ის საკვანძო რეგიონებში, როგორიცაა OFC- ის (ჩართულობის სიბრტყეში ჩართვა და მისი დარღვევები იძულებითი ქცევების დროს) და CG- ში (ჩართულია ინჰიბიტორული კონტროლი და შეცდომის მონიტორინგი და რომლის დარღვევა შედეგების იმპულსურია) (ნახ) [38, 39]. უფრო მეტიც, შესწავლილ იქნა ინდივიდუალურ (ს.ს. ± ± ასაკი, 24 ± 3 წელი) ოჯახური ისტორია ალკოჰოლიზმის ისტორიაში, მაგრამ რომლებიც არ იყვნენ ალკოჰოლიკები, ჩვენ ასევე გამოვლენილია მნიშვნელოვანი ასოციაციის შტამპური შიდსი და მეტაბოლიზმი ფრონტალურ რეგიონებში (CG , OFC და dorsolateral PFC) და ასევე წინა ინულაში (ჩართული interoception, თვითმმართველობის ცნობიერების და ნარკოტიკების craving) [40] (ბ. 6). საინტერესოა, რომ ამ პირებს ჰქონდათ უფრო მაღალი შაქრიანი დიამეტრი, ვიდრე ალკოჰოლიზმის ოჯახის ისტორიით, მიუხედავად იმისა, რომ არ განსხვავდებოდნენ შუბლის მეტაბოლიზმში. ასევე, კონტროლირებადში, არტერიული მეტაბოლიზმის კოლალაცია არ შეინიშნება. ეს გვაფიქრებინა, რომ ალკოჰოლიზმის მაღალი გენეტიკური რისკის მქონე პაციენტებში უფრო მაღალია, ვიდრე ჩვეულებრივი სტრუქტურული D2R მათ ალკოჰოლიზმზე იცავს მათ ნაწილობრივ პრიორიტეტულ რეგიონებში აქტივობის გაძლიერების გზით. კომბინირებული გამოყენებისას, ამ მონაცემების მიხედვით, D2R- ის მაღალი დონე შეიძლება დაიცვას ნარკოტიკების ბოროტად გამოყენება და დამოკიდებულება კონტროლის ქვეშ მყოფი იმუნური თვისებების დაცვით, ანუ, რეგულირების სქემები ჩართული ინჰიბირებით ქცევითი რეაგირება და კონტროლის ემოციებს.
ანალოგიურად, ჩვენ ვივარაუდოთ, რომ პრეპარატის რეგიონებში ჩართული არიან ფრაგმენტული DA- ის გათავისუფლება (და გაძლიერება), რომლებიც შეინიშნება ნარკოტიკულ ნივთიერებებში, რადგან ისინი არეგულირებენ DA- ს ცეცხლსასროლი იარაღის დაქვეითებასა და DA- ში გათავისუფლებას. ამ ჰიპოთეზის შესამოწმებლად მიგვაჩნია, რომ PFC- ში არსებულ საბაზისო მეტაბოლიზმს შორის ურთიერთობების შეფასება და მშრალი DA- ს ზრდის ტემპერატურის კონტროლი და დეტოქსიკაციური ალკოჰოლიქსი. ჰიპოთეზასთან ერთად, ალკოჰოლური სასმელებით ვერ აღმოვჩნდით საბაზისო პრეფრონტალური მეტაბოლიზმსა და დ.ა.-ში გათავისუფლების ოპერაციებს შორის ნორმალურ კავშირს, ვარაუდობს, რომ ალკოჰოლიქსში გამოვლენილი დრაიტის დგომის შემცირება აისახება თავის ტვინის აქტივობის არასათანადო რეგულირებით,34].
ამრიგად, ჩვენ აღმოვაჩინეთ ასოციაცია PFC- ში არსებულ შემცირებულ საბაზისო აქტივობასა და ნარკოტიკულ საავადმყოფოში მოქმედი სადაზღვევო D2R- ს შორის და იმ PFC- ის აქტივობისა და DA- ს გათავისუფლების ფონზე, რომელიც არ არის დამოკიდებული ნარკომანიებში. ეს ასოციაციები გამოხატავს PFC- ის გზების ნეიროდაგნაციებს შორის ძლიერი კავშირები DA- ს ჯილდოს და სამოტივაციო სისტემებში არსებულ დისფუნქციებს, სავარაუდოდ PFC- ის გავლენას გავლენა მოახდინა impulsivity და compulsivity. თუმცა, ეს არ ითვალისწინებს დამატებით ქცევაზე მოვლენას, მაგალითად, ნარკოტიკების ასოცირებული მინიშნებების ეფექტს, რომელიც ითვალისწინებს მზრუნველობას, რაც სავარაუდოდ ითვალისწინებს მეხსიერების და სწავლის სქემებს.
დამონტაჟებული მოგონებები და სტერეოტიპული ქცევები მძღოლად "მაღალი" შეცვლის
დრაიდის უჯრედების უჯრედების გადამეტება საბოლოო ჯამში ქმნის ახალ ფუნქციურ კავშირებს ტვინის დაკმაყოფილებისაკენ და მასთან დაკავშირებული სიტუაციური მოვლენები (მაგალითად, გარემო, ნარკოტიკების მომზადების რუტინული და ა.შ.), ახალი , ძლიერი შეიტყო ასოციაციები, რომლებიც შეიძლება გამოიწვიოს ქცევა. საბოლოო ჯამში, ნარკოტიკების მხოლოდ მეხსიერების ან მოლოდინით შეიძლება გამოიწვიოს იმპულსური ქცევები, რომლებიც დამახასიათებელ დამოკიდებულ პირებს ახასიათებენ. არაერთგზის ნარკოტიკების მოხმარებით, დრაიტის უჯრედების გათავისუფლება იწყება ფსევდონიუმის ნევროქიმიის შეცვლაზე. ეს ხელს უწყობს ნარკოტიკულ ნივთიერებასთან დაკავშირებული maladaptive მეხსიერების კვალითა კონსოლიდაციას, რომელიც ეხმარება ყველა სახის ნარკოტიკების ასოცირებულ სტიმულს (ამ ცოდნის გამოვლენისას მიღებული ცოდნის მიღებისას)41] ადვილად გამოიწვიოს DA უჯრედების გათავისუფლება. და DA- ს როლის მოტივაციის მოტივით, ამ DA ზრდის მოტივაციის დონეს,42]. სინამდვილეში, როდესაც ვირთხები ექვემდებარებიან ნეიტრალურ სტიმულს, რომელიც ნარკოტიკულ საშუალებებთან (პირობითად) დაწყებულია, შეიძლება გამოიწვიოს DA იზრდება და ნარკოტიკების თვითრეგულირების აღდგენა [43]. ასეთი განაპირობებული რეაქციები კლინიკურად აქტუალურია ნივთიერებების გამოყენების დარღვევებში, რადგან ისინი პასუხისმგებელნი არიან თვითნებურად მოპყრობისა და დეტოქსიკაციის ხანგრძლივი პერიოდის შემდეგ. ახლა, ტვინის ვიზუალიზაციის მეთოდები საშუალებას მოგვცემს, შეამოწმოთ თუ არა ნარკოტიკებთან დაკავშირებული მინიშნებების გამოვლენა ნარკოტიკების მოყვარულებს, როგორც ჩანს, ლაბორატორიულ ცხოველებში.
არაერთგზის ნარკოტიკების მოხმარებით, დრაიტის უჯრედების გათავისუფლება იწყება ფსევდონიუმის ნევროქიმიის შეცვლაზე. ეს ხელს უწყობს ნარკოტიკულ ნივთიერებასთან დაკავშირებული maladaptive მეხსიერების კვალითა კონსოლიდაციას, რომელიც ეხმარება ყველა სახის ნარკოტიკების ასოცირებულ სტიმულს (ამ ცოდნის გამოვლენისას მიღებული ცოდნის მიღებისას)41] ადვილად გამოიწვიოს DA უჯრედების გათავისუფლება. და DA- ს როლის მოტივაციის მოტივით, ამ DA ზრდის მოტივაციის დონეს,42]. სინამდვილეში, როდესაც ვირთხები ექვემდებარებიან ნეიტრალურ სტიმულს, რომელიც ნარკოტიკულ საშუალებებთან (პირობითად) დაწყებულია, შეიძლება გამოიწვიოს DA იზრდება და ნარკოტიკების თვითრეგულირების აღდგენა [43]. ასეთი განაპირობებული რეაქციები კლინიკურად აქტუალურია ნივთიერებების გამოყენების დარღვევებში, რადგან ისინი პასუხისმგებელნი არიან თვითნებურად მოპყრობისა და დეტოქსიკაციის ხანგრძლივი პერიოდის შემდეგ. ახლა, ტვინის ვიზუალიზაციის მეთოდები საშუალებას მოგვცემს, შეამოწმოთ თუ არა ნარკოტიკებთან დაკავშირებული მინიშნებების გამოვლენა ნარკოტიკების მოყვარულებს, როგორც ჩანს, ლაბორატორიულ ცხოველებში.
ეს საკითხი გამოკვლეულია აქტიური კოკაინის მოძალადეთა. PET- ის გამოყენება და [11C] raclopride- ს, ორი დამოუკიდებელი კვლევა აჩვენა, რომ კოკაინის მინიჭების ვიდეო (სუბიექტების მოწევის კოკაინის) გამოვლენა, მაგრამ არა ნეიტრალური ვიდეო (ბუნების სცენების) გაზრდილია დრატალური დ.ა.ბ. 7) და რომ DA იზრდება იყო დაკავშირებული ნარკოტიკების craving სუბიექტური ანგარიშები [44, 45]. უფრო მაღალია, რომ DA იზრდება კოკაინის შემცველობის ვიდეოზე, რაც უფრო ინტენსიურია ნარკოტიკების მომატება. უფრო მეტიც, DA- ს ზრდის სიდიდე ასევე შეესაბამებოდა დამოკიდებულების სიმძიმის ქულებს, ხაზგასმით აღინიშნა კლინიკური სინდრომის კლინიკურ სინდრომის რეაქცია.
მნიშვნელოვანია ხაზგასმით აღვნიშნოთ, რომ მიუხედავად იმისა, რომ ამ უარყოფითი კავშირების სავარაუდო სიმტკიცის მიუხედავად, ცოტა ხნის წინ შევქმენით ახალი მტკიცებულებები, რომ კოკაინის მოძალადეები მიზნად ისახავენ მიზანმიმართულად თრგუნავს მზრუნველობას. აქედან გამომდინარე, ფრონტო-სტრუქტურული რეგულირების გაძლიერების სტრატეგიებმა შესაძლოა პოტენციური თერაპიული შეღავათები შესთავაზოს [46].
აყენებს ყველა ერთად
ნარკოტიკების მომატების ზოგიერთი ყველაზე დამაზიანებელი თვისებაა ნარკოტიკული საშუალებების მიღება, რომელიც შეიძლება წლების განმავლობაში შეუმჩნეველი გახდეს და ნარკოტიკული ნივთიერებების მკაცრი კომპრომეტირებული უნარი ნარკოტიკული საშუალებების დათრგუნვას ცდილობს, როდესაც ერთხელ იწყება მწვავე უარყოფითი შედეგების მიუხედავად.
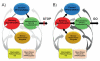
ჩვენ შესთავაზა მოდულის დამოკიდებულება [47], რომელიც განმარტავს ამ დაავადების მრავალგანზომილებიან ხასიათს, რომელიც დაკავშირებულია ოთხი ურთიერთდაკავშირებული სქემის ქსელის მიერ, რომელთა კომბინირებული ფუნქციურმა გამომავალმა შეიძლება გამოიწვიოს დამოკიდებულების სტერეოტიპული ქცევითი თვისებები: ა) ჯილდო, მათ შორის რამდენიმე ბირთვი ბაზალური გლდანის დროს, განსაკუთრებით კი ვენტრალური შრატი, რომლის ნაკადი იღებს ვენტრალური თერგმენტური ტერიტორიიდან შეყვანას და მიმართავს ინფორმაციას ვენტრალურ პალიიდუმში (VP); (ბ) OFC- ში მდებარე სუბილოზალური ქერქის, დორსალური შრატისა და საავტომობილო ქერქის მოტივაცია / დისკი; გ) მეხსიერება და სწავლა, რომელიც მდებარეობს ამიგდალაში და ჰიპოკამპუსში; დ) დორსალური თეორეტიკურ პრეორენტაციურ ქერქში, წინა CG და ქვედა ფრონტალური ქერქის ფარგლებში დაგეგმილი და კონტროლი. ეს ოთხი სქემა იღებს პირდაპირი უშუალო მიღებას DA ნეირონებისგან, მაგრამ ასევე უკავშირდება ერთმანეთს პირდაპირი ან არაპირდაპირი პროგნოზით (ძირითადად გლუტამათერგიული).
ოთხი სქემა ამ მოდელთან ერთად მუშაობს და მათი ოპერაციები იცვლება გამოცდილებით. თითოეული მათგანი მნიშვნელოვან კონცეფციას უკავშირდება: სალიტერატურო (ჯილდო), შიდა სახელმწიფო (მოტივაცია / დისკი), შეიტყო ასოციაციები (მეხსიერება, კონდიცირება) და კონფლიქტების მოგვარება (კონტროლი). გარდა ამისა, ეს სქემები ასევე ურთიერთქმედებენ წრეებში ჩართულნი (მათ შორის სტრესის რეაქტიულობა)48] და interoception (რაც იწვევს ცნობიერების ნარკოტიკების craving და განწყობა) [49]. ჩვენ შევთავაზეთ, რომ ოთხი წრიული ქსელის საქმიანობის ნიმუში აისახება, როგორ აისახება ნორმალური ინდივიდუალური არჩევანი ალტერნატივათა შორის. ეს არჩევანი გავლენას ახდენს სისტემატიურად ჯილდოს, მეხსიერების / კონდიცირების, მოტივაციისა და კონტროლის სქემების მიხედვით და ეს, თავის მხრივ, არის მოდულირებული სქემებით, რომლებიც განასხვავებენ განწყობილებას და ცნობიერების ამაღლებას (ნახაზი).
სტიმულზე რეაგირება გავლენას ახდენს მისი მომენტალური სილიანი, ანუ მოსალოდნელი ჯილდო. თავის მხრივ, ჯილდოს მოლოდინი ნაწილდება ნაწილობრივ დერმატოიდული ნეირონების მიერ პროტექციონირებისას, რომელიც გავლენას ახდენს ვენტრალურ შრატში და გავლენას ახდენს OFC- ის გლუტამატერგური პროგნოზით (რომელიც ასახავს საკმარის ღირებულებას კონტექსტის ფუნქციად) და ამიგგდალა / ჰიპოკამპმა (რაც შუამავლობით გამოწვეული პასუხებისა და მეხსიერების შეჯერების შუამავლობას). სტიმულირების ღირებულება სხვა ალტერნატიული სტიმულის საწინააღმდეგოდ (შედარებით) შედის, არამედ ცვლილებებს, როგორც ინდივიდუალური ინდივიდუალური საჭიროებების ფუნქციონირებას, რომლებიც განლაგებულია განწყობით (სტრესის რეაქტიურობის ჩათვლით) და ინტეროციპეციურ ცნობიერებაში. კერძოდ, სტრესული ექსპოზიცია აძლიერებს პრეპარატის Saliency ღირებულებას, ამავე დროს ამცირებს აჯგდალას ფუძემდებლურ რეგულაციას [50]. გარდა ამისა, მას შემდეგ, რაც ქრონიკული ნარკოლოგიური ზემოქმედების უკავშირდება გაძლიერებული სენსიტიზაცია სტრესი რეაგირება ეს განმარტავს, თუ რატომ სტრესი შეიძლება გამოიწვიოს ნარკოტიკების რეციდივის ასე ხშირად კლინიკურ სიტუაციებში. ძლიერი სტიმულის ღირებულების სტიმულაცია, ნაწილობრივ მემორანდუმის გამოცდილებით, უფრო მეტად მოტივირებული მიკროსქემის აქტივაციისა და მისი შეძენას უფრო ძლიერია. სტიმულირების მიზნით შემუშავებული შემეცნებითი გადაწყვეტილება ნაწილდება PFC- ისა და CG- ის მიერ, რომლებიც იწონებენ ბალანსს დაუყოვნებლივ დადებითი და დაბალ უარყოფით შედეგებს შორის, და ქვედა შუბლის ქერქის (Broadmann Area 44) რომელიც მოქმედებს წინასწარ საპასუხო რეაგირების მოქმედებაში [51].
ამ მოდელის მიხედვით, ნარკომანიის სუბიექტშინახ), ნარკოტიკების ბოროტად გამოყენების და მისი ასოცირებული მინიშნებების Saliency ღირებულება გაიზარდა სხვა (ბუნებრივი) ჯილდოს ხარჯზე, რომლის სალიკვიდაციო საგრძნობლად შემცირდა. ეს აისახება გაზრდილი მოტივაციისკენ მიმართოს ნარკოტიკების მიღებაზე. თუმცა, მწვავე ნარკოტიკების ექსპოზიცია ასევე აღადგენს ჯილდოებს, რის შედეგადაც ჯილდოს მარაგების მგრძნობელობა შემცირდა [52], რომელიც ასევე ხელს უწყობს ნარკოტიკული ნივთიერებების შემცირების ღირებულებას ნარკოტიკულ ნივთიერებაში. ნარკოტიკების მომატებული მგრძნობელობის კიდევ ერთი მიზეზი არის DA- ს რეაგირების ნაკლებობა ბოროტად გამოყენების (ტოლერანტობის) პრეპარატებთან შედარებით, შედარებით ნორმალურ მდგომარეობასთან,53].
უფრო მეტიც, პირობითი სტიმულის ზემოქმედება საკმარისია იმისათვის, რომ გაზარდოს ჯილდოები [54]; ამგვარად, ჩვენ ვფიქრობთ, რომ ნარკოტიკების მოხმარებისას გარემოზე ზემოქმედების პირობები კიდევ უფრო გამწვავდება მათი მგრძნობელობის ბუნებრივი ჯილდოს მიმართ. კონკურენციის არარსებობის შემთხვევაში სხვა რეინფტორებით, კონდიცირებული სწავლება აძლიერებს პრეპარატის მიღებას ინდივიდუალური ძირითადი მოტივაციის დონის დონემდე. ჩვენ ვასკვნით, რომ ნარკოტიკების მინიშნება (ან სტრესი) იწვევს დ.ა-ში სწრაფად იზრდება ვენტრალურ შრატში და დორსალური შრატში, რომლებიც ხელს უწყობენ პრეპარატის მიღების მოტივაციას და არ შეიძლება სათანადოდ ეწინააღმდეგებოდეს დისფუნქციური PFC- ს. ამრიგად, ნარკოტიკების მოხმარების და ინტოქსიკაციის დროს დ.ა. სიგნალების გაღრმავება გამოიწვევს მოტივაციული / სატრანსპორტო და მეხსიერების წრეების შესაბამისი გამტარუნარიანობას, რაც PFC- ის დეაქტივაციაა (prefrontal ინჰიბიცია ინტენსიური ამაღლების გააქტიურებით)50], დაბლოკვის ძალა PFC კონტროლი სამოტივაციო / დისკის ჩართვა. ამ ინჰიბიტორული კონტროლის გარეშე დადებითი უკუკავშირის მარყუჟი იქმნება, რაც იწვევს კომპრესიულ პრეპარატს. იმის გამო, რომ სქემებს შორის ურთიერთქმედება ორმხრივია, ინტოქსიკაციის დროს ქსელის გააქტიურება ემსახურება პრეპარატის სალიზინგო ღირებულებას და კონდიცირების საწინააღმდეგოდ.
დასკვნები
მოკლედ, ჩვენ ვთავაზობდით მოდელს, რომელიც დამოკიდებულია დამოკიდებულების შემდეგ: ნარკომანიის გაღრმავებისას მეხსიერების მიკროსქემის გაუმჯობესებული ღირებულება ჯილდოს მოლოდინშია და აძლიერებს ნარკოტიკების მოხმარების მოტივაციას, დააჩქარებს ინჰიბიტორულ კონტროლს, რომელსაც ახორციელებს უკვე ფუნქციონალური PFC. მიუხედავად იმისა, რომ ნარკოტიკების მომატებული DA ზრდა საგრძნობლად ადეკვატურია ნარკოტიკების მოხმარების სუბიექტებში, პრეპარატის ფარმაკოლოგიური ეფექტები თავისთავად განაპირობებს რეაგირებას, მოჰყვება პრეპარატის მიღების მოტივაციას და დადებითად გამოხატავს უკმაყოფილებას, პრეფრონტალური კონტროლის მიკროსქემის. ამავდროულად, დამოკიდებულება სავარაუდოა, რომ ასევე გადაიტანოს სქემები, რომლებიც ახდენენ განწყობის განცდას და ცნობიერების ამაღლებას (წარმოდგენილია ნაცრისფერი მუქი ნაცრისფერი)ნახ) იმგვარად, რომ თუ ექსპერიმენტულად დადასტურდება, ინარჩუნებს ბალანსს ინჰიბიტორული კონტროლიდან და იკავებს სამკურნალო და სავალდებულო წამლების მიღებას.
ჩვენ ადვილად ვაღიარებთ, რომ ეს არის გამარტივებული მოდელი: ჩვენ ვაცნობიერებთ, რომ ამ ტვინებში სხვა ტვინის რეგიონებიც უნდა იყვნენ ჩართულნი, რომ ერთი რეგიონი რამდენიმე წრეში წვლილი შეიტანოს და სხვა სქემებიც, შესაძლოა, ჩართულნი იქნას დამოკიდებულებაში. გარდა ამისა, მიუხედავად იმისა, რომ ეს მოდელი ყურადღებას ამახვილებს DA- ში, ის გამოირჩევა პრეკლინიკური კვლევებისაგან, რომ გლუტამოტარულ პროგნოზებში მოდიფიცირებული ცვლილებები შუამავლობაში არსებულ ბევრ ადაპტაციას ახდენს და აქ განვიხილეთ. ასევე გამოვლენილია პრეკლინიკური კვლევებიდან, რომ სხვა ნეიროტრანსმიტერები ჩართული არიან ნარკოტიკების, მათ შორის კანაბინოიდებისა და ოპიოიდების გაძლიერების ეფექტში. სამწუხაროდ, ცოტა ხნის წინ, PET ვიზუალიზაციის რადიომაუწყებლების შეზღუდულმა ხელმისაწვდომმა შეიზღუდა უნარი გამოიკვლიოს სხვა ნეიროტრანსმიტერების ჩართვა ნარკოტიკების ჯილდოს და ნარკომანიაში.
აბრევიატურები
- AMPA
- α-amino-xNUMX-hydroxyl-xNUMx-methyl-xNUMX-isoxazole-propionate
- CG
- გიურუზი
- CTX
- ქერქის
- D2R
- დოპამინის ტიპი 2 / 3 რეცეპტორი
- DA
- dopamine
- FDG
- ფლუოდოდეოქსიგლუკოზი
- GABA
- γ- ამინობური მჟავა
- HPA
- ჰიპოთალამური ჰიპოფიზის ღერძი
- MPH
- მეთილფენიდატი
- ნაკ
- ბირთვი accumbens
- NMDA
- n-მეთილ-d-მჟავას მჟავა
- OFC
- ორბიტატრონული ქერქის
- PET
- პოზიტრონ - ემისიური ტომოგრაფია
- PFC
- prefrontal ქერქის
- VP
- ვენტრალური პალიდიუმი
ლიტერატურა
55. Fowler JS, Volkow ND, Logan J, et al. ადამიანის ტვინში მეტამფეტამინის სწრაფი შეყვანა და ხანგრძლივად შეკავება: შედარება კოკაინთან. Neuroimage. 2008;43: 756-63. [PMC უფასო სტატია] [PubMed