뉴스 및보기
19 12월 2018
생쥐 중독에 대한 연구는 마약 중독과 관련된 강박 행동의 기초가되는 뇌 적응을 확인하고 일부 마약 사용자는 왜 강박 행동을하는지 설명 할 수 있습니다.
학대의 마약은 뇌의 기능에 많은 변화를 일으키는 복잡한 약리학 적 효과가 있습니다. 이러한 효과 중 하나는 신경 전달 물질 인 도파민을 방출하는 뉴런의 직접 또는 간접적 인 활성화로 모든 약물 남용에 흔히 발생하며 오랫동안 중독의 발달에 기여한 것으로 추측됩니다. 글쓰기 자연, Pascoli et al.1 일부 마약 사용자가 부정적인 결과에 직면 했음에도 불구하고 보상을 요구하는 이유를 설명 할 수있는 도파민 뉴런의 반복 된 활성화에 의해 유도 된 신경 생물학적 기전에 대한보고 - 인간 중독의 정의적인 특징 인 강박 행동 유형2.
저자들은 학대 약물에 의한 뇌 도파민 시스템의 활성화를 모방하기 위해 광학 유전학 접근법을 사용했다. 유전자 조작 마우스의 두뇌의 복부 피질 영역 (VTA)에서 도파민 뉴런을 활성화하기 위해 광섬유를 통해 전달되는 레이저 광선을 사용했다. 마우스는 레버를 누르면 이러한 뉴런 자체를 직접 자극 할 수 있었고 거의 40 주 동안 2 분의 테스트 기간 동안이 작용을 열성적으로 수행했습니다.
후일에, 쥐들은 무작위로 레버를 누르는 경우의 3 분의 1에 발끝에 짧은 전기 충격을 받았다. 이 상태에서의 행동은 흥미로운 가변성을 나타 냈습니다. 쥐의 40 % (renouncers라고 함)는 발 충격이 주어 졌을 때 레버 가압의 빈도를 크게 줄 였지만 (1a) 나머지 60 % (인내심)는 고통스럽게 받아 들였습니다. 도파민 신경 세포를 스스로 자극 할 수있는 기회에 대한 처벌 (그림 1b). 이 저자 중 일부는 이전에3, 끈기있는 쥐는 부정적인 결과에도 불구하고 지속적인 마약 사용을위한 모델을 제공하고 약물 사용이 강박적 인 인간 마약 사용자의 부분 집합과 병행합니다.
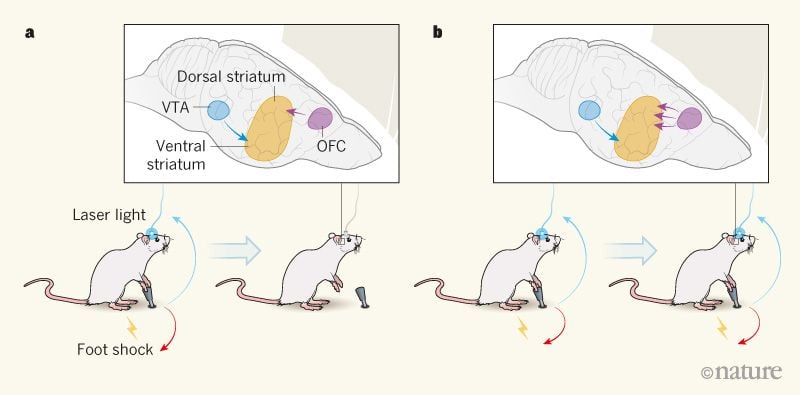
그림 1 | 뇌에서 도파민 뉴런의 강박적인 활성화. Pascoli의 연구에서 외.1마우스는 광섬유에 의해 전도 된 레이저 광의 전달을 통해 도파민 방출 뉴런을 활성화시키는 레버를 눌렀다. 복부 tegmental 영역 (VTA)에서 뇌의 복부 striatum에 투영 이러한 뉴런은 보상과 관련이 있습니다. arenouncer라고 불리는 일부 마우스는 발의 고통스러운 감전과 관련되어있을 때 레버를 누르는 동작을 줄였습니다. 등쪽 선상으로 돌출 된 안와 상 피질 (OFC)의 뉴런 사이의 연결 강도는이 생쥐에서 낮았다. b, 인내라고 불리는 다른 쥐들은 처벌에도 불구하고 계속해서 레버를 누르며 - 강박 행동의 특징입니다. 이 생쥐에서 OFC와 등 지느러미 사이의 신경 연결은 renouncers에서보다 컸다. 저자가 끈적 끈적한 생쥐에서 이러한 연결을 약화 시켰을 때 동물의 강박 행동이 감소했습니다 (표시되지 않음).
저자들은 다음으로 인내심의 두뇌와 renouncers의 차이점을 알아 내려고했습니다. 그들은 서로 다른 뇌 영역을 연결하는 뉴런의 활동을 실시간으로 측정하여 생쥐가 레버를 눌렀을 때 어떤 네트워크가 활성화되었는지 확인했습니다. 의사 결정에 관여하는 안와 외 피질 (OFC)과 자발적인 행동을하는 지느러미 줄무늬 사이의 의사 소통은 도파민 자기 자극과 함께 충격을 받기를 원하는 마우스의 레버를 누르기 전에 증가했다. 이 신경 경로의 Optogenetic 억제는 끈적 끈적한 생쥐가 포유 동물을 포기하게 만들었다. 이 결과는 OFC에서 등쪽의 선조로 돌출하는 뉴런의 증가 된 활성이 도파민 뉴런의 강박 반응 활성화에 필수적임을 보여준다.
그러나,이 행동 스위치는 일시적이었습니다 : optogenetic 억제가 해제되었을 때, 강박적인 행동은 참을성이 강한 생쥐에서 재개되었습니다. 저자들은 다발성 도파민 뉴런의 결과로 OFC와 등쪽의 줄무늬 뉴런을 연결하는 시냅스 - 뉴런 사이의 연결점에서의 오래 지속되는 변화가 발생할 수 있다고 추론했다. 이런 변화가 끈적 끈적한 생쥐에서만 발생한다면, 이는 그들의 지속적인 강박 행동을 설명 할 것입니다.
이 가설이 사실이라면 OFC와 지느러미 줄무늬 뉴런 사이의 시냅스 연결 강도는 renouncers보다 인내심이 커야 OFC 뉴런에 의한 더 효과적인 줄기 세포의 활성화가 가능해야합니다. 사실, Pascoli et al. 계속해서 OFC 뉴런과 등쪽 줄무늬 뉴런 사이의 시냅스의 힘이 참을성이있는 마우스에서 증가했다는 것을 보여 주었다 (그림 1). Renouncers는 실험 설정에 노출 된 적이없는 마우스와 충격을 받았지만 레버를 사용할 수없는 마우스와 함께 OFC와 등쪽 줄무늬 뉴런 사이의 낮은 시냅스 강도를 보여주었습니다.
놀랍게도 저자들은이 신경 연결의 강도를 각각 감소 시키거나 증가시킴으로써 강제 행동이 억제되거나 유발 될 수 있음을 발견했다. 영원한 생쥐에서 OFC와 등쪽 striatum 사이의 시냅스 연결의 약화는 발 충격의 가능성에 직면하여 스스로 자극하려는 의지를 감소시켰다. 반대로, renouncers는 이러한 시냅스 연결의 힘을 증가시켜 인내 할 수 있습니다. 등쪽 striatum에 투영 OFC 뉴런의 optogenetic 억제 후 관찰 일시적 반전과 달리, 시냅스 강도의 이러한 변화는 6 일 동안 지속 행동 스위치를 유도했다.
파스 콜리 et al. 쥐가 도파민 뉴런을 계속 활성화시키기 위해 고통스런 자극을 무시할 수있게 해주는 신경 적응증을 발견했다. 인간에 대한 학대 약물의 만성 소비는 동일한 도파민 보강 회로의 반복 된 활성화로 이어 지므로 유사한 신경 적응이 부정적인 결과에도 불구하고 약물 복용을 계속할 수 있습니다. 이 제안을 테스트하기 위해 우리는 OFC와 등쪽 줄무늬 뉴런 사이의 연결 강도의 변화가 쥐가 발의 충격을 받더라도 코카인, 암페타민 또는 아편 유사 제제를 투여하기 위해 지렛대를 누르는 것에서의 강박 행동을 매개하는지 결정해야합니다.
도파민 뉴런의 광 유발 자극은 학대 약물에 의한 도파민 뉴런의 활성화를 정확히 모방 하는가? optogenetic 자극 동안 레이저를 신속하게 켜고 끄는 것과 약물 작용의 시작 및 길게하는 것 사이에는 명백한 차이가 있습니다. 그럼에도 불구하고 저자들은 이전에4 코카인 섭취와 광 발생 적 활성화는 도파민 뉴런과 그 직접 하류 표적에서 거의 동일한 적응을 유도하여 현재 연구에서 사용 된 실험적 접근법에 대한 강력한 근거를 제공한다.
왜 도파민 신경 세포의 자기 자극은 개인의 부분 집합에서만 강박 행동을 유도합니까? 거의 동일한 시간과 발의 충격을 받기 전에 비슷한 수의 사건으로 쥐를 강박하고 포기하는 것은 두 가지 그룹의 두뇌가 서로 다른 방식으로 변하는 것처럼 보입니다. 마우스에 의해 자극 VTA의 도파민 뉴런은 OFC 또는 등쪽 striatum에 직접 연결하지 않으므로, 이러한 지역 간의 연결은 여러 시냅스 연결을 포함해야합니다. VTA 도파민 뉴런의 활성화가 지느러미 줄무늬의 변화를 일으킬 수있는 다중 시냅스 경로가 이전에 기재되어있다5, 비 강제적 인 약물 복용에서 강제적 인 약물 복용으로의 전환을 뒷받침하는 것으로 제안되었다6,7. 이 multisynaptic 회로의 기존 차이점은 왜 강박적인 행동과 시냅스 연결의 관련 변화가 단지 일부 마우스에서 발생하는지 설명 할 수 있습니다.
시냅스 변화는 수 일, 수년 또는 심지어 평생 지속될 수 있습니다. Pascoli에 의해 발견 된 변경 사항 외. 마약 중독의 특징 인 지속적인 행동 변화의 기초를 형성합니까? 이 문제를 해결하려면 부정적인 결과에도 불구하고 약물 자체 투여가 OFC와 등쪽 선조 사이의 연결을 강화시킴으로써 발생한다는 사실과 절정에 달하는 신경계 사슬을 움직이는 것이 도파민 시스템의 활성화라는 실험적 증거가 필요합니다. 강박제 마약 복용.
자연 564, 349-350 (2018)
doi : 10.1038 / d41586-018-07716-z