Диалози Clin Neurosci. 2013 Dec;15(4):431-43.
абстрактен
Въпреки важността на многото психосоциални фактори, в основата си, наркоманията включва биологичен процес: способността на повтаряща се експозиция на наркотици да предизвиква промени в уязвимия мозък, които предизвикват принудителното търсене и приемане на лекарства и загуба на контрол за употребата на наркотици, които определят състояние на пристрастяване. Тук разглеждаме видовете молекулярни и клетъчни адаптации, които се появяват в специфични участъци на мозъка, за да медиират свързаните с зависимостите поведенчески аномалии. Те включват промени в генната експресия, постигнати отчасти чрез епигенетични механизми, пластичност в неврофизиологичното функциониране на неврони и синапси, и свързана с нея пластичност в невроналната и синаптичната морфология, опосредствана отчасти чрез изменена сигнализация на невротрофичен фактор. Всеки от тези видове модифицирани от лекарството модификации може да се разглежда като форма на "клетъчна или молекулна памет". Нещо повече, учудващо е, че повечето форми на пластичност, свързани с пристрастяването, са много сходни с видовете пластичност, които са били свързани с по-класическите форми на „поведенческа памет“, може би отразяващи крайния репертоар на адаптивните механизми, достъпни за невроните, когато са изправени пред екологични проблеми. предизвикателства. И накрая, молекулярните и клетъчните адаптации, свързани с пристрастяването, включват повечето от същите участъци на мозъка, които медиират по-класическите форми на паметта, съобразени с мнението, че анормалните спомени са важни двигатели на синдромите на зависимост. Целта на тези проучвания, които имат за цел да обяснят молекулярната и клетъчната основа на наркоманиите, е да развият в крайна сметка биологично базирани диагностични тестове, както и по-ефективни лечения за нарушения на зависимостта.
Въведение
Пристрастяването към наркотици, което може да се определи като принудително търсене и приемане на наркотици, въпреки ужасните последствия или загуба на контрол върху употребата на наркотици, е причинено от дълготрайни промени, предизвикани от наркотици, които настъпват в някои области на мозъка.1 Само някои индивиди обаче се поддават на пристрастяване пред лицето на повтарящата се експозиция на наркотици, докато други са в състояние да използват лекарство случайно и да избягат от синдрома на пристрастяването. Генетичните фактори съставляват приблизително 50% от тази индивидуална вариабилност в уязвимостта на зависимостта и тази степен на наследственост важи за всички основни класове наркотични вещества, които предизвикват пристрастяване, включително стимуланти, опиати, алкохол, никотин и канабиноиди..2 Все още не е възможно да се идентифицират повечето от гените, които съдържат този генетичен риск, вероятно поради участието на може би стотици генетични вариации, които обобщават в един индивид, за да придадат зависимост от уязвимост (или, при други индивиди, резистентност).
Останалите 50% от риска за пристрастяване се дължи на множество фактори на околната среда, възникващи през целия живот, които взаимодействат с генетичния състав на индивида, за да го направят уязвим към пристрастяване в по-голяма или по-малка степен. Няколко вида фактори на околната среда са замесени в пристрастяването, включително психосоциални стресове, но най-мощният фактор е излагането на самия наркотик. Доказано е, че някои наркотици, по-специално никотин, повишават уязвимостта на човек към пристрастяване към друго лекарство.3 Освен това, има все повече доказателства, че въпреки редица генетични рискове за пристрастяване сред населението, излагането на достатъчно високи дози от лекарството за дълги периоди от време може да превърне някой, който има относително по-ниско генетично натоварване, в наркоман..4
През последните две десетилетия бе отбелязан голям напредък в идентифицирането както на отделните участъци на мозъка, които са важни за медииране на синдрома на пристрастяването, така и на видовете промени на молекулярно и клетъчно ниво, които лекарствата предизвикват в тези региони, за да заложат ключови аспекти. на пристрастяване.1,5 Веригата, която е получила най-голямо внимание, се нарича мезолимбична допаминова система, която включва допаминови неврони в вентралната тегментална област (VTA) на средния мозък, инервиращи средни бодливи неврони в nucleus accumbens (NAc, част от вентрален стриатум). Тези VTA неврони също иннервират много други предни мозъчни области, включително хипокампус, амигдала и префронтален кортекс (PFC).
Има смисъл да се разгледат тези лекарствени механизми за пристрастяване в този обем на паметта за три припокриващи се причини.6
- Първо, всички медикаментозни адаптации могат да се разглеждат като типове „молекулярна или клетъчна памет“: нервната клетка, подложена на такива промени, е различна в резултат на експозиция на лекарство и по този начин реагира различно на същото лекарство, към други лекарства, или в резултат на множество други стимули.
- Второ, интересно е, че много, може би повечето от видовете промени, които са били свързани със състоянието на пристрастяване (например, изменена транскрипция на ген, епигенетика, пластичност на синаптична и цяла клетка и невронална морфология и невротрофични механизми) също са замесени в традиционните форми на "поведенческа памет", като пространствена памет, кондициониране на страха и оперантно кондициониране, наред с други.
- Трето, сред зоните на мозъка, засегнати от наркотици, са тези, които са ключови неврални субстрати за поведенческа памет, включително хипокампус, амигдала и PFC. Това съвпада с нарастващото осъзнаване, че някои от най-важните характеристики на пристрастяване, наблюдавано клинично (например, жажда за наркотици и рецидив), отразяват аномалии в традиционните схеми на паметта, като дълготрайните спомени от лекарствения опит служат като мощни двигатели на патологията на зависимостта.4,7,8 Обратно, регионите за възнаграждение на мозъка (напр. VTA и NAc) силно влияят на поведенческата памет.
В тази статия се прави преглед на основните видове молекулярни и клетъчни промени, които настъпват в няколко мозъчни области в животински модели на пристрастяване, съсредоточени върху nucleus accumbens, за които понастоящем е налична повечето информация. Важно е да се отбележи, че е възможно все по-често да се валидират някои от тези промени в човешките наркомани въз основа на проучвания на мозъка след смъртта. Въпреки факта, че наркотиците на злоупотреба имат различни химически структури и действат на различни протеинови цели, поразително е, че много от известните адаптации, свързани с пристрастяването, са общи за много, а в някои случаи и за всички, злоупотребяващи с наркотици и вероятно допринасят за общи характеристики на синдром на пристрастяване.4,9 За разлика от това, много други медикаментозни адаптации са специфични за дадено лекарство и могат да медиират по-уникални аспекти на дадена зависимост. Тук се фокусираме върху стимулантните и опиатни наркотици, които предизвикват по-драматични ефекти в животинските модели в сравнение с други лекарства. Ние също така подчертаваме важни области за бъдещи изследвания, които допълнително ще увеличат познанията ни за синдромите на пристрастяването и ще преведат тези постижения в подобрени диагностични тестове и лечения.
Транскрипционни и епигенетични механизми
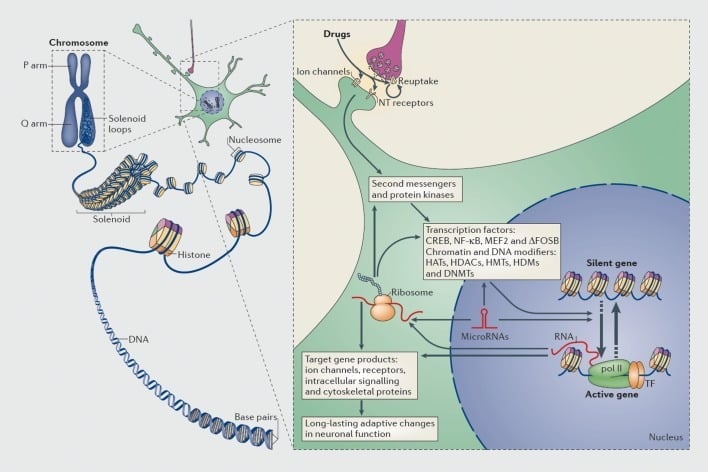
Знанието, че наркозависимите могат да останат с повишен риск от рецидив, въпреки годините на въздържание, означава, че пристрастяването включва предизвикани от наркотици промени в мозъка, които могат да бъдат много стабилни. Това накара няколко групи да разгледат промените в генната експресия като важен компонент на процеса на пристрастяване (Фигура 1). Съответно, проучвания на кандидат-гени или проучвания, обхващащи целия геном, включващи ДНК микрорайони и по-скоро RNA-seq (високопроизводително секвениране на експресирани РНК) е идентифицирал многобройни гени, чиято експресия се променя в дадена мозъчна област при модели на гризачи и примати при пристрастяване и при хора-зависими (напр. справки 10-17). Примери за такива гени са обсъдени в следващите раздели на този преглед.
Механизми на транскрипционно и епигенетично регулиране чрез наркотични средства. В еукариотните клетки, ДНК се организира чрез опаковане около хистонови октомери, за да се образуват нуклеозоми, които след това се организират и кондензират, за да образуват хромозоми (лява част). Само чрез временно разчупване на уплътнения хроматин ДНК на специфичен ген може да бъде достъпен за транскрипционния механизъм. Наркотиците от злоупотреба действат чрез синаптични цели, като механизми за обратното захващане, йонни канали и невротрансмитерни (NT) рецептори, за да променят вътреклетъчните сигнални каскади (дясна част). Това води до активиране или инхибиране на транскрипционни фактори (TFs) и на много други ядрени цели, включително хроматин-регулаторни протеини (показани с дебели стрелки); подробните механизми, включени в синаптичната регулация на хроматин-регулаторните протеини, остават слабо разбрани. Тези процеси в крайна сметка водят до индукция или потискане на определени гени, включително тези за некодиращи РНК, такива като микроРНК; променената експресия на някои от тези гени може на свой ред допълнително да регулира генната транскрипция. Предполага се, че някои от тези индуцирани от лекарството промени на ниво хроматин са изключително стабилни и по този начин са в основата на дълготрайното поведение, което определя пристрастяването. CREB, цикличен AMP-реагиращ свързващ протеин на елемента; DNMT, ДНК метилтрансферази; HATs, хистонови ацетилтрансферази; HDACs, хистонови деацетилази; HDMs, хистонови деметилази; HMTs, хистон метилтрансферази; MEF2, миоцит-специфичен усилващ фактор 2; NF-kB, ядрен фактор-КВ; pol II, РНК полимераза II. Възпроизвежда се от ref 44: Robison AJ, Nestler EJ. Транскрипционни и епигенетични механизми на пристрастяване. Нат Rev Neurosci. 2011: 12: 623-637.
По същия начин, много видове транскрипционни фактори - протеини, които се свързват с регулаторни области на гени и по този начин увеличават или намаляват транскрипцията на тези гени - са замесени в медиирането на дългосрочните ефекти на лекарството от злоупотреба върху генната експресия в мозъка, Известни примери включват CREB (cAMP реагиращ елемент свързващ протеин), ΔFosB (транскрипционен фактор на Fos фамилия), NFkB (ядрен фактор kB), MEF2 (миоцитен фактор-2) и глюкокортикоидни рецептори, между няколко други.5,10,18-22 Все по-възможно е да се разберат клетъчните сигнални пътища, чрез които злоупотребите с наркотици активират даден транскрипционен фактор в мозъка и причинно-следствената връзка на такова активиране с целевите гени на този транскрипционен фактор и със специфичните поведенчески аспекти на пристрастяването (вж. Фигура 1). Този напредък е илюстриран чрез разглеждане на CREB и ΔFosB, които са най-добре изучените транскрипционни фактори при модели на пристрастяване.
сАМП Реактивен елемент свързващ протеин
Стимулиращи и опиатни лекарства за злоупотреба се активират CREB в няколко области на мозъка, които са важни за пристрастяването, включително и в NAc.23,24 Известно е, че CREB се активира в други системи чрез сАМР, Са2+и пътища на растежния фактор,25 и все още не е известно кой от тях медиира неговото активиране в NAc чрез лекарствени средства за злоупотреба. Показано е, че активирането на CREB в NAc на лекарство представлява класически отрицателен механизъм за обратна връзка, при което CREB служи за намаляване на чувствителността на животното към възнаграждаващите ефекти на тези лекарства (толерантност) и за медииране на отрицателно емоционално състояние по време на отнемане на наркотици (зависимост).18,26,27 Неотдавна тези ефекти са показали, че предизвикват повишаване на самостоятелното приложение на лекарството и рецидив, вероятно чрез процес на отрицателно подсилване.28 Тези действия на CREB изглежда включват двата основни подтипа на NAc средни бодливи неврони, тези, които изразяват предимно D1 срещу D2 допаминови рецептори.24 IНеслучайно голяма част от литературата показва, че CREB, действащ в хипокампуса и амигдалата, е ключова молекула в поведенческата памет.29-31 Тази широка роля в пристрастяването и поведенческата памет вероятно отразява факта, че невроните са пропити с ограничен брой молекулярни механизми, с които да се адаптират към постоянно променящата се среда.
Целевите гени за CREB, които медиират този поведенчески фенотип, са идентифицирани чрез геном-анализи, както и по-избрани усилия.10,18,32 Един пример е опиоидният пептид динорфин: стимулиране на стимулация на експресия на динорфин в NAc неврони, медиирани чрез CREB, повишава активирането на динорфин на k опиоидни рецептори върху VTA допаминови неврони и по този начин потиска допаминергичното предаване към NAc и намалява възнаграждението.18 Няколко други CREB мишени са показали, че са важни за индуцирана от лекарството синаптична пластичност, както е обсъдено по-долу. Докато CREB се активира и в други области на мозъка чрез стимуланти и опиати,23,24 по-малко се знае за поведенческите последици от този ефект и целевите гени, чрез които те се появяват. По същия начин се знае по-малко за ролята на CREB при посредничеството в действията на други наркотици.19
ΔFosB
Острата експозиция на почти всяко лекарство за злоупотреба предизвиква всички факторни транскрипционни фактори на Fos в NAc и няколко други области на мозъка. Тази индукция е бърза, но също силно преходна, с нива на Fos протеин, които се връщат към нормални в рамките на 8 до 12 часа. Уникално сред тези протеини от семейството Fos е ΔFosB, пресечен продукт на гена FosB, което поради необичайната си стабилност постепенно се натрупва чрез курс на повторно излагане на лекарството и става преобладаващият Fos протеин, експресиран при тези условия.22,33 Освен това, поради тази стабилност, нивата на ΔFosB продължават седмици след оттегляне на лекарството. Такава хронична индукция на ΔFosB е демонстрирана за почти всички лекарства за злоупотреба34 и за повечето лекарства е селективен за Dl-тип NAc неврони.34,35 Също така беше доказани при хора-зависими.35 Голяма част от литературата показва, че такава индукция на ΔFosB в D1-тип NAc неврони повишава чувствителността на животното към лекарството, както и естествените награди и насърчава самоприлагането на лекарството, вероятно чрез процес на положително подсилване (виж референциите 34 до 38). Интересно е, че индуцирането на ΔFosB в NAc е по-драматично при юноши, време на по-голяма уязвимост при пристрастяване.,39 и неговото индуциране от никотин е доказано, че медиира подобряването на никотиновия шлюз подобряване на възнаграждението на кокаин.40
Що се отнася до CREB, многобройни целеви гени за ΔFosB са идентифицирани в NAc чрез използване на кандидат ген и подходи за широк геном.10,32 Докато CREB индуцира динорфин, ΔFosB го потиска, което допринася за ефектите на ΔFosB за възнаграждение.38 Друга мишена на ΔFosB е cFos: тъй като ΔFosB се натрупва с повтаряща се лекарствена експозиция, тя подтиска c-Fos и допринася за молекулярния превключвател, при който ΔFosB се индуцира селективно в хронично третирано състояние на лекарството.41 Много други ΔFosB мишени са доказали, че медиират способността на някои лекарства за злоупотреба да индуцират синаптична пластичност в NAc и свързаните с нея промени в дендритната arborization на NAc средни бодливи неврони, както ще бъде обсъдено по-долу.
Функционалните последици от индуцирането на ΔFosB в други участъци на мозъка са по-малко разбрани, въпреки че неговата индукция в орбитофронталния кортекс (OFC) е проучена по-подробно. Тук ΔFosB медиира толерантността, която се проявява към когнитивно нарушаващите ефекти на кокаина по време на хода на хронична експозиция, и тази адаптация е свързана с повишено самоконтрол на кокаина..42,43
Анализите, обхващащи целия геном, предполагат няколко потенциални целеви гена, които медиират тези ефекти.42 Въпреки уникалните времеви свойства на ΔFosB и знанието, че той се индуцира в традиционните схеми на паметта (напр. Хипокампус), все още не е изследвано ролята на ΔFosB в поведенческата памет, интересна тема за бъдещи изследвания.
Епигенетични механизми
През последните години проучванията на транскрипцията бяха изтласкани една стъпка напред към епигенетиката44 (Вж. Фигура 1)което може да бъде широко дефинирано като промяна в генната експресия, която се проявява в отсъствието на промяна в ДНК последователността. Епигенетичните механизми контролират опаковането на ДНК в клетъчното ядро чрез взаимодействия с хистони и много други видове ядрени протеини, които заедно съдържат хроматин. Експресията на ген се контролира от състоянието на тази опаковка чрез ковалентната модификация на хистони, други протеини и самата ДНК. Само някои примери ацетилиране на хистони има склонност да стимулира генна активация, метилирането на хистони може или да стимулира генна активация или репресия в зависимост от Lys остатъка, подложен на тази модификация, и метилирането на ДНК обикновено се свързва с генна репресия, въпреки че някои варианти на метилиране ( например, 5-хидроксиметилиране) може да бъде свързано с генна активация.
Епигенетиката е привлекателен механизъм, защото в други системи, например, в биологията на развитието и рака, някои епигенетични модификации могат да бъдат постоянни. Поради тази причина, епигенетиката е преследвана както в моделите на учене, така и в паметта (напр. справки 45-48), както и при пристрастяването;44,49 и в двете системи са докладвани дълбоки промени в ацетилирането и метилирането на хистони и в метилирането на ДНК. Като само един пример, хистон метилтрансферазата, G9a, е включена в двете памет50 и пристрастяване.51,52 В моделите за пристрастяване, Изразът G9a е понижен в NAc в отговор на стимулиращи или опиатни лекарства за злоупотреба и tДоказано е, че неговото усилване на благоприятните ефекти на тези лекарства.51,52 Интересно е, че подтискането на кокаина на G9a се медиира от ΔFosB. G9a катализира диметилирането на Lys9 на хистон H3 (H3K9me2), основен медиатор на генна репресия. ChIP-чип или ChIP-seq (имунопреципитация на хроматин, последвано съответно от промоторни чипове или последователност с висока пропускателна способност) се използва за получаване на карти на генома в гените в NAc, които показват променена H3K9me2 след експозиция на стимулант или опиат.32,52,53 Чрез припокриване на тези генни списъци с геномно-широки списъци на промени в генната експресия, както и с карти на генома на много други форми на епигенетични модификации (например, ΔFosB свързване, CREB свързване, други хистонови модификации и т.н.),32,53 би трябвало да е възможно да се идентифицира все по-пълен набор от гени, които се регулират от лекарства за злоупотреба и да се разберат основните епигенетични механизми.
Друга форма на епигенетична регулация, свързана с паметта и зависимостта, е генерирането на микроРНК. Тези малки, некодиращи РНК се свързват с комплементарни области на иРНК и по този начин потискат техния транслация или индуцират тяхното разграждане. Заличаването на Argonaut, протеин, който е от решаващо значение за обработката на miRNAs, променя поведенческите реакции към кокаина, с ясно изразени ефекти, наблюдавани за D1- срещу D2-тип средни бодливи неврони.54 Установено е също, че няколко специфични miPHKs се регулират от експозицията на лекарството и, от своя страна, да повлияват поведенческите реакции към лекарствата (например, refs 55,56). Ще бъде вълнуващо в бъдещите проучвания да се идентифицират целите на мРНК на тези miRNAs и да се характеризира как те влияят на процеса на пристрастяване.
Синаптична пластичност
Същите общи типове синаптични модификации при глутаматергични синапси, които са замесени в хипокампуса и амигдалата в поведенческата памет (виж други статии в този брой), също са показали, че се срещат в районите за награждаване на мозъци в модели на пристрастяване и са важни за медииране процеса на пристрастяване.57,58 Такава индуцирана от лекарството синаптична пластичност е описана в няколко области на мозъка, но тук се концентрираме върху NAc, където повечето от изследванията са съсредоточени досега (Фигура 2).
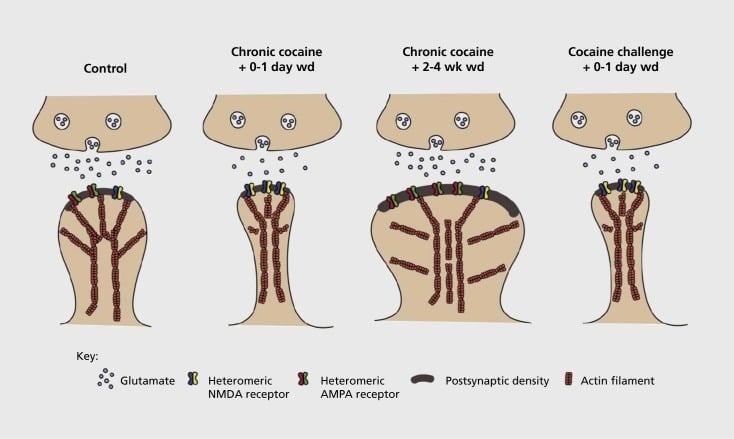
Модел на синаптична и структурна пластичност, свързана с зависимостта, в nucleus accumbens (NAc). Хроничното излагане на кокаин води до временна и преходна реорганизация на глутаматни рецептори на α-амино-ХНУМХ-хидрокси-ХНУМХ-метил-ХНУМХ-изоксазолпропионова киселина (АМРА) и N-метил-D-аспарагинова киселина (NMDA) в среда на NAc костни неврон (MSN) синапси, както и структурни промени в гръбначния стълб на NAc MSNs, които корелират с различни форми на синаптична пластичност. Например, хроничният кокаин индуцира повърхностна експресия на NMDA рецептори, тиха формация на синапса и дългосрочна депресия (LTD) в ранните точки на оттегляне. По време на по-продължително отнемане (wd), тези синаптични промени се променят, като резултатът е повишена експресия на повърхностни АМРА рецептори, консолидиране на синапса в гръбнака и дългосрочно усилване (LTP). Тези ефекти бързо се връщат отново при излагане на предизвикателна доза кокаин, което води до преструктуриране на гръбначния стълб в тънки бодли и понижаване на синаптичната сила.
Първоначалните експерименти показват, че многократното излагане на стимулантни лекарства на злоупотреба предизвиква LTD (дълготрайна депресия), подобно на състояние при глутаматергични синапси в NAc.59 Въпреки това, по-новите разработки са показали, че такава пластичност е силно зависима от времето, като LTD се появява рано след последната експозиция на кокаин, развивайки се в по-дълго състояние на LTP (дългосрочно усилване) след по-дълги точки на оттегляне.60,61 Тази работа, която досега е била извършвана предимно с помощта на изследовател, приложен - за разлика от самостоятелно прилаганите - лекарства, е определила необходимостта от по-систематични изследвания в моделите за самостоятелно администриране, които проследяват формите на синаптичната пластичност, които се срещат при глутаматергичните синапси в NAc по време на детайлен курс от придобиване на самостоятелно администриране до неговото поддържане, през различни времена на оттегляне и изчезване, и в отговор на стимулиращи рецидиви стимули. Досегашната работа също така дефинира някои от молекулярните механизми, които допринасят за тази индуцирана от лекарството синаптична пластичност, включително трафик на АМРА рецептори към синапса, може би медииран частично чрез CaMKII (Ca)2+/ калмодулин-зависима протеин киназа II) фосфорилиране на някои АМРА рецепторни субединици, както и променена експресия на АМРА рецепторни субединици (например, 60,62-65, Фигури 2 и 3). Ролята на CREB и ΔFosB е замесена в тези явления, както и в свързаните с тях промени в морфологията на глутаматергичните синапси (виж по-долу). Например, GluAl е мишена за CREB в NAc, където GluA2 и CaMKII са двете мишени на ΔFosB, в тази област на мозъка .35,36,66,67 Движейки се напред, ще бъде важно да се свържат специфичните адаптации към зависимите от времето промени в синаптичната функция и поведенческите характеристики на пристрастяването.
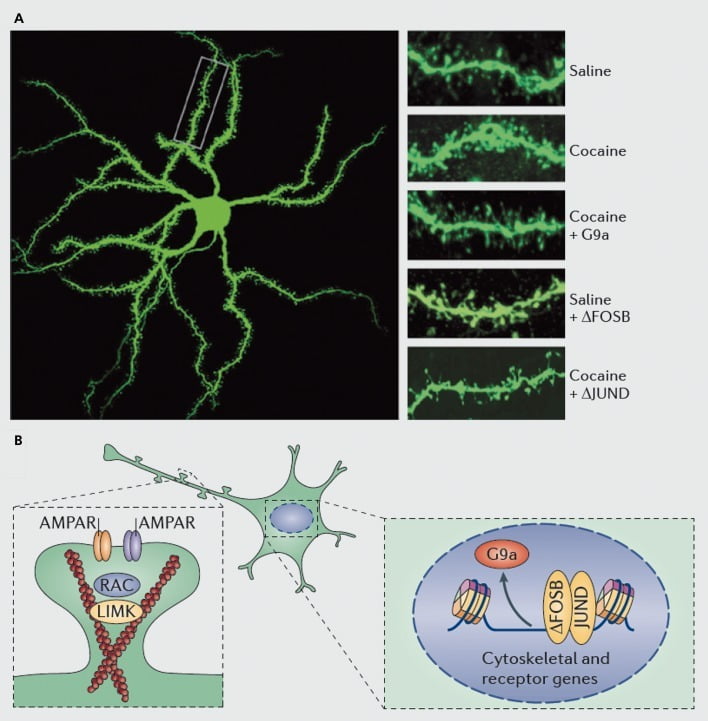
Молекулярни механизми, залегнали в основата на индуцирането на кокаин на дендритни бодли върху ядрено натрупване (NAc) средно бодливи неврони. А) показва индуцирано от кокаин увеличение на дендритния брой на гръбначния стълб, което може да бъде блокирано чрез вирусна свръхекспресия на G9a или JunD (антагонист на AP1-медиирана транскрипция) или имитирано от вирусна свръхекспресия на FosB. Б) Регулирането на трафика на AMPA рецептори (AMPAR) и на актиновия цитоскелет (вляво), както и регулирането на транскрипцията на глутаматни рецептори и регулаторните протеини на актина (например, медиирани чрез ΔFosB, вдясно) играят важна роля в посредничеството на регулирането на кокаина на NAc дендритна плътност на гръбначния стълб. UMK, LIM домейн киназа; RAC, свързан с Ras субстрат на C3 ботулинов токсин.
Новите експериментални инструменти правят възможно за пръв път да се дефинира с нарастваща прецизност кои конкретни вериги показват тези форми на синаптична пластичност и какви поведенчески аномалии те медиират. Например, tчерупките и ядрените подрегиони на NAc показват разлики в лекарствената индуцирана синаптична пластичност, както и D1- спрямо D2-тип средни бодливи неврони във всеки субрегион.60,63,64,67 По същия начин, оптогенетичните експерименти са предоставили ново разбиране за приноса на определена форма на синаптична пластичност (например, LTD) при специфични популации на глутаматергични синапси в NAc, например, тези, произтичащи от медиалния PFC срещу базалатералната амигдала срещу вентрален субикулум (основната продукция) на хипокампуса).68-70 В крайна сметка ще е необходимо да се припокрият индуцираните от лекарства молекулярни адаптации във всеки от тези аферентни неврони със специфични за синапса адаптации, които се случват в техните постсинаптични дендрити, за да се състави цялостно разбиране за това как злоупотребите с наркотици модифицират мозъчната верига, за да задвижат определени аспекти на пристрастена държава. Това начинание ще изисква по-голяма оценка на лекарствено-индуцираната пластичност при инхибиторните синапси в същите тези мозъчни региони, област, която е получила много малко внимание към днешна дата.65
Пластичност на цели клетки
Докато по-голямата част от изследванията, включващи неврофизиологични промени в невроните при явления на злоупотреба с наркотици, както при феномените на ученето и паметта, се фокусират върху синаптичната пластичност, има все повече доказателства за важността на пластичността на цялата клетка. Пластичност на цели клетки, наричана също хомеостатична пластичност,71 включва промени в присъщата възбудимост на цялата нервна клетка по начин, който не е синапсно-специфичен. Като се има предвид, че някои характеристики на пристрастяването към наркотици включват повишена или намалена чувствителност към лекарството, има смисъл, че повишената или намалена електрическа възбудимост на някои нервни клетки допринася за тези поведенчески адаптации.5
- най-добре установеният пример за пластичност на цяла клетка към лекарство от злоупотреба е способността на хроничните опиати да повишават присъщата възбудимост на норадренергичните неврони на locus coeruleus (LC)).72 Тази повишена възбудимост се медиира чрез CREB и неговата индукция на някои изоформи на аденилил циклаза, които предизвикват повишено изгаряне на LC неврони, може би чрез индукция на Na + канали.72-75 Тази свръхчувствителност на LC-невроните представлява класически механизъм на толерантност и зависимост и предизвиква някои от признаците и симптомите на оттегляне на опиатите. Интересно е, че CREB медиира подобна форма на цялата клетъчна пластичност в NAc средни бодливи неврони, които също се превръщат в свръхвъзбудими чрез хронично излагане на наркотици чрез злоупотреба чрез CREB.76 По този начин ще бъде от решаващо значение в бъдещите проучвания да се разбере как CREB-медиираната синаптична пластичност на глутаматергичните синапси върху NAc средни бодливи неврони65,66 съчетания с CREB-медиирана вътрешновъзбудимост на тези неврони76 да контролират поведенческите характеристики на пристрастяването.
Друг пример за пластичност на цяла клетка при моделите на пристрастяване е свръхвъзбудимостта на VTA допаминови неврони, която се появява след хронично излагане на опиатни лекарства с нарушенияи (Фигура 4).77,78 Тази адаптация, която е свързана с морфологични промени в тези нервни клетки (виж следващия раздел), не се медиира от CREB, а се постига чрез регулиране на невротрофични сигнални каскади, както е описано по-долу.

Работен модел на хронични индуцирани от морфин адаптации в неврони на допамин на вентрална тегментална област (VTA). Хроничният морфин намалява размера на VTA допамин (DA), но увеличава невронната възбудимост, докато допаминовото предаване към nucleus accumbens се намалява. Нетният ефект на морфина е по-малко реагиращ начин на възнаграждение, т.е. толерантност към възнаграждение. Регулирането на сигнализацията на IRS2-AKT във VTA медиира ефектите на хроничния морфин върху размера на сома и електрическата възбудимост; ефектът върху възбудимостта се медиира чрез намалени токове на γ-аминомаслена киселина (GABA) A и потискане на експресията на K 'канал, Индуцираната с морфин регулиране на активността на mTORC2 във VTA е от решаващо значение за тези морфо-индуцирани морфологични и физиологични адаптации, както и за толерантност към възнаграждение. За разлика от mT0RC2, хроничният морфин повишава активността на mTORCI, което не влияе на тези предизвикани от морфин адаптации. BDNF, получен от мозъка невротрофичен фактор; IRS, инсулинова рецепторна субстанция; mTORC, mTOR комплекс; AKT, протеин киназа В Възпроизведен от ref 77
Морфологична пластичност и невротрофични механизми
Все повече доказателства, много от тях от проучвания на хипокампалните и мозъчните кортикални неврони, показват, че промените в синаптичната пластичност са свързани с морфологични промени при синапсите. Например, LTD и генерирането на тихи синапси са свързани с образуването на тънки или къси дендритни бодли, докато LTP е свързан с по-големи, гъбообразни бодли.79,80 По този начин е интересно, че областта на злоупотребата с наркотици се фокусира върху промените, предизвикани от наркотици в дендритни бодли в продължение на> 15 години. Хронично излагане на стимулиращите лекарства за злоупотреба увеличават плътността на дендритните гръбначни стълбове на средните бодливи неврони на NAc, промяна, която преобладава за неврони от типа Dl.67,81,82 Индукцията на бодли се свързва в по-голямата си част с чувствителни поведенчески реакции към тези лекарства, въпреки че някои доказателства противоречат на тази гледна точка.
Както при проучванията на синаптичната пластичност, обаче, много повече работа е необходима, за да се дефинират системно промените в дендритните бодли, които възникват по време на хода на самостоятелно приложение, оттегляне и рецидив. Sдосегашни проучвания, включващи лекарство-изследовател и самостоятелно прилагано лекарство, предполагат много различни промени в.83-86 Също така ще бъде важно да се определят точните молекулярни механизми, чрез които кокаинът или друг стимулант произвежда тези зависими от времето и специфични за клетките ефекти. Показано е, че ΔFosB е едновременно необходимо и достатъчно за индуциране на незрели бодли на Dl-тип NAc неврони..35,51,67 Подобна регулация се случва в съгласие с регулирането на кокаин и ΔFosB на няколко протеини, за които е известно, че контролират реорганизацията на актиновия цитоскелет. Като един пример, транскрипционната регулация на няколко фактора за обмен на гуанин нуклеотид и GTP-аза активиращи протеини, обогатява Rac1, малка GTPase, за преходно намаляване на активността в отговор на всяка експозиция на кокаин, и такива пулсиращи понижения в активността на Rac1. Rac1, за да се медиира индукция на незрели бодли.87 Тези ефекти на Racl вероятно се появяват чрез неговия контрол на кофилин и други актинови регулаторни протеини, за които също е доказано, че медиират кокаиновата регулация на растежа на гръбначния стълб.87,88 Важно е обаче да се подчертае, че това е само един път, участващ в регулирането на кокаина на незрели бодли, тъй като е доказано, че и няколко други протеина играят съществена роля, включително CDK5 (циклин-зависима киназа-5), CaMKII, NFkB , MEF2, CREB, G9a и DNMT3 (ДНК метилтрансф ераза 3а), за да назовем само няколко.20,21,35,51,67,89,90 Интересно е, че кокаиновата регулация на няколко от тези гени, включително индуцирането на CDK5, CaMKII и NFkB и репресията на G9a, също се медиира чрез ΔFosB.20,35,51,91
Изненадващо, опиатните лекарства за злоупотреба упражняват противоположния ефект и намаляват плътността на дендритните гръбначни стълбове на NAc средните бодливи неврони..81 Малко се знае за последиците от поведението на тази адаптация и за включените молекулярни механизми. Това явление е, въпреки това, изненадващо, като се има предвид, че CREB и ΔFosB са индуцирани от двата стимуланта и опиатите и и двете са включени в стимулираната индуцирана индукция на NAc дендритна плътност на гръбначния стълб. Това повдига въпроса как опиатите потискат плътността на гръбначния стълб на NAc въпреки тяхното индуциране на тези фактори.
Другата основна форма на морфологична пластичност, наблюдавана в моделите за злоупотреба с наркотици, е физическото намаляване на размера на клетъчния сома на VTA допаминови неврони, предизвикани от хронично приложение на опиати..77,92,93 Подобна адаптация възниква в отговор на канабиноиди.94 Това свиване на VTA допаминови неврони, което се случва с опиатно самоуправление93 и е документиран при човешки хероинови наркомани, изследвани след смъртта,77 изглежда, че посредничи за толерантност към възнаграждението и е свързано с понижено освобождаване на допамин в NAc. Значителни доказателства сега показват, че това намаляване на размера на клетъчната сома се медиира от потискане на опиатите на експресия на невротрофичен фактор (BDNF), получена от мозъка, в рамките на тези неврони. Ние директно свързваме индуцираното с опиати отнемане на BDNF подкрепата и VTA невроновото свиване до намалена активност на низходящите BDNF сигнални каскади във VTA допаминови неврони, специфично намалена активност на IRS2 (инсулинов рецепторен субстрат-2), AKT (серин-треонин). киназа) и TORC2 (мишена на рапамицин-2, която е нечувствителна към рапамицин).77,93 Ние също така свързахме това регулиране на BDNF директно с повишената възбудимост, която морфинът индуцира в тези неврони, както бе отбелязано по-рано.77,78 Наистина, намаленият размер на клетъчния сома и повишената възбудимост са плътно свързани, тъй като индукцията на една води до другата и обратно. Този контрол върху клетъчната възбудимост включва потискане на К+ канали и GABAA ток в тези неврони.
Тази роля на BDNF в контрола на морфиновите отговори на нивото на VTA контрастира с много различното му участие в действията на кокаин и други стимуланти. Стимулантите индуцират BDNF сигнализиране към NAc, ефект, дължащ се на повишена локална синтеза на BDNF, както и повишено освобождаване от няколко аферентни области.95 Освен това, повишеното BDNF сигнализиране в NAc, но не и във VTA, е доказано, че насърчава поведенческите ефекти на тези лекарства, включително тяхното самостоятелно приложение.95,96 Противоположната регулация на сигнализирането на BDNF по пътя на VTA-NAc от опиати срещу стимуланти поражда възможността подобни различия да медиират противоположната регулация на наркотиците на дендритни гръбначни стълбове на NAc, която сега е в процес на разследване.
Бъдещи насоки
Горният разказ подчертава огромния напредък, постигнат в разбирането на молекулярните и клетъчните адаптации, които се появяват в районите за награждаване на мозъка в отговор на повтарящото се излагане на наркотици и в свързаните индивидуални адаптации към определени поведенчески характеристики на синдромите на пристрастяване при животински модели. , Въпреки тези постижения, основните въпроси остават. Повечето от съществуващите ни знания се фокусират върху VTA и NAc, с много по-малко информация за други ключови области на мозъка, които също са от решаващо значение за наркоманиите. В допълнение, всички експериментални демонстрации на причинната роля на молекулярно-клетъчната адаптация в свързано с наркотиците поведение са манипулирали индивидуалните адаптации един по един. Манипулирането на многобройни адаптации в същото време е далеч по-трудно, но също така е от съществено значение, тъй като знаем, че лекарствата произвеждат голям брой различни видове промени дори в отделните неврони, които вероятно се събират в сложни начини за влияние върху поведението. Такъв подход за системна биология ще бъде от решаващо значение за окончателното разрушаване на биологичните основи на пристрастяването. Накрая, усилията за разбиране на молекулярно-клетъчните механизми на спомените, свързани с пристрастяването, се намират в точката, в която всички други усилия за разбиране на биологичната основа на поведенческата памет сега се борят: способността ни да свързваме биологичните феномени с комплексната поведенческа памет остава изключително трудна. Преодоляването на това разделение представлява може би най-голямото предизвикателство в невронауките.
Благодарности
Тази работа е подкрепена от грантове от Националния институт за злоупотреба с наркотици.
Избрани съкращения и акроними
- Нак
- nucleus accumbens
- CREB
- сАМР отговорен елемент свързващ протеин
- ΔFosB
- фактор на транскрипция на фамилията на Fos
- VTA
- вентрална тегментова област
- AMPA
- а-амино-ХНУМХ-хидрокси-ХНУМХ-метил-ХНУМХ-изоксазолпропионова киселина
- LTD
- дългосрочна депресия
- LTP
- дългосрочно протентиране
- BDNF
- получен от мозъка невротрофичен фактор
- NKkB
- ядрен фактор kB
СПРАВКИ