Дијалози Клинични неврози. 2013 Dec;15(4):431-43.
Апстракт
И покрај важноста на бројните психосоцијални фактори, во суштината, зависностите од дрога подразбираат биолошки процес: способност за повторна изложеност на дрога злоупотреба да предизвика промени во ранлив мозок што го присилува компулсивното барање и земање дрога и губење на контролата преку употреба на лекови, кои дефинираат состојба на зависност. Еве, ги разгледуваме видовите молекуларни и клеточни адаптации што се случуваат во специфични региони на мозокот за да посредуваат во абнормалности во однесувањето поврзани со зависностите Овие вклучуваат измени во изразувањето на гени, што се постигнуваат делумно преку епигенетски механизми, пластичност во неврофизиолошкото функционирање на невроните и синапсите и придружната пластичност во невронската и синаптичката морфологија, посредувани делумно со изменето сигнализирање на невротрофичен фактор. Секој од овие типови модификации предизвикани од лекови може да се смета како форма на „мобилна или молекуларна меморија“. Покрај тоа, впечатливо е дека повеќето форми поврзани со зависност од пластика се многу слични на видовите пластичност кои се поврзани со повеќе класични форми на „однесување во однесувањето“, што можеби го рефлектира конечниот репертоар на адаптивни механизми кои им се достапни на невроните кога се соочуваат со животна средина предизвици. Конечно, молекуларните и мобилните адаптации поврзани со зависностите вклучуваат повеќето исти региони на мозокот кои посредуваат во повеќе класични форми на меморија, во согласност со ставот дека абнормалните спомени се важни двигатели на синдромите на зависност. Целта на овие студии кои имаат за цел да ја објаснат молекуларната и клеточната основа на зависноста од дрога е на крајот да развијат биолошки-базирани тестови за дијагностицирање, како и поефективни третмани за нарушувања на зависност.
Вовед
Зависноста од дрога, која може да се дефинира како компулсивно барање и земање дрога и покрај ужасните последици или губење на контролата врз употребата на дрога, е предизвикана од долготрајни промени предизвикани од дрога што се случуваат во одредени региони на мозокот.1 Меѓутоа, само некои лица подлегнуваат на зависност, при повторна изложеност на дрога, додека други се способни да користат лек повремено и да избегаат од синдром на зависност. Генетските фактори сочинуваат приближно 50% од оваа индивидуална варијабилност во зависност од ранливост и овој степен на наследност важи за сите поголеми класи на зависност од лекови, вклучително и стимуланси, опијати, алкохол, никотин и канабиноиди..2 Сè уште не е можно да се идентификуваат повеќето гени што го содржат овој генетски ризик, најверојатно поради вклученоста на стотици генетски варијации кои се собираат во една индивидуа за да се даде ранливост на зависност (или, кај други лица, отпор).
Останатите 50% од ризикот од зависност се должи на низа фактори на животната средина, кои се јавуваат во текот на целиот живот, кои комуницираат со генетскиот состав на една личност за да го направат ранлив на зависноста во поголема или помала мера. Неколку видови фактори на животната средина се вмешани во зависноста, вклучително и психосоцијални стресови, но далеку најмоќниот фактор е изложеност на дрога на злоупотреба сама по себе. Се покажа дека одредени „портални“ лекови, особено никотин, ја зголемуваат ранливоста на некој од зависноста од друга дрога.3 Покрај тоа, се зголемуваат докази дека, и покрај низа генетски ризици од зависност кај населението, изложеноста на доволно високи дози на лек за долги периоди на време може да преобрази некој кој има релативно пониско генетско оптеретување во зависник.4
Постигнат е голем напредок во текот на изминатите две децении во идентификувањето и на дискретните региони на мозокот, кои се важни во медијацијата на синдром на зависност, како и видовите на промени на молекуларно и клеточно ниво што лековите ги наметнуваат во овие региони да ги поткрепат клучните аспекти на зависност.1,5 Колото што привлече најголемо внимание е наведено како мезолимбичен допамин систем, кој вклучува допамин неврони во областа на вентралниот тегментален дел (VTA) на средниот мозок кој го инервира средното 'рбетниот неврон во јадрото акумулира (NAc, дел од вентралниот стритум). Овие VTA неврони исто така се вклопуваат во многу други области на мозокот, вклучувајќи хипокампус, амигдала и префронтален кортекс (ПФЦ).
Има смисла да се земат предвид овие механизми за зависности предизвикани од дрога во овој волумен на меморијата од три причини за преклопување.6
- Прво, сите адаптации предизвикани од дрога може да се сметаат како видови на „молекуларна или клеточна меморија:“ нервната клетка што се подложува на вакви промени е различна како резултат на изложеност на лекови и оттука реагира различно на истиот лек, на други лекови или на низа други стимули како резултат.
- Второ, интересно е што многу, можеби повеќето, од типовите промени што се поврзани со состојба на зависност (на пр., изменета транскрипција на гени, епигенетика, пластичност на синаптичка и цела клетка и невронска морфологија и невротрофни механизми) меѓу другите, исто така, се вклучени во традиционалните форми на „меморија во однесувањето“, како што се просторна меморија, климатизација на страв и климатизација.
- Трето, меѓу мозочните региони погодени од злоупотреба на лекови се оние кои се клучни нервни подлоги за меморија во однесувањето, вклучувајќи хипокампус, амигдала и ПФЦ. Ова се совпаѓа со зголемувањето на сфаќањето дека некои од најважните карактеристики на зависностите кои се гледаат клинички (на пр., Копнеж кон дрога и релапс), рефлектираат абнормалности во традиционалните мемориски кола, со долгорочни сеќавања на искуството со лекови кои служат како моќни двигатели на патологија на зависност.4,7,8 Спротивно на тоа, регионите на награда на мозокот (на пр., ВТА и NAc) потентно влијаат врз меморијата на однесувањето.
Оваа статија дава преглед на главните типови на молекуларни и клеточни промени што се случуваат во неколку региони на мозокот кај животински модели на зависност, концентрирајќи се на јаглеродните акуми, за кои повеќето информации се моментално достапни. Уште поважно, можно е се повеќе да се валидираат некои од овие промени кај зависниците од луѓе врз основа на студии за постмортамски мозоци. И покрај фактот дека дрогата за злоупотреба има различни хемиски структури и делува на различни протеински цели, зачудувачки е што многу истакнати адаптации поврзани со зависностите се вообичаени за многумина, а во некои случаи сите, дрога на злоупотреба и најверојатно придонесуваат за споделени одлики на синдром на зависност.4,9 Спротивно на тоа, многу други адаптации предизвикани од лекови се специфични за даден лек и може да посредуваат во повеќе уникатни аспекти на дадена зависност. Ние се фокусираме овде на стимулативни и опијатни лекови за злоупотреба, кои произведуваат драматични ефекти кај животинските модели во споредба со другите лекови. Ние, исто така, истакнуваме важни области за идно истражување што дополнително ќе го зголемат нашето знаење за синдромите на зависност и ќе ги преведеме овие достигнувања во подобрени дијагностички тестови и третмани.
Транскриптивни и епигенетски механизми
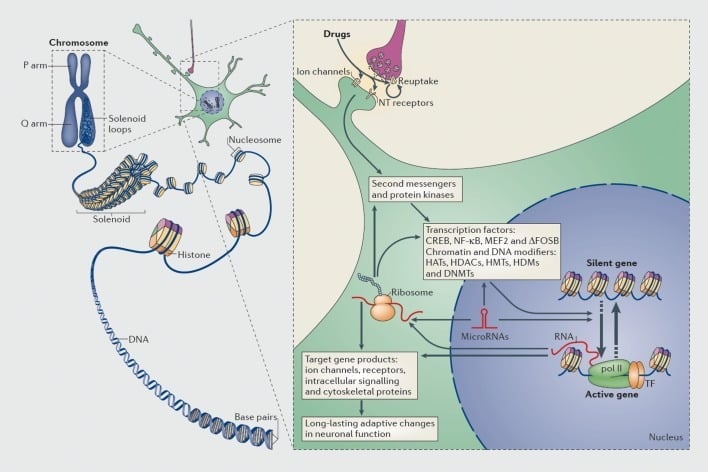
Знаењето дека зависниците можат да останат под зголемен ризик за релапс и покрај годините на апстиненција, значи дека зависноста вклучува промени предизвикани од дрога во мозокот кои можат да бидат многу стабилни. Ова доведе до тоа неколку групи да ги разгледаат промените во изразувањето на гени како важна компонента на процесот на зависност (Слика 1) Соодветно на тоа, студии за гени на кандидати или истражувања ширум геном, кои вклучуваат ДНК микроарези и неодамна РНК-сек (секвенционирање со голема моќност на изразени РНК) идентификуваше бројни гени чиј израз се менува во даден регион на мозок кај глодари и примарни модели на зависност и кај човечки зависници (на пример, refs 10-17). Примери за такви гени се дискутирани во следните делови од овој преглед.
Механизми на транскрипција и епигенетско регулирање со употреба на дрога. Во еукариотските клетки, ДНК е организирана со завиткување околу октомерите на хистонот за да се формираат нуклеозоми, кои потоа се организираат и кондензираат за да формираат хромозоми (лев дел). Само со привремено расклопување набиен хроматин, ДНК на специфичен ген може да се направи достапна за машините за транскрипција. Дрогата на злоупотреба делува преку синаптички цели, како што се механизми за поврат, јонски канали и рецептори на невротрансмитер (NT) за да ги променат меѓуклеточните сигнални каскади (десен дел). Ова доведува до активирање или инхибиција на факторите на транскрипција (TF) и на многу други нуклеарни цели, вклучително и регулаторни протеини со хроматин (прикажани со густи стрели); деталните механизми вклучени во синаптичката регулатива на хроматин-регулаторните протеини остануваат слабо разбрани. Овие процеси на крај резултираат со индукција или репресија на одредени гени, вклучително и на оние што не се кодираат РНК, како што се микроRNA; променетиот израз на некои од овие гени може пак да го регулира преносот на гени. Се предлага некои од овие промени предизвикани од лекови на ниво на хроматин се екстремно стабилни и со тоа се поткрепуваат долгорочните однесувања што ја дефинираат зависноста. CREB, цикличен протеин за врзувачки елемент кој одговара на AMP; ДНМТ, метилтрансферази на ДНК; ХАТ, хистон ацетилтрансферази; ХДАК, хистон деацетилази; ХДМ, хистон деметилази; ХМТ, метилтрансферази на хистон; MEF2, фактор за засилување специфичен за миоцитите 2; NF-kB, нуклеарен фактор-KB; пол II, РНК полимераза II. Репродуцирано од Ref 44: Robison AJ, Nestler EJ. Транскриптивни и епигенетски механизми на зависност. Нат Рев Невроски. 2011; 12: 623-637.
Исто така, многу видови на фактори на транскрипција - протеини кои се врзуваат за регулаторните региони на гените и со тоа ја зголемуваат или намалуваат транскрипцијата на тие гени - се вмешани во посредување на долгорочните ефекти на злоупотребата на лековите врз изразувањето на гени во мозокот. Истакнати примери вклучуваат CREB (врзувачки протеински елемент за одговор на cAMP), ΔFosB (фактор на транскрипција на семејството Фос), NFkB (нуклеарен фактор kB), MEF2 (фактор за подобрување на миоцитите-2), и глукокортикоидни рецептори, меѓу неколку други.5,10,18-22 Се повеќе е можно да се разберат патеките на мобилната сигнализација преку кои лековите на злоупотреба го активираат дадениот фактор на транскрипција во мозокот и каузално да ја поврзат таквата активација со целните гени на тој фактор на транскрипција и со специфичните аспекти на зависност во однесувањето (види Слика 1). Овој напредок е илустриран со разгледување на CREB и ΔFosB, кои се најдобро проучени фактори на транскрипција кај моделите на зависност.
cAMP Обврзувачки протеин на елементот за одговор
Активираат активирачки и опијатни лекови за злоупотреба CREB во неколку региони на мозокот важни за зависност, вклучително и значајно во НАЦ.23,24 CREB е познато дека се активира во други системи со cAMP, Ca2+и патеки на факторот на раст,25 и сè уште не е познато кој од овие посредува во неговото активирање во NAc со употреба на дрога. Активирањето на лекови на CREB во NAc се покажа како класичен механизам за негативни повратни информации, при што CREB служи за намалување на чувствителноста на животното на наградувачките ефекти на овие лекови (толеранција) и за посредување во негативна емоционална состојба при повлекување на лекот (зависност).18,26,27 Овие ефекти неодамна се покажаа како резултат на зголемена само-администрација на лекови и релапс, најверојатно преку процес на негативно засилување.28 Овие дејства на CREB се чини дека вклучуваат двата главни подтипови на NAc средни боцки на невроните, оние што изразуваат претежно Д1 наспроти Д2 рецептори на допамин.24 Iинтересно, голем дел од литературата покажа дека CREB, дејствувајќи во хипокампус и амигдала, е клучна молекула во меморијата во однесувањето.29-31 Оваа широка улога во зависности и меморија во однесувањето најверојатно го отсликува фактот дека невроните се преполни со конечен број молекуларни механизми со кои треба да се прилагодат на постојано менување на околината.
Целните гени за CREB кои го посредуваат овој однесен фенотип се идентификуваат преку анализи на геном широк и повеќе избрани напори.10,18,32 Еден пример е опиоиден пептид динорфин: стимулативна индукција на изразување динорфин кај невроните на NAc, со посредство преку CREB, ја зголемува активирањето на динорфин на к опиоидните рецептори на VTA допаминските неврони и со тоа се потиснува допаминергичкото пренесување на NAc и ја нарушува наградата.18 Неколку други цели на CREB се покажаа важни за синаптичката пластичност предизвикана од дрога, како што е дискутирано подолу. Додека CREB е исто така активиран во неколку други региони на мозокот со стимуланси и опијати,23,24 помалку се знае за последиците во однесувањето на овој ефект и целните гени преку кои тие се јавуваат. Исто така, помалку се знае за улогата на CREB во посредувањето во постапувањето на други лекови за злоупотреба.19
ΔFosB
Акутната изложеност на буквално злоупотреба на дрога ги предизвикува сите фактори на транскрипција на семејството Фос во НАЦ и неколку други региони на мозокот. Оваа индукција е брза, но исто така многу минлива, при што нивоата на протеини во Фос се враќаат во нормала во рок од 8 до 12 часа. Уникатно меѓу овие протеини на семејството Фос е ΔFosB, скратен производ на генот FosB, која заради својата необична стабилност, постепено се акумулира низ текот на повторната изложеност на лекови и станува доминантен протеин Фос изразен под овие услови.22,33 Покрај тоа, заради оваа стабилност, нивоата на ΔFosB опстојуваат со недели по повлекувањето на лековите. Таквата хронична индукција на ΔFosB е докажана за речиси сите злоупотреби на лекови34 и, за повеќето лекови, е селективен за невроните од типот Dl-тип NAc.34,35 Исто така беше демонстрирано кај зависници од луѓе.35 Голем дел од литературата покажа дека таквата индукција ΔFosB во Д1-типот NAc неврони ја зголемува чувствителноста на животното кон лекови, како и природните награди и промовира само-администрација на лекови, веројатно преку процес на позитивно зајакнување (видете ги упатствата 34 до 38). Интересно е што, индукцијата на дрога на ΔFosB во NAc е подраматична кај адолесцентните животни, време на поголема ранливост од зависност,39 и докажано е дека неговото индуцирање од страна на никотин посредува во подобрувањето на наградата за кокаин слично на портата на никотин.40
Што се однесува до CREB, бројни целни гени за ΔFosB се идентификуваат во NAc со употреба на ген на кандидат и пристапи за широк геном.10,32 Додека CREB предизвикува динорфин, ΔFosB го потиснува, што придонесува за ефекти на наградување на ΔFosB.38 Друга цел на ΔFosB е cFos: бидејќи ΔFosB се акумулира со повторна изложеност на лекови, го потиснува c-Fos и придонесува за молекуларниот прекинувач при што ΔFosB селективно е индуциран во хронична состојба третирана со лекови..41 Многу други цели на ΔFosB се покажаа како посредува во можноста на одредени лекови за злоупотреба да предизвикаат синаптичка пластичност во NAC и придружните промени во дендритската арборизација на NAC со средни боцки на NAC, како што ќе се дискутира подолу.
Функционалните последици од индукцијата ΔFosB во другите региони на мозокот се помалку разбрани, иако нејзината индукција во орбитофронталниот кортекс (OFC) е проучена во некои детали. Тука, ΔFosB посредува во толеранцијата што се јавува кај когнитивно-нарушувачките ефекти на кокаинот за време на хронична изложеност, а оваа адаптација е поврзана со зголемена само-администрација на кокаин.42,43
Анализата на широки геноми предложи неколку потенцијални целни гени кои ги посредуваат овие ефекти.42 И покрај уникатните временски својства του ΔFosB и сознанието дека тој е индуциран во традиционалните мемориски кола (на пример, хипокампус), сè уште немало истражување на улогата на ΔFosB во меморијата на однесувањето, интересна тема за идно истражување.
Епигенетски механизми
Во поновите години, студиите за транскрипција се наметнаа еден чекор подалеку до епигенетиката44 (Види Слика 1), што може широко да се дефинира како промена во изразот на ген што се јавува во отсуство на промена во ДНК секвенцата. Епигенетските механизми ја контролираат пакувањето на ДНК во клеточно јадро преку неговите интеракции со хистоните и многу други видови на нуклеарни протеини, кои заедно сочинуваат хроматин. Изразот на генот е контролиран од состојбата на ова пакување преку ковалентна модификација на хистоните, другите протеини и самата ДНК. Како само неколку примери, ацетилацијата на хистоните има тенденција да го промовира активирањето на генот, метилацијата на хистоните може да промовира гени активирање или репресија во зависност од остатокот на Лис што се подложува на оваа модификација, а метилацијата на ДНК е генерално поврзана со генска репресија, иако одредени варијанти форми на метилација ( на пример, 5-хидроксиметиелација) може да биде поврзана со активирање на гени.
Епигенетиката е привлечен механизам затоа што, во други системи, на пример, биологија на развој и карцином, одредени епигенетски модификации можат да бидат постојани. Од оваа причина, епигенетиката се спроведува како во моделите за учење така и во меморијата (на пр. Refs 45-48), како и во зависност;44,49 кај двата система се забележани големи промени во ацетилацијата на хистонот и метилацијата и во ДНК метилацијата. Како само еден пример, хистонот метилтрансфераза, G9a, е вмешан и во двете мемории50 и зависност.51,52 Во модели на зависност, Изразот G9a е минимизиран во НАЦ како одговор на стимулативни или опијатни лекови за злоупотреба и тсе покажа дека ги подобрува наградуваните ефекти на овие лекови.51,52 Интересно е што, потиснувањето на кокаинот на G9a е со посредство на ΔFosB. G9a ја катализира диметилацијата на Lys9 на хистонот H3 (H3K9me2), главен посредник на генската репресија. Чип-чип или ЧИП-сек (имунопреципитација на хроматин проследено, соодветно, со промотор чипови или секвенционирање со голема моќност) се користи за да се добијат мапи со широк опсег на гените во NAc кои прикажуваат изменета H3K9me2 по изложеност на опулант или опијат.32,52,53 Преклопувајќи ги овие гени списоци со списоци со геномски широк спектар на генски изразувања, и со мапи опфатени со геном на многу други форми на епигенетски модификации (на пр., Врзување ΔFosB, врзување за CREB, други модификации на хистон, итн.)32,53 треба да биде можно да се идентификуваат сè поцелосен збир на гени што се регулираат со злоупотреба на лекови и да се разберат основните епигенетски механизми кои се вклучени.
Друга форма на епигенетска регулатива вмешана во меморијата и зависноста е создавање на микроРНК. Овие мали, некодирачки РНК се врзуваат за комплементарни региони на mRNA и со тоа го потиснуваат нивниот превод или предизвикуваат нивна деградација. Бришење на Argonaut, протеин клучен за обработка на miRNAs, ги менува одговорите на однесувањето на кокаинот, со изразени ефекти забележани за D1-наспроти D2-тип на средни боцки неврони.54 Неколку специфични miRNAs, исто така, се покажаа регулирани со изложеност на лекови и, пак, влијаат на одговорите на однесувањето на лековите (на пр., Refs 55,56). Во идните студии ќе биде возбудливо да се идентификуваат целите на mRNA на овие miRNA и да се карактеризира како тие влијаат на процесот на зависност.
Синаптичка пластичност
Истите општи типови синаптички модификации кај глутаматергичните синапси, кои се вмешани во хипокампусот и амигдалата во меморијата во однесувањето (види други статии во овој број), на сличен начин се покажаа дека се појавуваат во регионите за наградување на мозокот кај моделите на зависност и се важни во медијацијата процесот на зависност.57,58 Ваквата синаптичка пластичност предизвикана од лекови е опишана во неколку региони на мозокот, сепак, ние се концентрираме овде на NAc каде повеќето истражувања се фокусираа до денес (Слика 2).
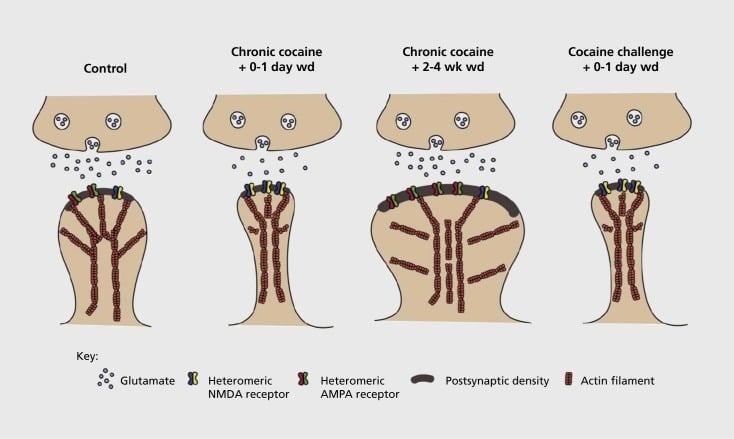
Модел на синаптичката и структурната пластичност поврзана со зависностите во јадрото на јадрото (NAc). Хроничната изложеност на кокаин резултира во временска зависна и привремена реорганизација на а-амино-3-хидрокси-5-метил-4-изоксазолепропионска киселина (АМПА) и Н-метил-Д-аспартална киселина (НМДА) глутамат на медиумите на NAc синапси на 'рбетниот неврон (МСН), како и структурни промени во главата на' рбетот на NAc MSN кои се поврзани со различни форми на синаптичка пластичност. На пример, хроничниот кокаин предизвикува површинско изразување на NMDA рецептори, тивка формација на синапс и долготрајна депресија (LTD) на почетокот на повлекувањето на времето. За време на подолготрајно повлекување (wd), овие синаптички промени се обратни со што резултатот е зголемен израз на површинските рецептори AMPA, консолидација на синапсот во 'рбетот во форма на печурки и долгорочно потенцирање (LTP). Овие ефекти брзо се враќаат повторно по изложеноста на предизвик доза кокаин што доведува до реструктуирање на 'рбетот во тенки' рбети и депресија на синаптичка јачина.
Првичните експерименти покажаа дека повторената изложеност на стимулантни лекови за злоупотреба предизвикува состојба наликувана на ДДВ (долготрајна депресија) кај глутаматергични синапси во НАЦ.59 Како и да е, неодамнешната работа покажа дека таквата пластичност е многу зависна од времето, со тоа што ДДВ се јавува рано, откако последната изложеност на кокаин се развива во повеќе на состојба на LTP (долгорочно потенцирање) по подолги временски точки на повлекување.60,61 Оваа работа, која до денес се спроведува првенствено со употреба на инспектор администриран - наспроти само-администрираните — лекови, ја дефинира потребата за посистематски истражувања кај моделите на само-администрација кои ги следат формите на синаптичка пластичност што се јавуваат кај глутаматергични синапси во NAC во текот на деталниот временски курс од стекнување на самоуправа до нејзино одржување, преку различни периоди на повлекување и истребување и како одговор на стимули за рецидив. Досегашната работа има дефинирано и некои молекуларни механизми кои придонесуваат за оваа синаптичка пластичност предизвикана од дрога, вклучително и трговија со рецептори АМПА до синапсот, можеби делумно посредуван преку CaMKII (Ca2+/ протеин киназа-зависен од калмодулин II) фосфорилација на одредени субјекти на рецептор АМПА, како и изменет израз на субјекти на рецептор АМПА (на пр. 60,62-65, Бројки 2 и 3). Улогата за CREB и ΔFosB е имплицирана во овие феномени, како и при поврзаните промени во морфологијата на глутаматергичните синапси (види подолу). На пример, GluAl е цел за CREB во NAc, каде што GluA2 и CaMKII се обете цели на ΔFosB, во овој мозочен регион .35,36,66,67 Продолжувајќи напред, ќе биде важно да ги поврзете специфичните адаптации со промените зависни од времето во синаптичката функција и карактеристиките на однесувањето на зависноста.
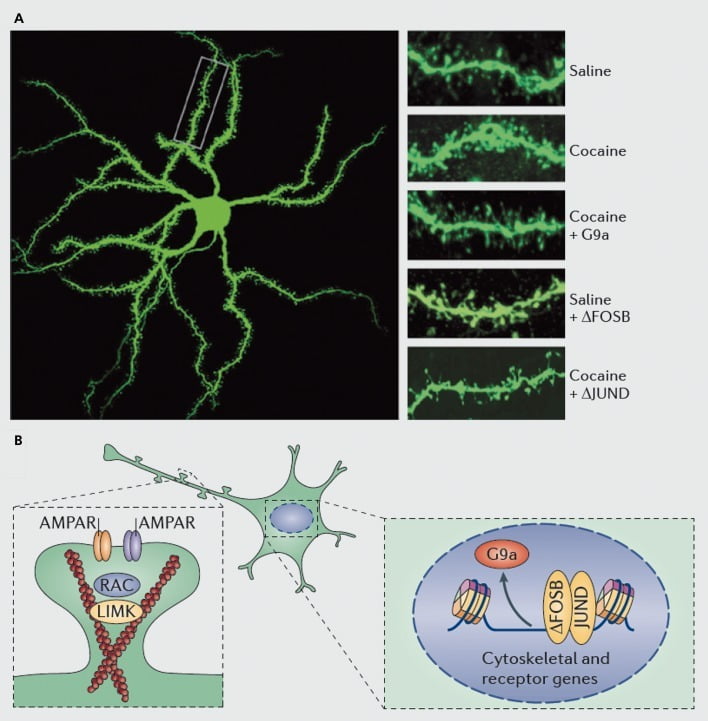
Молекуларни механизми кои лежат во основата на индукција на конд на дендритички 'рбет на нервни неврони со среден јадро (AC). А) покажува зголемување на бројот на дендритичен 'рбет, предизвикано од кокаин, што може да се блокира со вирусна прекумерна експресија на G9a или JunD (антагонист на АП1-медицирана транскрипција) или имитирана од вирусна преголема експресија на FosB. Б) Регулирањето на трговијата со рецептори АМПА (AMPAR) и цитоскелетот на актин (лево), како и регулирањето на транскрипцијата на глутаматските рецептори и активните регулаторни протеини (на пр., Како што се посредува преку ΔFosB, десно) се покажаа како важни улоги при посредување при регулирање на кокаинот за густината на Дендритичкиот 'рбет на NAc. Киназа на доменот UMK, LIM; RAC, супстрат на ботулински токсин поврзан со Рас.
Новите експериментални алатки овозможуваат за прв пат да се дефинираат со зголемена прецизност кои конкретни кола ги прикажуваат овие форми на синаптичка пластичност и какви абнормалности во однесувањето тие посредуваат. На пример, ттој и основните подрегиони на NAc покажуваат разлики во синаптичката пластичност предизвикана од дрога, како и D1 - наспроти D2-видот на средни зачинети неврони во рамките на секој подрегион.60,63,64,67 На сличен начин, оптогенетските експерименти обезбедија нов увид во придонесот на одредена форма на синаптичка пластичност (на пр., LTD) кај специфични популации на глутаматергични синапси во NAc, на пример, оние што произлегуваат од медијален PFC наспроти базолатерална амигдала наспроти вентрална поткожна програма (најголем излез на хипокампус).68-70 На крајот на краиштата, ќе биде потребно да се преклопат молекуларните адаптации предизвикани од лекови во секој од овие аферентни неврони со адаптации специфични за синапсата што се јавуваат во нивните постсинаптички дендрити за да се состави целосно разбирање за тоа како лекови за злоупотреба ги модифицираат мозочните кола за да управуваат со посебни аспекти на зависна држава. Овој потфат ќе бара поголема проценка на пластичноста предизвикана од лекови при инхибиторни синапси во истите овие мозочни региони, област на која до сега му било посветено многу малку внимание.65
Пластичност на целата клетка
Додека поголемиот дел од истражувањата кои вклучуваат неврофизиолошки промени во невроните во феномени за злоупотреба на дроги, како во феномените за учење и меморија, се фокусираа на синаптичката пластичност, има се поголеми докази за важноста на пластичноста на целиот клетки, исто така. Пластичност на целокупната клетка, исто така наречена хомеостатска пластичност,71 вклучува промени во внатрешната ексцитабилност на целата нервна клетка на начин што не е специфичен за синапс. Со оглед на тоа што одредени карактеристики на зависност од дрога вклучуваат зголемена или намалена чувствителност на лек, има смисла дека подобрената или намалената електрична ексцитабилност на одредени нервни клетки придонесува за овие прилагодувања во однесувањето.5
на Најдобар воспоставен пример за пластичност на цели клетки на дрога на злоупотреба е можноста на хронични опијати да ја зголемат вродената ексцитабилност на норадренергичните неврони на локус корелеус (ЛК)).72 Оваа зголемена ексцитабилност е посредувана преку CREB и неговото индуцирање на одредени изоформи на аденилен циклаза, што предизвикува зголемено отпуштање на LC невроните можеби преку индукција на Na + канали.72-75 Оваа хиперекцитабилност на ЛК неврони претставува класичен механизам на толеранција и зависност и вози некои од знаците и симптомите на повлекување на опијат. Интересно е тоа што, CREB посредува слична форма на пластичност во целост на клетките во NAC со средни исипливи неврони, кои исто така се покажуваат како хиперексексибилни со хронично изложување на лекови на злоупотреба преку CREB.76 На тој начин ќе биде клучно во идните истражувања да се разбере како CREB-посредувана синаптичка пластичност на глутаматергичните синапси на NAC со средни боцкави неврони65,66 сумира со CREB-посредувана интринтна хиперрезистенција на овие неврони76 за контрола на однесувањето карактеристики на зависност.
Друг пример на пластичност на цели клетки кај моделите за зависности е хиперрезибилноста на ВТА допамин невроните што се јавуваат по хронично изложување на опијатни лекови на абсусe (Слика 4).77,78 Оваа адаптација, поврзана со морфолошки промени во овие нервни клетки (видете во следниот дел), не е посредувана од CREB, туку се постигнува преку регулирање на невротрофни сигнали за каскади, како што е опишано подолу.

Работен модел на хронични адаптации предизвикани од морфиум во вентрална тегментална област (VTA) допамин неврони. Хроничниот морфин ја намалува големината на сомата на VTA допамин (ДА), но сепак ја зголемува невронската ексцитабилност, додека преносот на допамин во јадрото на амбулантите е намален. Нето ефектот на морфиум е помалку реагирачка награда, т.е. награда толеранција. Дарегулацијата на сигнализацијата IRS2-AKT во VTA ги посредува ефектите на хроничниот морфиум врз големината на сома и електричната ексцитабилност; ефектот врз ексцитабилноста е посредуван преку намалена струја на γ-аминобутирна киселина (ГАБА) А и сузбивање на изразот на К 'каналот. Дерегулацијата предизвикана од морфиум на mTORC2 активност во ВТА е клучна за овие морфино-индуцирани морфолошки и физиолошки адаптации, како и за толеранција на награда. За разлика од mT0RC2, хроничниот морфиум ја зголемува mTORCI активност, што не влијае на овие адаптации предизвикани од морфиум. BDNF, невротрофичен фактор добиен од мозок; IRS, супстанција рецептор за инсулин; mTORC, mTOR комплекс; АКТ, протеин киназа Б Репродуцирана од рефлексот 77
Морфолошка пластичност и невротрофни механизми
Зголемените докази, голем дел од студиите за хипокампални и церебрални кортикални неврони, покажаа дека промените во синаптичката пластичност се поврзани со морфолошки промени на синапсите. На пример, LTD и генерацијата на тивки синапси се поврзани со формирање на тенки или никулци дендрични боцки, додека LTP е поврзана со поголеми боцки во форма на печурки.79,80 Затоа е интересно што полето за злоупотреба на дрога е насочено кон промени предизвикани од лекови во 'рбетниот столб за повеќе од 15 години. Хронична изложеност на стимулативни лекови за злоупотреба ја зголемува дендритската густина на 'рбетот на средните боцки на невроните на NAc, промена која преовладува за невроните од типот Dl.67,81,82 Индукцијата на 'рбетите во најголем дел е поврзана со сензибилизирани реакции на однесување на овие лекови, иако некои докази се во спротивност со овој став.
Како и со студиите за синаптичка пластичност, сепак, потребна е многу поголема работа за системски дефинирање на промените во дендритичните боцки што се случуваат за време на само-администрација на лекови, повлекување и релапс. Sденес, вклучително истражувач и само-администриран лек, сугерираат многу различни промени на 'рбетот кои се случуваат на различни места за повлекување и во обвивката NAc наспроти основните подрегиони.83-86 Исто така, ќе биде важно да се дефинираат прецизни молекуларни механизми со кои кокаинот или друг стимуланс ги произведува овие специфични ефекти зависни од време и од клеточен тип. Се покажа дека ΔFosB е неопходен и доволен за индукција на незрели боцки на невроните од типот Dl, NAc.35,51,67 Ваквата регулатива се јавува во комбинација со кокаинот и ΔFosB регулирање на неколку протеини, познати за контрола на реорганизацијата на цистинскиот скелет на актин. Како само еден пример, прикажана е транскрипциска регулатива на неколку гванински нуклеотидни размени фактори и активирани протеини активирани со ГТПАС Rac1, мала GTPase, за минливо намалување на активност како одговор на секоја изложеност на кокаин, а покажани се и такви пулсирачки намалувања во активност Rac1, користејќи оптогенетска контрола на Rac1, да посредува во индукција на незрели боцки.87 Овие ефекти на Racl веројатно се случуваат преку нејзина контрола на кофилин и други регулаторни протеини на актин, за кои исто така се покажало дека посредуваат во регулирањето на кокаинот за раст на 'рбетот.87,88 Сепак, важно е да се нагласи дека ова е само една патека вклучена во регулацијата на незрели 'рбетници на кокаин, бидејќи се покажа дека и неколку други протеини играат суштинска улога, вклучително и CDK5 (киназа-зависна од циклин-5), CaMKII, NFkB , МЕФ2, КРЕБ, Г9а и ДНМТ3 (ДНК метилтрансфот ја брише 3а), за да наведеме неколку.20,21,35,51,67,89,90 Интересно е што, регулативата со кокаин на неколку од овие гени, вклучително и индукција на CDK5, CaMKII и NFkB и репресија на G9a, исто така е посредувана преку ΔFosB.20,35,51,91
Изненадувачки, опојните лекови за злоупотреба вршат спротивен ефект и ја намалуваат дендритската густина на 'рбетот на NAc средните боцки на невроните.81 Малку е познато за последиците во однесувањето на оваа адаптација и основните молекуларни механизми кои се вклучени. Овој феномен е, Како и да е, изненадувачки, со оглед на тоа што CREB и ΔFosB се предизвикани од стимуланси и опијати и и двајцата се вмешани во стимулативно посредување во индукција на NAc дендрична густина на 'рбетот. Ова го поставува прашањето како опијатите ја потиснуваат густината на рбетот на NAC и покрај нивното поттикнување на овие фактори.
Другата главна форма на морфолошка пластичност која се гледа во моделите на злоупотреба на дроги е физичкото намалување на големината на клетките сома на ВТА допамин невроните предизвикани од хронична администрација на опијат..77,92,93 Слична адаптација се јавува како одговор на канабиноидите.94 Оваа намалување на VTA допамин неврони, што се јавува со опијатна само-администрација93 и е документирано кај зависници од човечки хероин, кои биле испитани постмремот,77 се чини дека посредува во толеранцијата на награда и е поврзано со намалено ослободување на допамин во НАЦ. Значителни докази сега укажуваат на тоа дека ова намалување на големината на клетките на сомот е посредувано со сузбивање на опијат на изразот на невротрофичен фактор (BDNF) изведен од мозок во рамките на овие неврони. Ние директно го поврзавме ова повлекување предизвикано од опијат од поддршката на BDNF и намалувањето на VTA невроните, со намалената активност на низводните каскади на сигналот BDNF во ВТА допаминските неврони, конкретно намалената активност на IRS2 (супстрат за инсулин рецептор-2), AKT (серин-треонин) киназа), и TORC2 (цел на рапамицин-2, кој е нечувствителен на рапамицин).77,93 Ние, исто така, ја поврзавме оваа дерегулација на сигнализацијата на BDNF директно со зголемената ексцитабилност што морфиумот предизвикува кај овие неврони, како што е забележано порано.77,78 Навистина, намалената големина на клетките на сома и зголемената ексцитабилност се цврсто споени, бидејќи индукцијата на едниот води кон другиот и обратно. Оваа контрола врз ексцитабилност на клетките вклучува потиснување на К+ канали и на ГАБАA струја кај овие неврони.
Оваа улога за BDNF во контролата на реакциите на морфиум на ниво на ВТА е во спротивност со многу различното учество во дејствата на кокаинот и другите стимуланси. Стимуланси предизвикуваат сигнализација на BDNF кон NAC, ефект како резултат на зголемена локална синтеза на BDNF, како и зголемено ослободување од неколку аферентни региони.95 Покрај тоа, зголемената сигнализација на BDNF кај NAc, но не и во VTA, се покажа дека ги промовира ефектите во однесувањето на овие лекови, вклучително и нивната само-администрација.95,96 Спротивното регулирање на сигнализацијата на BDNF во патеката VTA-NAc од опијати наспроти стимуланси ја покренува можноста ваквите разлики да посредуваат во спротивното регулирање на лековите со NAc дендритичните 'рбети, можност што сега се испитува.
Идните насоки
Горенаведениот наратив го потенцира огромниот напредок што е направен во разбирањето на молекуларните и клеточните адаптации што се случуваат во регионите на наградување на мозокот како одговор на повторената изложеност на дрога на злоупотреба и во врска индивидуалните адаптации на одредени карактеристики на однесувањето на синдромите на зависност кај животинските модели . И покрај овие достигнувања, остануваат големи прашања. Повеќето од нашите постојни знаења се фокусираат на VTA и NAc, со многу помалку достапни информации за другите клучни региони на лимбниот мозок, кои се исто така клучни за зависноста од дрога. Покрај тоа, сите експериментални демонстрации на каузалната улога на молекуларно-клеточна адаптација во однесување поврзано со дрога, манипулираа со индивидуални адаптации едно по едно. Да се манипулира со бројни адаптации во исто време е јасно многу потешко, но исто така е суштинско, бидејќи знаеме дека лековите создаваат голем број на различни типови на промени дури и во рамките на индивидуалните неврони, што веројатно сумира на комплицирани начини за да влијае на однесувањето. Ваквиот пристап кон биологијата на системите ќе биде клучен за крајно пукање на биолошките основи на зависност. Конечно, напорите да се разберат молекуларно-клеточните механизми на сеќавања поврзани со зависност се наоѓаат во моментот кога сите други напори за разбирање на биолошката основа на меморија во однесувањето сега се борат: нашата способност да ги поврземе биолошките феномени со сложената меморија во однесувањето останува исклучително тешка. Надминувањето на оваа поделеност претставува можеби најголемиот предизвик во невронауките.
Признанија
Оваа работа беше поддржана од грантови од Националниот институт за злоупотреба на дрога.
Избрани кратенки и акроними
- Нац
- јадрото accumbens
- CREB
- врзувачки протеин елемент за реакција на cAMP
- ΔFosB
- фактор на транскрипција на семејството Фос
- VTA
- вентрална тегенментална област
- AMPA
- а-амино-3-хидрокси-5-метил-4-изоксазозолпропионска киселина
- ООД
- долгорочна депресија
- LTP
- долгорочно протетирање
- BDNF
- мозочен невротрофичен фактор
- НКкБ
- нуклеарен фактор kB
Користена литература