PRIPOMBE: Ena od redkih študij, ki zajema, kako abstinenca vpliva na ravni dopaminskih receptorjev pri primatih.
- D2 receptorji se dokaj hitro vrnejo nazaj - manj kot mesec dni
- D1 receptorji so na mesec previsoki, vendar se vračajo v 90 dneh.
- Visoki ali nizki D1 receptorji so lahko ključni za akutno odtegnitev in apetit
Thomas JR Beveridge1, Hilary R Smith1, Michael A Nader1 in Linda J Porrino1
1Oddelek za fiziologijo in farmakologijo, Center za nevrobiološka raziskovanja zlorabe drog, Medicinska fakulteta Univerze Wake Forest, Winston-Salem, NC, ZDA
Korespondenca: dr. LJ Porrino, Oddelek za fiziologijo in farmakologijo, Center za nevrobiološko preiskavo zlorabe drog, Medicinska fakulteta Univerze Wake Forest, Medical Center Boulevard, Winston-Salem, NC 27157-1083, ZDA. Tel: + 1 336 716 8575; Faks: + 1 336 716 8501; E-naslov: [e-pošta zaščitena]
Prejeto 29. aprila 2008; Revidirano 25. julija 2008; Sprejeto 30. julija 2008; Objavljeno na spletu 3. septembra 2008.
Minimalizem
Čeprav je disregulacija v sistemu dopamina (DA) značilna značilnost kronične izpostavljenosti kokainu, vprašanje o tem, ali te spremembe ostajajo v abstinenci, ostaja v veliki meri neodgovorjeno. Nečloveški primati predstavljajo idealen model za ocenjevanje učinkov abstinence na sistem DA po kronični izpostavljenosti kokainu. V tej študiji so moške rezusne opice samostojno dajale kokain (0.3 mg/kg na injekcijo, ojačevalniki 30 na sejo) pod fiksnim intervalom 3-min surnik za dneve 100, ki mu sledi abstinenca za 30 ali 90 dni. To trajanje samoinjiciranja kokaina je bilo prej dokazano, da zmanjša gostoto receptorjev, podobnih DA D2, in poveča ravni D1-podobnih receptorjev in DA transporterjev (DAT).. Odziv nadzornih opic je potekal s predstavitvijo hrane po enakem protokolu in istih abstinenčnih obdobjih. [3H]SCH 23390 se veže na Receptorji DA D1 po 30 dneh abstinence so bili znatno višji v vseh delih striatuma v primerjavi z kontrolnimi živalmi, [3H]vezava racloprida na receptorje DA D2 ni bila različna med skupinami. [3H]WIN 35 428 vezava na DAT je bila prav tako bistveno višja v skoraj vseh delih hrbtnega in ventralnega striatuma po 30 dneh abstinence. Po 90 dneh abstinence pa se ravni DA D1 receptorjev in DAT niso razlikovale od kontrolnih vrednosti. Čeprav ti rezultati kažejo na morebitno obnovo ločenih elementov sistema DA, poudarjajo tudi dinamično naravo teh sestavin v začetnih fazah abstinence pri kronični samokontroli kokaina.
ključne besede:
kokain, dopamin, avtoradiografija, abstinenca, striatum
UVOD
Uporaba kroničnega kokaina med odvisniki od ljudi je povezana z nevroadaptacijami v sistemu dopamina (DA) (Malison sod, 1998; Volkow sod, 1993, 1997). Ti vključujejo povečanje gostote DA transporterjev (DAT) in zmanjšanje koncentracij receptorjev, podobnih DA D2 (malo sod, 1999; Mash sod, 2002; Volkow sod, 1993). Poleg tega so opazili tudi spremembe v sproščanju DA. Na primer, raziskovalci, ki uporabljajo študije s pozitronsko emisijsko tomografijo (PET) [11C]Racloprid in metilfenidat sta pokazala zmanjšanje sproščanja DA v striatumu kroničnih uporabnikov kokaina (Volkow sod, 1997; Wong sod, 2006). Eden od problemov je, da je pogosto težko izključiti vpliv drugih dejavnikov, kot so uporaba drugih nezakonitih in zakonitih drog, razlike v predhodnih vzorcih uživanja in uporabe drog ter razlike v življenjskem slogu. Te razlike, pa tudi obstoj pogojev, ki lahko povzročijo uporabo drog, lahko omejijo razlago študij pri ljudeh.
Modeli nečloveških primatov, pri katerih je mogoče sistematično manipulirati s spremenljivkami, predstavljajo alternativni pristop k preučevanju posledic kronične samokontrole kokaina in kasnejše abstinence. Prejšnje študije so pokazale, da kronično izpostavljenost kokainu spremljajo pomembna zmanjšanja koncentracij receptorjev DA D2, kot tudi zvišanje ravni receptorjev D1 in gostota DAT (Letchworth sod, 2001; Moore sod, 1998a, 1998b; Nader sod, 2002, 2006). Ti učinki odražajo tiste, ki so jih opazili pri ljudeh, kar potrjuje koristnost teh modelov izpostavljenosti drogam.
Čeprav obstaja veliko dokazov za moteno regulacijo sistemov DA, se je izkazalo, da je težje oceniti, ali obstajajo dokazi za oživitev po prenehanju uporabe drog (Malison sod, 1998; Jacobsen sod, 2000; Volkow sod, 1993) ali te spremembe trajajo dlje od časovnega okvira nadaljnje izpostavljenosti kokainu. Tudi modeli nečloveških primatov lahko zagotovijo vpogled v to fazo odvisnosti. Farfel sod (1992) poročali o znižanju koncentracije DAT in D1 podobnih receptorjev v striatumu opic po abstinenci zaradi kronične nekontrolirane izpostavljenosti kokainu. Posebno vlogo abstinence je bilo težko določiti zaradi pomanjkanja meritev v skupini brez abstinenčnega obdobja. Podobno, \ t Melega sod (2008) poročali so o bistveno nižjih ravneh DAT v striatumu opic vervetov po 3 tednih abstinence zaradi naraščajočega režima metamfetamina. Vendar pa je bilo dajanje stimulansov v obeh študijah nezadostno. Pot uporabe (kontingent vs dokazano, da vpliva na možgane različno glede na obe sproščanji DA (Hemby sod, 1997) in presnovo glukoze (Graham in Porrino, 1995; Porrino sod, 2002). Zato uporaba samoupravljanja v tej študiji zaobide to vprašanje. Poleg tega so bili učinki dolgotrajnega samo-dajanja kokaina na možganske sisteme DA obsežno preučevani z uporabo tega modela samouporabe v opicah rezusov, s čimer so zagotovili izhodišče za ocenjevanje nevroadaptacij, ki se pojavijo med abstinenco.
Namen teh študij je bil torej ugotoviti, ali so bile spremembe koncentracij DAT in DA D1 in D2 receptorjev, ki so bile prej dokazane pri živalih, izpostavljenih kokainskemu samoupravljanju (Letchworth sod, 2001; Moore sod, 1998a, 1998b; Nader sod, 2002) bi se obrnil po daljših obdobjih abstinence. Na podlagi študij o ljudeh, ki uživajo droge (prim Volkow sod, 1993), smo domnevali, da se bodo te spremembe v sistemu DA nadaljevale tudi po 3 mesecih abstinence. V ta namen so opice samostojno dajale kokain za seje 100, s popolnim vnosom 900-a mg/sledi bodisi 30 ali 90 dni abstinence od zdravila. Receptorji DA D1 in D2 ter DAT so bili izmerjeni s kvantitativnim in vitro receptorska autoradiografija.
METODE
Predmeti
Skupaj 17 eksperimentalno naivne odrasle moške rezusne opice (Macaca mulatta), ki tehta med 7.7 in 13 kg (povprečje ± SD, 10.2 ± 1.32) na začetku študije je služil kot predmet. Vsi postopki so bili izvedeni v skladu z uveljavljeno prakso, kot je opisano v Nacionalni inštituti za zdravje Vodnik za oskrbo in uporabo laboratorijskih živali. Poleg tega so vse postopke pregledali in odobrili odbor za nego živali in uporabo Univerze Wake Forest. Opice so bile posamično nameščene v kletkah iz nerjavnega jekla z vodo ad libitum; živali so imele fizični in vizualni stik. Njihova telesna teža se je ohranila na približno 90 – 95% uteži proste hranjenja s peletami z okusom banan, pridobljenimi med poskusnimi urami, in z dodatnim hranjenjem Lab Diet Monkey Chow, pod pogojem, da ne prej kot 30 min po seji. Poleg tega so jim vsaj trikrat na teden dali sveže sadje ali arašide. Vsaka opica je bila tehtana enkrat na teden, in če je bilo potrebno, so bile njihove prehrane prilagojene za vzdrževanje stabilnih uteži.
Vedenjski aparat
Poskusne seje so bile izvedene v prezračevanih in zvočno oslabljenih operantnih komorah (1.5 × 0.74 × 0.76) m; Med Associates Inc., East Fairfield, VT) je zasnovan tako, da sprejme primate stol (model R001; izdelki iz primatov, Redwood City, CA). Komora je vsebovala inteligentno ploščo (48 × 69 cm), ki je sestavljen iz dveh zložljivih vzvodov (5 cm) in tri lučke za stimulacijo. Vzvodi so bili nameščeni na dosegu roke opice, ki je sedela na stolu primata. Živilski peleti z aromo banane (1. \ T g; Bio-Serv, Frenchtown, NJ) so bili dostavljeni iz napajalnika na vrhu komore. Peristaltično infuzijsko črpalko (7531-10; Cole-Parmer Co., Chicago, IL) smo uporabili za dovajanje injekcij zdravila s hitrostjo približno 1 ml na 10 s tistimi živalmi, ki samo dajo kokain. Delovanje komor in pridobivanje podatkov je bilo izvedeno z računalniškim sistemom Power Macintosh z vmesnikom (Med Associates Inc.).
Kirurški postopki
Vse opice, vključno s kontrolami, smo kirurško pripravili pod sterilnimi pogoji z notranjimi intravenoznimi katetri in žilnimi dostopnimi vrati (Model GPV; Access Technologies, Skokie, IL). Opice so bile anestezirane s kombinacijo ketamina (15 mg/kg, im) in butorfanol (0.03 mg/kg, im) in naredimo rez v bližini femoralne vene. Po topi disekciji in izolaciji vene smo proksimalni konec katetra vstavili v veno za razdaljo, izračunano za zaključek v spodnji veni cavi. Daljni konec katetra smo navrtali subkutano na rez, ki je bil nekoliko oddaljen od vzdolžne osi hrbta. Žično dostopno odprtino je bilo nameščeno v žepu, ki ga je tvorila topa disekcija v bližini tega reza. Opice so dobile 24 – 48 h čas obnovitve pred vrnitvijo v odziv na živila. Približno 5 dni pred terminalnim postopkom je vsaka opica implantirana s kroničnim ohranjenim katetrom v sosednjo femoralno arterijo za zbiranje vzorcev časovne arterijske krvi. Kirurški postopki so bili identični tistim, ki so opisani za venske katetre. Na dan zadnje seje je bila izvedena študija končne cerebralne presnove glukoze, v kateri so opice injicirali z 2-[14C]deoksiglukoza (2-DG) približno 2 min po koncu seje in krvni vzorci so bili pridobljeni preko arterijskega katetra preko 45 min (glej Beveridge sod, 2006 za podrobnosti). Podatki o presnovi iz teh študij tukaj niso predstavljeni.
Postopki samoupravljanja
Opice so bile sprva usposobljene, da se odzovejo na eno od dveh vzvodov s krepitvijo vsakega odziva na pravilni vzvod s peletami za hrano. V približno 3-tedenskem obdobju se je interval med razpoložljivostjo živilskih peletov postopoma povečeval, dokler ni bil dosežen interval 3-min (tj. Urnik ojačitve s fiksnim intervalom 3-min; FI 3-min). V pogojih končnega urnika je prvi odziv na vzvodu po 3 min je povzročilo dostavo peletov za hrano; seje so se končale po predstavitvah hrane 30. Ob koncu vsakega zasedanja so bili vzvodi odziva umaknjeni, svetilke za hišo in dražljajske luči so ugasnile, živali pa so ostale v zatemnjeni komori za približno 30. min pred vrnitvijo v kletke. Vsi opici so se odzvali pod razporedom predstavitve hrane za FI 3-min za najmanj 20 sej in dokler niso dosegli stabilne lastnosti (± 20)% povprečja za tri zaporedne seje, brez trenda odzivnosti). Ko je bil odziv, ki ga vzdržuje hrana, stabilen, je bil napajalnik odklopljen in učinki izumrtja na odziv so bili pregledani pet zaporednih sej, po katerih je bil odziv ponovno vzpostavljen in vzdrževan s predstavitvijo hrane.
Po ugotovitvi izhodiščne zmogljivosti so vse opice kirurško pripravili z venskimi katetri, kot je opisano zgoraj, in naključno razporedili v eno od treh skupin. Ena skupina opic je služila kot kontrolna skupina in se je še naprej odzivala pod razporedom predstavitve živil FI 3-min za skupno sejo 100 (N=6). Preostale opice 11 so bile dodeljene skupinam za samo-dajanje kokaina (0.3 mg/kg na injekcijo). Ker 0.3 mg/kg kokaina na injekcijo je veljalo za velik odmerek za opice, ki so bile prej kokainsko naiven, pri večini živali pa je bil ta odmerek dosežen v dveh seansah, tako da je opica najprej dovolila samoupravljanju 0.1. mg/kg kokaina. Po operaciji (približno 4 – 6 dni) je bilo pred začetkom kokainske samouprave dovoljeno stabilizirati delovanje hrane. Pred vsako poskusno sejo so hrbet živali očistili z 95% čiščenje etanola in betadina ter merilnik 22 Huber Point Needle (model PG20-125) je bil vstavljen v odprtino, ki je vodila do venskega katetra, s povezavo infuzijske črpalke z raztopino kokaina na kateter. Pred začetkom seje je črpalka delovala približno 3 s polnjenjem pristanišča z odmerkom kokaina, ki je bil na voljo med poskusno sejo. Seje so se končale po injekcijah 30; pod nadzorovanimi pogoji so opice ostale v temnejši komori približno 30 min. Na koncu vsake seje je bilo pristanišče napolnjeno s heparinizirano slanico (100 U/ml), da preprečite strjevanje.
Eksperimentalne seje so potekale približno ob istem času vsak dan in se je nadaljevalo za skupno sejo 100. Po zaključku sej 100 smo uvedli abstinenčno obdobje 30 ali 90 dni, medtem ko so kateterji vsakodnevno splaknili s heparinizirano fiziološko raztopino, vendar kokainov ali samooskrbe s hrano niso izvajali. Za kontrolno skupino so bila abstinenčna obdobja 30 dni določena v štirih živalih in 90 dni v drugih dveh. Za kokainsko skupino so bila abstinenčna obdobja 30 dni osem živali in 90 dni na treh živalih. Ob koncu obdobja abstinence je bila izvedena ena zadnja seja samouprave (nadzor živil ali kokain) in takoj po zasedanju je bila sprožena procedura 2-DG. Pri dveh kontrolnih živalih in štirih živalskih kokainih v skupini, ki je prejemala 30 dnevno, na zadnji seji kokaina ni bilo. Živali so humano usmrtili s prevelikim odmerkom pentobarbitala (100 mg/kg, iv) na koncu 45 obdobje prevzema sledilca.
Obdelava tkiv
Po usmrtitvi so bili možgani takoj odstranjeni, blokirani in zamrznjeni v izopentanu pri -35 do -55 ° C in nato shranjeni pri -80 ° C. Tkane bloke, ki vsebujejo striatum, so nato razrezani v kriostatu pri -20 ° C v koronalni ravnini v 20 μm sekcij, zberemo na elektrostatično nabita stekelca, osušimo pod vakuumom preko noči pri 4 ° C, nato shranimo pri -80 ° C do obdelave za avtoradiografijo. Odseki možganov so bili zbrani iz delov caudatnega jedra, putamena in nucleus accumbens, ki ležijo rostralno do sprednje komisure. Ta regija se imenuje precommissural striatum. Nadaljnje, rostralne in kaudalne ravni precommissural striatum so bile določene glede na nucleus accumbens. Roštralni prekomisuralni striatum je območje, kjer se nucleus accumbens ne razlikuje v ločene lupine in jedrne pododdelke. Kaudalni prekomisuralni striatum je območje, ki je skladno z videzom lupine in jedra nucleus accumbens, ki je posteriorna od pojava vohalne tuberkule. Za vsako študijo vezave sta bila na vsakem od petih nivojev (dva rostralna in tri kaudalna) odvzeta dva sosednja odseka skozi precommissural striatum za celotno sekcijo 10 na žival.
Vezava receptorjev D1
Določili smo gostoto vezavnega mesta receptorja DA D1 [3H]SCH 23390 (specifična dejavnost - 85 Ci/mmol; PerkinElmer, Boston, MA) in vitro receptorsko avtoradiografijo v skladu s postopki, prilagojenimi od Lidow sod (1991) in Nader sod (2002). Razdelki so bili predinkubirani za 20 min v pufru (50 mM Tris, 120 mM NaCl, 5 mM KCl, 2 mM CaCl2, 1 mM MgCl2, pH 7.4, 25 ° C) za odstranitev endogenega DA, kokaina in. \ t [14C] iz postopka 2-DG. Sekcije so bile nato inkubirane za 30 min v istem pufru, pH 7.4, 25 ° C, ki vsebuje 1 mM askorbinska kislina, 40 nM ketanserin in 1 nM [3H]SCH 23390. Po inkubaciji se sekcije dvakrat sperejo za 20 s v pufru, ki vsebuje 1 mM askorbinske kisline pri pH 7.4, 4 ° C, nato potopimo v destilirano vodo pri 4 ° C in posušimo v toku hladnega zraka. Nespecifična vezava je bila določena z inkubacijo sosednjih odsekov v inkubacijski raztopini v prisotnosti 5. μM (+) -butaclamol. Odseki, skupaj z umerjenimi [3H] avtoradiografski standardi (Amersham, Piscataway, NJ) so bili dodani Kodak Biomax MR filmu (Fisher Scientific, Pittsburgh, PA) za 6 tedne.
Vezava receptorjev D2
Določili smo gostoto in porazdelitev vezavnih mest DA D2 receptorjev [3H]racloprid (specifična aktivnost, 87 Ci/mmol; PerkinElmer) v skladu s postopki, prilagojenimi od Lidow sod (1991) in Nader sod (2002). Razdelki so bili predinkubirani za 20 min v pufru (50 mM Tris, 120 mM NaCl, 5 mM KCl, pH 7.4, 25 ° C) za odstranitev endogenega DA, kokaina in [14C] iz postopka 2-DG. Prosojnice smo nato inkubirali za 30 min v istem pufru, ki vsebuje 5 mM askorbinska kislina in 2 nM [3H]racloprid. Sekcije so bile sprane 3 × 2 min v pufru pri pH 7.4, 4 ° C, nato potopimo v destilirano vodo pri 4 ° C in posušimo v toku hladnega zraka. Nespecifična vezava je bila določena z inkubacijo sosednjih odsekov v inkubacijski raztopini v prisotnosti 1. μM (+) - butaclamol. Odseki, skupaj z umerjenimi [3H] Avtoradiografski standardi so bili priloženi Kodak Biomax MR filmu za 8 tedne.
Vezava transporterja dopamina
Gostoto DAT vezavnih mest smo določili z uporabo [3H]WIN 35,428 (posebna dejavnost, 87 Ci/mmol; PerkinElmer) avtoradiografijo v skladu s postopki, prilagojenimi iz Canfield sod (1990) in Letchworth sod (2001). Tkivne dele smo predhodno inkubirali v pufru (50 mM Tris, 100 mM NaCl, pH 7.4, 4 ° C) za 20 min za odstranitev kakršnega koli ostanka DA, kokaina in [14C] iz postopka 2-DG. Sekcije so bile nato inkubirane za 2 h pri 4 ° C v istem pufru, ki vsebuje 5 nM [3H]WIN 35 428. Sekcije so bile sprane skupaj za 2 min v pufru pri 4 ° C, nato potopimo v destilirano vodo pri 4 ° C in posušimo v toku hladnega zraka. Nespecifična vezava je bila določena z inkubacijo sosednjih odsekov v inkubacijski raztopini v prisotnosti 30. μM kokain. Odseki, skupaj z umerjenimi [3H] Avtoradiografski standardi so bili priloženi Kodak Biomax MR filmu za 6 tedne.
Denzitometrija in analiza podatkov
Filmi so bili razviti z razvijalcem Kodak GBX, stopbath in Rapid Fixer (VWR, West Chester, PA) in nato sprani. Analiza avtoradiogramov je bila izvedena s kvantitativno denzitometrijo z računalniškim sistemom za obdelavo slik (MCID, Imaging Research; InterFocus Imaging Ltd, Cambridge, UK). Vrednosti optične gostote so bile pretvorjene v fmol/mg (tkiva v mokrem maso) glede na umerjeno [3H] standardov. Specifična vezava je bila določena z digitalno odštevanjem slik nespecifične vezave iz superponiranih sosednjih slik popolne vezave. Strukture so bile identificirane z Nissl-obarvanjem odsekov, ki so sosednji tistim, ki so bili analizirani za vezavo na receptor. Podatki iz vsakega testa so bili analizirani neodvisno s pomočjo enosmerne analize variance, ki ji sledijo najmanjše kvadratne razlike naknadnega testov za večkratne primerjave. Vsaka regija je vsebovala ločeno analizo. Ker se podatki o vezavi, pridobljeni iz kontrolnih živali abstinentnih za 30 in 90 dni, med seboj niso bistveno razlikovali, podobno kot v prejšnjih študijah (Nader sod, 2002), podatki iz kontrolnih skupin so bili kombinirani. Poleg tega ni bilo bistvenih razlik med podatki o tistih živalih, ki so prejele kokain, in tistimi, ki niso bile na zadnji seji, zato so bili tudi podatki iz teh skupin kombinirani.
REZULTATI
Učinki odsotnosti iz kroničnega kokainskega samoupravljanja za dneve 30
Koncentracije [3H]SCH 23390, ki se veže na receptorje DA D1 v precommissural striatum, so prikazani v Tabela 1. Posebna vezava. \ T [3H]SCH 23390 je obračunal več kot 90% popolne vezave. V skladu s prejšnjimi poročili (Moore sod, 1998a; Nader sod, 2002), vezavo [3H]SCH 23390 na D1 receptorje pri kontrolnih živalih, ki niso bile izpostavljene zdravilu, je bilo heterogeno z znatnimi razlikami v stopnji vezave med podregijami striatuma. Označevanje je bilo gostejše v bolj rostralnih in medialnih delih v striatumu.
Po 30 dneh abstinence zaradi izpostavljenosti kokainu je bila za vezavo na receptorje D1 značilna razširjena povišanja po celotnem rostralno-kaudalnem obsegu precommissural striatuma, v primerjavi z gostoto vezave v kontrolnih živalih, ki niso izpostavljene zdravilu (Tabela 1; Slika 1). V bolj rostralnem striatumu so bile koncentracije bistveno višje v kavdatnem jedru, vključno z dorzolateralno (+27%), centralno (+27%), dorsomedial (+27%) in ventromedial (+23%), kot tudi v hrbtni (+17%), centralno (+22%) in ventralno (+23%) dele putamena v primerjavi z gostoto živali, ki niso izpostavljene zdravilu. Pomembna povišanja so bila vidna tudi pri nucleus accumbens (+23%) na tej ravni. Na ravni striatuma, kjer so jedro in lupina jedra nucleus accumbens najbolj diferencirani, so bile tudi gostote D1-podobnih receptorjev bistveno višje v celotnem dorzolateralu (+31%), centralno (+29%), dorsomedial (+30%) in ventromedial (+18%) caudate jedro in hrbtno (+23%), centralno (+29%) in ventralno (+28%) putamena v primerjavi z gostoto kontrol, ki niso izpostavljene zdravilu. Znotraj ventralnega striatuma na tej ravni je koncentracija D1 vezavno mesto receptorjev je bilo večje v jedru nucleus accumbens (+45%) in lupine (+20%), kot tudi v vohalni tuberkulozi (+26%), v primerjavi z gostoto kontrol.
Slika 1.
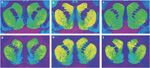 Reprezentativni avtoradiogrami [3H] SCH 23390, ki se veže na D1 receptorje (zgornja plošča) in [3H]WIN 35428 se veže na dopaminske transporterje (spodnji del) v koronalnih odsekih striatuma rezus opice. (a, d) kontrolna žival, ki se odziva za okrepitev hrane. (b, e) žival kokainske samouprave z abstinenco 30 dni. (c, f) žival z lastno uporabo kokaina z abstinenco 90 dni.
Reprezentativni avtoradiogrami [3H] SCH 23390, ki se veže na D1 receptorje (zgornja plošča) in [3H]WIN 35428 se veže na dopaminske transporterje (spodnji del) v koronalnih odsekih striatuma rezus opice. (a, d) kontrolna žival, ki se odziva za okrepitev hrane. (b, e) žival kokainske samouprave z abstinenco 30 dni. (c, f) žival z lastno uporabo kokaina z abstinenco 90 dni.
Koncentracije [3H]Racloprid, ki se veže na receptorje DA D2 v precommissural striatumu, so prikazani v Tabela 2. Posebna vezava z [3H]racloprid je bil večji od 90% popolne vezave. Porazdelitev. \ T [3H]vezava na receptorje D2 je bila tudi heterogena po subregijah hrbtnega in ventralnega striatuma kot v prejšnjih poročilih (Moore sod, 1998b; Nader sod, 2002). V kontrolnih skupinah, ki niso bile izpostavljene zdravilu, so bile v hrbtu prisotne višje koncentracije vezavnih mest D2 v primerjavi z ventralnim striatumom. Poleg tega so obstajali dokazi o medialnem do lateralnem gradientu z višjimi koncentracijami vezavnih mest, ki so prisotni v bolj lateralnih delih striatuma.
Po 30 dneh abstinence se ravni vezave na D2 receptorje pri živalih, izpostavljenih kokainu, in živalih, ojačanih s hrano, v večini regij striatuma niso bistveno razlikovale. V ventralnem putamenu so opazili višje koncentracije veznih mest (+10%) in anterior nucleus accumbens (+12%) v tkivu opic, izpostavljenih kokainu, v primerjavi s kontrolami. Druge pomembne razlike niso bile opažene.
Koncentracije [3H]WIN 35428 se veže na DAT v precommissural striatum Tabela 3. V skladu s prejšnjimi poročili (Letchworth sod, 2001), je bila vezava na mesta DAT pri živalih, ki niso bile izpostavljene zdravilu, višja v hrbtu v primerjavi z ventralnim striatumom. V jedru so opazili večje gostote v jedru v primerjavi z lupino. Nazadnje, nespecifična vezava je predstavljala manj kot 10% skupnega zneska.
Po 30 dneh abstinence pred izpostavljenostjo kokainu je bila vezava na DAT v večini regij striatum rostral do anteriorne komisarke bistveno višja v primerjavi z vezavo pri kontrolnih živalih, ki niso izpostavljene zdravilu (Slika 1). Konkretno, koncentracije mest vezave DAT na rostralnih nivojih so bile znatno višje v osrednji (+22%), dorsomedial (+25%) in ventromedial (+28%) caudate jedro in v hrbtni (+16%) in centralno (+23%) putamen v primerjavi s kontrolami, okrepljenimi s hrano. Poleg tega je bilo v anteriorni jedru accumbens tudi znatno višja vezava na DAT (+37%) pri kokainu v primerjavi z opicami, ojačanimi s hrano. V večjih repnih delih precommissuralnega striatuma so bile gostote vezavnih mest DAT v osrednjem jedru kaudatov bistveno višje (+21%), in putamen, central (+20%) in ventralno (+19%; Slika 1). Znotraj ventralnega striatuma na tej ravni je bila vezava na DAT bistveno višja v jedru nucleus accumbens (+20%) in vohalne tuberkule (+24%) v tkivih iz kokaina vs opice, ojačane s hrano.
Učinki odsotnosti iz kroničnega kokainskega samoupravljanja za dneve 90
V nasprotju s široko razširjenimi razlikami v gostoti vezavnih mest D1 receptorjev, opaženih pri živalih, izpostavljenih kokainu po 30 dneh abstinence, po 90 dneh abstinence, ni bilo pomembnih razlik v primerjavi s kontrolami, okrepljenimi s hrano, v katerem koli delu precommisuralne kontrole. striatumTabela 1; Slika 1). Podobno koncentracije [3H]vezave na receptorje DA D2 v precommissural striatumu po 90 dneh abstinence, prav tako niso bistveno drugačne od tistih pri živalih, ki niso izpostavljene zdravilu (Tabela 2).
Koncentracije. \ T [3H]WIN 35428, ki se veže na DAT, je pokazal podoben vzorec kot tisti, ki so ga opazili pri receptorjih D1 in D2. Ni bilo bistvenih razlik v gostoti DAT med opicami, izpostavljenimi kokainu, po 90 dneh abstinence v primerjavi z ravnmi pri kontrolah, ki niso izpostavljeni zdravilu (Tabela 3; Slika 1), čeprav je treba opozoriti, da je prišlo do trenda višjih ravni vezave v anteriorni nucleus accumbens.
DISKUSIJA
Prejšnje študije iz naše skupine so pokazale, da kronično izpostavljenost kokainu samoupravljanju spremlja pomembna disregulacija sistema DA za nečloveške primate (Letchworth sod, 2001; Moore sod, 1998a, 1998b; Nader sod, 2002, 2006). Rezultati te študije kažejo, da je ta disregulacija očitna po prenehanju izpostavljenosti kokainu. Po 30 dnevih abstinence so bile koncentracije receptorjev DA D1 in DAT znatno povečane v striatumu opic s preteklimi obdobji kroničnega samo-dajanja kokaina v primerjavi s kontrolami, ojačanimi s hrano. Vendar pa ta študija zagotavlja tudi jasne dokaze za okrevanje v sistemu DA po daljših obdobjih abstinence (dnevi 90), kar dokazuje pomanjkanje pomembnih razlik med kokainom in kontrolnimi živalmi v tem trenutku. Ti podatki kažejo, da izpostavljenost kokainu morda ne bo povzročila trajnih sprememb v sistemu DA, vendar se lahko okrevanje pojavi z daljšo abstinenco zaradi uporabe drog.
Disregulacija koncentracij DAT, prikazana tukaj po abstinenci, je skladna s prejšnjimi poročili o primatih, ki niso človeški (Letchworth sod, 2001), ki je pokazala znatno povečanje gostote vezavnih mest DAT v ventralnem in hrbtnem striatumu. Čeprav niso izrecno testirani, se zdi, da so po prenehanju izpostavljenosti drog višje gostote vezavnega mesta DAT vsaj tako velike in bolj razširjene po regijah striatuma kot tiste, ki so bile prijavljene brez kakršne koli karence (Letchworth sod, 2001). Podobno so tudi povišane koncentracije D1 receptorskih vezavnih mest, ki so bile opažene tukaj po 30 dnevih abstinence, skladne s prejšnjimi študijami, ki so pokazale povečano gostoto D1 receptorskih vezav v striatumu nečloveških primatov, izpostavljenih enakemu režimu kokainske samouprave (Nader sod, 2002). V nasprotju pa niso opazili pomembnih razlik med stopnjama vezave receptorjev D2, ki so podobne gostoti receptorja v striatumu pri živalih, izpostavljenih kokainu, in kontrolnih živalih. To pomanjkanje disregulacije je bilo prisotno kljub velikemu zmanjšanju koncentracij receptorjev D2, o katerih so poročali pri obeh ljudeh (Volkow sod, 1993) in živalskih modelov kokainske samouprave (\ tMoore sod, 1998a, 1998b; Nader sod, 2002, 2006). Sedanji podatki torej kažejo na hitrejšo normalizacijo za nadzorne ravni v tem sistemu v primerjavi z D1-podobnimi receptorji in DAT. Skupaj spremembe v DA receptorjih in DAT jasno kažejo, da je obdobje takoj po prenehanju samoupravljanja kokaina zelo labilno, pri čemer pride do znatnih sprememb v regulaciji sistema DA, vendar sledi ponovna ureditev Sistem se približuje bolj normalni porazdelitvi DA receptorjev in DAT po daljši abstinenci.
Spremembe D1 receptorjev
Razširjena zvišana gostota receptorjev D1, ki so jih opazili po prenehanju uporabe kokaina, je skladna s poročili, ki kažejo povečano občutljivost receptorjev D1 med umikom. Merjenje občutljivosti D1 je bilo opravljeno v študiji Henry in White (1991)v katerih je bilo ugotovljeno, da so posnetki posameznih nevronov v jedru nucleus accumbens bolj občutljivi na agonist D1 receptorjev SKF 38393 po kroničnih dnevnih injekcijah kokaina v primerjavi s kontrolami, ki so jih zdravili s slanico. Ta učinek je bil trajen, saj je povečana občutljivost ostala očitna do enega meseca po prenehanju zdravljenja. Avtorji so postavili hipotezo, da je senzibilizacija D1 receptorjev posledica avtoreceptorja D2 v podrocju somatodendriticnega A10a, s cimer se zmanjša zaviralni impulzni tok skozi sistem mesoaccumbens DA (Henry in White, 1991). Podatki iz te študije kažejo na povečano vezavno mesto D1 receptorjev v abstinenci, kar lahko pojasni to povečano občutljivost dopaminergičnih nevronov na neposredno delujoči agonist D1 receptorjev. Poleg tega okrepljeni učinek SKF 38393 na nevrone nucleus accumbens ni bil viden dva meseca po umiku, kar kaže, da je prišlo do okrevanja občutljivosti receptorjev D1 (Henry in White, 1991); rezultat, ki je skladen z okrevanjem gostote receptorjev D1, ki so bile zabeležene v tej študiji po 90 dneh abstinence. Druga poročila prav tako podpirajo pomembno vlogo receptorjev D1 pri ponovitvi bolezni. Neposredna stimulacija D1 receptorjev v lupini nucleus accumbens lahko ponovno vzpostavi kokain pri iskanju glodalcev z abstinenco (Schmidt sod, 2006). Vendar pa je literatura nekoliko nedosledna, ker lahko tako agonisti kot antagonisti D1 ublažijo iskanje drog, ki jih sprožijo kokainski primesi ali dražljaji, povezani s kokainom (Alleweireldt sod, 2002; De Vries sod, 1999; Khroyan sod, 2000; Self sod, 1996; Bela sod, 2001). Nedavno, Khroyan sod (2003) so poročali, da agonisti in antagonisti D1-a zmanjšujejo recidiv pri modelu kokaina, ki ni v človeškem primatu. Ti avtorji so predlagali, da lahko obstaja kritično območje aktivnosti D1 receptorjev, ki je potrebno za iskanje kokaina, in da lahko antagonisti in agonisti premaknejo aktivnost iz tega okna. Povečane koncentracije receptorjev D1, ki spremljajo abstinenco, lahko spremenijo to območje, kar povzroči spremembo občutljivosti tega sistema. Druga ugotovitev je, da lahko aktivnost D1 modulira aktivnost na receptorjih D2 (Nolan sod, 2007; Ruskin sod, 1999; Walters sod, 1987). Predstavljeni podatki kažejo, da se razmerje med D1 in D2 receptorji premika med abstinenco in lahko s tem spremeni učinkovitost te modulacije.
Čeprav so v nasprotju s sedanjimi podatki poročali o zmanjšanju ravni receptorjev D1 po kroničnem kokainskem samoupravljanju (Moore sod, 1998a) med temi študijami obstajajo precejšnje razlike, kot so odmerek in dolžina izpostavljenosti kokainu, skupnemu vnosu in primerjalnim kontrolnim skupinam. Skupaj zato konvergenčni dokazi močno kažejo, da je sistem D1 po prenehanju uporabe kronične uporabe kokaina v precejšnjem pretoku.
Spremembe dopaminskega transporterja
Ugotovitve zvišanih koncentracij DAT v striatumu pri živalih, izpostavljenih kokainu, po prenehanju uporabe drog razširjajo tiste iz naših prejšnjih študij, ki kažejo povečane ravni mest vezave DAT, ki spremljajo samouporabo kokaina pri nečloveških primatih. Sedanji podatki kažejo, da ta neurejenost traja v začetnih fazah abstinence. Poleg tega kažejo, da izterjava na kontrolne ravni sledi razmeroma dolgemu poteku (do 90 dni v tej študiji). V naših prejšnjih študijah smo pokazali, da se je sprememba gostote vezavnih mest DAT, čeprav je bila sprva omejena na večinoma ventralne striatne regije, razširila, da bi zajela več hrbtnih in rostralnih delov striatuma z daljšimi obdobji izpostavljenosti kokainu (Letchworth sod, 2001; Porrino sod, 2004). V tej študiji se je pokazalo, da je vrnitev na kontrolne ravni koncentracij DAT med abstinenco večja in hitrejša v dorzalnem striatumu kot v ventralnem striatumu, in tako se zdi, da sledi obratni anatomski poti do vzorca učinkov, ki jih povzroča kronična izpostavljenost kokainu .
Sedanji podatki so tudi skladni s poročili o uporabnikih kokaina pri ljudeh (malo sod, 1999; Malison sod, 1998; Mash sod, 2002; Staley sod, 1994), ki so pokazale povišane vrednosti vezave na mesta DAT v striatumu v primerjavi s kontrolami, pri čemer so najbolj izrazita povečanja v ventralnem striatumu. V zadnjem času se je pokazalo, da ta zvišanja spremljajo pomembna zmanjšanja vezave vezikularnega monoaminskega transporterja 2 (VMAT2) (malo sod, 2003), ki nakazujejo dejansko izgubo DA nevronov. Avtorji so sklenili, da je povišana vrednost DAT verjetno neposredno posledica kompenzacijskega odgovora na farmakološko blokado, ki jo povzroča kokain, medtem ko je zmanjšanje VMAT2 verjetno odražalo splošne spremembe v presnovi DA, kar je imelo za posledico hipodopaminergično funkcijo.
Poročali so, da imajo človeški odvisniki od kokaina zmanjšane koncentracije DA v ventralnem striatumu, kot so izmerili s PET, kot odziv na izziv metilfenidata v primerjavi z zdravimi kontrolami (Volkow sod, 1997). Nedavno, Martinez sod (2007) Poročali so, da so imeli uporabniki kokaina zatopljen odziv na izziv amfetamina v ventralnem striatumu in putamenu. Poleg tega je bilo to zmanjšanje sproščanja amfetamina, povzročenega z DA, povezano z izbiro kokaina na ločenih sejah samouprave, tako da so tisti uporabniki z najnižjo stopnjo sproščanja DA kot odgovor na amfetamine najverjetneje izbrali kokain nad alternativnim ojačevanjem (Martinez sod, 2007). Nedavne študije o uporabi kokaina pri glodalcih podpirajo tudi to zamisel. Mateo sod (2005)na primer poročali, da je izpostavljenost kroničnemu kokainskemu samoupravljanju povezana s spremembami v funkciji DAT. Ti raziskovalci so pokazali, da je bil osnovni sprejem DA povečan, kar je povzročilo hitrejši očistek sinaptičnega DA, zato so se znižale bazalne ravni zunajceličnega DA ali hipodopaminergičnega stanja. Zato je verjetno, da so povečane koncentracije DAT po umiku iz kronične samo-dajanja kokaina, opažene v tej študiji, kompenzacijski odziv, kar ima za posledico nižje izhodiščne ravni zunajceličnega DA.
Spremembe D2 receptorjev
Eden od rezultatov te študije je bil, da so se koncentracije receptorjev D2 vrnile na kontrolne vrednosti po 30 dneh abstinence, v primerjavi s pomembnimi zmanjšanji, ugotovljenimi pri živalih brez karenčne dobe (Nader sod, 2002). V nasprotju s sedanjo raziskavo so študije slikanja pri ljudeh na splošno ugotovile, da so ravni D2 receptorjev nižje od tistih pri kontrolah po daljši abstinenci zaradi kronične izpostavljenosti kokainu (Martinez sod, 2004; Volkow sod, 1993). Potencialne razlage razlik med temi študijami na ljudeh in trenutno nečloveško preiskavo primatov vključujejo razlike v vzorcu in trajanju vnosa kokaina, kot tudi možnost obstoja nižjih ravni D2 receptorjev pri človeških odvisnikih.
V skladu s slednjo idejo obstajajo dokazi, ki kažejo, da nižje bazalne ravni receptorjev D2 pri zdravih ljudeh napovedujejo povečanje učinkovitosti stimulansov, kot so metilfenidatinVolkow sod, 1999), in podobno pri opicah so izhodiščne ravni receptorjev D2 napovedale nagnjenost k samokontroli kokaina (Morgan sod, 2002; Nader sod, 2006). V skladu z vzporedno naravo teh ugotovitev med vrstami, tako človeškimi (Volkow sod, 1993) in nečloveški primati (Nader sod, 2006) Slikovne študije so pokazale nižjo raven razpoložljivosti D2 receptorjev po abstinenci zaradi izpostavljenosti kokainu. Predvsem časovni načrt samoupravljanja kokaina v slednjem poskusu (Nader sod, 2006) je bil podoben načrtu ojačitve, uporabljenem v tej študiji. Zato ni verjetno, da bi bili različni izidi teh dveh študij posledica metodoloških razlik, kot je časovni razpored okrepitve ali kumulativnega vnosa med samouporabo kokaina.
Bolj verjetna razlaga vključuje funkcionalno dinamiko sistema DA. Ukrepi razpoložljivosti D2 receptorjev s PET so bili opisani kot "funkcionalni", ker je signal povezan s količino beljakovin (v tem primeru gostote receptorjev D2) in ravni cirkulirajočega nevrotransmiterja. (Glej Laruelle, 2000; Nader in Czoty, 2008 za nadaljnjo razpravo). jazNasprotno, receptorska avtoradiografija ni kontaminirana s krožečimi ravnmi DA. Tako ta študija, skupaj z našimi prejšnjimi deli, nakazuje, da se gostota D2 receptorjev zmanjša zaradi samo-dajanja kokaina, vendar pa se zdi, da se ravni receptorjev okrevajo med abstinenco. V podobni raziskavi PET (\ tNader sod, 2006), okrevanje je bilo opaženo pri treh od petih opic. Sedanje ugotovitve kažejo, da se te opice verjetno niso razlikovale pri gostoti D2 receptorjev, ampak morda odzivnost sistema DA (tj. Stopnje kroženja DA med abstinenco) razlikujejo med "izterjanimi" in "neobratenimi" subjekti.
Omejitve
Ena od pomembnih omejitev trenutnih študij je, da naše študije ne morejo obravnavati funkcionalnosti receptorjev D1 in D2 ali DAT. Namesto tega smo pregledali samo spremembe v gostoti receptorskih proteinov. Čeprav rezultati vplivajo na potencialne vloge teh sistemov, bodo potrebne nadaljnje študije, da se osvetlijo vedenjske posledice tukaj prikazanih sprememb. Druga omejitev te študije je, da avtoradiografski ligandi pogosto ne ločijo med znotrajceličnimi in citoplazmatskimi lokacijami svojih tarč, ker so radioaktivno označeni antagonisti pogosto prepustni za membrano. malo sod (2002) so pokazali, da kronična izpostavljenost kokainu vodi do pomembnega povišanja DAT na površini membrane, hkrati z zmanjšanjem znotrajcelične koncentracije DAT v transficiranih celicah. Nedavno, Samuvel sod (2008) podobne ugotovitve pri sinaptosomskih pripravkih pri striatnih podganah. Ti rezultati kažejo, da spremembe v distribuciji DAT, opažene v tej študiji, lahko predstavljajo spremembe na površini membrane, ne pa v znotrajceličnih mestih.
Nazadnje je potrebna previdnost pri razlagi študij o podaljšani abstinenci (90 dni), saj so te ugotovitve temeljile na relativno majhni skupini živali (N=3). Kljub majhnemu številu preiskovancev so bili podatki, pridobljeni iz te skupine, precej dosledni, kar je razvidno iz razpredelnice, prikazane na sliki Slika 2. Koncentracija vezavnih mest D1 receptorjev v striatumu je pokazala majhno variabilnost znotraj skupin, kar kaže na zanesljivost teh ugotovitev. Podobna konsistenca je bila očitna tudi v podatkih iz testov D2 receptorja in DAT vezave. Čeprav je potrebna previdnost, ti podatki močno kažejo, da se lahko ob dolgotrajni abstinenci ponovno vzpostavi koncentracija DAT in DA receptorjev znotraj striatuma.
Slika 2.
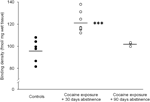 Vezavne gostote receptorjev D1 za posamezne živali so bile povprečene za celotno striatum po okrepitvi hrane (kontrole) ali 30 ali 90 dni vzdržljivosti kroničnega kokainskega samoinjiciranja. Sredstva za skupine so prikazana s črnimi črtami, ***p<0.001 v primerjavi s hrano okrepljeno kontrolo.
Vezavne gostote receptorjev D1 za posamezne živali so bile povprečene za celotno striatum po okrepitvi hrane (kontrole) ali 30 ali 90 dni vzdržljivosti kroničnega kokainskega samoinjiciranja. Sredstva za skupine so prikazana s črnimi črtami, ***p<0.001 v primerjavi s hrano okrepljeno kontrolo.
SKLEPI
Skratka, izpostavljenost kokainski samoupravi je povzročila pomembne spremembe v regulaciji sistemov DA, ki so obstajale v zgodnjih fazah (prvih 30 dni) abstinence. To je bilo najbolj očitno pri regulaciji koncentracije D1 receptorjev in DAT, tako glede njihove velikosti sprememb kot topografskega obsega. Nasprotno pa so obstajali dokazi za normalizacijo z daljšim trajanjem abstinence pred izpostavljenostjo kokainu, saj se koncentracije receptorjev DAT, D1 in D2 po 90 dneh abstinence niso razlikovale od tistih pri kontrolah, ki niso izpostavljene zdravilu. Tvendar pa ni nujno, da sledijo istemu časovnemu poteku okrevanja, kar nakazuje, da obstaja verjetnost, da bo določena stopnja DA še posebej nestabilna, zlasti v zgodnji abstinenci.. Ta dopaminergična disregulacija lahko vpliva na učinkovitost morebitne farmakoterapije, ki se daje apstinentnim odvisnikom od kokaina, zlasti če se zdravilo zanaša na sistem DA za njegov mehanizem delovanja.
Reference
- Alleweireldt AT, Weber SM, Kirschner KF, Bullock BL, Neisewander JL (2002). Blokada ali stimulacija receptorjev D1 dopamina zmanjša ponovno vzpostavitev ponavljajočega se vedenja pri iskanju kokaina pri podganah. Psihofarmakologija (Berl) 159: 284–293. | Člen | PubMed | ChemPort |
- Beveridge TJ, Smith HR, Daunais JB, Nader MA, Porrino LJ (2006). Samo-dajanje kroničnega kokaina je povezano s spremenjeno funkcionalno aktivnostjo v temporalnih režah nečloveških primatov. Eur J Neurosci 23: 3109–3118. | Člen | PubMed |
- Canfield DR, Spealman RD, Kaufman MJ, Madras BK (1990). Avtoradiografska lokalizacija lokacij za vezavo kokaina s pomočjo [3H] CFT ([3H] WIN 35428) v opičjih možganih. Synapse 6: 189–195. | Člen | PubMed | ChemPort |
- De Vries TJ, Schoffelmeer AN, Binnekade R, Vanderschuren LJ (1999). Dopaminergični mehanizmi, ki posredujejo spodbudo za iskanje kokaina in heroina po dolgotrajnem prenehanju samoinjiciranja IV zdravila. Psihofarmakologija (Berl) 143: 254–260. | Člen | PubMed | ChemPort |
- Farfel GM, Kleven MS, Woolverton WL, Seiden LS, Perry BD (1992). Učinki ponavljajočih se injekcij kokaina na vezavna mesta kateholaminskih receptorjev, mesta vezave dopaminskega transporterja in obnašanje pri rezus opici. Brain Res 578: 235–243. | Člen | PubMed | ChemPort |
- Graham J, Porrino LJ (1995). Nevroanatomski substrati samoupravljanja kokaina. CRC: Boca Raton, FL.
- Hemby SE, Co C, Koves TR, Smith JE, Dworkin SI (1997). Razlike v koncentracijah zunajceličnega dopamina v nucleus accumbens med odzivno odvisno kokainsko aplikacijo in na odziv neodvisno od podgan. Psihofarmakologija (Berl) 133: 7–16. | Člen | PubMed | ChemPort |
- Henry DJ, bel FJ (1991). Ponavljajoča uporaba kokaina povzroča trajno povečanje občutljivosti dopaminskih receptorjev D1 v podganah. J Pharmacol Exp Ther 258: 882–890. | PubMed | ChemPort |
- Jacobsen LK, Staley JK, Malison RT, Zoghbi SS, Seibyl JP, Kosten TR sod (2000). Povišana centralna vezava serotoninskih transporterjev je na voljo pri akutno abstinentnih bolnikih, odvisnih od kokaina. Am J Psychiatry 157: 1134–1140. | Člen | PubMed | ISI | ChemPort |
- TV Khroyan, Barrett-Larimore RL, Rowlett JK, Spealman RD (2000). Mehanizmi receptorjev, podobni dopamin D1 in D2, pri ponovitvi obnašanja, ki išče kokain: učinki selektivnih antagonistov in agonistov. J Pharmacol Exp Ther 294: 680–687. | PubMed | ISI | ChemPort |
- Khroyan TV, Platt DM, Rowlett JK, Spealman RD (2003). Pomanjkanje relapsa kokaina, ki ga iščejo agonisti in antagonisti receptorjev za dopamin D1 pri primatih, razen človeka. Psihofarmakologija (Berl) 168: 124–131. | Člen | PubMed | ChemPort |
- Laruelle M (2000). Oblikovanje sinaptične nevrotransmisije z vivo zavezujoče tehnike konkurence: kritični pregled. J Cereb krvnega tlaka Metab 20: 423–451. | Člen | PubMed | ISI | ChemPort |
- Letchworth SR, Nader MA, Smith HR, Friedman DP, Porrino LJ (2001). Napredovanje sprememb gostote vezavnega mesta na transporter dopamina, ki je posledica samo-dajanja kokaina v opicah rezusov. J Neurosci 21: 2799–2807. | PubMed | ISI | ChemPort |
- Lidow MS, Goldman-Rakic PS, Gallager DW, Rakic P (1991). Porazdelitev dopaminergičnih receptorjev v možganski skorji primata: kvantitativna avtoradiografska analiza z uporabo [3H] racloprida, [3H] spiperona in [3H] SCH 23390. Nevroznanost 40: 657–671. | Člen | PubMed | ChemPort |
- Little KY, Elmer LW, Zhong H, Scheys JO, Zhang L (2002). Kokainska indukcija prenosa dopaminskega transporterja na plazemsko membrano. Mol Pharmacol 61: 436–445. | Člen | PubMed | ISI | ChemPort |
- Little KY, Krolewski DM, Zhang L, Cassin BJ (2003). Izguba striatnega vezikularnega monoaminskega transporterja (VMAT2) pri uporabnikih kokaina pri ljudeh Am J Psychiatry 160: 47–55. | Člen | PubMed |
- Little KY, Zhang L, Desmond T, Frey KA, Dalack GW, Cassin BJ (1999). Strimatalne dopaminergične nepravilnosti pri uporabnikih kokaina pri ljudeh. Am J Psychiatry 156: 238–245. | PubMed | ChemPort |
- Malison RT, Best SE, van Dyck CH, McCance EF, Wallace EA, Laruelle M sod (1998). Zvišani striatni dopaminski transporterji med akutno kokainsko abstinenco, merjeno z [123I] beta-CIT SPECT. Am J Psychiatry 155: 832–834. | PubMed | ChemPort |
- Martinez D, Broft A, Foltin RW, Slifstein M, Hwang DR, Huang Y sod (2004). Odvisnost od kokaina in razpoložljivost receptorjev d2 v funkcionalnih delih striatuma: odnos do vedenja, ki išče kokain. Neuropsychopharmacology 29: 1190–1202. | Člen | PubMed | ISI | ChemPort |
- Martinez D, Narendran R, Foltin RW, Slifstein M, Hwang DR, Broft A sod (2007). Sproščanje dopamina, povzročeno z amfetaminom: izrazito zavito v odvisnosti od kokaina in napovedovanje izbire za samo-dajanje kokaina. Am J Psychiatry 164: 622–629. | Člen | PubMed | ISI |
- Mash DC, Pablo J, Ouyang Q, Hearn WL, Izenwasser S (2002). Prenosna funkcija dopamina pri uporabnikih kokaina je povišana. J Neurochem 81: 292–300. | Člen | PubMed | ChemPort |
- Mateo Y, Lack CM, Morgan D, Roberts DC, Jones SR (2005). Zmanjšana funkcija dopaminskega terminala in neobčutljivost na kokain po samoupravljanju in pomanjkanju kokaina. Neuropsychopharmacology 30: 1455–1463. | Člen | PubMed | ISI | ChemPort |
- Melega WP, Jorgensen MJ, Lacan G, Way BM, Pham J, Morton G sod (2008). Dolgoročna uporaba metamfetamina v modelih vervetnih opic je izpostavljena človeku: možganska nevrotoksičnost in vedenjski profili. Neuropsychopharmacology 33: 1441–1452. | Člen | PubMed | ChemPort |
- Moore RJ, Vinsant SL, Nader MA, Porrino LJ, Friedman DP (1998a). Vpliv samo-dajanja kokaina na receptorje dopamina D1 v striatah pri rezusnih opicah. Synapse 28: 1–9. | Člen | PubMed | ChemPort |
- Moore RJ, Vinsant SL, Nader MA, Porrino LJ, Friedman DP (1998b). Vpliv samo-dajanja kokaina na receptorje dopamin D2 v rezusnih opicah. Synapse 30: 88–96. | Člen | PubMed | ChemPort |
- Morgan D, Grant KA, Gage HD, Mach RH, Kaplan JR, Prioleau O sod (2002). Družbena prevlada pri opicah: receptorji za dopamin D2 in samouporaba kokaina. Nat Neurosci 5: 169–174. | Člen | PubMed | ISI | ChemPort |
- Nader MA, Czoty PW (2008). Slikanje možganov pri nečloveških primatih: vpogled v odvisnost od drog. ILAR J 49: 89–102. | PubMed | ChemPort |
- Nader MA, Daunais JB, Moore T, Nader SH, Moore RJ, Smith HR sod (2002). Učinki samo-dajanja kokaina na striminske dopaminske sisteme pri opicah rezus: začetna in kronična izpostavljenost. Neuropsychopharmacology 27: 35–46. | Člen | PubMed | ISI | ChemPort |
- Nader MA, Morgan D, Gage HD, Nader SH, Calhoun TL, Buchheimer N sod (2006). PET slikanje receptorjev dopamin D2 med kronično samo-dajo kokaina pri opicah. Nat Neurosci 9: 1050–1056. | Člen | PubMed | ChemPort |
- Nolan EB, Harrison LM, Lahoste GJ, Ruskin DN (2007). Vedenjski sinergizem med D (1) in D (2) dopaminskimi receptorji pri miših ni odvisen od vrzeli. Synapse 61: 279–287. | Člen | PubMed | ChemPort |
- Porrino LJ, Lyons D, Miller MD, Smith HR, Friedman DP, Daunais JB sod (2002). Metabolično preslikavanje učinkov kokaina v začetnih fazah samoupravljanja v primatih, ki niso človeški. J Neurosci 22: 7687–7694. | PubMed | ChemPort |
- Porrino LJ, Lyons D, Smith HR, Daunais JB, Nader MA (2004). Samouprava kokaina povzroči progresivno vpletanje limbične, asociacijske in senzorimotorne striatne domene. J Neurosci 24: 3554–3562. | Člen | PubMed | ISI | ChemPort |
- Ruskin DN, Bergstrom DA, Walters JR (1999). Večsekundna nihanja v stopnji žganja v globusnem pallidusu: sinergistična modulacija z dopaminskimi receptorji D1 in D2. J Pharmacol Exp Ther 290: 1493–1501. | PubMed | ISI | ChemPort |
- Samuvel DJ, Jayanthi LD, Manohar S, Kaliyaperumal K, Glej RE, Ramamoorthy S (2008). Disregulacija trgovine s prevoznimi sredstvi za dopamin in delovanje po abstinenci zaradi samo-dajanja kokaina pri podganah: dokazi za diferencialno regulacijo pri caudate putamenu in nucleus accumbens. J Pharmacol Exp Ther 325: 293–301. | Člen | PubMed | ChemPort |
- Schmidt HD, Anderson SM, Pierce RC (2006). Stimulacija D1-podobnih ali D2 receptorjev dopamina v lupini, ne pa tudi jedra, nucleus accumbens ponovno vzpostavlja obnašanje pri iskanju kokaina pri podganah. Eur J Neurosci 23: 219–228. | Člen | PubMed |
- Self DW, Barnhart WJ, Lehman DA, Nestler EJ (1996). Nasprotno modulacijo obnašanja, ki išče kokain, povzročajo agonisti D1- in D2-podobnih dopaminskih receptorjev. Znanost 271: 1586–1589. | Člen | PubMed | ISI | ChemPort |
- Staley JK, Hearn WL, Ruttenber AJ, Wetli CV, Mash DC (1994). Visoko afinitetna mesta prepoznavanja kokaina na dopaminskem transporterju so povišana pri žrtvah prevelikega odmerka s kokainom. J Pharmacol Exp Ther 271: 1678–1685. | PubMed | ChemPort |
- Volkow ND, Fowler JS, Wang GJ, Hitzemann R, Logan J, Schlyer DJ sod (1993). Zmanjšana razpoložljivost receptorjev za dopamin D2 je povezana z zmanjšano frontalno presnovo pri uživalcih kokaina. Synapse 14: 169–177. | Člen | PubMed | ISI | ChemPort |
- Volkow ND, Wang GJ, Fowler JS, Logan J, Gatley SJ, Gifford A sod (1999). Napovedovanje krepitve odzivov na psihostimulante pri ljudeh z možganskimi dopaminskimi receptorji D2. Am J Psychiatry 156: 1440–1443. | PubMed | ISI | ChemPort |
- Volkow ND, Wang GJ, Fowler JS, Logan J, Gatley SJ, Hitzemann R sod (1997). Zmanjšan dopaminergični odziv pri striatah pri detoksificiranih osebah, odvisnih od kokaina. Narava 386: 830–833. | Člen | PubMed | ISI | ChemPort |
- Walters JR, Bergstrom DA, Carlson JH, Chase TN, Braun AR (1987). Aktivacija dopaminskega receptorja D1, potrebna za postsinaptično izražanje D2 agonističnih učinkov. Znanost 236: 719–722. | Člen | PubMed | ChemPort |
- Weiss F, Martin-Fardon R, Ciccocioppo R, KerrTM, Smith DL, Ben-Shahar O (2001). Odpornost proti izumrtju obnašanja, ki išče kokain, ki ga povzročajo droge. Neuropsychopharmacology 25: 361–372. | Člen | PubMed | ISI | ChemPort |
- Wong DF, Kuwabara H, Schretlen DJ, Bonson KR, Zhou Y, Nandi A sod (2006). Povečana zasedenost dopaminskih receptorjev v človeškem striatumu med kokainsko željo. Neuropsychopharmacology 31: 2716–2727. | Člen | PubMed | ChemPort |
![Tabela 1 - Vpliv dni apstinence 30 ali 90 po kronični samokontroli kokaina na gostoto [lsqb] 3H [rsqb] SCH 23390 Vezava na receptorje D1 v predsodnem Striatumu rezusnih opic - Žal ne moremo zagotoviti dostopnega nadomestnega besedila za to. Če potrebujete pomoč za dostop do te slike, se obrnite na help@nature.com ali avtorja](https://yourbrainonporn.com/wp-content/uploads/2020/01/table_thumb.gif)
