MEGJEGYZÉSEK: Amint a későbbi vizsgálatok feltárják, a DeltaFosB a molekuláris kapcsoló mind a kábítószer, mind a viselkedési függőségekben. Ez egy transzkripciós faktor, ami azt jelenti, hogy befolyásolja a be- vagy kikapcsolandó gének működését. Amint azt máshol elmondták, az addiktív szerek csak a normális mechanizmusokat térítik el. Ezért butaság azt sugallni, hogy viselkedési függőségek nem létezhetnek.
Proc Natl Acad Sci US A. 2001 szeptember 25; 98 (20): 11042 – 11046.
doi: 10.1073 / pnas.191352698.
Eric J. Nestler *, Michel Barrot és David W. Self
Pszichiátriai Tanszék és Alapvető Idegtudományi Központ, University of Texas Southwestern Medical Center, 5323 Harry Hines Boulevard, Dallas, TX 75390-9070
Absztrakt
A kábítószer-függőséget jellemző néhány viselkedési rendellenesség hosszú élettartama azt sugallta, hogy a neurális génexpresszió szabályozása részt vehet abban a folyamatban, amelyben a visszaélés gyógyszerei függőségi állapotot okoznak. énA növekvő bizonyítékok arra utalnak, hogy az ΔFosB transzkripciós faktor egy olyan mechanizmust képvisel, amellyel a visszaélés gyógyszerei viszonylag stabil változásokat hoznak létre az agyban, amelyek hozzájárulnak a függőség fenotípusához. ΔfosBa transzkripciós faktorok Fos családjának tagja, a nukleáris accumbens és a dorsalis striatum (a függőség szempontjából fontos agyi régiók) idegsejtjeinek egy részhalmaza alatt halmozódik fel, sokféle visszaélésszerű gyógyszer beadása után. A ΔFosB hasonló felhalmozódása a kompulzív futás után következik be, ami arra utal, hogy az ΔFosB felhalmozódhat a kényszeres viselkedések sok típusára adott válaszként.. Fontos, hogy az AFosB a neuronokban rendkívül hosszú ideig fennmarad rendkívüli stabilitása miatt. Ezért az ΔFosB olyan molekuláris mechanizmust jelent, amely megindíthatja, majd fenntarthatja a génexpresszió változásait, amelyek hosszú ideig fennmaradnak a gyógyszer expozíciót követően. Indukálható transzgenikus egereken végzett vizsgálatok, amelyek túlzottan expresszálják a ΔFosB-t vagy a fehérje domináns negatív inhibitorát, közvetlen bizonyítékot szolgáltatnak arra, hogy az ΔFosB fokozott érzékenységet okoz a kábítószerek viselkedési hatásainak, és esetleg a megnövekedett kábítószer-kereső viselkedésnek. Ez a munka alátámasztja azt a nézetet, hogy az ΔFosB olyan „tartós„ molekuláris kapcsolóként ”funkcionál, amely fokozatosan átalakítja az akut hatóanyag-válaszokat viszonylag stabil adaptációkká, amelyek hozzájárulnak a függőség alapját képező hosszú távú neurális és viselkedési plaszticitáshoz.
A függőség kutatása arra összpontosít, hogy megértsék a bántalmazás összetett módjait, amelyek megváltoztatják az agyat a függőséget jellemző viselkedési rendellenességek okozására. Az egyik kritikus kihívás a területen az agy viszonylag stabil gyógyszerindukált változásainak azonosítása, amelyek figyelembe veszik azokat a viselkedési rendellenességeket, amelyek különösen hosszú életűek. Például egy humán rabja fokozott kockázattal járhat a visszaesés után még évekig tartó absztinencia után is.
Ezeknek a viselkedési rendellenességeknek a stabilitása azt sugallta, hogy legalább részben gén-expresszió (1 – 3) változásai közvetíthetik őket. Ebből a nézetből következik, hogy a visszaélés ismételt expozíciója többször zavarja az átvitelt, különösen az agy szinapszisait, amelyek érzékenyek a gyógyszerre. Az ilyen perturbációk végül intracelluláris hírvivő kaszkádokon keresztül jelennek meg a magra, ahol először kezdeményeznek, majd fenntartanak változásokat a specifikus gének expressziójában. Az elsődleges mechanizmus, amelyen keresztül a jelátviteli útvonalak befolyásolják a génexpressziót, a transzkripciós faktorok szabályozása, a gének szabályozó régióira kötődő fehérjék, és ezek transzkripciójának módosítása.
A függőségkutatás egyik célja tehát azon transzkripciós faktorok azonosítása volt, amelyek a függőséggel összefüggő agyi régiókban megváltozottak a kábítószerrel való visszaélés utáni gyógyszerek krónikus beadása után. Az elmúlt évtizedben számos ilyen transzkripciós tényezőt azonosítottak (1 – 6). A felülvizsgálat középpontjában az egyik ΔFosB nevű transzkripciós faktor áll.
ΔFosB indukálása a visszaélés kábítószerekkel
A foszB gén által kódolt AFosB a transzkripciós faktorok Fos családjának tagja, amely magában foglalja a c-Fos, a FosB, a Fra1 és a Fra2 (7). Ezek a Fos családfehérjék júniusi családfehérjékkel (c-Jun, JunB vagy JunD) heterodimerizálnak, hogy aktív AP-1 (aktivátor protein-1) transzkripciós faktorokat hozzanak létre, amelyek az AP-1 helyekhez kötődnek (konszenzus szekvencia: TGAC / GTCA). bizonyos gének promotereit, hogy szabályozzák transzkripciójukat.
Ezek a Fos családfehérjék gyorsan és átmeneti jelleggel indukálódnak az egyes agyi régiókban, miután sok kábítószer-fogyasztás akut beadása következett be (1. Ábra) (8 – 11). A kiemelkedő régiók az accumbens és a dorsalis striatum, amelyek fontos szerepet játszanak a gyógyszerekre adott viselkedési válaszok, különösen azok előnyös és mozgásszervező hatásai (12, 13). Ezek a fehérjék a gyógyszer beadásától számított órán belül visszatérnek a bazális szintre.
ábra 1
Az AFosB fokozatos felhalmozódását mutatja az egyéb Fos családfehérjék gyors és átmeneti indukciójával, amely a visszaélés gyógyszereire reagál. (A) Az autoradiogram a különböző fehérjék differenciális indukcióját mutatja az akut stimulációval (1 – 2 óra egyszeri hatóanyag-expozíció után) a krónikus stimuláció ellen (1 nap az ismételt gyógyszer-expozíció után). (B) Fos-szerű fehérjék több hulláma [c-Fos (52-58-kDa izoformák), FosB (46-50-kDa izoformák), AFosB (33-kDa izoform) és Fra1 vagy Fra2 ( 40 kDa)] a nukleáris accumbensben és a dorsalis striatális neuronokban indukálódik egy visszaélésszerű gyógyszer akut beadásával. Indukáltak az ΔFosB (35 – 37 kDa) biokémiailag módosított izoformái is; az akut gyógyszeradagolás után is (bár alacsony szinten) indukálnak, de stabilitásuk miatt hosszú ideig az agyban maradnak. (C) Ismétlődő (pl. Naponta kétszer) gyógyszeradagolás esetén minden akut inger alacsony stabilitást indukál a stabil AFosB izoformákban, amit az alsó, egymást átfedő vonalak halmaza jelez, amelyek az egyes akut ingerek által indukált ΔFosB-t jelzik. Ennek eredményeképpen fokozatosan növekszik az AFosB teljes szintjei ismétlődő ingerekkel a krónikus kezelés során, amit a növekvő lépcsősor jelez a grafikonban.
Nagyon különböző válaszok jelentkeznek a kábítószer-használat krónikus alkalmazása után (1. Ábra). Az AFosB biokémiailag módosított izoformái (molekulatömeg 35 – 37 kDa) ugyanazon agyrégiókban felhalmozódnak ismételt gyógyszer-expozíció után, míg az összes többi Fos család tagja toleranciát mutat (azaz csökkentett indukció a kezdeti hatóanyag-expozícióhoz képest). A ΔFosB ilyen felhalmozódását a kokain, a morfin, az amfetamin, az alkohol, a nikotin és a ficiklidin esetében figyelték meg.e (11, 14 – 18). Bizonyos bizonyíték van arra, hogy ez az indukció szelektív a közepes tüskés neuronok dinorphin / anyag P-tartalmú részhalmazára, amely ezekben az agyrégiókban található (15, 17), bár több munkára van szükség annak biztosításához. Az AFosB 35-37-kDa izoformái dimerizálódnak főleg JunD-vel, hogy aktív és hosszú ideig tartó AP-1 komplexet képezzenek ezekben az agyi régiókban (19, 20). Ezek az αFosB izoformák rendkívül hosszú felezési idejük (21) miatt krónikus hatóanyag-expozícióval akkumulálódnak, és ezért a neuronokban legalább néhány héttel a gyógyszerbevitel leállítása után fennmaradnak. Érdekes megjegyezni, hogy ezek az αFosB izoformák egy közvetlen korai gén (fosB) rendkívül stabil termékei. Az AFosB izoformák stabilitása új molekuláris mechanizmust eredményez, amellyel a gyógyszerek által kiváltott változások a génexpresszióban továbbra is fennmaradhatnak a kábítószer-visszavonás viszonylag hosszú ideje ellenére.
Bár a nukleáris accumbens kritikus szerepet játszik a kábítószer-fogyasztás előnyös hatásaiban, úgy vélik, hogy normálisan működik a természetes erősítőkre adott válaszok, például az étel, az ital, a szex és a társadalmi kölcsönhatások szabályozása által (12, 13). Ennek eredményeképpen jelentős az érdeklődés ezen agyrégió lehetséges szerepe iránt más kényszeres viselkedésekben (pl. Patológiás overeating, szerencsejáték, edzés stb.). Emiatt megvizsgáltuk, hogy a ΔFosB-t egy kompulzív futás állati modellje szabályozza. Valójában az ΔFosB stabil 35-37-kDa-izoformái szelektíven indukálódnak a patkányok magvakban, amelyek kompulzív viselkedést mutatnak.
A stabil ΔFosB izoformák biokémiai azonossága
Amint fentebb említettük, az abuseFosB izoformák, amelyek a visszaélésszerű vagy kényszeres futást okozó gyógyszer krónikus beadása után felhalmozódnak, az 35 – 37 kDa molekulatömegét mutatják. Ezek különböztethetők meg az ΔFosB 33-kDa izoformájától, amelyet gyorsan, de átmenetileg egyetlen gyógyszer-expozíció után indukálnak (1. Ábra) (14, 19, 22). A jelenlegi bizonyítékok arra utalnak, hogy az 33-kDa izoform a fehérje natív formája, amely megváltozik a stabilabb 35-37-kDa termékek (19, 21) előállításához. Azonban a biokémiai módosítás jellege, amely az instabil 33-kDa izoformot stabil 35-37-kDa izoformává alakítja át, továbbra is homályos. Feltételezték, hogy a foszforiláció felelős (11). Például az AFosB indukciója csillapodik az olyan egerekben, amelyekben nincs DARPP-32, egy striatálisan dúsított fehérje (23, 24). Mivel a DARPP-32 szabályozza a fehérje-foszfatáz-1 és a protein-kináz A (25, 26) katalitikus aktivitását, a stabil AFosB izoformák normális felhalmozódásához szükséges fehérje szükségessége a stabil foszforiláció lehetséges szerepét sugallja.
Az ΔFosB szerepe a viselkedéses plaszticitásban a kábítószerekkel szemben
A osFosB szerepe a kábítószer-függőségben nagyrészt a transzgenikus egerek tanulmányozásából származik, amelyekben az AFosB szelektíven indukálható a felnőtt állatok magvakban és más striatális régióiban (27, 28). Fontos, hogy ezek az egerek túlzott mértékben expresszálják az AFosB-t szelektíven a dinorphin / anyag P-tartalmú közepes tüskés neuronokban, ahol a gyógyszerekről úgy gondolják, hogy a fehérjét indukálják. A 1 táblázatban összefoglaljuk az AFosB-t túlzottan expresszáló egerek viselkedési fenotípusát, amely sok esetben hasonlít az állatokra a krónikus hatóanyag-expozíció után. Az egerek fokozott lokomotoros választ mutatnak a kokainra akut és krónikus beadás után (28). Továbbá fokozott érzékenységet mutatnak a kokain és a morfin jutalmazó hatásaira helymeghatározó vizsgálatokban (11, 28), és önmagukban alacsonyabb dózisú kokainot adnak be, mint az ΔFosB-t nem túlérzékeny alomtársaiknak. érzékenység a kokainra és a normál térbeli tanulásra a Morris vízi labirintusában (28). Tezek az adatok azt mutatják, hogy a ΔFosB növeli az állat érzékenységét a kokainra és esetleg más bántalmazó szerekre nézve, és mechanizmust jelenthet a gyógyszerek viszonylag elhúzódó érzékenységéhez.
 striatum
striatum
| A fokozott lokomotoros aktiváció az akut és ismételt kokain-adagolás hatására. |
| A helymeghatározó vizsgálatokban a kokainra és a morfinra adott fokozott jutalmazási válasz. |
| Az alacsony dózisú kokain fokozott önadagolása. |
| A kokain fokozott motivációja progresszív arányú vizsgálatokban. |
| Az alkohollal szembeni fokozott anxiolitikus válaszok. |
| Megnövekedett kompulzív futási viselkedés. |
A refs adatok alapján. 28 és a 29.† ‡ §¶
Az ΔFosB által közvetített viselkedési plaszticitás a nukleáris accumbens-dorsal striatumban
IEzen túlmenően előzetes bizonyíték van arra, hogy az ΔFosB hatásai jóval túlmutathatnak a kábítószer-érzékenység szabályozásán túl, a függőségi folyamathoz kapcsolódó bonyolultabb viselkedésekhez. Az AFosB-t expresszáló egerek keményebben dolgoznak a kokain önadagolásában progresszív arányú önadagolási vizsgálatokban, suhogy az ΔFosB érzékenyítheti az állatokat a kokain ösztönző motivációs tulajdonságaira, és ezáltal a visszaesés utáni hajlamhoz vezethet a gyógyszer visszavonása utánl. ‡ A osFosB-t expresszáló egerek az alkohol fokozott anxiolitikus hatását is mutatják, § fenotípus, amely az alkohollal való fokozott alkoholfogyasztáshoz kapcsolódik. Ezek a korai eredmények együttesen arra utalnak, hogy az ΔFosB a kábítószerekkel szembeni fokozott érzékenység mellett minőségi viselkedési változásokat is eredményez, amelyek elősegítik a kábítószer-kereső viselkedést. Tehát az ΔFosB fenntartható „molekuláris kapcsolóként” működhet, amely segíti a függőségi állapot döntő szempontjainak megindítását és fenntartását. A jelenlegi vizsgálat egyik fontos kérdése, hogy a ΔFosB felhalmozódása a kábítószer-expozíció során elősegíti-e a kábítószer-kereső viselkedést hosszabb kilépési időszakok után, még akkor is, ha az ΔFosB szintek normalizálódtak (lásd alább).
Felnőtt egerekben, amelyek túlzottan expresszálják az AFosB-t a nukleáris accumbensben és a dorzális striatumban, szintén nagyobb kényszerfutást mutatnak a kontroll littermatesekhez képest. † Ezek a megfigyelések felvetik azt a érdekes lehetőséget, hogy az ΔFosB felhalmozódása ezeken a neuronokon általánosabb szerepet játszik a szokásos emlékek kialakításában és fenntartásában. viselkedésmódok, talán a neurális áramkörök hatékonyságának megerősítésével, amelyben ezek a neuronok működnek.
Az AFosB felhalmozódik bizonyos magterületeken, amelyek a magon kívül helyezkednek el, és a dorsalis striatumot a kokain krónikus expozíciója után. Ezek közül kiemelkedik a régiók az amygdala és a mediális prefrontális kéreg (15). A jelenlegi kutatás egyik fő célja, hogy megértsük az ΔFosB indukciónak ezekben a régiókban való hozzájárulását a függőség fenotípusához.
A fosB knockout egereken végzett korábbi munka során kiderült, hogy ezek az állatok nem képesek szenzibilizálni a kokain mozgásszervi hatásait, ami összhangban áll a fent említett ΔFosB-túlexpresszáló egerek megállapításával (22). A fosB mutánsok azonban fokozott érzékenységet mutattak a kokain akut hatásai iránt, ami nincs összhangban ezekkel a más megállapításokkal. A fosB mutánsokkal végzett eredmények értelmezését azonban bonyolítja az a tény, hogy ezeknek az állatoknak nemcsak ΔFosB, hanem teljes hosszúságú FosB-je is hiányzik. Ezenkívül a mutánsokból hiányzik mindkét fehérje az agyban és a fejlődés legkorábbi szakaszától kezdve. Valójában egy újabb munka alátámasztja a ΔFosB túlexpresszáló egerek következtetéseit: a c-Jun csonka mutánsának indukálható túlexpressziója, amely a ΔFosB domináns negatív antagonistájaként működik, szelektíven a nucleus accumbensben és a dorsalis striatum csökkent érzékenységet mutat a kokain jutalmazó hatásaival szemben Ezek a megállapítások hangsúlyozzák az óvatosságot, amelyet a konstitutív mutációval rendelkező egerek eredményeinek értelmezésénél kell alkalmazni, és bemutatják az indukálható és sejttípus-specifikus mutációkkal rendelkező egerek fontosságát a felnőtt agy plaszticitásának vizsgálatában.
Célgének az ΔFosB számára
Mivel az ΔFosB egy transzkripciós faktor, feltételezhetően a fehérje viselkedési plaszticitást okoz más gének expressziójának megváltoztatásával. A FosB-t a fosB gén alternatív splicingjével generáljuk, és hiányzik a teljes hosszúságú FosB-ben jelen lévő C-terminális transzaktivációs domén egy része. Ennek eredményeként eredetileg azt javasoljuk, hogy az AFosB transzkripciós represszorként (29) működjön. A sejtkultúrában végzett munka azonban egyértelműen kimutatta, hogy ΔfosB indukálhat vagy elnyomhat AP-1 által közvetített transzkripció az adott AP-1 helytől függően (21, 29 – 31). A teljes hosszúságú FosB ugyanazokat a hatásokat fejti ki, mint az ΔFosB bizonyos promóterfragmensekre, de más hatásokra másra. További munkára van szükség ahhoz, hogy megértsük az osFosB és a FosB ezen változatos fellépéseit.
Csoportunk két megközelítést alkalmazott a ΔFosB célgének azonosítására. Az egyik a jelölt gén megközelítés. Kezdetben az α-amino-3-hidroxi-5-metil-4-izoxazol-propionsav (AMPA) glutamát receptorokat vélt célpontoknak tekintettük, tekintettel a glutamaterg transzmissziónak a nucleus accumbensben betöltött fontos szerepére. Az eddigi munka azt mutatta, hogy egy adott AMPA glutamát receptor alegység, a GluR2 jóhiszemű célpont lehet a FosB számára (2. ábra). A GluR2 expresszió, de más AMPA receptor alegységek expressziója nem, megnő a nucleus accumbens-ben (de nem a dorsalis striatumban) a ΔFosB túlzott expressziója esetén (28), és egy domináns negatív mutáns expressziója gyengíti a kokain fehérjeindukciós képességét.¶ Ezenkívül a GluR2 gén promótere tartalmaz konszenzusos AP-1 helyet, amely megköti a FosB-t (28). A GluR2 túlzott mértékű expressziója a nucleus accumbensben, vírus által közvetített géntranszfer alkalmazásával növeli az állat érzékenységét a kokain jutalmazó hatásaival szemben, utánozva ezzel a ΔFosB-expresszáló egerekben látható fenotípus egy részét (28). A GluR2 indukciójának oka lehet a nucleus accumbens neuronok csökkent elektrofiziológiai érzékenysége az AMPA receptor agonistákkal szemben a krónikus kokain beadása után (32), mivel a GluR2-t tartalmazó AMPA receptorok csökkent teljes vezetőképességet és csökkent Ca2 + permeabilitást mutatnak. Ezeknek az idegsejteknek az ingerlő bemenetekre adott csökkent reakciókészsége ezután fokozhatja a visszaélésekre adott válaszokat. Azonban továbbra sem ismeretes, hogy a nucleus accumbens dopaminerg és glutamaterg jelei hogyan szabályozzák az addiktív viselkedést; ehhez szükség lesz egy neurális áramkör megértésére, amely még nem áll rendelkezésre.
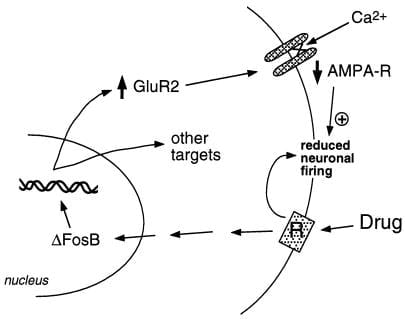
ábra 2
Az AMPA glutamát receptor alegység, a GluR2 feltételezett célpont a FosB számára. Bemutatták, hogy a GluR2 ΔFosB által közvetített indukciója hogyan változtathatja meg a nucleus accumbens neuronok fiziológiás reakciókészségét, és hogyan vezethet szenzibilizált válaszokhoz a bántalmazás kábítószerére. E séma szerint a bántalmazás drogjai a nucleus accumbens idegsejtek gátlásán keresztül eredményezik akut erősítő hatásukat. Ismételt expozíció esetén a gyógyszerek ΔFosB-t indukálnak, amely számos célgént szabályoz, beleértve a GluR2-t is. Ez megnöveli az AMPA-receptorok (AMPA-R) azon sejtmagok neuronjainak arányát, amelyek tartalmazzák a GluR2 alegységet, ami csökkentett általános AMPA áramot és csökkent Ca2 + áramot okoz. Ez a csökkent ingerlékenység érzékenyebbé teheti az idegsejteket a gyógyszerek akut gátló hatásaival és ezáltal a gyógyszerek erősítő hatásaival szemben..
Egy másik feltételezett cél az AFosB számára a dinamorfint kódoló gén. Amint azt korábban említettük, a dinamorfin expressziója a nukleáris accumbens közepes tüskés neuronok részhalmazában van, amelyek ΔFosB indukcióját mutatják.. Úgy tűnik, hogy a Dynorphin egy intercelluláris visszacsatolási hurokban működik: felszabadulása gátolja a dopaminerg neuronokat, amelyek a dopaminerg idegvégződésekben jelenlévő közepes tüskés neuronokat, valamint a ventrális tegmentális területen a sejtek és dendritek ervisálják. (3. Ábra) (33 – 35). Ez az elképzelés összhangban van egy κ receptor agonista képességével a két agyrégió egyikébe történő beadásakor, hogy csökkentsék a drog újraértékelését.d (35).
RAz ecent munka azt jelzi, hogy az ΔFosB csökkenti a dinorfin expresszióját, ami hozzájárulhat az osFosB indukció során tapasztalt jutalommechanizmusok fokozásához. Érdekes, hogy egy másik gyógyszerrel szabályozott transzkripciós faktor, a CREB (cAMP válaszelem kötő fehérje) (2, 3) ellentétes hatást fejt ki: dinamorfin expressziót indukál a magban, és csökkenti a kokain és a morfin jutalmazó tulajdonságait. (4). **
BA CREB hatóanyag-indukálta aktiválása a gyógyszer beadása után gyorsan eloszlik, a CREB és a ΔFosB ilyen dinamikus dinorfin szabályozása megmagyarázhatja a visszavonás korai és késői fázisaiban bekövetkező kölcsönös viselkedési változásokat, negatív érzelmi tünetekkel és a korai fázisban domináns csökkent érzékenységgel. a későbbi időpontokban uralkodó gyógyszerek jutalmazó és ösztönző hatásaira.
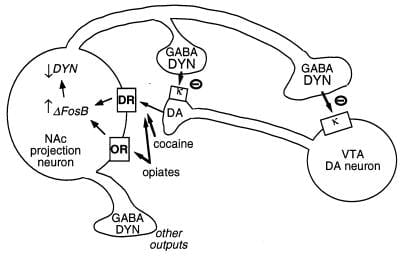
ábra 3
A Dynorphin az ΔFosB feltételezett célpontja. Egy ventrális tegmentális terület (VTA) dopamin (DA) neuron, amely a dororfint (DYN) expresszáló GABAerg projekciós neuron egy osztályát idegezi. A Dynorphin visszacsatolási mechanizmust szolgáltat ebben az áramkörben: a NAc neuronok termináljaiból felszabaduló dinamorfin hatással van a DA neuronok idegvégződményein és sejttestén található κ opioid receptorokra, hogy gátolja a működésüket. ΔfosBa dinamorfin expresszió gátlásával ez a visszacsatolási hurok szabályozható, és fokozhatja a visszaélésszerű gyógyszerek előnyös tulajdonságait. Nem látható a CREB kölcsönös hatása erre a rendszerre: a CREB fokozza a dinamorfin expressziót, és ezáltal gyengíti a visszaélésszerű gyógyszerek előnyös tulajdonságait (4). GABA, y-aminovajsav; DR, dopamin receptor; VAGY, opioid receptor.
A ΔFosB célgénjeinek azonosítására használt második megközelítés DNS mikroarray elemzést tartalmaz. A ΔFosB indukálható túlexpressziója növeli vagy csökkenti számos gén expresszióját a nucleus accumbens-ben (36). Bár jelentős munkára van szükség ezen gének mindegyikének ΔFosB fiziológiai célpontjaként való érvényesítéséhez és az addikciós fenotípushoz való hozzájárulásuk megértéséhez, az egyik fontos cél a Cdk5 (ciklinfüggő kináz-5). Így a Cdk5-t eredetileg mikro-sugarak használatával ΔFosB-szabályozással azonosították, majd később krónikus kokain beadása után kimutatták, hogy a nucleus accumbensben és a dorsalis striatumban indukálódik (37). A ΔFosB aktiválja a cdk5 gént a gén promóterében lévő AP-1 helyen keresztül (36). Ezek az adatok együttesen támogatják azt a sémát, amelyben a kokain Cdk5 expressziót indukál ezekben az agyrégiókban ΔFosB-n keresztül. A Cdk5 indukciója úgy tűnik, legalább részben megváltoztatja a dopaminerg jelátvitelt a DARPP-32 fokozott foszforilációja révén (37), amely a fehérje foszfatáz-1 inhibitorából a protein kináz A gátlójává alakul át, miután Cdk5 foszforileződik (26).
Az ΔFosB szerepe az „Állandó” plaszticitás közvetítésében a kábítószerekkel szemben
Bár az ΔFosB jel viszonylag hosszú élettartamú, nem állandó. A ΔFosB fokozatosan lebomlik, és az 1 – 2 gyógyszerkölcsönző hónapok után nem észlelhető az agyban, még akkor is, ha bizonyos viselkedési rendellenességek sokáig hosszabb ideig fennmaradnak. Ezért úgy tűnik, hogy az ΔFosB önmagában nem képes közvetíteni ezeket a félig állandó viselkedési rendellenességeket. A függőséggel kapcsolatos rendkívül stabil viselkedési változások alapjául szolgáló molekuláris adaptációk megtalálásának nehézségei hasonlóak a tanulás és a memória területén tapasztalt kihívásokhoz. Bár a tanulás és a memória elegáns, sejtes és molekuláris modelljei vannak, eddig nem volt lehetséges olyan molekuláris és celluláris adaptációk azonosítására, amelyek eléggé hosszú életűek ahhoz, hogy figyelembe vegyék a rendkívül stabil viselkedési emlékeket. Valójában a ΔFosB a leghosszabb életű adaptáció, amely ismerten előfordul a felnőtt agyban, nemcsak a bántalmazás kábítószereire reagálva, hanem bármilyen más zavarra is (amely nem jár elváltozásokkal). Két javaslat alakult ki, mind az addikció, mind a tanulás, mind a memória terén, ennek az ellentmondásnak a számbavétele érdekében.
Az egyik lehetőség az, hogy a génexpresszió több átmeneti változása, mint például az ΔFosB vagy más transzkripciós faktorok által közvetített változások (pl. CREB), közvetítheti a neuronális morfológia és a szinaptikus szerkezet hosszabb életű változásait. Például, a dendritikus gerincek sűrűségének növekedése (különösen a kétfejű tüskék növekedése) a kísérlethez kapcsolódik a glutamaterg szinapszisok fokozott hatékonysága a hippokampális piramis idegsejtekben a hosszú távú potencírozás során (38 – 40), és párhuzamos a megnövekedett viselkedési érzékenységgel a kokain mediálta a nukleáris accumbens (41) közepes tüskés neuronjainak szintjén. Nem ismert, hogy az ilyen szerkezeti változások eléggé hosszú életűek-e ahhoz, hogy figyelembe vegyék a viselkedés nagyon stabil változásait, bár ez utóbbi legalább 1 hónapig fennmarad a gyógyszer visszavonásától. A legfrissebb bizonyítékok felvetik annak a lehetőségét, hogy az AFosB és a Cdk5 indukciója a szinaptikus struktúrában a kábítószer-indukált változások egyik közvetítője (4. Ábra) ‡‡ Így a Cdk5 inhibitor infúziója a nukleáris magba kerül. az ismétlődő kokain-expozíció képessége a dendritikus gerincsűrűség növelésére ebben a régióban. Ez összhangban van azzal a nézettel, hogy az agyban dúsított Cdk5 szabályozza a neurális struktúrát és a növekedést (lásd az 36 és az 37 hivatkozásokat). Lehetséges, bár semmilyen módon nem bizonyított, hogy az idegrendszeri morfológiában bekövetkező ilyen változások meghaladhatják az ΔFosB jelet.
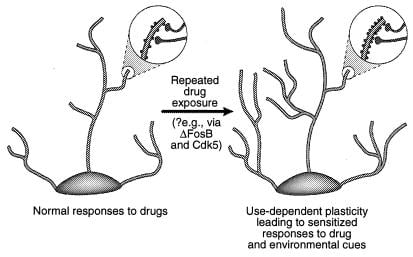
ábra 4
A dendritszerkezet szabályozása visszaélésekkel. Látható, hogy az idegsejt dendritfája kitágult a bántalmazás kábítószerével való krónikus expozíció után, amint azt a kokain esetében megfigyelték a nucleus accumbens és a prefrontális kéregben (41). A nagyítási területek a dendrit tüskék növekedését mutatják, amelyről feltételezik, hogy az aktivált idegterminálokkal együtt fordul elő. A dendritikus gerincsűrűség ezen növekedését a ΔFosB és az ebből következő Cdk5 indukció közvetítheti (lásd a szöveget). A dendritikus szerkezet ilyen változásai, amelyek hasonlóak az egyes tanulási modellekben megfigyeltekhez (pl. Hosszú távú potencírozás), közvetíthetik a visszaélések kábítószerével vagy a környezeti jelzésekkel kapcsolatos, hosszú életen át tartó érzékeny reakciókat. [Reprodukálva a ref. Engedélyével 3 (Copyright 2001, Macmillian Magazines Ltd.)].
Egy másik lehetőség, hogy a transzkripciós faktor átmeneti indukciója (pl. ΔFosB, CREB) a kromati módosításával a génexpresszió állandó változásához vezetn. Ezek és sok más transzkripciós faktor úgy vélik, hogy aktiválják vagy elnyomják a célgén transzkripcióját azáltal, hogy elősegítik a gén (42) közelében lévő hisztonok acetilezését vagy dezacetilezését. Bár az ilyen acetilezés és a hisztonok dezacetilezése nyilvánvalóan nagyon gyorsan előfordulhat, lehetséges, hogy az ΔFosB vagy CREB hosszabb ideig tartó adaptációkat eredményezhet a hiszton-acetilezést szabályozó enzimatikus gépben. Az AFosB vagy a CREB előmozdíthatja a génexpresszió hosszabb életű változásait a kromatin más módosításainak szabályozásával (pl. DNS vagy hiszton-metiláció), amelyek szerepet játszanak a fejlődési folyamat során bekövetkező gén transzkripció állandó változásaiban (lásd 42 és 43). . Bár ezek a lehetőségek spekulatívak maradnak, olyan mechanizmust hozhatnak létre, amellyel a visszaélés kábítószerének (vagy más zavarásnak) az átmeneti adaptációi lényegében élethosszig tartó viselkedési következményekkel járhatnak.
Referenciák
- ↵
- Nestler EJ
- Hope BT,
- Widnell KL
(1993) Neuron 11: 995 – 1006.
CrossRefMedlineháló of Science
- ↵
- Berke JD,
- Hyman SE
(2000) Neuron 25: 515 – 532.
CrossRefMedlineháló of Science
- ↵
- Nestler EJ
(2001) Nat Rev Neurosci 2: 119 – 128.
CrossRefMedlineháló of Science
- ↵
- Carlezon WA Jr,
- Thome J,
- Olson VG,
- Lane-Ladd SB,
- Brodkin ES,
- Hiroi N,
- Duman RS
- Neve RL,
- Nestler EJ
(1998) Tudomány 282: 2272 – 2275.
Absztrakt / ingyenes teljes szöveg
- O'Donovan KJ,
- Tourtellotte WG,
- Millbrandt J,
- Baraban JM
(1999) Trendek Neurosci 22: 167 – 173.
- ↵
- Mackler SA,
- Korutla L,
- Cha XY,
- Koebbe MJ,
- Fournier KM,
- Bowers MS,
- Kalivas PW
(2000) J Neurosci 20: 6210 – 6217.
Absztrakt / ingyenes teljes szöveg
- ↵
- Morgan JI,
- Curran T
(1995) Trendek Neurosci 18: 66 – 67.
- ↵
- Fiatal ST,
- Porrino LJ
- Iadarola MJ
(1991) Proc Natl Acad Sci USA 88: 1291 – 1295.
Absztrakt / ingyenes teljes szöveg
- Graybiel AM
- Moratalla R
- Robertson HA
(1990) Proc Natl Acad Sci USA 87: 6912 – 6916.
Absztrakt / ingyenes teljes szöveg
- B remény,
- Kosofsky B,
- Hyman SE,
- Nestler EJ
(1992) Proc Natl Acad Sci USA 89: 5764 – 5768.
Absztrakt / ingyenes teljes szöveg
- ↵
- Kelz MB,
- Nestler EJ
(2000) Curr Opinion Neurol 13: 715 – 720.
CrossRefMedlineháló of Science
- ↵
- Koob GF,
- Sanna PP
- Bloom FE
(1998) Neuron 21: 467 – 476.
CrossRefMedlineháló of Science
- ↵
- Bölcs RA
(1998) Kábítószer-alkohol-függőség 51: 13 – 22.
CrossRefMedlineháló of Science
- ↵
- Hope BT,
- Nye HE
- Kelz MB,
- Önálló DW,
- Iadarola MJ
- Nakabeppu Y
- Duman RS
- Nestler EJ
(1994) Neuron 13: 1235 – 1244.
- ↵
- Nye H
- Hope BT,
- Kelz M,
- Iadarola M,
- Nestler EJ
(1995) J Pharmacol Exp Ther 275: 1671 – 1680.
Absztrakt / ingyenes teljes szöveg
- Nye HE
- Nestler EJ
(1996) Mol Pharmacol 49: 636 – 645.
- ↵
- Moratalla R
- Elibol B,
- Vallejo M,
- Graybiel AM
(1996) Neuron 17: 147 – 156.
CrossRefMedlineháló of Science
- ↵
- Pich EM,
- Pagliusi SR
- Tessari M,
- Talabot-Ayer D,
- Hooft van Huijsduijnen R
- Chiamulera C
(1997) Tudomány 275: 83 – 86.
Absztrakt / ingyenes teljes szöveg
- ↵
- Chen JS
- Nye HE
- Kelz MB,
- Hiroi N,
- Nakabeppu Y
- Hope BT,
- Nestler EJ
(1995) Mol Pharmacol 48: 880 – 889.
- ↵
- Hiroi N,
- Brown J,
- Ye H
- Saudou F
- Vaidya VA
- Duman RS
- Greenberg ME
- Nestler EJ
(1998) J Neurosci 18: 6952 – 6962.
Absztrakt / ingyenes teljes szöveg
- ↵
- Chen J,
- Kelz MB,
- Hope BT,
- Nakabeppu Y
- Nestler EJ
(1997) J Neurosci 17: 4933 – 4941.
Absztrakt / ingyenes teljes szöveg
- ↵
- Hiroi N,
- Brown J,
- Haile C
- Ye H
- Greenberg ME
- Nestler EJ
(1997) Proc Natl Acad Sci USA 94: 10397 – 10402.
Absztrakt / ingyenes teljes szöveg
- ↵
- Fienberg AA,
- Hiroi N,
- Mermelstein P,
- Song WJ
- Snyder GL
- Nishi A
- Cheramy A,
- O'Callaghan JP,
- Miller D
- Cole DG,
- és mtsai.
(1998) Tudomány 281: 838 – 842.
Absztrakt / ingyenes teljes szöveg
- ↵
- Hiroi N,
- Feinberg A,
- Haile C
- Greengard P,
- Nestler EJ
(1999) Eur J Neurosci 11: 1114 – 1118.
CrossRefMedlineháló of Science
- ↵
- Greengard P,
- Allen PB,
- Nairn AC
(1999) Neuron 23: 435 – 447.
CrossRefMedlineháló of Science
- ↵
- Bibb JA,
- Snyder GL
- Nishi A
- Yan Z,
- Meijer L
- Fienberg AA,
- Tsai LH
- Kwon YT
- Girault JA,
- Czernik AJ,
- és mtsai.
(1999) Természet (London) 402: 669 – 671.
- ↵
- Chen JS
- Kelz MB,
- Zeng GQ,
- Sakai N,
- Steffen C,
- Shockett PE,
- Picciotto M,
- Duman RS
- Nestler EJ
(1998) Mol Pharmacol 54: 495 – 503.
Absztrakt / ingyenes teljes szöveg
- ↵
- Kelz MB,
- Chen JS
- Carlezon WA
- Whisler K
- Gilden L
- Beckmann AM
- Steffen C,
- Zhang YJ
- Marotti L
- Önálló SW,
- és mtsai.
(1999) Természet (London) 401: 272 – 276.
- ↵
- Dobrazanski P
- Noguchi T
- Kovary K,
- Rizzo CA
- Lazo PS
- Bravo R
(1991) Mol Cell Biol 11: 5470 – 5478.
Absztrakt / ingyenes teljes szöveg
- Nakabeppu Y
- Nathans D
(1991) 64: 751 – 759.
CrossRefMedlineháló of Science
- ↵
- Yen J,
- Bölcsesség RM,
- Tratner I
- Verma IM
(1991) Proc Natl Acad Sci USA 88: 5077 – 5081.
Absztrakt / ingyenes teljes szöveg
- ↵
- Fehér FJ,
- Hu XT,
- Zhang XF,
- Wolf ME
(1995) J Pharmacol Exp Ther 273: 445 – 454.
Absztrakt / ingyenes teljes szöveg
- ↵
- Hyman SE
(1996) Neuron 16: 901 – 904.
- Kreek MJ
(1997) Pharmacol Biochem Behav 57: 551 – 569.
CrossRefMedlineháló of Science
- ↵
- Shippenberg TS
- Rea W
(1997) Pharmacol Biochem Behav 57: 449 – 455.
CrossRefMedlineháló of Science
- ↵
- Chen JS
- Zhang YJ
- Kelz MB,
- Steffen C,
- Ang ES,
- Zeng L
- Nestler EJ
(2000) J Neurosci 20: 8965 – 8971.
Absztrakt / ingyenes teljes szöveg
- ↵
- Bibb JA,
- Chen JS
- Taylor JR,
- Svenningsson P,
- Nishi A
- Snyder GL
- Yan Z,
- Sagawa ZK,
- Nairn AC
- Nestler EJ
- és mtsai.
(2001) Természet (London) 410: 376 – 380.
- ↵
- Luscher C
- Nicoll RA
- Malenka RC,
- Muller D
(2000) Nat Neurosci 3: 545 – 550.
CrossRefMedlineháló of Science
- Malinow R
- Mainen ZF,
- Hayashi Y
2000 10: 352 – 357.
CrossRefMedlineháló of Science
- ↵
- Scannevin RH,
- Huganir RL
(2000) Nat Rev Neurosci 1: 133 – 141.
CrossRefMedlineháló of Science
Robinson, TE és Kolb, B. (1999) (1997) Eur. J. Neurosci.11, 1598-1604.
- ↵
- Carey M,
- Smale ST
(2000) Transkripciós szabályozás az Eukariótákban (Cold Spring Harbor Lab. Press, Plainview, NY).
- ↵
- Spencer VA
- Davie JR
(1999) Gene 240: 1 – 12.
CrossRefMedlineháló of Science
A cikkre hivatkozó HighWire Press-hosted cikkek
- Természetes és drogdíjakról szóló törvény a közös neurális plaszticitási mechanizmusokról a {Delta} FosB-vel, mint kulcsközvetítő J. Neurosci. 2013 33 (8) 3434-3442
- Kábítószerek, bűnözés és a hedonikus allosztázis epigenetikája 2012 28 (3) 314-328
- Absztrakt
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- Absztrakt
- Teljes szöveg (HTML)
- Teljes szöveg (PDF)
- A morfin aktiválja az E huszonnégy hasonló transzkripciós faktor-1 / szérum válaszfaktor útját az 1 / 2 extracelluláris jelszabályozott kinázok segítségével a Dorsal Root Ganglia Neuronokból származó F11 sejtekben J. Pharmacol. Exp. Ther. 2012 342 (1) 41-52
- Az átjáró molekuláris mechanizmusa: a nikotin Prime Gene Expression által a kokain által indított epigenetikus változások Sci Transl Med 2011 3 (107) 107ra109
- Fokozott szacharóz és kokain önigazgatás és a Cue által kiváltott kábítószer-keresés a VGLUT2 vesztesége után az egerek közepén lévő dopamin neuronokban J. Neurosci. 2011 31 (35) 12593-12603
- A krónikus szakaszos hipoxia fokozza a vérnyomást és a FosB / {Delta} FosB expresszióját központi autonóm régiókban Am. J. Physiol. Regul. Integr. Comp. Physiol. 2011 301 (1) R131-R139
- A GPR37 / PAEL receptor hiánya rontja a striatális Akt és ERK2 foszforilációját, {Delta} FosB expresszióját, és az amfetamin és a kokain kondicionált hely preferenciáját FASEB J. 2011 25 (6) 2071-2081
- A kezdeti alkohol expozíció időtartama és a molekuláris tolerancia tartóssága közötti összefüggés jelentősen nemlineáris J. Neurosci. 2011 31 (7) 2436-2446
- In vivo in vivo biolumineszcencia képalkotás Revox-szabályozott aktivátorprotein-1 aktivációt mutat az egerek Paraventricularis Nucleusában. Hypertonia 2011 57 (2) 289-297
- A {Delta} FozB Striatus túlzott expressziója Krónikus Levodopa által kiváltott akaratlan mozgásokat reprodukál J. Neurosci. 2010 30 (21) 7335-7343
- Környezeti hatások epigenetikus mediációja a nagy pszichotikus rendellenességekben Schizophr Bull 2009 35 (6) 1045-1056
- DNS-alapú MRI-próbák az amfetamin krónikus expozíciójának specifikus kimutatására az élő brainokban J. Neurosci. 2009 29 (34) 10663-10670
- Módosított dendritikus gerinc plaszticitása a kokain-kivont patkányokban J. Neurosci. 2009 29 (9) 2876-2884
- A Drosophila túlexpresszió képernyője A GSK-3 {beta} / shaggy neuronális szerepét azonosítja az AP-1-függő fejlődési plaszticitás szabályozójaként Genetika 2008 180 (4) 2057-2071
- Transkripciós MRI: egy új nézet az élő agyról 2008 14 (5) neurológus 503-520
- {Delta} FosB indukció az orbitofrontális Cortex-ben A kokain által indukált kognitív diszfunkció toleranciáját közvetíti J. Neurosci. 2007 27 (39) 10497-10507
- Tartós sebezhetőség a metamfetamin kereső viselkedés visszaállítására a glia sejtvonalból származó neurotróf faktor mutáns egerekben FASEB J. 2007 21 (9) 1994-2004
- {Delta} FosB a Nucleus Accumbensben szabályozza az élelmiszer-megerősített instrumentális viselkedést és motivációt J. Neurosci. 2006 26 (36) 9196-9204
- A {Delta} FosB stabilitásának szabályozása foszforilációval. J. Neurosci. 2006 26 (19) 5131-5142
- A mutáns NMDA receptorok expressziója a dopaminban D1 Receptor-tartalmú sejtek Megakadályozza a kokainszenzibilizációt és csökkenti a kokainpreferenciát J. Neurosci. 2005 25 (28) 6651-6657
- D1 Dopamin receptorok modulálják a {Delta} FosB indukciót patkánystriatumban az időszakos morfin beadása után J. Pharmacol. Exp. Ther. 2005 314 (1) 148-154
- A nagy önkéntes kerékvezetési tevékenységre kiválasztott egerek neurobiológiája Integr. Comp. Biol. 2005 45 (3) 438-455
- A vízhiány és a rehidratáció hatása a c-Fos-ra és a FosB-festésre a patkány szupraoptikus magjában és a lamina terminalis régióban Am. J. Physiol. Regul. Integr. Comp. Physiol. 2005 288 (1) R311-R321
- FosB / {Delta} FosB gén transzkripciós indukciója mechanikai stresszel Osteoblastokban J Biol Chem 2004 279 (48) 49795-49803
- A {Delta} FosB indukciója a krónikus stressz utáni jutalmú agyi szerkezetekben J. Neurosci. 2004 24 (47) 10594-10602
- A Sim1 géndózis az egerekben a fokozott táplálkozási zsírra adott homeosztatikus táplálási választ modulálja Am. J. Physiol. Endocrinol. Metab. 2004 287 (1) E105-E113
- A gének expressziójának DNS-mikroarray-analízise a humán látóideg fej-asztrocitáiban a hidrosztatikus nyomás hatására Physiol. 2004 17 (2) 157-169 genomika
- A szuperoxid részt vesz a központi idegrendszer aktiválásában és a szívizominfarktus által kiváltott szívelégtelenség szimpathoexcitációjában Circ. Res. 2004 94 (3) 402-409
- Adenozin A2A receptorok neuroadaptációban ismételt dopaminerg stimulációhoz: Következmények a dyskinesiák kezelésére Parkinson-kórban Neurológia 2003 61 (90116) S74-81
- A Fos-ral összefüggő fehérjék citoplazmás versus nukleáris lokalizációja a béka, Rana esculenta, Testis: Gonadotropin-felszabadító hormon agonista in vivo és közvetlen in vitro hatása Biol. Repród. 2003 68 (3) 954-960
- Periadolescent egerek mutatják a fokozott Delta FosB Upregulation-et a kokain és az amfetamin hatására J. Neurosci. 2002 22 (21) 9155-9159
- Delta FosB szabályozza a kerék futását J. Neurosci. 2002 22 (18) 8133-8138
- A CREB aktivitás a magban az accumbens héjában szabályozza az érzelmi ingerekre adott viselkedési válaszok gatingét Proc. Nati. Acad. Sci. USA 2002 99 (17) 11435-11440
- Pszichogenomika: a függőség megértésének lehetőségei J. Neurosci. 2001 21 (21) 8324-8327
