Фронт. Психіатрія, 25 Лютий 2016 | http://dx.doi.org/10.3389/fpsyt.2016.00024
Джарід Гудман та Марк Паккард*
- Департамент психології, Техаський інститут неврології A&M, Техаський університет A&M, Коледж-Стейшн, штат Техас, США
Велику підтримку отримала думка, що анатомічно відмінні системи пам'яті диференційно сприяють розвитку наркоманії та рецидивів. Цей короткий огляд переглядає цю гіпотезу, як це було спочатку запропоновано 20 років тому (1) і підкреслює кілька останніх подій. Широкі дослідження, що використовують різноманітні парадигми вивчення тварин, свідчать про те, що диссоційовані нейронні системи опосередковують різні види навчання і пам'яті. Кожна система пам'яті потенційно сприяє унікальним компонентам для вивченої поведінки, що підтримує наркоманію і рецидив. Зокрема, перехід від рекреаційного вживання наркотиків до компульсивного наркоманії може відображати нейроанатомічний зсув від когнітивного контролю поведінки, опосередкованого гіпокампом / дорсомедіальним стриатумом, до звичного контролю поведінки, опосередкованого дорсолатеральним стриатумом (DLS). Крім того, стрес / тривога може становити кофактор, який полегшує DLS-залежну пам'ять, і це може служити як нейро-поведінковий механізм, що лежить в основі посиленого вживання наркотиків і рецидивів у людей після стресових подій життя. Докази, що підтверджують думку про множинних системах наркоманії, надходять переважно з досліджень навчання та пам'яті, які використовуються як підсилюючі речовини, що викликають звикання, які часто розглядаються в контексті досліджень наркоманії, включаючи кокаїн, алкоголь та амфетаміни. Крім того, недавні дані свідчать про те, що підхід до систем пам'яті також може бути корисним для розуміння актуальних джерел залежності, які відображають нові проблеми зі здоров'ям, включаючи використання марихуани, дієти з високим вмістом жирів і відеоігри.
Вступ
Слідчі часто шукають механізми навчання і поведінки, щоб пояснити, як набуває і виражається людська психопатологія. Прикладом такої програми став Норман Уайт, який використовував принципи класичної теорії навчання та експериментальні докази, що підтверджують існування декількох систем пам'яті в головному мозку для забезпечення нового, впливового підходу до наркоманії (1). Зокрема, Уайт зазначив, що наркотики можуть відігравати роль «підсилювачів», які, наприклад, харчування або вода в навчальному завданні, посилюють асоціації між пов'язаними з наркотиками стимулами, контекстом і поведінкою, що сприяє вживанню наркотиків і, згодом, залежністю. Білий також включив виникаючу гіпотезу, що існують різні типи пам'яті, які опосередковуються диссоційованими нейронними системами. Згідно з цим новим поглядом, лікарські засоби можуть безпосередньо модулювати кілька нейронних систем, і ці нейронні системи йдуть на кодування окремих компонентів пам'яті, пов'язаної з наркотиками, що, при вираженні, сприяє подальшому прийому ліків.
Рік 2016 відзначає 20 річницю багаторазової системи пам'яті про наркоманію, як описано Білим. Цей огляд переглядає цю впливову гіпотезу, підкреслюючи деякі важливі останні події, які не тільки обґрунтували первісну гіпотезу, але й дали додаткове розуміння того, як багато систем пам'яті потенційно підтримують наркоманію.
Кілька систем пам'яті Погляд на залежність
Збігаються докази з досліджень, що використовують людей і нижчих тварин, свідчать про те, що пам'ять ссавців опосередковується відносно незалежними нейронними системами [див. (2-4)]. Ранні експерименти, що дисоціюють декілька систем пам'яті, в основному проводилися в радіальному лабіринті і вказували на унікальні мнемонічні функції для гіпокампу, дорсального стриатума і мигдалини (5, 6). Гіпокамп опосередковує когнітивну / просторову форму пам'яті, тоді як спинний стриатум опосередковує пам'ять звички стимулу-відповіді (S – R). Амигдала опосередковує відносини Павлова і стимулу-афекту-асоціативного (6, 7), одночасно підтримуючи модуляторну роль емоційного збудження на інших типах пам'яті (8-12).
У контексті перегляду декількох систем пам'яті, білий (1) припустив, що гіпокамп, спинний стриатум і амигдала кодують унікальні компоненти спогадів, пов'язаних з наркотиками (див. малюнок) 1). Гіпокамп кодує явні знання, що стосуються взаємозв'язку між сигналами та подіями (тобто асоціаціями стимулів-стимулів) у контексті наркотиків. Важливо відзначити, що гіпокамп не кодує поведінкові реакції, але, скоріше, інформація, отримана гіпокампом, може бути використана для генерування відповідних поведінкових реакцій для отримання підкріплення наркотиків. З іншого боку, спинний стриатум кодує асоціації між пов'язаними з наркотиками подразниками і поведінковими реакціями. Це може дозволити представлення пов'язаного з наркотиками мітки для активації автоматичної поведінкової реакції, що призводить до прийому наркотиків (наприклад, підхід, що наближається, або прес для інструментальних важелів). Амигдала кодує павлово-асоціативні відносини, дозволяючи таким чином нейтральні сигнали в контексті наркотиків пов'язуватися з винагородою за лікарський засіб. Тварини пізніше реагують на ці обумовлені сигнали подібно до того, як вони спочатку реагували на препарат. Зокрема, обумовлені сигнали активізують обумовлені емоційні реакції, включаючи внутрішні афективні стани та умовний підхід до (або, у деяких випадках, уникнення) умовного сигналу. Іншою важливою складовою гіпотези Білого є те, що ліки можуть модулювати функцію пам'яті кожного з цих областей мозку. Таким чином, препарати можуть потенційно підвищити рівень власного самоврядування шляхом збільшення консолідації пов'язаних з наркотиками спогадів, кодованих гіпокампом, мигдалиною і спинним стриатумом (див. Малюнок). 1).
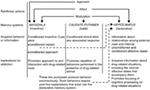
Малюнок 1. Білий (1) системи множинної пам'яті з урахуванням наркоманії. Як і природні підсилювачі, наркотичні речовини, що викликають залежність, мають декілька «підсилюючих дій», включаючи здатність викликати позитивний / негативний вплив, підхід та модуляцію систем пам'яті. Мигдалина, хвостатий путамен (тобто дорсальний смугастий вузол) та гіпокамп опосередковують роз’єднані системи пам’яті, і кожна система пам’яті, мабуть, кодує унікальні компоненти спогадів, пов’язаних із наркотиками. Враховуючи властивості модуляції пам’яті, наркотичні речовини, що викликають залежність, можуть потенційно посилити власне самовведення шляхом посилення функції цих систем. (Передруковано з White з дозволу John Wiley & Sons.)
Відповідно до системи множинних систем пам'яті про наркоманію, обширні докази вказують на критичну роль гіпокампу, спинного стриатума та мигдалини в наркоманії та рецидиві для різних зловживаних речовин [див. (13)]. Дорсальний гіпокамп, здається, відіграє певну роль у контекстному контролі пошуку наркотиків кокаїном (14-16). Латеральна область спинного стриатума (DLS) опосередковує звичний важіль пресування S – R для кокаїну та алкоголю (17, 18), а базолатеральна мигдалина (BLA) опосередковує кондиціювання наркотиків для кокаїну, алкоголю та героїну (19-22). Також узгоджується з гіпотезою Білого, речовини зловживання можуть модулювати мнемонічні функції гіпокампу, спинного стриатума і мигдалини (23-31).
Недавні дослідження сприяли новим змінам у підходах до систем множинної пам'яті до наркоманії. Ключові особливості цього сучасного погляду включають (1) нейроанатомічний зсув у часі до DLS-залежної пам'яті звички, (2) конкурентних взаємодій між системами пам'яті, (3) роль стресу і тривоги у підвищенні звичного пошуку наркотиків, і (4) застосування цієї гіпотези до нових виникаючих джерел залежності.
Нейроанатомічний перехід від пізнання до звички
У експериментальних ситуаціях навчання суб'єкти зазвичай використовують цілеспрямоване поведінку, коли спочатку вирішують завдання. Проте, після тривалої підготовки, поведінка стає автономною і може виконуватися з невеликою увагою, наміром або пізнавальним зусиллям, що становить «звичку» [для перегляду, див. (32)]. На ранніх демонстраціях цього переходу від когнітивного контролю поведінки до звички, гризунів навчали з використанням харчової винагороди у завданнях з двома розчинами плюс-лабіринт (33-35). У цьому завданні щурів звільняли з тієї самої початкової позиції (наприклад, з південної руки) і повинні були здійснювати послідовний поворот тіла на перехресті лабіринту, щоб отримати винагороду за їжею, завжди розташовану в одній руці цілі (наприклад, завжди робити ліворуч) поверніть, щоб знайти їжу в західній руці). Щури могли б вирішити це завдання, або вивчивши послідовну реакцію на поворот тіла, або зробивши будь-яку відповідь, необхідну для того, щоб перейти до того ж просторового розташування. Щоб визначити, яку стратегію використовували щури, дослідники провели тест-зонд, в якому звільнені тварини з протилежної стартової руки (наприклад, північна рука). Якщо тварини зробили протилежне тіло-поворот, щоб перейти до вихідного місця розташування цілі, вони були ідентифіковані як місце навчання. Якщо тварини робили той же поворот тіла, що і під час тренування (тобто, переходячи на руку, протилежну до місця розташування початкової мети), тварини були ідентифіковані як відповідні учні. Докази свідчать про те, що після деяких тренувань більшість тварин виявляють місце навчання, тоді як після тривалого навчання тварини переходять до звичного навчання відповіді (34-36). Цікаво, що цей перехід від місця навчання до навчання відповіді може відображати нейроанатомічний зсув. Початкове використання місцевого навчання в цьому завданні опосередковується гіпокампом і дорсомедіальним стриатумом [DMS (36, 37)], в той час як використання навчання відповіді після тривалого навчання опосередковується DLS (36).
Окрім ранніх демонстрацій, які використовують плюс-лабіринт (34, 35), поведінковий зсув до пам'яті звички був пізніше продемонстрований з використанням парадигм натискання оперантного важеля (38-42). У цих інструментальних навчальних завданнях, тварини спочатку цілеспрямовано натискають на натискання, щоб отримати результат, і припинять натискання важеля, коли результат харчування знецінюється. Проте, після великої тренування тварини перейдуть до звичного відповіді і продовжуватимуть натискати на важіль навіть після того, як результат харчування буде знецінений (40). Як це спочатку було продемонстровано в плюс-лабіринті (36), перехід від пізнання до звички в інструментальних завданнях навчання також можна віднести до нейроанатомічного зрушення. Початковий когнітивний контроль поведінки в цих інструментальних навчальних завданнях опосередковується гіпокампом і DMS (43, 44), тоді як пізніші звичні відповіді опосередковуються DLS (18, 45, 46).
Численні дослідники припустили, що нейроанатомічний зсув до пам'яті звички, продемонстрований у лабіринті та інструментальних навчальних завданнях, також може бути підставою для переходу від рекреаційного вживання наркотиків до компульсивного наркоманії (13, 47-50). Відповідно до цієї гіпотези, дослідники продемонстрували для різних зловживаних речовин, що DMS опосередковує цілеспрямоване реагування на підкріплення наркотиків, і DLS опосередковує звичні відповіді на посилення наркотиків (18, 31, 51-53).
Враховуючи високий потенціал зловживань деякими препаратами, дослідники припускають, що наркотичні засоби, що викликають звикання, можуть підвищити функцію пам'яті, що залежить від DLS і тим самим прискорити перехід від когнітивного до звичного контролю поведінки. Відповідно до цієї гіпотези, повторне вплив амфетаміну або кокаїну полегшує перехід від цілеспрямованого до звичного реагування на посилення їжі в інструментальних завданнях натискання важеля (31, 54-59). Крім того, натискання важеля для залежних речовин (наприклад, алкоголю або кокаїну) та винагороди за їжею було пов'язане з більшою звичною реакцією проти цілеспрямованого реагування (24, 60, 61). У людини індивідууми, що залежать від алкоголю, виявляють більшу звичну реакцію в інструментальному навчальному завданні, порівняно з індивідуумами, які не залежать від контролю (62). Це підвищення DLS-залежної пам'яті звички залежними від наркотиків також спостерігалося в навчальних завданнях лабіринта гризунів. Експозиція кокаїну, амфетаміну та алкоголю пов'язана з розширеним навчанням в DLS-залежних задачах лабіринту або більшим використанням стратегій DLS-залежного реагування в версіях лабіринту з двома рішеннями (25, 63, 64). У людях використання зловживаних речовин, включаючи алкоголь і тютюн, співвідноситься з більш широким використанням дорзальних стриатум-залежних навігаційних стратегій у віртуальному лабіринті (65). Таким чином, деякі наркотичні засоби можуть підвищити DLS-залежну пам'ять звички, і це підвищене залучення системи пам'яті DLS може прискорити перехід від рекреаційного вживання наркотиків до звичного зловживання наркотиками. Цей запропонований механізм узгоджується з1) оригінальне твердження про те, що наркотичні засоби можуть іноді полегшувати власне самоврядування шляхом посилення функції систем пам'яті.
Конкуренція між системами пам'яті
Хоча можливо, що звикаючі препарати посилюють пам'ять звички безпосередньо за рахунок посилення функції DLS [наприклад, вих. (29)], інша можливість полягає в тому, що лікарські засоби зловживання посилюють пам'ять звички опосередковано через модуляцію інших систем пам'яті. Цей альтернативний механізм викликає гіпотезу про те, що в деяких навчальних ситуаціях системи пам'яті конкурують за контроль над навчанням і що, погіршуючи функцію однієї системи пам'яті, функція іншої недоторканої системи може бути посилена (11, 66). Слід зазначити, що гіпокампи і DLS можуть іноді конкурувати за контроль навчання, завдяки чому ураження гіпокампу посилює функцію пам'яті, залежної від DLS (5, 6, 67, 68). Конкурентні взаємодії також можуть бути продемонстровані в задачах з двома рішеннями, коли порушення однієї системи пам'яті призводить до використання стратегії, опосередкованої іншою недоторканою системою. Наприклад, тварини, яким надано ураження DMS, відображають залежне від DLS звичне реагування на винагороду за їжу в інструментальних завданнях навчання (44).
Враховуючи конкурентні взаємодії, які іноді виникають між системами пам'яті, одна з можливостей полягає в тому, що деякі наркотичні засоби можуть посилити залежну від DLS пам'ять звички, опосередковано порушуючи механізми когнітивної пам'яті, опосередкованого DMS і гіпокампом. Як зазначалося раніше, алкоголь пов'язаний з більшим використанням пам'яті DLS-залежної звички в лабіринті і операндних парадигмах натискання важеля (24, 61, 62, 64, 65). Докази також вказують на те, що алкоголь погіршує навчання в задачах просторової пам'яті, залежних від гіпокампу [64, 69-72); для перегляду див. (73)], а також у залежних від DMS завдань навчання74-77). Відповідно до конкурентної взаємодії між системами пам'яті, було висунуто гіпотезу, що алкоголь може полегшити DLS-залежну пам'ять звички опосередковано через погіршення механізмів когнітивної пам'яті (78).
Слід зазначити, що, крім алкоголю, численні препарати були пов'язані з дефіцитом когнітивної пам'яті. Вплив морфіну, героїну, метамфетаміну, МДМА (екстазі) або хронічного кокаїну аналогічно призводить до просторових порушень пам'яті, що залежать від гіпокампу, в різних завданнях (79-89). Спокусливо спекулювати, що, як було запропоновано для алкоголю, порушення когнітивної пам'яті, спричинені звиканнями, можуть опосередковано посилити DLS-залежну пам'ять звички, і що це може бути один механізм, що дозволяє самостійному адмініструванню наркотиків стати звичним для людей, які вживають наркотики. З іншого боку, також можливо, що просторові дефіцити навчання, викликані звиканнями, можуть виникати опосередковано через посилення процесів пам'яті, залежної від DLS. Відповідно до цієї гіпотези, стимулювання активності CREB в DLS погіршує залежну від гіпокампу просторову пам'ять (90), тоді як інгібування активності CREB в DLS змінює порушення просторової пам'яті, що виробляється морфіном (91).
Роль стресу та тривоги
Додаткове врахування підходу до систем множинної пам'яті до наркоманії - роль стресу. Конвергентні дані свідчать про те, що надійне емоційне збудження полегшує пам'ять, що залежить від DLS, у гризунів і людей [див. (9-12)]. Застосування анксиогенних препаратів підвищує DLS-залежне відповідне навчання у воді плюс-лабіринт (92-97). Це покращення DLS-залежної пам'яті звички також спостерігається після впливу безумовних поведінкових стресорів [наприклад, хронічного обмеження, хвостового шоку, запаху хижаків і т.д.98-101)] і вплив на страх обумовлені подразники [тон, попередньо поєднаний з шоком (102, 103)]. Хоча спочатку продемонстровано у гризунів (92), це посилення пам'яті звички, викликане сильним емоційним збудженням, також було продемонстровано на людях (99, 104-110).
Механізми, що дозволяють стрес / тривога для полегшення пам'яті звички залишаються в основному невідомими; однак, докази вказують на критичну модуляторську роль BLA (93-95, 100). Відповідно до конкурентної взаємодії між системами пам'яті, деякі докази також свідчать про те, що стрес / тривожність може посилити залежну від DLS пам'ять звички, опосередковано погіршуючи функцію гіпокампа (94, 95).
Підвищення пам'яті звички після стресу або тривоги може бути актуальним для розуміння деяких важливих факторів, що призводять до зловживання наркотиками. А саме, стресові події життя або хронічні тривалі періоди стресу / тривоги пов'язані з підвищеною вразливістю до наркоманії та рецидивів у людини (111-117), та подібні спостереження були зроблені на тваринних моделях самостійного застосування препаратів [на розгляд, див. (118)]. Дослідники припустили, що узгоджується з впливом емоційного збудження на декілька систем пам'яті (10), гострий або хронічний стрес може підвищити залежність від наркотиків і рецидив у людини шляхом залучення процесів пам'яті, що залежать від DLS (9, 49, 119). У відповідності з цією пропозицією, стрес у осіб, залежних від кокаїну, пов'язаний зі зниженням активності в крові з киснем-залежним (BOLD) активністю в гіпокампі і підвищеною активністю в дорзальному стриатумі, і ці зміни активності BOLD пов'язані зі стресом, викликаним тягою кокаїну (120).
Нові джерела залежності
Крім наркоманії, недавно була застосована гіпотеза множинних систем пам'яті для розуміння інших виникаючих джерел залежності. Наприклад, зростання ожиріння за останні кілька десятиліть призвело до порівняльного сплеску експериментального інтересу, причому багато дослідників проводили паралелі між наркотичною залежністю та переїданням [див. (121-123)]. Деякі недавні докази свідчать про те, що, як наркоманія, харчова залежність може бути частково пов'язана з підвищеним залученням пам'яті, що залежить від DLS. У щурів споживання їжі, подібне до випивання, полегшує перехід від когнітивного до звичного контролю поведінки (124, 125). Більше того, звична поведінка у тварин, пов'язаних з переливанням, пов'язана з підвищеною активністю DLS і може бути запобігана блокуванням рецепторів АМРА або дофамінових D1 в DLS (125). Дієто-індуковане ожиріння також недавно було пов'язане з використанням пам'яті звички в Y-лабіринті (126).
Іншим виникаючим поведінковим розладом, який паралельно з деякими особливостями наркоманії, є патологічна гра в відеоіграх або залежність від відеоігор [див. (127)]. Подібно до наркоманії, тривале надмірне відтворення відео-ігор пов'язано зі зниженням зв'язування дофамінових рецепторів D2 у спинному стриатумі (128). Відтворення відеоігор також корелює з підвищеною активацією спинного стриатума (129, 130), і більші обсяги дорсальних стриатів передбачають більш високий рівень майстерності відеоігор (131). Люди, які регулярно грають у відеоігри, найімовірніше використовують дорсальну смужку залежної від пам'яті пам'яті у віртуальному лабіринті (132), а попередня підготовка відеоігор призводить до звичного реагування на цілеспрямоване реагування у двоступеневій задачі прийняття рішення (133). Таким чином, як запропоновано для наркотиків, грати у відеоігри можуть підвищити залежність від відеоігор через залучення системи пам'яті, що залежить від DLS.
Нарешті, підхід до систем множинної пам'яті також може бути корисним для розуміння залежності від марихуани. Хоча марихуана може мати більш низький потенціал зловживання, ніж інші заборонені речовини, які класично розглядаються в контексті досліджень наркоманії (наприклад, кокаїн, морфін, героїн тощо), важке використання каннабісу може, однак, сприяти наркотичній залежності та симптомів відміни, як це спостерігається з іншими лікарськими засобами зловживання (134-137). Нещодавно було висловлено припущення, що наркоманія марихуани може бути частково пов'язана з посиленням залучення пам'яті, залежної від DLS (138). Враховуючи, що гострий вплив каннабіноїдів погіршує функцію пам'яті, що залежить від DLS (139, 140), повторне опромінення каннабіноїдів призводить до більшої залежної від DLS звичної реакції в інструментальному навчальному завданні (141). Крім того, важкі користувачі каннабісу проявляють більшу активацію спинного стриатума, порівняно з не-користувачами, при виконанні версії марихуани завдання неявного об'єднання (142), і учасники з історією використання каннабісу частіше використовують дорсальну смужку-залежну пам'ять віртуального лабіринту (65).
Враховуючи успішне застосування підходу до систем пам'яті до нових джерел залежності, доцільно припустити, що багато систем пам'яті також можуть бути залучені до інших поведінкових патологій, пов'язаних із залежністю, таких як компульсивна покупка, залежність від Інтернету та сексуальна залежність. Справді, чи може підхід для систем пам'яті бути корисним для розуміння патологічної азартної гри, також приділяється певна увага (143, 144).
Висновок
Двадцять років експериментальних доказів значною мірою підтвердили Білий1) підхід до множинних систем пам'яті до наркоманії. Докази вказують на те, що гіпокамп опосередковує контекстний контроль самостійного застосування препарату, DLS опосередковує звичний відповідь S-R на підкріплення лікарського засобу, а амігдала опосередковує необхідний пошук наркотиків. Крім того, подальші дослідження призвели до додаткових уявлень щодо множинних систем пам'яті щодо наркоманії, включаючи перехід до пам'яті звичок, конкуренцію між системами пам'яті та роль стресу та тривоги.
Подальші дослідження повинні спробувати інтегрувати підхід системних пам'яті до інших теорій наркоманії, таких як мотиваційні процеси противника (145). Також було б корисно включити в системи пам'яті додаткові особливості наркоманії, такі як лікарська залежність, толерантність і відмінність. Незважаючи на те, що даний огляд переважно зосереджений на областях головного мозку, які спочатку вважалися білими (тобто, гіпокампу, спинного стриатума і мигдалині), слід зазначити, що додаткові області мозку, пов'язані з навчанням і пам'яттю, також критично втягнуті в наркоманію і рецидив , включаючи медіальну префронтальну кору і nucleus accumbens [для огляду, див. (13)]. Нарешті, незважаючи на те, що виходять за рамки цього огляду, слід визнати, що обширні дані свідчать про те, що клітинні і молекулярні зміни в дофамінергічній системі середнього мозку також сприяють залежності (146).
Незважаючи на те, що спогади про звичку можуть бути особливо складними для керування, деякі докази вказують на те, що DLS-залежну пам'ять, після набуття, в деяких випадках може бути припинена (147) або навіть скасовано (148, 149). Таким чином, можливо, що фармакологічні маніпуляції та поведінкові процедури, що призводять до скасування або придушення пам'яті звички в моделях тварин, що навчаються, потенційно можуть бути адаптовані для лікування наркоманії та рецидивів у людей.
Внески автора
Я. Г. і М. П. і сприяли ідеям і написанню цього міні-огляду.
Заява про конфлікт інтересів
Автори заявляють, що дослідження проводилося за відсутності будь-яких комерційних або фінансових відносин, які могли б бути витлумачені як потенційний конфлікт інтересів.
посилання
1. Білий Н.М. Залежні препарати як підсилювачі: множинні часткові дії на системи пам'яті. Наркоманія (1996) 91(7):921–50. doi: 10.1111/j.1360-0443.1996.tb03586.x
2. Білий Н.М., Макдональд Р.Я. Кілька паралельних систем пам'яті в головному мозку щура. Neurobiol Learn Mem (2002) 77(2):125–84. doi:10.1006/nlme.2001.4008
3. Сквайр ЛР. Системи пам'яті мозку: коротка історія та поточна перспектива. Neurobiol Learn Mem (2004) 82(3):171–7. doi:10.1016/j.nlm.2004.06.005
4. White NM, Packard MG, McDonald RJ. Дисоціація систем пам'яті: історія розгортається. Behav Neurosci (2013) 127(6):813–34. doi:10.1037/a0034859
5. Packard MG, Hirsh R, White NM. Диференціальні ефекти ураження язика і хвостатого ядра на двох задачах радіального лабіринту: свідчення множинних систем пам'яті. J Neurosci (1989) 9(5): 1465-72.
6. McDonald RJ, White NM. Потрійна дисоціація систем пам'яті: гіпокампу, мигдалина і спинний стриатум. Behav Neurosci (1993) 107(1):3–22. doi:10.1037/0735-7044.107.1.3
7. Марен С. Невробіологія Павлова страхування. Annu Rev Neurosci (2001) 24(1):897–931. doi:10.1146/annurev.neuro.24.1.897
8. McGaugh JL. Амігдала модулює консолідацію спогадів про емоційно збуджуючі переживання. Annu Rev Neurosci (2004) 27: 1 – 28. doi: 10.1146 / annurev.neuro.27.070203.144157
9. Packard MG. Тривожність, пізнання і звичка: перспективи кількох систем пам'яті. Brain Res (2009) 1293: 121 – 8. doi: 10.1016 / j.brainres.2009.03.029
10. Пакард М.Г., Гудман Дж. Емоційне збудження і множинні системи пам'яті в мозку ссавців. Фронт Бехав Нейроці (2012) 6: 14. doi: 10.3389 / fnbeh.2012.00014
11. Packard MG, Goodman J. Фактори, що впливають на відносне використання декількох систем пам'яті. Гіпокамп (2013) 23(11):1044–52. doi:10.1002/hipo.22178
12. Шваб Л. Стрес і залучення декількох систем пам'яті: інтеграція досліджень тварин і людини. Гіпокамп (2013) 23(11):1035–43. doi:10.1002/hipo.22175
13. Everitt BJ, Robbins TW. Нейронні системи підкріплення для наркоманії: від дій до звичок до примусу. Nat Neurosci (2005) 8(11):1481–9. doi:10.1038/nn1579
14. Фукс Р.А., Еванс К.А., Ледфорд С.К., Паркер М.П. Роль дорсомедіального префронтального кори головного мозку, базолатеральної мигдалини і дорсального гіпокампу в контекстуальному відновленні кокаїну у щурів. Нейропсіхофармакологіі (2005) 30(2):296–309. doi:10.1038/sj.npp.1300579
15. Fuchs RA, Eaddy JL, Su ZI, Bell GH. Взаємодії базолатеральної мигдалини з дорсальним гіпокампом і дорсомедіальною префронтальною корою регулюють відновлення ін'єкційного наркотичного контексту кокаїну у щурів. Eur J Neurosci (2007) 26(2):487–98. doi:10.1111/j.1460-9568.2007.05674.x
16. Kramar CP, Barbano MF, Medina JH. Рецептори дофаміну D1 / D5 в дорсальному гіпокампі необхідні для отримання і експресії пам'яті, пов'язаної з кокаїном. Neurobiol Learn Mem (2014) 116: 172 – 80. doi: 10.1016 / j.nlm.2014.10.004
17. Сапата А, Мінней В.Л., Шиппенберг Т.С. Перехід від цільової спрямованої до звичного кокаїну після тривалого досвіду у щурів. J Neurosci (2010) 30(46):15457–63. doi:10.1523/JNEUROSCI.4072-10.2010
18. Corbit LH, Nie H, Janak PH. Звичні пошуки алкоголю: час і внесок субрегіонів спинного стриатума. Біол Психіатрія (2012) 72(5):389–95. doi:10.1016/j.biopsych.2012.02.024
19. Whitelaw RB, Марку A, Роббінс TW, Everitt BJ. Екситотоксичні ураження базолатеральної мигдалини погіршують придбання кокаїноподібної поведінки за графіком другого порядку армування. Психофармакология (1996) 127(1–2):213–24. doi:10.1007/BF02805996
20. Alderson HL, Robbins TW, Everitt BJ. Вплив екситотоксичних уражень базолатеральной мигдалини на придбання героїнопоглинаючої поведінки у щурів. Психофармакология (2000) 153(1):111–9. doi:10.1007/s002130000527
21. Габріеле А. Див. Зворотна інактивація базолатеральної мигдалини, але не дорсолатерального хвостатого путамена, послаблює консолідацію асоціативного навчання кокаїну в моделі відновлення пошуку наркотиків. Eur J Neurosci (2010) 32(6):1024–9. doi:10.1111/j.1460-9568.2010.07394.x
22. Sciascia JM, Reese RM, Janak PH, Chaudhri N. Алкогольний пошук, викликаний дискретними павловськими сигналами, підсилюється алкогольними контекстами і опосередкований глутаматною сигналізацією в базолатеральной мигдалині. Нейропсіхофармакологіі (2015) 40: 2801 – 12. doi: 10.1038 / npp.2015.130
23. Packard MG, Teather LA. Амігдальна модуляція множинних систем пам'яті: гіппокамп і хвостатий-путамен. Neurobiol Learn Mem (1998) 69(2):163–203. doi:10.1006/nlme.1997.3815
24. Dickinson A, Wood N, Smith JW. Алкоголь шукає щурів: дія або звичка? QJ Exp Psychol B (2002) 55(4):331–48. doi:10.1080/0272499024400016
25. Udo T, Ugalde F, DiPietro N, Eichenbaum HB, Kantak KM. Вплив персистентного самоконтролю кокаїну на амигдал-залежне і дорзальне стриатум-залежне навчання у щурів. Психофармакология (2004) 174(2):237–45. doi:10.1007/s00213-003-1734-1
26. Wood SC, Fay J, Sage JR, Anagnostaras SG. Кондиціонування кокаїну та павлова: аналіз дози-ефекту. Behav Brain Res (2007) 176(2):244–50. doi:10.1016/j.bbr.2006.10.008
27. Wood SC, Anagnostaras SG. Пам'ять і психостимулятори: модуляція обумовленості страхування павлова амфетаміном у мишей C57BL / 6. Психофармакология (2009) 202(1–3):197–206. doi:10.1007/s00213-008-1185-9
28. Iñiguez SD, Charntikov S, Baella SA, Герберт М.С., Bolaños-Guzmán CA, Crawford CA. Експозиція кокаїну після тренування полегшує консолідацію просторової пам'яті у мишей C57BL / 6. Гіпокамп (2012) 22(4):802–13. doi:10.1002/hipo.20941
29. DePoy L, Daut R, Brigman JL, MacPherson K, Crowley N, Gunduz-Cinar O, et al. Хронічний алкоголь виробляє нейроадаптації для основного дорсального стриатального навчання. Proc Natl Acad Sci США (2013) 110(36):14783–8. doi:10.1073/pnas.1308198110
30. Leri F, Nahas E, Хендерсон K, Limebeer CL, Parker LA, White NM. Вплив пост-тренінгового героїну та d-амфетаміну на консолідацію навчання виграшного перебування та кондиціонування страху. J Psychopharmacol (2013) 27(3):292–301. doi:10.1177/0269881112472566
31. Schmitzer-Torbert N, Apostolidis S, Amoa R, O'Rear C, Kaster M, Stowers J, et al. Адміністрування кокаїну після навчання сприяє вивченню звички і вимагає інфралімбічної кори і дорсолатерального стриатуму. Neurobiol Learn Mem (2015) 118: 105 – 12. doi: 10.1016 / j.nlm.2014.11.007
32. Knowlton BJ. Базальні ганглії: формування звички. У: Jaeger D, Jung R, редактори. Енциклопедія обчислювальної неврології. Нью-Йорк: Springer (2014). стор. 1 – 17.
33. Толман Е.К., Річі Б.Ф., Каліш Д. Дослідження в області просторового навчання. IV. Перенесення місця навчання на інші пускові шляхи. J Exp Psychol (1947) 37(1):39–47. doi:10.1037/h0062061
34. Річі Б.Ф., Ешліман Б., Пірс П. Вивчення просторового навчання. VIII. Місце виконання і придбання місця розташування. J Comp Physiol Psychol (1950) 43(2):73–85. doi:10.1037/h0055224
35. Hicks LH. Вплив перетренованості на придбання та зміна місця та відповіді на навчання. Psychol Rep (1964) 15(2):459–62. doi:10.2466/pr0.1964.15.2.459
36. Packard MG, McGaugh JL. Інактивація гіппокампа або хвостатого ядра лідокаїном диференційно впливає на експресію місця і реакції навчання. Neurobiol Learn Mem (1996) 65(1):65–72. doi:10.1006/nlme.1996.0007
37. Yin HH, Knowlton BJ. Внесок стриатичних субрегіонів до місця та відповіді на навчання. Дізнайтеся Mem (2004) 11(4):459–63. doi:10.1101/lm.81004
38. Адамс CD, Дікінсон А. Інструментальна реакція після підсилення девальвації. QJ Exp Psychol (1981) 33B: 109 – 12. doi: 10.1080 / 14640748108400816
39. Адамс CD, Дікінсон А. Дії та звички: варіації в асоціативних уявленнях під час інструментального навчання. У: Спис NE, Miller RR, редактори. Обробка інформації у тварин: Механізми пам'яті. Hillsdale, NJ: Erlbaum (1981). стор. 143 – 65.
40. CD Адамс. Відмінності в чутливості інструментального реагування на посилення девальвації. QJ Exp Psychol (1982) 34B: 77 – 98. doi: 10.1080 / 14640748208400878
41. Дікінсон А, Микола DJ. Нерелевантне стимулююче навчання під час інструментального кондиціонування: роль підсилювача драйву та відносин, що підсилюють реакцію. QJ Exp Psychol (1983) 35B: 249 – 63. doi: 10.1080 / 14640748308400909
42. Дікінсон А, Ніколас DJ, Адамс CD. Вплив інструментальної непередбаченості на схильність до посилення девальвації. QJ Exp Psychol (1983) 35B: 35 – 51. doi: 10.1080 / 14640748308400912
43. Corbit LH, Balleine BW. Роль гіпокампу в інструментальному кондиціонуванні. J Neurosci (2000) 20(11): 4233-9.
44. Yin HH, Ostlund SB, Knowlton BJ, Balleine BW. Роль дорсомедіального стриатума в інструментальному кондиціонуванні. Eur J Neurosci (2005) 22:513–23. doi:10.1111/j.1460-9568.2005.04218.x
45. Yin HH, Knowlton BJ, Balleine BW. Ураження дорсолатерального стриатуму зберігають тривалість результату, але порушують формування звички в інструментальному навчанні. Eur J Neurosci (2004) 19:181–9. doi:10.1111/j.1460-9568.2004.03095.x
46. Quinn JJ, Pittenger C, Lee AS, Пірсон JL, Тейлор JR. Стриат-залежні звички нечутливі як до збільшення, так і до зниження посилюючого значення у мишей. Eur J Neurosci (2013) 37: 1012 – 21. doi: 10.1111 / ejn.12106
47. Yin HH. Від дій до звичок: нейроадаптації, що ведуть до залежності. Алкоголь Res Health (2008) 31(4): 340-4.
48. Бєлін Д., Йонкман С., Дікінсон А., Роббінс Т.В., Еверітт Б.Я. Паралельні та інтерактивні навчальні процеси в базальних гангліях: актуальність для розуміння залежності. Behav Brain Res (2009) 199(1):89–102. doi:10.1016/j.bbr.2008.09.027
49. Schwabe L, Dickinson A, Wolf OT. Стрес, звички та наркоманія: психоневроендокринологічна перспектива. Exp Clin Psychopharmacol (2011) 19(1):53–63. doi:10.1037/a0022212
50. Hogarth L, Balleine BW, Corbit LH, Killcross S. Механізми асоціативного навчання, що лежать в основі переходу від рекреаційного вживання наркотиків до наркоманії. Енн Нью-Йорк Acad Sci (2013) 1282(1):12–24. doi:10.1111/j.1749-6632.2012.06768.x
51. Murray JE, Belin D, Everitt BJ. Подвійна дисоціація дорсомедіального і дорсолатерального стритального контролю над придбанням і працездатністю кокаїну. Нейропсіхофармакологіі (2012) 37(11):2456–66. doi:10.1038/npp.2012.104
52. Clemens KJ, Castino MR, Корніш JL, Goodchild AK, Холмс NM. Поведінкові та нервові субстрати формування звички у щурів внутрішньовенно самостійно вводять нікотин. Нейропсіхофармакологіі (2014) 39: 2584 – 93. doi: 10.1038 / npp.2014.111
53. Corbit LH, Nie H, Janak PH. Звичайне реагування на алкоголь залежить від сигналізації АМРА та рецептора D2 у дорсолатеральному стриатумі. Фронт Бехав Нейроці (2014) 8: 301. doi: 10.3389 / fnbeh.2014.00301
54. Schoenbaum G, Setlow B. Кокаїн робить дії нечутливими до результатів, але не до вимирання: наслідки для зміненої орбітофронтально-мигдаликової функції. Cereb Cortex (2005) 15(8):1162–9. doi:10.1093/cercor/bhh216
55. Нельсон А, Killcross S. Експозиція амфетаміну підвищує формування звички. J Neurosci (2006) 26(14):3805–12. doi:10.1523/JNEUROSCI.4305-05.2006
56. Nordquist RE, Voorn P, De Mooij-ван Malsen JG, Joosten RNJMA, Пеннарц CMA, Vanderschuren LJMJ. Посилене підсилювальне значення і прискорене формування звички після повторного лікування амфетаміном. Eur Neuropsychopharmacol (2007) 17(8):532–40. doi:10.1016/j.euroneuro.2006.12.005
57. LeBlanc KH, Maidment NT, Ostlund SB. Повторне опромінення кокаїну полегшує вираження стимулюючої мотивації і викликає звичний контроль у щурів. PLoS One (2013) 8: e61355. doi: 10.1371 / journal.pone.0061355
58. Nelson AJ, Killcross S. Прискорене формування звички після впливу амфетаміну скасовується D1, але посилюється D2, антагоністами рецепторів. Передні нейроци (2013) 7: 76. doi: 10.3389 / fnins.2013.00076
59. Corbit LH, Chieng BC, Balleine BW. Вплив повторного впливу кокаїну на засвоєння звички та розворот N-ацетилцистеїном. Нейропсіхофармакологіі (2014) 39(8):1893–901. doi:10.1038/npp.2014.37
60. Miles FJ, Everitt BJ, Dickinson A. Оральний кокаїн, який шукають щури: дія або звичка? Behav Neurosci (2003) 117(5):927–38. doi:10.1037/0735-7044.117.5.927
61. Mangieri RA, Cofresí RU, Гонсалес РА. Етанол, який шукають щури Long Evans, не завжди є спрямованою на цілі. PLoS One (2012) 7: e42886. doi: 10.1371 / journal.pone.0042886
62. Sjoerds Z, De Wit S, Ван Ден Брінк W, Роббінс Т.В., Beekman ATF, Penninx BWJH та ін. Поведінкові та нейровизуализирующие докази для надмірного навантаження на засвоєння звички у хворих на алкоголь. Transl Psychiatry (2013) 3(12): e337. doi: 10.1038 / tp.2013.107
63. Packard MG, McGaugh JL. Кінпірол і d-амфетаміновая терапія після тренування підвищує пам'ять про просторову та керовану дискримінацію у водному лабіринті. Психобіологія (1994) 22(1): 54-60.
64. Matthews DB, Ilgen M, White AM, Best PJ. Управління гострим етанолом погіршує просторову продуктивність, одночасно полегшуючи непросторову продуктивність у щурів. Neurobiol Learn Mem (1999) 72(3):169–79. doi:10.1006/nlme.1998.3900
65. Bohbot VD, Balso D, Conrad K, Konishi K, Leyton M. Коадативні стратегії, що залежать від ядра, пов'язані з підвищеним використанням наркотичних засобів. Гіпокамп (2013) 23(11):973–84. doi:10.1002/hipo.22187
66. Poldrack RA, Packard MG. Конкуренція між кількома системами пам'яті: збіжні докази з досліджень тварин і мозку людини. Neuropsychologia (2003) 41(3):245–51. doi:10.1016/S0028-3932(02)00157-4
67. Matthews DB, Кращий PJ. Ураження фімбрії / форнікса полегшують вивчення завдання непросторового реагування. Psychon Bull Rev (1995) 2(1):113–6. doi:10.3758/BF03214415
68. Шредер JP, Wingard JC, Packard MG. Пост-тренувальна оборотна інактивація гіпокампу виявляє інтерференцію між системами пам'яті. Гіпокамп (2002) 12(2):280–4. doi:10.1002/hipo.10024
69. Matthews DB, Simson PE, Best PJ. Гострий етанол погіршує просторову пам'ять, але не запам'ятовує стимул / реакцію у щурів. Алкоголь Clin Exp Res (1995) 19(4):902–9. doi:10.1111/j.1530-0277.1995.tb00965.x
70. Білий AM, Elek TM, Beltz TL, Best PJ. Просторова продуктивність є більш чутливою до етанолу, ніж непросторову продуктивність, незалежно від близькості кия. Алкоголь Clin Exp Res (1998) 22(9):2102–7. doi:10.1111/j.1530-0277.1998.tb05922.x
71. Matthews DB, Morrow AL, Tokunaga S, McDaniel JR. Застосування гострого етанолу та гострий прийом аллопрегнанолону погіршують просторову пам'ять у водному завданні Морріса. Алкоголь Clin Exp Res (2002) 26(11):1747–51. doi:10.1111/j.1530-0277.2002.tb02479.x
72. Berry RB, Matthews DB. Застосування гострого етанолу вибірково погіршує просторову пам'ять у мишей C57BL / 6J. Алкоголь (2004) 32(1):9–18. doi:10.1016/j.alcohol.2003.09.005
73. Silvers JM, Tokunaga S, Berry RB, White AM, Matthews DB. Порушення в просторовому навчанні та пам'яті: етанол, аллопрегнанолон і гіпокамп. Brain Res Rev (2003) 43(3):275–84. doi:10.1016/j.brainresrev.2003.09.002
74. Баданіч К.А., Беккер Х.С. Ефекти хронічного переривчастого опромінення етанолом на орбітофронтальні і медіальні префронтальні залежності від поведінки у мишей. Behav Neurosci (2011) 125(6):879–91. doi:10.1037/a0025922
75. Coleman LG Jr, He J, Лі J, Styner M, Crews FT. Підліткове пиття алкоголю змінює експресію гена нейромедіатора мозку дорослих, поведінку, регіональні обсяги мозку і нейрохімію у мишей. Алкоголь Clin Exp Res (2011) 35(4):671–88. doi:10.1111/j.1530-0277.2010.01385.x
76. Кузьмін А., Лільіквіст С, Мейс Дж, Чефер V, Шіппенберг Т., Балаккін Г. Повторні помірні дози етанолу погіршують когнітивні функції у щурів Вістар. Addict Biol (2012) 17(1):132–40. doi:10.1111/j.1369-1600.2010.00224.x
77. Coleman LG, Лю W, Oguz I, Styner M, Crews FT. Підліткове лікування етанолу впливає на регіональні обсяги дорослого головного мозку, кортикальний білок позаклітинного матриксу і гнучкість поведінки. Pharmacol Biochem Behav (2014) 116: 142 – 51. doi: 10.1016 / j.pbb.2013.11.021
78. Matthews DB, Silvers JR. Застосування гострого етанолу як засобу для дослідження декількох систем пам'яті. Neurobiol Learn Mem (2004) 82(3):299–308. doi:10.1016/j.nlm.2004.06.007
79. Брінінг HW, Morford LL, Inman-Wood SL, Fukumura M, Vorhees CV. Навчання, обумовлене 3, 4-метилендіоксиметамфетамін (екстазі) і порушення пам'яті залежать від віку опромінення під час раннього розвитку. J Neurosci (2001) 21(9): 3228-35.
80. Williams MT, Morford LL, Wood SL, Wallace TL, Fukumura M, Broening HW, et al. Розробка d-метамфетамінового лікування селективно індукує просторові навігаційні порушення в довідковій пам'яті в водному лабіринті Морріса, зберігаючи робочу пам'ять. Синапс (2003) 48(3):138–48. doi:10.1002/syn.10159
81. Vorhees CV, Reed TM, Skelton MR, Williams MT. Вплив 3, 4-метилендіоксиметамфетамін (MDMA) на післяпологові дні Int J Dev Neurosci (2004) 22(5):247–59. doi:10.1016/j.ijdevneu.2004.06.003
82. Коен М.А., Скелтон М.Р., Шефер Т.Л., Гудельський Г.А., Vorhees CV, Williams MT. Навчання та пам'ять після неонатального впливу 3, 4-метилендіоксиметамфетамін (екстазі) у щурів: взаємодія з опроміненням у дорослому віці. Синапс (2005) 57(3):148–59. doi:10.1002/syn.20166
83. Skelton MR, Williams MT, Vorhees CV. Лікування МДМА з P11-20 перешкоджає вивченню просторового навчання та інтеграції шляхів у підлітків-щурів, але лише у просторовому навчанні у старих щурів. Психофармакология (2006) 189(3):307–18. doi:10.1007/s00213-006-0563-4
84. Ma MX, Chen YM, He J, Zeng T, Wang JH. Вплив морфіну та його виведення на Y-лабіринт пам'яті просторового розпізнавання у мишей. Неврологія (2007) 147(4):1059–65. doi:10.1016/j.neuroscience.2007.05.020
85. Белчер А.М., Фейнштейн Е.М., О'Делл С.Ю., Маршалл Дж. Метамфетамін впливає на пам'ять розпізнавання: порівняння ескалації і одноденних режимів дозування. Нейропсіхофармакологіі (2008) 33(6):1453–63. doi:10.1038/sj.npp.1301510
86. Tramullas M, Martínez-Cué C, Hurlé MA. Хронічне введення героїну мишам створює підвищену регуляцію білків, пов'язаних з апоптозом головного мозку, і погіршує просторове навчання і пам'ять. Нейрофармакологія (2008) 54(4):640–52. doi:10.1016/j.neuropharm.2007.11.018
87. North A, Swant J, Salvatore MF, Gamble-George J, Prins P, Butler B, et al. Хронічна експозиція метамфетаміну викликає затримку, тривалий дефіцит пам'яті. Синапс (2013) 67(5):245–57. doi:10.1002/syn.21635
88. Fole A, Martin M, Morales L, Del Olmo N. Вплив хронічного лікування кокаїну під час підліткового віку у щурів Lewis та Fischer-344: нове порушення розпізнавання розташування та зміни синаптичної пластичності у дорослому віці. Neurobiol Learn Mem (2015) 123: 179 – 86. doi: 10.1016 / j.nlm.2015.06.001
89. Zhou M, Luo P, Lu Y, Li CJ, Wang DS, Lu Q, et al. Дисбаланс експресії HCN1 і HCN2 в області гіпокампу CA1 погіршує просторове навчання і пам'ять у щурів з хронічною експозицією морфіну. Prog Neuropsychopharmacol Biol Psychiatry (2015) 56: 207 – 14. doi: 10.1016 / j.pnpbp.2014.09.010
90. Kathirvelu B, Коломбо PJ. Вплив lentivirus-опосередкованої експресії CREB у дорсолатеральній стриатумі: покращення пам'яті та свідчення конкурентних та кооперативних взаємодій з гіпокампом. Гіпокамп (2013) 23(11):1066–74. doi:10.1002/hipo.22188
91. Baudonnat M, Guillou JL, Husson M, Vandesquille M, Corio M, Decorte L та ін. Порушуючий ефект від індукованої лікарським засобом винагороди на просторове, але не кий-кероване навчання: наслідки шляху стриктурного протеїнкінази А / цАМФ-зв'язуючий білок. J Neurosci (2011) 31:16517–28. doi:10.1523/JNEUROSCI.1787-11.2011
92. Packard MG, Wingard JC. Амигдала і «емоційна» модуляція відносного використання декількох систем пам'яті. Neurobiol Learn Mem (2004) 82(3):243–52. doi:10.1016/j.nlm.2004.06.008
93. Elliott AE, Packard MG. Внутрішньоамігдальна інфузія анксіогенного препарату до вилучення змінює щурів на використання пам'яті звички. Neurobiol Learn Mem (2008) 90(4):616–23. doi:10.1016/j.nlm.2008.06.012
94. Wingard JC, Packard MG. Амігдала та емоційна модуляція конкуренції між когнітивною та звичною пам'яттю. Behav Brain Res (2008) 193(1):126–31. doi:10.1016/j.bbr.2008.05.002
95. Packard MG, Gabriele A. Ін'єкції периферичного анксіогенного препарату диференційовано впливають на когнітивну і навичку пам'яті: роль базалотеральной мигдалини. Неврологія (2009) 164(2):457–62. doi:10.1016/j.neuroscience.2009.07.054
96. Leong KC, Goodman J, Packard MG. Буспірон блокує посилюючий ефект анксиогенного препарату RS 79948-197 на консолідацію пам'яті звички. Behav Brain Res (2012) 234(2):299–302. doi:10.1016/j.bbr.2012.07.009
97. Goodman J, Leong KC, Packard MG. Глюкокортикоидное посилення дорсолатеральної смугасто-залежної пам'яті звички вимагає одночасної норадренергічної активності. Неврологія (2015) 311: 1 – 8. doi: 10.1016 / j.neuroscience.2015.10.014
98. Kim JJ, Lee HJ, Han JS, Packard MG. Амігдала є критично важливою для стрес-індукованої модуляції довгострокового потенціювання та навчання гіпокампу. J Neurosci (2001) 21(14): 5222-8.
99. Schwabe L, Dalm S, Schachinger H, Oitzl MS. Хронічний стрес модулює використання стратегій просторового та стимулюючого навчання у мишей і людини. Neurobiol Learn Mem (2008) 90(3):495–503. doi:10.1016/j.nlm.2008.07.015
100. Leong KC, Packard MG. Вплив запаху хижака впливає на відносне використання декількох систем пам'яті: роль базалотеральної мигдалини. Neurobiol Learn Mem (2014) 109: 56 – 61. doi: 10.1016 / j.nlm.2013.11.015
101. Тейлор С.Б., Англін Дж.М., Паод ПР, Ріггерт А.Г., Олив О.Ф., Конрад КД. Хронічний стрес може полегшити прийом нейроциклів, пов'язаних з звичками та наркоманіями, шляхом реструктуризації нервової смуги. Неврологія (2014) 280: 231 – 42. doi: 10.1016 / j.neuroscience.2014.09.029
102. Leong KC, Goodman J, Packard MG. Пост-тренінгове повторне опромінення страждаючих обумовлених стимулів посилює консолідацію пам'яті і упереджує щурів до використання дорсолатерального стриатум-залежного навчання. Behav Brain Res (2015) 291: 195 – 200. doi: 10.1016 / j.bbr.2015.05.022
103. Goode TE, Leong KC, Goodman J, Maren S, Packard MG. Посилення стриатум-залежної пам'яті шляхом обумовленого страху опосередковується бета-адренергічними рецепторами в базолатеральной мигдалині. Нейробіологія стресу (в пресі). doi: 10.1016 / j.ynstr.2016.02.004
104. Schwabe L, Oitzl MS, Philippsen C, Richter S, Bohringer A, Wippich W, et al. Стрес модулює використання просторових проти стимулів-відповідей стратегій навчання у людей. Дізнайтеся Mem (2007) 14(1–2):109–16. doi:10.1101/lm.435807
105. Schwabe L, Schachinger H, Kloet ER, Oitzl MS. Кортикостероїди діють як перемикач між системами пам'яті. J Cogn Neurosci (2010) 22(7):1362–72. doi:10.1162/jocn.2009.21278
106. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Паралельна глюкокортикоїдна і норадренергічна активність зміщує інструментальну поведінку від цільового до звичного контролю. J Neurosci (2010) 30(24):8190–6. doi:10.1523/JNEUROSCI.0734-10.2010
107. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Блокада мінералокортикоїдних рецепторів запобігає індуковану стресом модуляцію декількох систем пам'яті в мозку людини. Біол Психіатрія (2013) 74(11):801–8. doi:10.1016/j.biopsych.2013.06.001
108. Schwabe L, Wolf OT. Стрес викликає поведінку людини. J Neurosci (2009) 29(22):7191–8. doi:10.1523/JNEUROSCI.0979-09.2009
109. Schwabe L, Wolf OT. Соціально оцінений холодний пресовий стрес після інструментального навчання сприяє навичкам над цілеспрямованими діями. Психоневроендокринологія (2010) 35(7):977–86. doi:10.1016/j.psyneuen.2009.12.010
110. Guenzel FM, Wolf OT, Schwabe L. Глюкокортикоїди підвищують формування пам'яті стимулу-відповіді у людей. Психоневроендокринологія (2014) 45: 21 – 30. doi: 10.1016 / j.psyneuen.2014.02.015
111. Higgins RL, Marlatt GA. Страх перед міжособистісною оцінкою як детермінант споживання алкоголю у чоловіків, які п'ють. J Abnorm Psychol (1975) 84(6):644–51. doi:10.1037/0021-843X.84.6.644
112. Марлатт Г.А., Гордон Дж. Детермінанти рецидиву: наслідки для підтримки зміни поведінки. У: Davidson PO, Davidson SM, редактори. Поведінкова медицина: зміна способу життя. Нью-Йорк: Brunne / Mazel (1980). стор. 410 – 52.
113. Newcomb MD, Bentler PM. Вплив підліткового вживання наркотиків та соціальна підтримка на проблеми молоді: довготривале дослідження. J Abnorm Psychol (1988) 97:64–75. doi:10.1037/0021-843X.97.1.64
114. Wallace BC. Психологічні та екологічні детермінанти рецидиву у тютюнопаління. J Забороняти підпорядкування (1989) 6(2):95–106. doi:10.1016/0740-5472(89)90047-0
115. Kaplan HB, Johnson RJ. Взаємовідносини між обставинами, що стосуються початкового незаконного вживання наркотиків, та ескалація вживання наркотиків: пом'якшуючий вплив гендерного та раннього підлітків. У: Glantz M, Pickens R, редактори. Вразливість до зловживання наркотиками. Вашингтон, округ Колумбія: Американська психологічна асоціація (1992). стор. 200 – 358.
116. Харрісон П.А., Фулкерсон Ю.А., Beebe TJ. Багаторазове вживання наркотичних речовин серед потерпілих від фізичного та сексуального насилля. Нехтування зловживанням дітей (1997) 21:529–39. doi:10.1016/S0145-2134(97)00013-6
117. Chilcoat HD, Breslau N. Посттравматичний стресовий розлад і лікарські розлади: тестування причинних шляхів. Arch Gen Psychiatry (1998) 55(10):913–7. doi:10.1001/archpsyc.55.10.913
118. Пьяцца П.В., Ле Моаль М. Роль стресу в саморегулюванні препарату. Trends Pharmacol Sci (1998) 19(2):67–74. doi:10.1016/S0165-6147(97)01115-2
119. Goodman J, Leong KC, Packard MG. Емоційна модуляція множинних систем пам'яті: наслідки для нейробіології посттравматичного стресового розладу. Рев. Нейроші (2012) 23(5–6):627–43. doi:10.1515/revneuro-2012-0049
120. Sinha R, Lacadie C, Skudlarski P, Fulbright RK, Rounsaville BJ, Kosten TR, et al. Нейронна активність, пов'язана зі стресом, викликаним стресом: функціональне дослідження магнітно-резонансної томографії. Психофармакология (2005) 183(2):171–80. doi:10.1007/s00213-005-0147-8
121. Авена Н.М., Рада П, Хобель Б.Г. Докази залежності цукру: поведінкові та нейрохімічні ефекти переривчастого, надмірного споживання цукру. Neurosci Biobehav Rev (2008) 32(1):20–39. doi:10.1016/j.neubiorev.2007.04.019
122. Gearhardt AN, Corbin WR, Brownell KD. Харчова залежність: вивчення діагностичних критеріїв залежності. J Addict Med (2009) 3(1):1–7. doi:10.1097/ADM.0b013e318193c993
123. Сміт Д.Г., Роббінс Т.В. Нейробіологічні основи ожиріння та переїдання: обґрунтування прийняття моделі харчової залежності. Біол Психіатрія (2013) 73(9):804–10. doi:10.1016/j.biopsych.2012.08.026
124. де Йонг JW, Meijboom KE, Vanderschuren LJ, Adan RA. Низький контроль над приємним прийомом їжі у щурів пов'язаний із звичною поведінкою і вразливістю до рецидивів: індивідуальні відмінності. PLoS One (2013) 8(9): e74645. doi: 10.1371 / journal.pone.0074645
125. Furlong TM, Jayaweera HK, Balleine BW, Corbit LH. Перевантажувальне споживання смачної їжі прискорює звичний контроль поведінки і залежить від активації дорсолатерального стриатума. J Neurosci (2014) 34(14):5012–22. doi:10.1523/JNEUROSCI.3707-13.2014
126. Харгрейв С.Л., Девідсон Т.Л., Чженг В., Кінціг К.П. Західні дієти індукують витікання гематоенцефалічного бар'єру і змінюють просторові стратегії у щурів. Behav Neurosci (2016) 130(1):123–35. doi:10.1037/bne0000110
127. Сміт KL, Hummer TA, Hulvershorn LA. Патологічні відеоігри та її зв'язок з порушеннями вживання речовин. Curr Addict Rep (2015) 2(4):302–9. doi:10.1007/s40429-015-0075-6
128. Вайнштейн А.М. Залежність від комп'ютерних і відеоігор - порівняння між користувачами гри і користувачами, що не є іграми. Am J зловживання алкоголем (2010) 36(5):268–76. doi:10.3109/00952990.2010.491879
129. Kätsyri J, Харі R, Ravaja N, Nummenmaa L. Суперник має значення: підвищений fMRI нагорода відповіді на перемогу проти людини проти комп'ютерного опонента під час інтерактивного відтворення відеоігор. Cereb Cortex (2013) 23(12):2829–39. doi:10.1093/cercor/bhs259
130. Kätsyri J, Hari R, Ravaja N, Nummenmaa L. Просто спостерігати за грою не достатньо: стриативуючу відповідь на успіх і невдачі у відеоіграх під час активної та чужої гри. Передній Hum Neurosci (2013) 7: 278. doi: 10.3389 / fnhum.2013.00278
131. Erickson KI, Boot WR, Basak C, Neider MB, Prakash RS, Voss MW, et al. Стріатальний обсяг передбачає рівень набуття навичок відеоігор. Cereb Cortex (2010) 20: 2522 – 30. doi: 10.1093 / cercor / bhp293
132. West GL, Drisdelle BL, Konishi K, Джексон J, Jolicoeur P, Bohbot VD. Звична гра відеоігор пов'язана з навігаційними стратегіями, залежними від хвостатого ядра. Proc R Soc (2015) 282(1808). doi: 10.1098 / rspb.2014.2952
133. Лю С, DJ Schad, Kuschpel MS, Рапп М., Хайнц А. Музика та відеоігри під час перерв: вплив звичного і цілеспрямованого прийняття рішень. Доповідь на 45th щорічному засіданні Товариства неврології. Чикаго, штат Іллінойс: Товариство неврології (2015).
134. де Фонсека Ф.Р., Каррера МРА, Наварро М, Кооб Г.Ф., Вайсс Ф. Активація кортикотропін-рилізинг-фактора в лімбічній системі під час виведення канабіноїдів. наука (1997) 276(5321):2050–4. doi:10.1126/science.276.5321.2050
135. Cornelius JR, Chung T, Martin C, Wood DS, Clark DB. Зняття канабісу є поширеним серед підлітків, які шукають лікування, з залежністю від канабісу та великою депресією, і пов'язане з швидким рецидивом до залежності. Addict Behav (2008) 33(11):1500–5. doi:10.1016/j.addbeh.2008.02.001
136. Greene MC, Kelly JF. Поширеність виведення канабісу та його вплив на відповідь та результати лікування підлітків: 12-місячне проспективне дослідження. J Addict Med (2014) 8: 359 – 67. doi: 10.1097 / ADM.0000000000000064
137. Wagner FA, Anthony JC. Від першого вживання наркотиків до наркотичної залежності; періоди розвитку ризику залежності від марихуани, кокаїну та алкоголю. Нейропсіхофармакологіі (2002) 26:479–88. doi:10.1016/S0893-133X(01)00367-0
138. Goodman J, Packard MG. Вплив канабіноїдів на процеси навчання і пам'яті спинного стриатума. Neurobiol Learn Mem (2015) 125: 1 – 14. doi: 10.1016 / j.nlm.2015.06.008
139. Rueda-Orozco PE, Сорія-Гомез Е, Монтес-Родрігес CJ, Мартінес-Варгас М., Галиція О, Наварро Л, та ін. Потенційна функція ендоканнабіноїдів при виборі навігаційної стратегії щурами. Психофармакология (2008) 198(4):565–76. doi:10.1007/s00213-007-0911-z
140. Goodman J, Packard MG. Периферичні та внутрішньо-дорсолатеральні ін'єкції стриатума агоністом каннабіноїдних рецепторів WIN 55,212-2 погіршують консолідацію пам'яті стимулу-відповіді. Неврологія (2014) 274: 128 – 37. doi: 10.1016 / j.neuroscience.2014.05.007
141. Nazzaro C, Greco B, Cerovic M, Baxter P, Rubino T, Trusel M, et al. Модуляція каналу СК рятує стриатичну пластичність і контролює звичку в тональності канабіноїдів. Nat Neurosci (2012) 15: 284 – 93. doi: 10.1038 / nn.3022
142. Ames SL, Grenard JL, Stacy AW, Xiao L, He Q, Wong SW, et al. Функціональна візуалізація неявних асоціацій марихуани під час виконання на неявному тесті асоціації (IAT). Behav Brain Res (2013) 256: 494 – 502. doi: 10.1016 / j.bbr.2013.09.013
143. Redish AD, Jensen S, Johnson A. Уніфіковані рамки для наркоманії: уразливості в процесі прийняття рішень. Behav Brain Sci (2008) 31(04):415–37. doi:10.1017/S0140525X0800472X
144. Brevers D, Bechara A, Клереманс A, Noël X. Азартна гра Айова (IGT): двадцять років після розладу азартних ігор і IGT. Передній психол (2013) 4: 665. doi: 10.3389 / fpsyg.2013.00665
145. Koob GF, Le Moal M. Нейробіологічні механізми мотиваційних процесів противника в залежності. Філос Транс Р Соцік Б (2008) 363(1507):3113–23. doi:10.1098/rstb.2008.0094
146. Hyman SE, Malenka RC, Nestler EJ. Нейронні механізми наркоманії: роль нагородженого навчання і пам'яті. Annu Rev Neurosci (2006) 29: 565 – 98. doi: 10.1146 / annurev.neuro.29.051605.113009
147. Goodman J, Packard M. Система пам'яті, задіяна під час придбання, визначає ефективність різних протоколів вимирання. Фронт Бехав Нейроці (2015) 9: 314. doi: 10.3389 / fnbeh.2015.00314
148. Паленсія CA, Ragozzino ME. Вклад NMDA-рецепторів у дорсолатеральний стриатум до егоцентричного навчання. Behav Neurosci (2005) 119(4):953–60. doi:10.1037/0735-7044.119.4.953
149. Rueda-Orozco PE, Монтес-Родрігес CJ, Сорія-Гомез Е, Мендес-Діаз М., Prospéro-García O. Нейрофармакологія (2008) 55(1):55–62. doi:10.1016/j.neuropharm.2008.04.013
Ключові слова: пам'ять, наркоманія, гіпокамп, стриатум, мигдалина, стрес, тривога
Цитування: Системи пам'яті Goodman J і Packard MG (2016) і пристрасний мозок. Фронт. Психіатрія 7: 24. doi: 10.3389 / fpsyt.2016.00024
Отримано: 01 грудень 2015; Прийнято: 11 лютого 2016;
Опубліковано: 25 лютого 2016
Редаговано:
Девід Вінсент, Національний центр наукових досліджень (CNRS), Франція
Відгук:
Жак Мішо, Університет Бордо 1, Франція
Роберто Чикосіоппо, Університет Камерино, Італія
Авторські права: © 2016 Гудман і Паккард. Це стаття з відкритим доступом, яка поширюється за умовами Ліцензія на використання Creative Commons (CC BY). Використання, розповсюдження або відтворення на інших форумах дозволяється за умови зарахування оригінального автора (авторів) або ліцензіара, а також цитування оригінальної публікації в цьому журналі відповідно до прийнятої академічної практики. Не дозволяється використання, розповсюдження або відтворення, які не відповідають цим умовам.
* Переписка: Марк Паккард, [захищено електронною поштою]