KOMEN: Ulasan oleh ketua Institut Nasional Penyalahgunaan Dadah, Nora Volkow, dan pasukannya. Ulasan ini menyenaraikan 3 disfungsi neurobiologi utama yang terlibat dalam semua ketagihan. Secara ringkasnya: a) Desensitization: tindak balas keseronokan yang disebabkan oleh penurunan isyarat dopamin; b) Sensitisasi: tindak balas dopamin yang dipertingkatkan kepada isyarat ketagihan, pencetus atau tekanan; dan c) Hypofrontality: litar kawalan diri yang lemah kerana penurunan jumlah dan fungsi korteks frontal. Perubahan otak yang sama ini dijelaskan oleh American Society for Addiction Medicine (ASAM) di dalamnya takrif baru ketagihan dikeluarkan pada bulan Ogos, 2011.
Volkow ND, Wang GJ, Fowler JS, Tomasi D, Telang F, Baler R. Bioessays. 2010 Sep; 32 (9): 748-55.
Institut Kebangsaan Penyalahgunaan Dadah, NIH, Bethesda, MD 20892, Amerika Syarikat.
Abstrak
Berdasarkan penemuan pencitraan otak, kami membentangkan model mengikut ketagihan yang muncul sebagai ketidakseimbangan dalam pemprosesan maklumat dan integrasi di antara pelbagai litar dan fungsi otak.
Disfungsi ini mencerminkan:
(a) mengurangkan kepekaan litar ganjaran,
(b) sensitiviti litar memori yang dipertingkatkan untuk dijangkakan jangkaan kepada ubat dan isyarat dadah, kereaktifan stres, dan perasaan negatif,
(c) dan litar kawalan yang lemah.
Walaupun percubaan awal dengan ubat penyalahgunaan adalah sebahagian besarnya tingkah laku sukarela, penggunaan dadah yang berterusan akhirnya dapat menjejaskan litar neuron di otak yang terlibat dalam kehendak bebas, menjadikan penggunaan dadah menjadi tingkah laku kompulsif automatik. Keupayaan ubat-ubatan ketagihan untuk menggabungkan isyarat neurotransmitter antara neuron (termasuk dopamin, glutamat, dan GABA) mengubah fungsi litar neuron yang berbeza, yang mula terputus pada pelbagai tahap trajektori ketagihan. Apabila terdedah kepada dadah, isyarat dadah atau tekanan ini menyebabkan hiperaktivasi yang tidak terkawal dari litar motivasi / memandu yang mengakibatkan pengambilan dadah kompulsif yang menyerupai ketagihan.
Pengenalan
Penyelidikan neurosains tahun 25 yang terakhir telah menghasilkan bukti bahawa ketagihan adalah penyakit otak, memberikan argumen yang kuat untuk menegakkan piawai penjagaan perubatan yang sama kepada individu yang kecanduan sebagai yang biasa dengan penyakit lain dengan kesan umum yang besar, seperti diabetes. Sesungguhnya, penyelidikan mengenai ketagihan telah mula membongkar urutan peristiwa dan sekuel lama yang boleh berlaku akibat penyalahgunaan bahan penyebab yang berterusan. Kajian-kajian ini menunjukkan betapa berulang penggunaan dadah dapat mensasarkan molekul utama dan litar otak, dan akhirnya mengganggu proses pesanan yang lebih tinggi yang mendasari emosi, kognisi dan tingkah laku. Kami telah mempelajari bahawa ketagihan dicirikan oleh kitaran berkembang pesat disfungsi otak. Kerosakan biasanya bermula di kawasan evolusi yang lebih primitif otak yang memproses ganjaran, dan kemudian bergerak ke kawasan lain yang bertanggungjawab untuk fungsi kognitif yang lebih kompleks. Oleh itu, sebagai tambahan kepada ganjaran, individu kecanduan boleh mengalami gangguan yang teruk dalam pembelajaran (ingatan, penyesuaian, kebiasaan), fungsi eksekutif (perencatan impuls, membuat keputusan, menanggung penyerahan), kesedaran kognitif (interpersonal) fungsi.
Melukis sebahagian besarnya daripada hasil kajian pencitraan otak yang menggunakan tomografi pelepasan positron (PET), kami memperkenalkan litar otak utama yang dipengaruhi oleh penyalahgunaan dadah yang kronik dan kemudian membentangkan model yang koheren, menurut ketagihan yang muncul sebagai hasil bersih pemprosesan maklumat yang tidak seimbang di dalam dan di antara litar ini. Pemahaman menyeluruh tentang proses otak penyesuaian (neuroplastik) yang beransur-ansur ini, dan faktor kelemahan biologi dan alam sekitar yang mempengaruhi kemungkinan mereka, adalah penting untuk pembangunan pendekatan pencegahan dan rawatan yang lebih berkesan untuk memerangi ketagihan.
Tinggi, tetapi ringkas, letupan dopamin diperlukan untuk ketagihan
Ketagihan adalah, pertama dan paling utama, penyakit sistem ganjaran otak. Sistem ini menggunakan dopamin neurotransmitter (DA) sebagai mata wang utamanya untuk menyampaikan maklumat. Otak DA memainkan peranan penting dalam pemprosesan maklumat mengenai ketokohan [1, 2], yang merupakan keupayaan untuk mengawalselia atau mempengaruhi ganjaran [3, 4], harapan jangkaan [5], motivasi, emosi, dan perasaan senang. Pelepasan sementara DA di striatum ventral otak adalah perlu, walaupun tidak mencukupi, dalam proses kompleks yang menimbulkan sensasi ganjaran: peningkatan DA nampaknya berkaitan secara positif dengan intensitas "tinggi" yang dialami oleh subjek. Respons yang dikondisikan hanya muncul apabila DA dilepaskan berulang kali kerana lonjakan tajam, sementara, sebagai tindak balas terhadap ubat-ubatan atau petunjuk yang berkaitan dengan ubat.
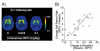
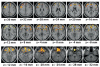
Menariknya, secara langsung atau tidak langsung, semua ubat-ubatan ketagihan berfungsi dengan mencetuskan peningkatan yang terlalu tinggi tetapi sementara dalam DA ekstrelelular dalam sistem ganjaran (limbik) utama [6, 7], khususnya, dalam nukleus accumbens (Nac) yang terletak di striatum ventral. Lonjakan DA seperti menyerupai, dan dalam beberapa keadaan melampaui, peningkatan fisiologi yang dicetuskan oleh rangsangan semula jadi yang menyenangkan (biasanya dirujuk sebagai penguat semula atau ganjaran semula jadi). Seperti yang kita jangkakan, kajian pencitraan otak manusia menggunakan tomography emission positron (PET), dengan jelas menunjukkan bahawa DA meningkat disebabkan oleh pelbagai jenis ubat (contohnya.. perangsang (Rajah 1A), [8, 9], nikotin [10], dan alkohol [11]) dalam striatum ventral, dikaitkan dengan pengalaman subjektif euforia (atau tinggi) semasa mabuk [12, 13, 14]. Memandangkan kajian PET boleh dilakukan dalam subjek manusia yang sihat, ia juga mungkin untuk merancang hubungan antara laporan subjektif kesan dadah dan perubahan relatif dalam tahap DA. Kebanyakan kajian melaporkan bahawa mereka yang memaparkan DA yang paling besar meningkatkan pendedahan dadah berikut [amphetamine, nikotin, alkohol, methylphenidate (MPH)] juga melaporkan yang paling sengit atau euforia (Rajah 1B).
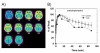
Kajian haiwan dan manusia telah menunjukkan bahawa kelajuan yang mana ubat memasuki, bertindak ke atas, dan meninggalkan otak (iaitu profil farmakokinetik) memainkan peranan penting dalam menentukan kesan pengukuhannya. Sesungguhnya, setiap ubat penyalahgunaan yang farmakokinetik otak telah diukur dengan PET (kokain, MPH, methamphetamine, dan nikotin) mempamerkan profil yang sama apabila pentadbiran intravena, iaitu, tahap puncak dalam otak manusia dicapai dalam min 10 (Rajah 2A) dan pengambilan cepat ini dikaitkan dengan "tinggi" (Rajah 2B). Berdasarkan persatuan ini, ia memastikan bahawa ubat ketagihan yang memasuki otak secara perlahan mungkin merupakan cara yang berkesan untuk meminimumkan potensi pengukuhannya, oleh itu tanggungjawab penyalahgunaannya. Kami merancang eksperimen untuk menguji dengan tepat hipotesis ini dengan MPH dadah perangsang, yang, seperti kokain, meningkatkan DA dengan memperlambat pengangkutannya kembali ke neuron presinaptik (iaitu dengan menghalang pengangkut DA), dengan itu membesar isyarat DA. Sesungguhnya, kita mendapati bahawa, walaupun pentadbiran intravena MPH sering euphhorigenik, secara lisan ditadbir MPH, yang juga meningkatkan DA di striatum [15], tetapi dengan 6- hingga 12-kali ganda farmakokinetik yang lebih perlahan, tidak biasanya dilihat sebagai mengukuhkan [16, 17]. Oleh itu, kegagalan oral MPH - atau amphetamine [18] untuk perkara itu - untuk mendorong tinggi kemungkinan cerminan pengambilan perlahan mereka ke dalam otak [19]. Oleh itu, adalah munasabah untuk mencadangkan kewujudan hubungan rapat antara kadar di mana ubat penyalahgunaan memasuki otak, yang menentukan kelajuan di mana DA meningkat di stratum ventral, dan kesan pengukuhannya [20, 21, 22]. Dalam erti kata lain, untuk ubat untuk menguatkan kesan menguatkan ia telah menaikkan DA mendadak. Kenapa harus demikian?
Berdasarkan magnitud dan tempoh penembakan neuron, isyarat DA boleh mengambil salah satu daripada dua bentuk asas: phasic atau tonik. Isyarat Phasic dicirikan oleh amplitud tinggi dan tembakan pecah pendek, manakala isyarat tonik biasanya amplitudo rendah dan kursus waktu yang lebih berlarutan atau berterusan. Perbezaan ini adalah penting kerana ternyata bahawa isyarat DA phasic diperlukan untuk ubat penyalahgunaan untuk mendorong "tanggapan yang dikondisikan," yang merupakan salah satu penyesuaian awal yang mengikuti pendedahan untuk memperkuat rangsangan (termasuk ubat). Salah satu aspek yang membezakan yang menghubungkan isyarat fasa dengan pengkondisian adalah penglibatan D2R dan glutamat n-methyl-dreseptor asid aspal (NMDA) [23]. Sebaliknya, isyarat DA tonik memainkan peranan dalam modulasi memori kerja dan proses eksekutif lain. Beberapa ciri yang membezakan mod isyarat ini dari jenis phasic adalah ia beroperasi kebanyakannya melalui reseptor DA afiniti yang lebih rendah (reseptor DA D1). Walau bagaimanapun, dan walaupun terdapat mekanisme yang berbeza, pendedahan dadah yang berlarutan (dan perubahan dalam tonik DA yang memberi isyarat melalui penerima ini) juga telah terbabit dalam perubahan neuroplastik yang akhirnya menyebabkan pengkondisian [25] melalui pengubahsuaian reseptor glutamat NMDA dan dan alpha-amino-3-hydroxyl-5-methyl-4-isoxazone-propionate (AMPA)24].
Bukti menunjukkan bahawa peningkatan yang disebabkan oleh dadah yang mendadak di DA meniru penembusan sel DA phasic. Ini membantu menjelaskan mengapa penggunaan kronik bahan adiktif boleh menyebabkan tindak balas berkuasa yang kuat terhadap ubat itu sendiri, harapannya, dan isyarat pelbagai (orang, benda dan tempat) yang berkaitan dengan penggunaannya. Walau bagaimanapun, walaupun kesan pengukuhan akut ubat-ubatan penyalahgunaan yang bergantung pada kenaikan DA yang cepat mungkin "perlu" untuk pembangunan ketagihan, mereka jelas tidak "mencukupi." Pendedahan ubat yang berulang menyebabkan perubahan dalam fungsi otak DA yang mengambil masa untuk berkembang kerana ia berpunca daripada neuroadaptations sekunder dalam sistem neurotransmitter lain (contohnya glutamat [26] dan juga asid γ-aminobutyiric (GABA)) yang akhirnya mempengaruhi litar otak tambahan yang dimodulasi oleh DA. Litar ini adalah fokus bahagian seterusnya.
Penyalahgunaan dadah kronik mengecilkan reseptor dopamin dan pengeluaran dopamin: "tinggi" adalah tumpul
Hakikat bahawa penggunaan dadah mesti menjadi kronik sebelum penagihan mengambil akar adalah petunjuk yang jelas bahawa penyakit itu bersifat predicated, pada individu yang terdedah, pada gangguan yang berulang sistem ganjaran. Pertentangan ini akhirnya boleh membawa kepada neuroadaptations di banyak litar lain (motivasi / pemacu, kawalan kawalan / fungsi eksekutif, dan memori / pengkondisian) yang juga dimodulasi oleh DA [27]. Antara penyesuaian neuro yang telah dilaporkan secara konsisten dalam subjek ketagihan ialah pengurangan ketara dalam tahap reseptor D2R (afinitas tinggi) dan dalam jumlah DA yang dikeluarkan oleh sel DA [28] (Rajah 3). Yang penting, defisit ini dikaitkan dengan aktiviti metabolis serantau yang lebih rendah dalam bidang korteks prefrontal (PFC) yang kritikal untuk prestasi eksekutif yang betul (iaitu anting cingulate gyrus (CG) dan cortex orbitofrontal (OFC)) (Rajah 4A). Pemerhatian ini membawa kita untuk menyatakan bahawa ini mungkin salah satu mekanisme yang menghubungkan gangguan yang disebabkan oleh dadah dalam DA yang memberi isyarat kepada pentadbiran dadah yang kompulsif dan kekurangan kawalan ke atas pengambilan dadah yang mencirikan ketagihan [29]. Juga, keadaan hipodopaminergik yang dihasilkan akan menjelaskan penurunan kepekaan seseorang yang ketagihan terhadap ganjaran semula jadi (contohnya makanan, seks, dan lain-lain) dan pengekalan penggunaan dadah sebagai kaedah untuk mengimbangi defisit ini buat sementara waktu [30]. Satu corollary penting pengetahuan ini adalah bahawa menangani defisit ini (dengan meningkatkan tahap D2R yang teguh dan meningkatkan pembebasan DA di striatum dan wilayah prefrontal) boleh menawarkan strategi klinikal untuk memperbaiki kesan penagihan [31]. Adakah terdapat bukti yang membalikkan keadaan hipodopaminergik boleh memberi kesan positif terhadap tingkah laku yang berkaitan dengan penyalahgunaan kandungan? Jawapannya adalah ya. Kajian kami menunjukkan bahawa dengan memaksa pengeluaran lebih banyak D2R, jauh di dalam sistem ganjaran cocaine atau tikus yang beralkohol yang beralkohol, kita dapat mengurangkan pengambilan diri kokain [31] atau alkohol [32] masing-masing. Lebih-lebih lagi, dalam tikus, dan juga dalam penyalahgunaan methamphetamine manusia [33], tahap tekanan D2R yang dikurangkan juga dikaitkan dengan impulsif, dan dalam tikus ia meramalkan pola kompulsif pentadbiran diri dadah (lihat di bawah).
Kajian pencitraan juga menunjukkan bahawa, pada manusia, ketagihan dikaitkan dengan pengurangan pembebasan DA di stratum ventral dan di kawasan lain di striatum, dan tindak balas yang menyenangkan yang menyenangkan terhadap ubat yang aktif dan dalam pengguna ubat detoksifikasi (Rajah 5) [34]. Ini adalah satu penemuan yang tidak dijangka kerana ia telah dihipoteskan bahawa ketagihan mencerminkan sensitiviti yang dipertingkatkan untuk memberi ganjaran (dan dengan itu dopaminergik) tindak balas terhadap ubat-ubatan. Dalam penyalahguna dadah, pengurangan dalam pembebasan DA boleh mencerminkan neurofisiologi yang terganggu dalam litar ganjaran (iaitu dalam neuron DA yang melepaskan DA di striatum) atau, secara alternatif, peraturan pemberhentian umpan balik yang mengganggu litar ganjaran oleh laluan prefrontal (kawalan eksekutif) atau amygdalar (emosi) (laluan glutamatergik prefrontal-striatal, amygdalarstriatal). Sejak disfungsi dopaminergik tulen di striatum, seperti yang dilihat dalam penyalahguna dadah kronik, tidak menganggap ciri-ciri yang mencirikan kelakuan ketagihan, seperti impulsif, nafsu, dan kambuh semula yang dicetuskan oleh isyarat dadah, kemungkinan besar bahawa kawasan prefrontal (seperti juga amygdala) juga terlibat di sini, kerana gangguan mereka akan membolehkan atau sekurang-kurangnya mempengaruhi ciri-ciri tingkah laku ini.
Penurunan tahap reseptor dopamin (DR2) mengurangkan kawalan impulsiviti oleh korteks prefrontal
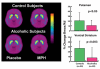
Telah dihipotesiskan bahawa kawalan terjejas ke atas pengambilan ubat pengambilan dadah yang mencirikan ketagihan mungkin disebabkan sebahagiannya untuk disfungsi tertentu di kawasan hadapan di otak [35]. Sekarang terdapat banyak keterangan yang menyokong idea ini, bermula dengan kajian haiwan yang meneroka hubungan antara D2R dan kawalan tingkah laku. Eksperimen dengan tikus jelas menunjukkan korelasi antara D2R rendah dan impulsivity [36], dan di antara impulsiviti dan pentadbiran diri dadah [37]. Tetapi apa hubungannya? Seperti yang dinyatakan sebelum ini, dalam penderaan ubat, D2R yang lebih rendah berkisar dengan korelasi dengan metabolisme glukosa otak yang lebih rendah di kawasan-kawasan utama PFC, seperti OFC (terlibat dengan penonjolan dan gangguan yang menyebabkan tingkah laku kompulsif) dan dalam CG (terlibat dengan kawalan kendalian dan pemantauan ralat dan gangguan yang menyebabkan impulsivity) (Rajah 4B) [38, 39]. Selain itu, dalam satu kajian yang dilakukan oleh individu (umur SD, 24 ± 3 tahun), sejarah keluarga alkoholisme, tetapi yang tidak mempunyai alkohol sendiri, kami juga mendapati persefahaman yang signifikan antara D2R dan metabolisme striatal di rantau frontal (CG , OFC, dan PFC dorsolateral) dan juga anterior insula (terlibat dalam interpersonal, kesedaran diri, dan ubat keinginan) [40] (Rajah 6). Menariknya, individu-individu ini mempunyai D2R yang lebih tinggi daripada kawalan yang sepadan dengan sejarah keluarga tanpa alkohol, walaupun mereka tidak berbeza dalam metabolisme terdahulu. Juga, dalam kawalan, D2R striatal tidak berkaitan dengan metabolisme terdepan. Ini membawa kita untuk membuat spekulasi bahawa D2R yang lebih tinggi daripada normal dalam subjek dengan risiko genetik yang tinggi untuk alkohol melindungi mereka daripada alkoholisme sebahagiannya dengan menguatkan aktiviti di kawasan prefrontal. Apabila digabungkan, data ini menunjukkan bahawa tahap D2R yang tinggi di striatum dapat melindungi daripada penyalahgunaan dadah dan kecanduan dengan mengekalkan sifat-sifat impulsif yang terkawal, iaitu, dengan mengawal litar yang terlibat dalam menghalang tindak balas tingkah laku dan mengawal emosi.
Begitu juga, kami menegaskan bahawa kawasan prefrontal juga terlibat dalam pengurangan pembebasan DA (dan tetulang) yang diperhatikan dalam subjek ketagihan kerana mereka mengawal tembakan sel DA di barisan tengah dan DA dilepaskan di striatum. Untuk menguji hipotesis ini, kita menilai hubungan antara metabolisme asas dalam PFC dan kenaikan DA striatal yang disebabkan oleh pentadbiran intravena MPH dalam kawalan dan dalam alkohol detoksifikasi. Selaras dengan hipotesis, dalam alkoholik kita gagal untuk mengesan persamaan normal antara metabolisme prefrontal basikal dan DA pelepasan di striatum, menunjukkan bahawa penurunan yang ketara dalam pembebasan DA dalam striatum yang dilihat dalam alkoholik mencerminkan peraturan yang tidak wajar dalam aktiviti otak oleh kawasan otak prefrontal [34].
Oleh itu, kami telah menemui perhubungan antara aktiviti baseline yang berkurang di PFC dan menurunkan D2R yang teguh dalam subjek ubat-ubatan, dan antara aktiviti PFC asas dan pembebasan DA dalam kawalan yang tidak hadir dalam individu kecanduan. Persatuan-persatuan ini membuktikan hubungan yang kukuh antara neuroadaptations di laluan PFC dan disfungsi hiliran dalam ganjaran DA dan sistem motivasi, mungkin disebabkan oleh pengaruh PFC terhadap impulsif dan pengunduran. Walau bagaimanapun, ini gagal untuk mengambil kira fenomena tingkah laku tambahan, seperti kesan isyarat berkaitan dadah dalam mencetuskan keinginan, yang mungkin akan melibatkan memori dan litar pembelajaran.
Kenangan yang dianggarkan dan tingkah laku stereotypik menggantikan "tinggi" sebagai pemandu
Lebih-rangsangan sel-sel DA di stratum ventral akhirnya mewujudkan sambungan fungsi baru di otak antara tindakan memuaskan dorongan, dan kejadian keadaan di sekelilingnya (contohnya, persekitaran, rutin penyediaan ubat, dll), meletakkan baru , persatuan belajar yang kuat yang boleh mencetuskan tingkah laku. Pada akhirnya, ingatan semata-mata atau perangsang dadah dapat mencetuskan perilaku impulsif yang mencirikan individu yang kecanduan. Dengan penggunaan ubat berulang, penembakan sel DA dalam striatum mula mengubah neurokimia yang mendasari pembelajaran bersekutu. Ini memudahkan penggabungan jejak ingatan maladaptive yang berkaitan dengan ubat, yang membantu menjelaskan keupayaan segala macam rangsangan yang berkaitan dengan dadah (dalam jangkaan belajar menerima ganjaran dadah apabila terdedah kepada rangsangan ini) [41] untuk mencetuskan tembakan DA dengan mudah. Dan kerana peranan DA dalam motivasi, DA ini meningkatkan pencetus pemacu motivasi yang diperlukan untuk menjamin ganjaran [42]. Sesungguhnya, apabila tikus didedahkan berulang kali kepada rangsangan neutral yang dipasangkan dengan ubat (terkondisi), ia dapat menimbulkan peningkatan DA dan menghidupkan kembali pentadbiran diri dadah [43]. Respons terkondisi sedemikian adalah berkaitan secara klinikal dalam masalah penggunaan bahan kerana mereka bertanggungjawab untuk kemungkinan besar seseorang yang ketagih berulang walaupun selepas tempoh detoksifikasi yang berlarutan. Sekarang, teknik pencitraan otak membolehkan kita menguji sama ada pendedahan manusia kepada isyarat berkaitan ubat boleh mencetuskan keinginan ubat seperti yang ditunjukkan dalam haiwan makmal.
Dengan penggunaan ubat berulang, penembakan sel DA dalam striatum mula mengubah neurokimia yang mendasari pembelajaran bersekutu. Ini memudahkan penggabungan jejak ingatan maladaptive yang berkaitan dengan ubat, yang membantu menjelaskan keupayaan segala macam rangsangan yang berkaitan dengan dadah (dalam jangkaan belajar menerima ganjaran dadah apabila terdedah kepada rangsangan ini) [41] untuk mencetuskan tembakan DA dengan mudah. Dan kerana peranan DA dalam motivasi, DA ini meningkatkan pencetus pemacu motivasi yang diperlukan untuk menjamin ganjaran [42]. Sesungguhnya, apabila tikus didedahkan berulang kali kepada rangsangan neutral yang dipasangkan dengan ubat (terkondisi), ia dapat menimbulkan peningkatan DA dan menghidupkan kembali pentadbiran diri dadah [43]. Respons terkondisi sedemikian adalah berkaitan secara klinikal dalam masalah penggunaan bahan kerana mereka bertanggungjawab untuk kemungkinan besar seseorang yang ketagih berulang walaupun selepas tempoh detoksifikasi yang berlarutan. Sekarang, teknik pencitraan otak membolehkan kita menguji sama ada pendedahan manusia kepada isyarat berkaitan ubat boleh mencetuskan keinginan ubat seperti yang ditunjukkan dalam haiwan makmal.
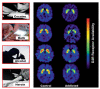
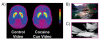
Soalan ini telah disiasat dalam penderaan kokain aktif. Menggunakan PET dan [11C] raclopride, dua kajian bebas menunjukkan pendedahan kepada video cocaine-cues (kokain merokok subjek) tetapi tidak kepada video yang neutral (adegan alam) meningkatkan DA striatal dalam subjek manusia yang kecanduan kokain (Rajah 7) dan bahawa peningkatan DA dikaitkan dengan laporan subjektif keinginan ubat [44, 45]. Semakin tinggi kenaikan DA yang dicetuskan oleh pendedahan kepada video kokain-cues, semakin sengit keinginan ubat. Selain itu, magnitud peningkatan DA juga dikaitkan dengan skor keparahan ketagihan, yang menonjolkan kaitan respon yang terkondisi dalam sindrom klinikal ketagihan.
Adalah penting untuk menekankan bahawa walaupun terdapat kekuatan persatuan maladaptive ini, kami baru-baru ini telah mengumpulkan bukti-bukti baru yang menunjukkan bahawa penyalahgunaan kokain mengekalkan keupayaan untuk sengaja menghalang keinginan. Oleh itu, strategi untuk menguatkan peraturan fronto-striatal boleh menawarkan manfaat terapeutik yang berpotensi [46].
Menggabungkannya bersama
Antara ciri-ciri ketagihan dadah yang paling merosakkan adalah keinginan besar untuk mengambil ubat-ubatan yang dapat muncul semula selepas bertahun-tahun menahan diri, dan keupayaan yang sangat dikompromi oleh orang-orang yang kecanduan untuk menghalang narkoba mencari begitu keinginan meletus walaupun akibat negatif yang terkenal.
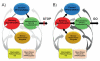
Kami telah mencadangkan satu model ketagihan [47yang menerangkan sifat multidimensi penyakit ini dengan mencadangkan satu rangkaian empat litar yang saling berkaitan, yang keluaran gabungan fungsional dapat menerangkan banyak ciri tingkah laku stereotip terhadap ketagihan: (a) ganjaran, termasuk beberapa nukleus dalam ganglia basal, terutama striatum ventral, yang Nac menerima input dari kawasan tegegal ventral dan menyampaikan maklumat kepada pallidum ventral (VP); (b) motivasi / pemacu, yang terletak di OFC, korteks subcallosal, striatum dorsal dan korteks motor; (c) memori dan pembelajaran, terletak di amygdala dan hippocampus; dan (d) perancangan dan kawalan, terletak di korteks prefrontal dorsolateral, CG anterior dan korteks frontal inferior. Keempat litar ini menerima penerimaan langsung daripada neuron DA tetapi juga berkaitan dengan satu sama lain melalui unjuran langsung atau tidak langsung (kebanyakannya glutamatergik).
Empat litar dalam model ini bekerja bersama dan operasi mereka berubah dengan pengalaman. Setiap dikaitkan dengan konsep penting, masing-masing: kesungguhan (ganjaran), keadaan dalaman (motivasi / pemacu), persatuan yang dipelajari (ingatan, pengkondisian), dan resolusi konflik (kawalan). Di samping itu, litar ini juga berinteraksi dengan litar yang terlibat dengan mood (termasuk kereaktifan tekanan) [48] dan dengan interception (yang mengakibatkan kesadaran keinginan ubat dan mood) [49]. Kami telah mencadangkan bahawa corak aktiviti dalam rangkaian litar empat yang digariskan di sini mempengaruhi bagaimana individu biasa membuat pilihan di antara alternatif yang bersaing. Pilihan ini dipengaruhi secara sistematik oleh ganjaran, ingatan / penyesuaian, motivasi, dan litar kawalan dan ini pula dimodulasi oleh litar yang mendasari suasana hati dan kesedaran yang sedar (Rajah 8A).
Tanggapan kepada rangsangan dipengaruhi oleh kesenjangan sesaat, iaitu ganjaran yang diharapkan. Sebaliknya, jangkaan ganjaran diproses sebahagiannya oleh neuron DA yang memperlihatkan striatum ventral dan dipengaruhi oleh unjuran glutamatergik dari OFC (yang memberikan nilai kesamaan sebagai fungsi konteks) dan amygdala / hippocampus (yang menengahi respon yang terkondisi dan memori ingatan). Nilai rangsangan adalah tertimbang (dibandingkan) dengan rangsangan alternatif lain, tetapi juga berubah sebagai fungsi keperluan dalaman individu, yang dimodulasi oleh mood (termasuk kereaktifan stres) dan kesedaran interceptif. Khususnya, pendedahan tegasan meningkatkan nilai kesederhanaan ubat-ubatan sementara pada masa yang sama ia mengurangkan peraturan prefrontal amygdala [50]. Di samping itu, sejak pendedahan dadah kronik dikaitkan dengan pemekaan dipertingkatkan untuk tekanan tindak balas ini menjelaskan mengapa tekanan boleh mencetuskan kambuh dadah sering sekali dalam keadaan klinikal. Semakin kuat nilai rangsangan rangsangan, sebahagiannya dibentuk oleh pengalaman menghafal sebelumnya, semakin besar pengaktifan litar motivasi dan semakin kuat pemacu untuk mendapatkannya. Keputusan kognitif untuk bertindak (atau tidak) untuk mendapatkan rangsangan diproses sebahagiannya oleh PFC dan CG, yang menimbang keseimbangan antara positif yang positif berbanding hasil negatif yang tertangguh, dan oleh korteks frontal inferior (Broadmann Area 44) yang berfungsi menghalang tindak balas ramalan untuk bertindak [51].
Menurut model ini, dalam subjek ketagihan (Rajah 8B), nilai keterujaan ubat penyalahgunaan dan isyarat yang dikaitkan dipertingkatkan dengan mengorbankan ganjaran yang lain (semulajadi), yang ketinggalannya dikurangkan. Ini akan menjelaskan motivasi meningkat untuk mencari ubat. Walau bagaimanapun, pendedahan dadah akut juga menetapkan semula ambang ganjaran, menyebabkan sensitiviti penurunan litar ganjaran kepada penguat [52], yang juga membantu menjelaskan nilai berkurang penguat bukan ubat pada orang yang kecanduan. Satu lagi sebab untuk kecanggihan yang dipertingkatkan adalah ubat kekurangan kebimbangan DA terhadap ubat-ubatan penyalahgunaan (toleransi) berbanding dengan kebiasaan normal yang wujud untuk ganjaran semula jadi dan yang mengakibatkan rasa kenyang [53].
Selain itu, pendedahan kepada rangsangan terkondisi cukup untuk meningkatkan ambang ganjaran [54]; Oleh itu, kita akan meramalkan bahawa dalam orang yang kecanduan, pendedahan kepada persekitaran dengan isyarat yang berhawa dingin akan terus memburukkan sensitiviti mereka yang menurun kepada ganjaran semula jadi. Dalam ketiadaan persaingan oleh pasukan bantuan lain, pembelajaran terkondisi akan meningkatkan pengambilan ubat ke tahap pemacu motivasi utama bagi individu. Kami menghipnotiskan bahawa isyarat dadah (atau tekanan) menyebabkan DA cepat meningkat di Nac di stratum ventral dan di striatum dorsal yang memacu motivasi untuk mengambil ubat dan tidak boleh ditentang dengan betul oleh PFC yang tidak berfungsi. Oleh itu, apabila penggunaan dadah dan mabuk, peningkatan isyarat DA akan mengakibatkan terlalu banyak operasi litar motivasi / pemacu dan memori, yang menyahaktifkan PFC (inhibisi prefrontal berlaku dengan pengaktifan amygdala yang sengit) [50], menyekat kuasa PFC untuk mengawal litar motivasi / pemacu. Tanpa kawalan kendali ini, gelung umpan balik positif ditubuhkan, yang mengakibatkan pengambilan ubat kompulsif. Kerana interaksi antara litar adalah dua hala, pengaktifan rangkaian semasa mabuk berfungsi untuk mengukuhkan lagi nilai kebarangkalian dadah dan penyesuaian kepada isyarat dadah.
kesimpulan
Ringkasnya, kami mencadangkan model yang menyumbang ketagihan seperti berikut: Semasa ketagihan, nilai tambah isyarat dadah dalam litar memori mendorong jangkaan ganjaran dan meningkatkan motivasi untuk mengambil ubat, mengatasi kawalan kendalian yang dikenakan oleh PFC yang sudah tidak berfungsi. Walaupun kenaikan DA yang disebabkan oleh dadah telah dilemahkan dengan ketara dalam subjek ketagihan dadah, kesan farmakologi dari ubat menjadi respon yang dikondisikan dalam diri mereka sendiri, memacu lagi motivasi untuk mengambil dadah dan memihak kepada gelung umpan balik yang positif kini tidak dapat ditahan, kerana pemotongan litar kawalan prefrontal. Pada masa yang sama, ketagihan mungkin juga menyusun semula litar yang memberi contoh mood dan kesedaran (diwakili oleh warna kelabu yang lebih gelap) (Rajah 8B) dengan cara yang, jika eksperimen diperkuatkan, akan terus mencairkan keseimbangan dari kawalan perencatan dan ke arah pengambilan ubat ketagihan dan kompulsif.
Kami dengan mudah mengakui bahawa ini adalah model mudah: kami menyedari bahawa kawasan otak lain juga mesti terlibat dalam litar ini, bahawa satu kawasan boleh menyumbang kepada beberapa litar, dan litar lain mungkin juga terlibat dalam ketagihan. Di samping itu, walaupun model ini memberi tumpuan kepada DA, adalah jelas dari kajian praklinikal bahawa pengubahsuaian dalam unjuran glutamatergik memeterai banyak penyesuaian yang dilihat dalam ketagihan dan yang kita dibincangkan di sini. Ia juga dapat dilihat dari kajian-kajian praplinikal yang melibatkan neurotransmitter yang lain dalam kesan menguatkan dadah termasuk cannabinoids dan opioid. Malangnya, sehingga baru-baru ini, akses terhad kepada pengesan radio untuk pengimejan PET telah mengehadkan keupayaan untuk menyiasat penglibatan neurotransmitter lain dalam ganjaran dadah dan ketagihan.
Singkatan
- AMPA
- α-amino-3-hydroxyl-5-methyl-4-isoxazole-propionate
- CG
- cingulate gyrus
- CTX
- korteks
- D2R
- reseptor jenis dopamin 2 / 3
- DA
- dopamin
- FDG
- fluorodeoxyglucose
- GABA
- asid γ-aminobutyiric
- HPA
- paksi pituitari hipotalamus
- MPH
- methylphenidate
- Nac
- nukleus accumbens
- NMDA
- n-methyl-dasid asparat
- OFC
- korteks orbitofrontal
- PET
- tomografi pelepasan positron
- PFC
- korteks prefrontal
- VP
- ventral pallidum
Rujukan
55. Fowler JS, Volkow ND, Logan J, et al. Pengambilan cepat dan pengikatan methamphetamine yang berkekalan dalam otak manusia: perbandingan dengan kokain. Neuroimage. 2008;43: 756-63. [Artikel percuma PMC] [PubMed