Doniesienia naukowe Tom 9, Numer artykułu: 16918 (2019)
Abstrakcyjny
Nadmierne spożycie sacharozy wywołuje głodowe uzależnienie, które może być przyczyną epidemii otyłości. Opioidy i dopamina pośredniczą w nagradzającym działaniu narkotyków i naturalnych nagród z bodźców, takich jak smaczne jedzenie. Zbadaliśmy wpływ sacharozy za pomocą obrazowania PET za pomocą [11C] karfentanyl (agonista receptora μ-opioidowego) i [11C] raclopryd (antagonista receptora dopaminy D2 / 3) u siedmiu samic znieczulonych miniaturowych świnek z Göttingen. Następnie daliśmy świnkom miniaturowym dostęp do roztworu sacharozy przez jedną godzinę przez 12 kolejnych dni i ponownie wykonaliśmy obrazowanie 24 godziny po ostatecznym dostępie sacharozy. W mniejszej próbce pięciu miniaturowych świnek wykonaliśmy dodatkowe [11C] sesja PET z karfentanylem po pierwszej ekspozycji na sacharozę. Obliczyliśmy wokselowe potencjały wiązania (BPND), wykorzystując móżdżek jako region wiązania nieusuwalnego, przeanalizował różnice za pomocą statystycznego mapowania nieparametrycznego i przeprowadził analizę regionalną. Po 12 dniach dostępu do sacharozy BPND oba znaczniki znacznie spadły w prążkowiu, jądrze półleżącym, wzgórzu, ciele migdałowatym, korze obręczy i korze przedczołowej, zgodnie z obniżeniem gęstości receptorów. Po jednorazowej ekspozycji na sacharozę stwierdziliśmy zmniejszone wiązanie [11C] karfentanyl w jądrze półleżącym i korze obręczy, zgodnie z uwalnianiem opioidów. Niższa dostępność receptorów opioidowych i dopaminowych może wyjaśniać uzależniający potencjał związany z przyjmowaniem sacharozy.
Wprowadzenie
Pięć procent światowej populacji jest klinicznie otyłych1. Cechą charakterystyczną zespołu metabolicznego jest otyłość związana z cukrzycą typu 2, chorobami sercowo-naczyniowymi, problemami z oddychaniem oraz ryzykiem depresji i prawdopodobnie demencji2. Zwiększone zużycie żywności o dużej zawartości energii wyolbrzymiło fizjologiczne rozróżnienie między głodem homeostatycznym, który następuje po pozbawieniu żywności, a głodem hedonicznym, czyli „głodem”, który występuje przy braku deprywacji3,4. Ponieważ sama regulacja homeostatyczna nie może wyjaśnić obecnego wzrostu otyłości, obowiązkowe jest przetestowanie wpływu na mózg mechanizmów nagradzania i przyjemności uzależniających właściwości bardzo smacznego jedzenia.
Spożycie sacharozy wiąże się z otyłością, a sacharoza jest coraz częściej uważana za substancję uzależniającą5. Niektóre ustalenia są sprzeczne z tym twierdzeniem ze względu na trudności w oddzieleniu konsumpcji niesmacznego jedzenia od hedonicznych odpowiedzi pokarmowych oraz w określeniu uzależniającego składnika w przetworzonej żywności, a także różnych mechanizmów, dzięki którym żywność zmienia obwody mózgowe poprzez naturalne ścieżki6. Niemniej jednak, w szczególnych kontekstach, spożycie sacharozy wywołuje nagrodę i głód, porównywalny pod względem wielkości z tymi wywoływanymi przez uzależniające leki, które prowadzą do nadmiernego spożycia i ostatecznie otyłości6,7.
Głód jest związany z „chęcią”, która jest ściśle związana z efektami neurotransmisji dopaminergicznej w wielu nagród8, ale pozostaje niejasne, w jaki sposób działanie dopaminy (DA) jest modulowane w odpowiedzi na kompulsywne jedzenie. Spożycie smacznego jedzenia wiąże się z „lubieniem”, w którym pośredniczy przede wszystkim endogenny układ opioidowy, szczególnie receptor μ-opioidowy (μOR)9,10, co może sprzyjać nadmiernemu zużyciu w przypadku rozregulowania. W niniejszym raporcie testujemy twierdzenie, że sacharoza prowadzi do uwalniania opioidów i dopaminy, co obniża dostępność receptorów μOR i DA D2 / 3. Dostępność jest wskaźnikiem liczby niezajętych receptorów dostępnych do wiązania znacznika i zasadniczo nie rozróżnia zajętości ligandu i gęstości receptora11.
Początek kompulsywnego jedzenia zależy od wielu czynników, a badania przyczynowe na ludziach poruszają kwestie etyczne. Większość badań koncentruje się zatem na zachowaniach żywieniowych u szczurów12. Chociaż szczury mają „słodycze”, ich mechanizmy homeostatyczne ważne dla przybierania na wadze, metabolizmu i rodzaju gromadzenia tłuszczu różnią się znacznie od ludzkich. Minipig z Göttingen jest dużym wszystkożernym zwierzęciem z dobrze rozwiniętym mózgowym żyłyfalicznym mózgiem, który można obrazować z wystarczającą rozdzielczością. Jego dobrze zdefiniowane podkorowe i przedczołowe obszary korowe13 umożliwiają bardziej bezpośrednie tłumaczenie na funkcję ludzkiego mózgu. W tym celu używamy obrazowania metodą pozytronowej tomografii emisyjnej (PET) in vivo Dostępność μOR i DA D2 / 3 w miniaturowym modelu subchronicznej ekspozycji na sacharozę. W mniejszej próbce zbadaliśmy bezpośredni wpływ na obłożenie μOR po pierwszej ekspozycji na sacharozę. Na koniec przetestowaliśmy związek między zmianami dostępności receptorów dwóch znaczników.
Efekt
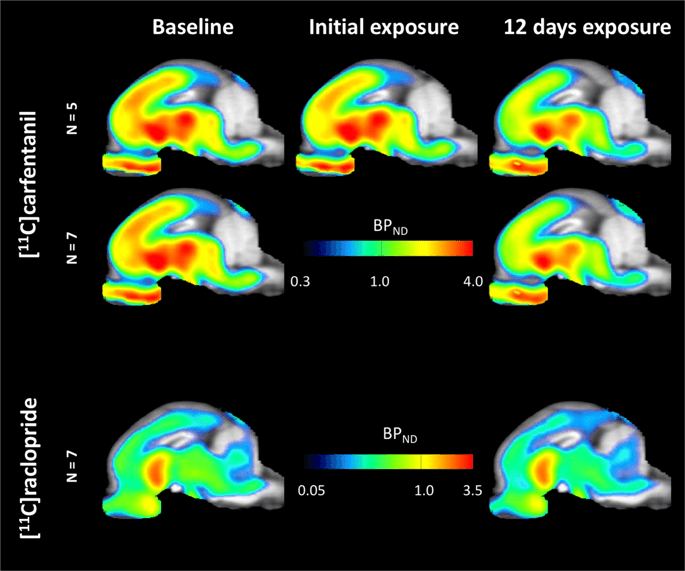
Średnie mapy parametryczne [11C] carfentanil i [11C] potencjał wiązania raclopridu (BPND) pokazano na ryc. 1. Aby przeanalizować zmiany występujące po pierwszej ekspozycji na sacharozę u pięciu świnek miniaturowych w porównaniu do wartości początkowej i jeden dzień po 12th dostęp do sacharozy w siedmiu świnkach miniaturowych w porównaniu do wartości początkowej, zastosowaliśmy teorię permutacji i nieregionalnie ograniczoną analizę całego mózgu, preferowaną metodę dla próbek tej wielkości14.
Średni potencjał wiązania niemożliwy do przemieszczenia (wokND) mapy nałożone na obrazy MRI w widoku strzałkowym. Dane są prezentowane dla [11C] carfentanil BPND z 5 świnek miniaturowych zobrazowanych na początku, po początkowej ekspozycji na sacharozę i po 12 dniach ekspozycji na sacharozę (górny rząd). [11C] carfentanil BPND ze wszystkich 7 świnek miniaturowych zobrazowanych na początku i po 12 dniach dostępu do sacharozy przedstawiono w środkowym rzędzie. [11C] raclopopride BPND wszystkich 7 świnek miniaturowych zobrazowanych na początku i po 12 dniach dostępu do sacharozy pokazano w dolnym rzędzie. Pamiętaj, że skala kolorów jest wykładnicza, aby wyróżnić [11C] raclopopride BPND w regionach pozastriatalnych.
Początkowa ekspozycja na sacharozę
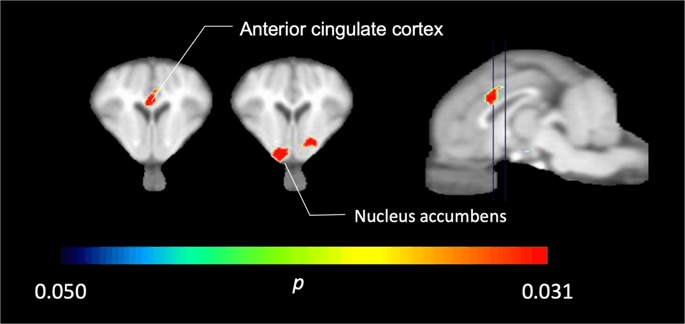
W pięciu miniaturowych świnkach z [11C] karfentanyl na początku i natychmiast po pierwszej ekspozycji na sacharozę stwierdziliśmy znacznie zmniejszone wiązanie znacznika w przedniej części kory obręczy i jądrze półleżącym w odpowiedzi na sacharozę, co pokazano kolorem na ryc. 2, co wskazuje na p <0.05. Wykryliśmy aż 14% zmniejszone wiązanie znacznika w obu obszarach w porównaniu z wartością wyjściową.
Znaczące spadki [11C] carfentanil BPND po pierwszym wystawieniu na działanie sacharozy w porównaniu do wartości początkowej (n = 5). Tylko woksele ze znaczącymi (p <0.05) ubytki przedstawiono jako kolorowe obszary rzutowane na wycięcia MRI ważone T1 na poziomie przedniej kory zakrętu obręczy (po lewej) i jądra półleżącego (w środku) ze stereotaktycznego atlasu mózgu minipig. Należy zauważyć, że maksymalny poziom istotności możliwy do osiągnięcia przy 5 zwierzętach wynosi 2-5 ≈ 0.031 (patrz pasek kolorów). Dane są prezentowane w przekrojach koronalnych mózgu świni na poziomach wskazanych na obrazie strzałkowym (po prawej).
12 dni dostępu do sacharozy
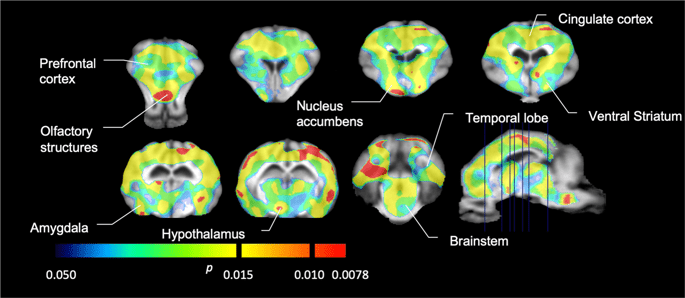
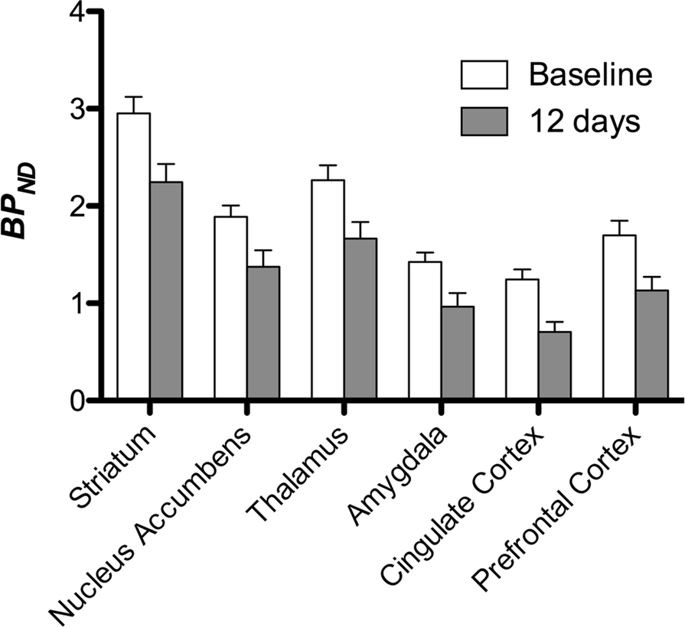
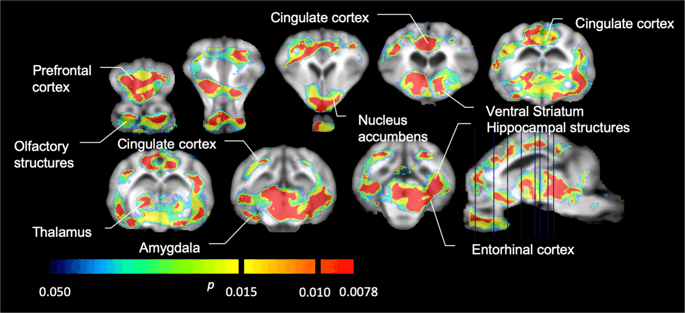
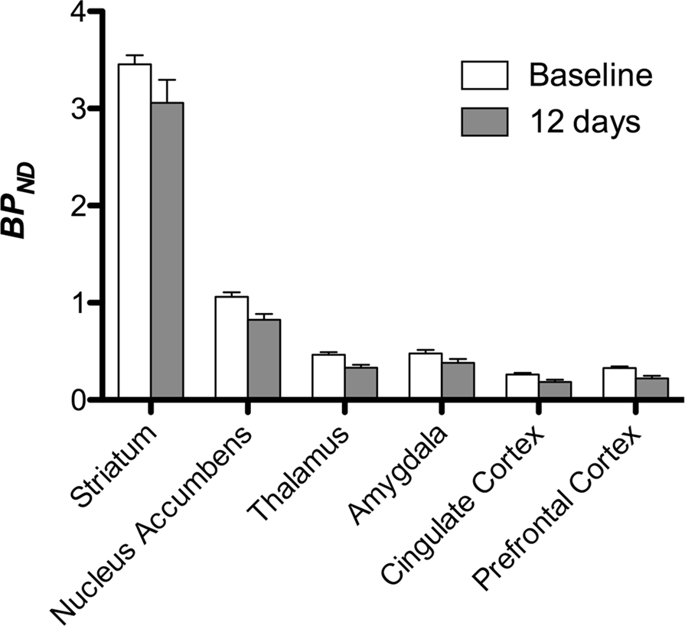
Następnie przeprowadziliśmy analizę siedmiu świnek miniaturowych zobrazowanych za pomocą [11C] karfentanyl na początku i po 12 dniach dostępu do sacharozy i stwierdzono znacznie zmniejszone wiązanie znacznika u zwierząt eksponowanych na sacharozę w porównaniu do wartości początkowej. Najbardziej dotknięte regiony pokazano na czerwono na ryc. 3 (p <0.01) i obejmuje części struktur węchowych, jądro półleżące / prążkowia brzuszną i korę / płat skroniowy, a następnie obszary zaznaczone na żółto (p <0.015), które obejmowały części kory przedczołowej, kory zakrętu obręczy, ciało migdałowate i pień mózgu . W celu uzyskania BPND wartości i oceny zmiany procentowej, przeprowadziliśmy analizę regionalną i uzyskaliśmy średnie wartości w każdym regionie na początku i po spożyciu sacharozy (ryc. 4).
Znaczące spadki [11C] potencjał wiązania karfentanylu (BPND) między wartością początkową a po 12 dniach ekspozycji na sacharozę (n = 7). Woksele o znaczącym (p <0.05) ubytki pokazano jako kolorowe obszary rzutowane na wycinki MRI ważone T1 ze stereotaktycznego atlasu mózgu minipig. Dane przedstawiono na koronalnych przekrojach mózgu na poziomach wskazanych na obrazie strzałkowym (na dole po prawej). Należy zauważyć, że maksymalny poziom istotności możliwy do osiągnięcia przy 7 zwierzętach wynosi 2-7 ≈ 0.0078 (patrz pasek kolorów).
Użyliśmy [11C] raclopryd jako znacznik receptorów DA D2 / 3 w prążkowanych i pozastriatalnych obszarach mózgu u świnek miniaturowych na początku i po 12 dniach dostępu do sacharozy (ryc. 1). Stwierdziliśmy zmniejszone wiązanie znacznika u zwierząt narażonych na sacharozę, w porównaniu do wartości wyjściowych, z największymi skutkami (p <0.01) w obszarach kory przedczołowej, jądra półleżącego / prążkowia brzusznego, kory zakrętu obręczy, ciała migdałowatego, wzgórza, śródmózgowia, obszarów hipokampu i obszarów węchowych (Figa. 5). Dane z analizy regionalnej przedstawiono na ryc. 6.
Znaczące spadki [11C] potencjał wiązania raclopridu (BPND) między wartością początkową a po 12 dniach ekspozycji na sacharozę (n = 7). Woksele o znaczącym (p <0.05) ubytki pokazano jako kolorowe obszary rzutowane na wycinki MRI ważone T1 ze stereotaktycznego atlasu mózgu minipig. Dane przedstawiono na koronalnych przekrojach mózgu świni na poziomach wskazanych na obrazie strzałkowym (na dole po prawej). Należy zauważyć, że maksymalny poziom istotności możliwy do osiągnięcia przy 7 zwierzętach wynosi 2-7 ≈ 0.0078 (patrz pasek kolorów).
Korelacje między [11C] raclopopride i [11C] dane dotyczące karfentanylu
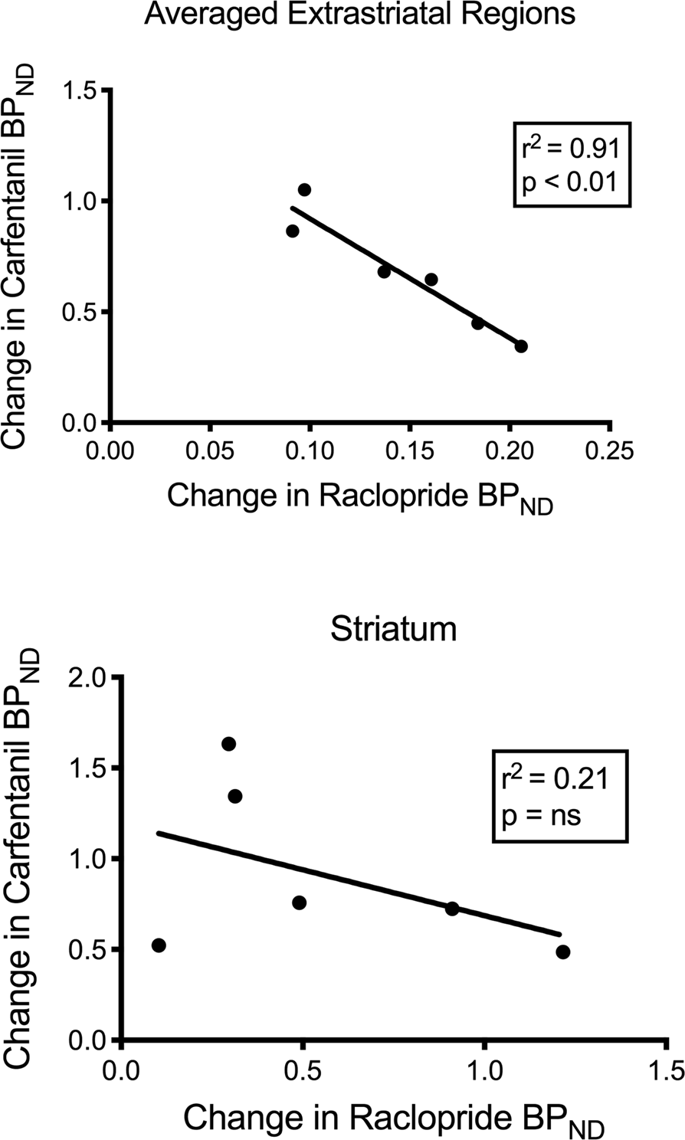
Testowaliśmy potencjalną korelację między [11C] raclopopride i [11C] wartości karfentanylu w BPND w obszarach prążkowanych i niestriatalnych u świnek miniaturowych na początku badania i po 12 dniach przyjmowania sacharozy, nie zaobserwowano związku. Następnie przetestowaliśmy, czy spadki wiązania znacznika były skorelowane, i porównaliśmy zmiany BPND dla [11C] raclopride ze zmianami BPND dla [11C] karfentanyl tylko u świnek miniaturowych o niższym BPND obu znaczników po spożyciu sacharozy (n = 6). Znaleźliśmy znaczące ujemne korelacje w uśrednionych pozastriatalnych (r2 = 0.91, p <0.01), ale nie w rejonach prążkowia (ryc. 7).
Korelacje między spadkami przed i po spadku [11C] raclopopride i [11C] potencjały wiązania karfentanylu (BPND) u świnek miniaturowych ze zmniejszonym wiązaniem znacznika po spożyciu sacharozy (n = 6). Przedstawiono dane z uśrednionych regionów pozastriatalnych (u góry) i prążkowia (u dołu). Współczynnik determinacji (r2), a wartości p są pokazane dla każdego wykresu.
Dyskusja
Ustaliliśmy wpływ powtarzającego się przerywanego dostępu do sacharozy na neurotransmisję opioidów i DA w mózgu ssaków. Wzdłużny in vivo Obrazowanie PET receptorów μOR i DA D2 / 3 ujawniło zmniejszoną dostępność receptorów w całym obwodzie nagrody, w tym w jądrze półleżącym, korze przedczołowej i przedniej części kory zakrętu obręczy. Wyniki wyraźnie pokazują, że sacharoza wpływa na mechanizmy wynagradzania w sposób podobny do narkotyków uzależniających.
Przyjmowanie sacharozy jako smacznej substancji jest znane z uwalniania DA i wywoływania zależności u gryzoni15, w których sacharoza okazała się w niektórych przypadkach nawet bardziej przyjemna niż kokaina u gryzoni. Tak więc gryzonie intensywniej pracują, aby uzyskać sacharozę niż kokainę, nawet przy braku żywności5. Jednak działanie sacharozy jest regulowane zarówno przez układ homeostatyczny, jak i przez hedoniczne obwody nagrody16,17 które mogą pośredniczyć w rozróżnieniu między żywieniowymi a hedonicznymi aspektami działania sacharozy18. Zdecydowaliśmy się na harmonogram jednogodzinny dziennie, aby promować „bingowanie”, ponieważ wcześniejsze badania na szczurach wykazały wyższe spożycie w ciągu pierwszej godziny codziennego dostępu w przerywanym harmonogramie15,19. Badania behawioralne przyjmowania pokarmu często dotyczą zwierząt z ograniczoną ilością pokarmu, ale projekt niekoniecznie odzwierciedla te same mechanizmy neuronalne aktywne w otyłości. Świnie w niniejszym badaniu nie były ograniczone pożywieniem i były karmione zwykłymi ilościami swojej normalnej diety, oprócz dostępu do sacharozy.
Receptory opioidowe (OR) są szeroko wyrażane w mózgu, szczególnie w strukturach znanych z modulowania procesów jedzenia i nagradzania20. Wykazano, że RNO odgrywają istotną rolę w nagradzającym i nawracającym działaniu kokainy21,22,23,24. Zmiany w wiązaniu zostały również powiązane z reakcjami homeostatycznymi na jedzenie i przyjemnością związaną z smacznym jedzeniem25. W szczególności „lubienie” pożywienia jest związane z endogennym układem opioidowym, zwłaszcza μOR9,10 w skorupie jądra półleżącego i brzusznej dłoniowate26. Wlewy agonisty μOR do różnych części jądra półleżącego i brzusznej paletki silnie wzmacniają zachowania „lubiące”, w tym wypukłości języka i lizanie łap, po zwiększonym smacznym przyjmowaniu pokarmu27,28,29. Dalsze dowody na sygnalizację opioidową w przetwarzaniu regulacji hedonicznej pochodzą od antagonistów μOR, które osłabiają konsumpcję smacznej karmy u obu ad libitum- zwierzęta karmione i o ograniczonej żywności, ale o bardziej ograniczonym wpływie na przyjmowanie niesmacznych standardowych granulek30,31. U ludzi antagoniści μOR zmniejszają krótkotrwałe przyjmowanie pokarmu i zmniejszają przyjemność smacznego jedzenia32,33,34. Sygnalizacja opioidów w bazowo-bocznym ciele migdałowatym przyczynia się również do „braku” pożywienia poprzez modulację poszukiwania nagrody i wartość zachęty pożywienia35.
Z [11C] karfentanyl, uzyskaliśmy obrazy wiązania znacznika, który jest wrażliwy zarówno na poziomy μOR, jak i na uwalnianie przez mózg endogennych opioidów36,37. Wykryliśmy natychmiastową utratę dostępności μOR w obszarach jądra półleżącego i przedniej kory zakrętu, specyficznych obszarach mózgu szlaku nagrody, po początkowym spożyciu sacharozy przez pięć świnek miniaturowych, zgodnie z endogennym uwalnianiem opioidów. Poprzednie badania wykazały, że smaczne jedzenie może prowadzić do poczucia przyjemności38 stymulując uwalnianie opioidów. Po 12 dniach dostępu do sacharozy zaobserwowaliśmy zmniejszenie [11C] wiązanie karfentanylu, które ma kilka możliwych wyjaśnień39 w tym endogenne uwalnianie opioidów i wiązanie z μOR, internalizacja μOR w wyniku zwiększonego wiązania opioidów oraz zwiększona aktywacja receptora DA D2 / 3 prowadząca do heterologicznego odczulania μOR40.
Na poparcie obecnych ustaleń [11C] badania karfentanylu u pacjentów z bulimią41otyłość42,43,44i zaburzenia objadania się45, pokazują zmniejszoną dostępność receptorów. Są to jednak stany przewlekłe, podczas gdy świnki miniaturowe otrzymywały sacharozę tylko przez 12 dni. W badaniu ostrych zachowań żywieniowych u zdrowych mężczyzn karmienie prowadziło do silnego i powszechnego endogennego uwalniania opioidów w mózgu, zarówno w obecności, jak i bez hedonii, co sugeruje, że uwalnianie opioidu odzwierciedla reakcje metaboliczne i homeostatyczne, a także hedoniczne25. To badanie, wraz z innym, które zobrazowało pacjentów po płynnym posiłku o smaku czekoladowym44, jest bezpośrednio związany z ostrym badaniem pięciu świnek miniaturowych po pierwszej ekspozycji na sacharozę, ale różni się od podchronicznego badania ekspozycji na sacharozę przez 12 dni, w którym zmniejszona dostępność receptora najprawdopodobniej odzwierciedla powtarzające się nadmierne pobudzenie i jednoczesne zmniejszenie regulacji μOR.
Kora przedczołowa jest ważna przy podejmowaniu decyzji i przypisywaniu wartości przedmiotom, dlatego też μOR w korze przedczołowej może być odpowiedzialny za zmienioną ocenę zasolenia żywności, co może zwiększać uzależniający potencjał żywności. Stwierdziliśmy zmniejszone wiązanie w korze przedczołowej, zgodnie z wcześniejszymi badaniami wykazującymi, że dieta wysokotłuszczowa zmniejsza poziomy μOR mRNA w korze przedczołowej46 a ten wlew agonisty μOR do kory przedczołowej zwiększa spożycie słodkiej żywności47. Ponownie pojawia się jednak kwestia, czy dieta wysokotłuszczowa jest bardziej chronicznym stanem, który bardziej prawdopodobne jest pośredniczenie w regulacji receptora w porównaniu z krótkoterminowym schematem karmienia sacharozą, co sugeruje przedłużone uwalnianie endogennych opioidów, które wypierają znacznik karfentanil związany z μOR , nawet po 12 dniach sacharozy.
DA była zaangażowana w nagrody zarówno od narkotyków, jak i za zachowanie. Stwierdzono, że przewlekłe używanie kokainy hamuje sygnalizację DA48. Poziomy receptorów DA D1 i D2 / 3 są zmieniane przez nikotynę w mózgu świni49oraz u zwierząt z rzędu ssaków naczelnych z historią nadużywania kokainy50, co jest zgodne z obniżoną regulacją receptorów D2 / 3 w mózgach osób uzależnionych od kokainy51,52. Jeśli chodzi o nadużywanie narkotyków, wykazano, że sacharoza reguluje w górę receptory DA D119 i zwiększ wydanie DA53, wzmacniając rolę DA w „pragnieniu” w stosunku do smacznego jedzenia. Wcześniejsze badania PET wykazały zmniejszenie dostępności prążkowia receptora DA D2 / 3 w chorobliwej otyłości w porównaniu do średniej masy ciała54,55, podobny pod względem wielkości u pacjentów uzależnionych od narkotyków56oraz u zwierząt z modelami otyłości57. W badaniach na gryzoniach powalenie receptora D2 / 3 w prążkowiu sprzyja rozwojowi kompulsywnego poszukiwania pokarmu u szczurów z dostępem do smacznego pokarmu57.
Nasze obserwacje zmniejszonej dostępności receptora D2 / 3 u świni mogą wskazywać na podwyższony poziom DA w odpowiedzi na bodziec motywacyjny związany z przyjmowaniem sacharozy, ponieważ DA jest uwalniany w ramach braku środków odurzających i innych przyjemnych czynności52,58,59,60. Ponieważ świnie znieczulono podczas obrazowania i nie otrzymały sacharozy w ciągu 24 godzin, obniżone D2 / 3 BPND bardziej prawdopodobne jest odzwierciedlenie zmniejszenia liczby receptorów w odpowiedzi na przedłużony wzrost uwalniania DA w każdym z 12 dni dostępu do sacharozy. Zmniejszenie może podnieść progi nagrody dla mózgu, związane z regulacją w dół prążkowatych receptorów DA D2. Może to tłumaczyć zwiększoną podatność na nadużywanie narkotyków obserwowaną we wcześniejszych badaniach szczurów przejadających się sacharozą, która doprowadziła do uczulenia krzyżowego na kokainę, nadaktywność po niskiej dawce amfetaminy, zwiększone spożycie alkoholu przy powstrzymywaniu się od sacharozy oraz tolerancję na przeciwbólowe działanie opiatów6.
Wcześniejsze badanie otyłości u minipig Göttingen zidentyfikowało zmniejszony mózgowy przepływ krwi w jądrze półleżącym, brzusznym obszarze nakrywkowym (VTA) i korze przedczołowej, z tomografią komputerową emisji pojedynczego fotonu (SPECT) mózgu61. Zgodnie z tymi odkryciami, zaobserwowaliśmy zmniejszone wiązanie DA D2 / 3 w regionie brzuszno-mózgowym zawierającym jądro półleżące i w korze przedczołowej. Pozakomórkowe poziomy DA są 3-krotnie zwiększone w jądrze półleżącym po spożyciu sacharozy u swobodnie poruszających się szczurów poddawanych mikrodializie62. U zwierząt zależnych od sacharozy powtarzane przyjmowanie sacharozy może prowadzić do uwolnienia DA z powłoki jądra półleżącego63. Zwierzęta karmione ograniczoną dietą z ograniczonym dostępem do sacharozy miały niższe wiązanie receptora DA D2 w skorupie jądra półleżącego i prążkowiu grzbietowym64. Ograniczone diety wysokotłuszczowe i sacharozowe mogą prowadzić do trwałego obniżenia poziomu mRNA receptora D1 i D2 w jądrze półleżącym65. Badanie mikrodializy dotyczące efektów smacznego jedzenia ujawniło zwiększone uwalnianie DA w jądrze półleżącym i korze przedczołowej, gdy pokarm był nadal uważany za nowy; gdy szczury przyzwyczaiły się do nowego pokarmu, zwiększone uwalnianie zostało stępione w jądrze półleżącym, ale nie w korze przedczołowej66. Zróżnicowana podatność na przyzwyczajenie i uwarunkowanie aktywności w dwóch regionach może tłumaczyć większy wzrost obserwowany w korze przedczołowej niż w jądrze półleżącym świnek miniaturowych narażonych na tę samą smakowitą substancję, która straciła nowość po dwunastu dniach. Ponieważ jednak nie wyobrażaliśmy sobie miniaturowych świnek z [11C] raclopryd po pierwszym podaniu sacharozy, wyjaśnienie to jest spekulacyjne.
Kora przedczołowa moduluje funkcję wykonawczą, podejmowanie decyzji i samokontrolę67. Dysfunkcjonalna neuroprzekaźnictwo DA w korze przedczołowej zaburza modulację przetwarzania nagrody, sugerując upośledzoną funkcję wykonawczą i umiejętności decyzyjne u osób otyłych68,69. Co więcej, badanie PET na ludziach korelowało obniżony metabolizm kory czołowej ze zmniejszonym wiązaniem prążkowia D2 w otyłości70. Tutaj znajdujemy zmniejszoną dostępność receptora D2 / 3 w korze przedczołowej, w tym w korze oczodołowo-czołowej świń poddanych reżimowi sacharozy.
Neurony dopaminergiczne VTA wysyłają projekcje do hipokampa i ciała migdałowatego, gdzie wspierają zachowania podobne do nawyków71 i pośredniczy w kodowaniu i wyszukiwaniu warunkowania w narkotyki72,73 i wskazówki żywnościowe74,75. Obrazowanie ludzkiego mózgu wykazało aktywację hipokampa w odpowiedzi na głód i smak jedzenia76. Zgodnie z naszymi ustaleniami dotyczącymi zmniejszonej dostępności receptora D2 / 3 w hipokampie i ciele migdałowym w odpowiedzi na sacharozę, mapowanie ludzkiego mózgu za pomocą [18F] fallypryd wykazał indukowane przez kokainę uwalnianie DA w ciele migdałowatym i hipokampie77. W mózgach gryzoni ekspozycja na kokainę spowodowała uwolnienie DA w ciele migdałowatym78, a zmiany poziomów DA ciała migdałowatego wpłynęły na wywołane przez wskazówki zachowania związane z poszukiwaniem kokainy79.
W badaniu osób otyłych związek między dostępnością D2 / 3 a μOR, o którym wiadomo, że występuje w obszarach prążkowanych osób szczupłych, został zakłócony w brzusznym prążkowiu80. Porównaliśmy wartości BPND z dwóch znaczników do sprawdzenia, czy dane odtwarzają ten efekt. W przeciwieństwie do szczupłych ludzi, obecne mózgi świń nie miały korelacji między wartościami BPND z dwóch znaczników, na początku lub po ekspozycji na sacharozę. Następnie sprawdziliśmy, czy zwierzęta z największym spadkiem wiązania racloprydu znacznikowego miałyby również największy spadek wiązania karfentanylu znacznika, ale zamiast tego znaleźliśmy ujemną korelację w uśrednionych regionach pozastriatalnych, co sugeruje, że zwierzęta o największej zmianie potencjału wiązania raclopryd znacznika miał najniższą zmianę potencjału wiązania karfentanylu znacznika. Odwrotna zależność między zmianami sugeruje, że wpływ spożycia sacharozy na dostępność odpowiednich receptorów jest regulowany w przeciwnych kierunkach. Wiadomo, że nadmierne spożywanie smacznego jedzenia lub narkotyków może być spowodowane chęcią lub upodobaniem, lub jednym i drugim60,81. Możliwe jest, że wielkość pożądania napędzanego przez dopaminę neguje wielkość lubienia napędzanego przez opioidy lub odwrotnie. Ostatnie dowody wskazują na role GABAA receptory w VTA i cholinergiczne zakończenia w prążkowiu i ewentualnie korze, które działają jako przełączniki między mechanizmami działania opioidów zależnymi od dopaminy i niezależnymi od dopaminy82,83 co może tłumaczyć wzajemność efektów dopaminowych i opioidowych w określonych tutaj obszarach pozatratowych świń.
Wadą PET, również u stosunkowo dużych zwierząt, jest ograniczona rozdzielczość przestrzenna tomografii, która wpływa na wyniki z małych obszarów mózgu zaangażowanych w zachowania związane z jedzeniem. Jednak pomimo tych obaw [11Wiązanie C] raclopride poprzednio rejestrowano zarówno w obszarach prążkowia, jak i poza nim84,85,86,87. Sposób użycia [11C] raclopryd do znakowania tego samego typu receptorów nie budzi obaw o potencjalne różnice powinowactwa, które mogą wpływać na stosowanie oddzielnych znaczników dla tych samych receptorów w różnych regionach. Ostatnie badania obejmowały zapisy dotyczące pozastriatalnego wiązania [11C] raclopride. Alakurtti i wsp. stwierdzono dobrą odtwarzalność miar wiązania racloprydu prążkowia w prążkowiu, z dobrą lub umiarkowaną odtwarzalnością w korze85. W późniejszym badaniu Svensson i wsp. omówiono kilka kwestii wpływających na korzystanie z [11C] raclopryd jako marker pozastriatalnych receptorów D2 / 3 w badaniu na zdrowych ludziach, w tym słabej odtwarzalności w korze mózgowej i ograniczonego spadku pozastriatalnego wiązania w korze czołowej w odpowiedzi na czynnik blokujący D2 / 388. Porównanie testu-testu wykazało zmienność 4–7% w prążkowiu i 13–59% w obszarach korowych, ale czas między badaniami wynosił średnio 20 dni, w przeciwieństwie do bardziej pouczających 1–2 dni większości badań. Wiele czynników w życiu tych osób mogło mieć czas, aby wpłynąć na wyniki. Rzeczywiście, pokazujemy tutaj, że samo dodanie spożycia sacharozy do porannej rutyny przez 12 dni mogło mieć wpływ na środki wiążące uzyskane dwa tygodnie później. Inne czynniki, tak powszechne jak granie w gry wideo, zakupy, wchodzenie w nowe romantyczne relacje i aktywność seksualną, używanie narkotyków lub zmiana diety i ćwiczeń fizycznych, mogą wpływać na pozapriatrialne poziomy dopaminy z potencjalnym dużym zróżnicowaniem zbiorów danych. Obecne badanie u świnek miniaturowych wprowadziło dobrze kontrolowaną konfigurację, a jedyną zmienną jest brak lub obecność sacharozy w diecie. W tym kontekście dane z siedmiu zwierząt wykazywały wystarczająco niską zmienność w odpowiednich regionach pozastriatalnych, aby zidentyfikować statystycznie istotne zmniejszenie wiązania w odpowiedzi na sacharozę.
Ograniczeniem obecnego badania jest stosowanie środków znieczulających wymaganych do zapewnienia unieruchomienia podczas in vivo obrazowanie zwierząt. Skutki określonych środków znieczulających i ich interakcje z lekami lub innymi interwencjami mogą zakłócać wiązanie radioligandów89,90. Ketamina jest lekiem przeciw glutaminianergicznym o szybkim działaniu przeciwdepresyjnym w dawkach pod znieczulających91,92,93, które nie zmniejszają prążkowia [11C] wiązanie racloprydu u ludzi94. Jednak stwierdzono, że S-ketamina zmniejsza dostępność wiązania receptorów dopaminy D2 / 3 w prążkowiu przytomnych przytomnych zwierząt z rzędu naczelnych95. Izofluran jest powszechnym środkiem znieczulającym u zwierząt PET. W poprzednich badaniach stwierdziliśmy nagromadzenie prążkowia [11C] SCH23390, radioligand receptorów dopaminy D1 ma być znacznie wyższy u świnek miniaturowych znieczulonych raczej izofluranem niż propofolem, co sugeruje podatność neurotransmisji dopaminergicznej na działanie znieczulenia96. W bieżącym badaniu wszystkie świnki miniaturowe zostały sfotografowane w obu punktach czasowych pod premedykacją ketaminą i znieczuleniem izofluranem, dzięki czemu obecne porównania są ważne.
Wnioski
Nadmierne spożywanie smacznego jedzenia może zarówno powodować uzależnienie, jak i być jego skutkiem, a otyłość ma bezpośrednie konsekwencje dla zdrowia. Przetestowaliśmy twierdzenie, że opioidy i dopamina pośredniczą w nagrodach, ważnych zarówno dla przeżycia, jak i nadużywania narkotyków. Świnki miniaturowe z przerywanym dostępem do roztworu sacharozy przez 12 kolejnych dni wykazały zmniejszoną dostępność receptorów dopaminy D2 / 3 i μ-opioidów w obszarach prążkowia i pozastriatalnych mózgu, co sugeruje, że pokarmy bogate w sacharozę wpływają na obwody wynagrodzeń w mózgu w sposób podobny do tych obserwowanych podczas uzależnień są konsumowane. Początkowa jednorazowa ekspozycja na sacharozę była zgodna z uwalnianiem opioidów w regionach mózgu aktywnych w nagrodę. Zmiany dostępności opioidów i dopaminy wyjaśniają uzależniający potencjał sacharozy spożywanej w nadmiarze.
Materiały i Metody
Etyka zwierząt
Badanie zostało zatwierdzone i uregulowane przez duński inspektorat ds. Doświadczeń na zwierzętach, a wszystkie doświadczenia przeprowadzono zgodnie z dyrektywą Parlamentu Europejskiego i Rady 2010/63 / UE w sprawie ochrony zwierząt wykorzystywanych do celów naukowych oraz wytycznymi ARRIVE. Wykorzystaliśmy siedem czternastomiesięcznych miniaturowych świnek z Göttingen (Ellegaard, Dalmose, Dania). Świnki miniaturowe otrzymywały dietę granulowaną (6 dl, 2 razy dziennie, Special Dietts Services, Aarhus, Dania) z dostępną wodą z kranu ad libitum. Temperatura otoczenia wynosiła 20–22 ° C, wilgotność względna 50–55%, a powietrze zmieniano osiem razy co godzinę.
Przerywane spożycie sacharozy
Zobrazowaliśmy siedem miniaturowych świń z [11C] raclopopride i [11C] karfentanyl na początku badania i ponownie jeden dzień po 12 kolejnych dniach ekspozycji na wodę sacharozową. Ekspozycja na sacharozę składała się z jednej godziny dostępu do wody (sacharozy, Dansukker, Kopenhaga, Dania) (500 gramów sacharozy w 2 litrach wody) dziennie przez okres 12 dni. Rejestrowano ilość spożycia sacharozy i wszystkie świnki miniaturowe spożywały 2 litry każdego dnia. Zobrazowaliśmy również pięć takich samych świnek miniaturowych z [11C] karfentanyl, 30 minut po pierwszym dostępie do sacharozy, w celu zbadania ostrego uwalniania opioidów.
Świnie miniaturowe zyskały średnio 13.6% masy ciała z 25.4 kg (± 0.73 SEM) na początku badania do 28.9 kg (± 0.69 SEM) po 12-dniowej ekspozycji na sacharozę, co było istotnie wyższe (jednostronny test t, p < 0.001) niż wzrosty obserwowane w próbie kontrolnych świnek miniaturowych uzyskanych we wcześniejszych badaniach, gdzie masy ciała wzrosły średnio tylko o 4.9% w tym samym okresie rozwojowym.
Obrazowanie PET mózgu
Poszczymy świnie przez noc z wolnym dostępem do wody przed obrazowaniem. Mamy wstępnie leczone i znieczulone świnki miniaturowe, jak opisano wcześniej97 i umieścił je na wznak w urządzeniu PET / CT (Siemens Biograph 64 Truepoint PET). Przed każdym akwizycją PET wykonaliśmy skan CT z małą dawką w celu określenia anatomicznej definicji i korekcji tłumienia danych emisji PET. Podaliśmy dożylnie [11C] raclopryd na początku (360 ± 18 MBq, aktywność właściwa 77 ± 76 GBq / μmol, wstrzyknięta masa 0.12 ± 0.08 μg / kg) i po 12 dniach sacharozy (374 ± 54 MBq, aktywność właściwa 127 ± 85 GBq / μmol, wstrzyknięta masa 0.06 ± 0.05 μg / kg) i [11C] karfentanyl na początku (377 ± 43 MBq, aktywność właściwa 311 ± 195 GBq / μmol, wstrzyknięta masa 0.03 ± 0.02 μg / kg) i po 12 dniach sacharozy (337 ± 71 MBq, aktywność właściwa 177 ± 157 GBq / μmol, wstrzyknięta masa 0.06 ± 0.08 μg / kg) przez żyłę uszną, w 10 ml soli fizjologicznej, podczas pierwszej minuty 90-minutowego skanu. Zrekonstruowaliśmy dane PET przy użyciu TrueX 3D OSEM (3 iteracje, 21 podzbiorów), macierzy 256 × 256 × 109 i 2-mm filtr Gaussa, przy użyciu struktury czasowej 5 × 60, 3 × 300, 4 × 600 , 2 × 900 sekund (łącznie 14 klatek, 90 minut). Na początku i po 12 dniach sacharozy, świnki miniaturowe były obrazowane za pomocą obu znaczników wstrzykniętych w odstępie co najmniej 100 minut, ze względu na okres półtrwania [11C] Wskaźniki PET. Po zakończeniu ostatniej sesji PET uśmierciliśmy świnki miniaturowe w głębokim znieczuleniu przez dożylne przedawkowanie pentobarbitalu (100 mg / kg).
Analizy i statystyki ilościowe
Wykonaliśmy kroki przetwarzania wstępnego przy użyciu PMOD 3.7 (PMOD Technologies Ltd, Zurych, Szwajcaria). Aby zdefiniować parametry transformacji stereotaktycznej na podstawie uśrednionych czasowo obrazów PET, wykorzystaliśmy szablony specyficzne dla ligandów. Zastosowaliśmy wygenerowane macierze transformacji i pola wypaczenia do odpowiednich dynamicznych szeregów czasowych PET. Wygenerowaliśmy obrazy parametryczne z [11C] potencjał wiązania raclopridu (BPND) za pomocą wieloliniowej metody tkanki odniesienia Ichise i współpracowników98. Stworzyliśmy niestandardową maskę móżdżku, która wykluczała robaki, aby uzyskać promieniotwórczość tkanki móżdżku w czasie w regionie o znikomej gęstości receptora DA D2 / 3. Wygenerowaliśmy obrazy parametryczne z [11C] karfentanyl z zastosowaniem modelu tkanki odniesienia Logana99,100 z t * = 30 min. Studia [11Wiązanie C] karfentanylu w ludzkim mózgu wykorzystało korę potyliczną jako region odniesienia36; jednak u świni, zgodnie z krzywymi czas-aktywność, wiązanie nieodwracalne było niższe w móżdżku niż w korze potylicznej, zgodnie z wynikami badań autoradiograficznych na szczurach101. Dlatego w bieżącym badaniu wybraliśmy móżdżek jako region odniesienia.
Analiza statystyczna
Poddaliśmy mapy analizie wokselowej za pomocą statystycznego mapowania nieparametrycznego (SnPM 13.01, http://warwick.ac.uk/snpm) Przybornik SPM, który wykorzystuje nieparametryczną teorię permutacji w celu zapewnienia ram dla wnioskowania statystycznego, które to podejście dobrze sprawdza się w przypadku małych próbek ze względu na ścisłą kontrolę wyników fałszywie dodatnich14 i stosowane zgodnie z wcześniejszym opisem102. Ekspert w dziedzinie neuroanatomii świń (DO) porównał uzyskane obrazy progowe do poziomu istotności 5% z wysokiej rozdzielczości atlantyckim minipigiem103,104 w celu zdefiniowania i oznakowania regionów obniżonego DA D2 / 3 i μOR BPND od stanu początkowego do stanu po sacharozie. Następnie przeprowadziliśmy analizę regionu zainteresowania (ROI) w celu wyodrębnienia BPND wartości określonych regionów, które mogą być interesujące na podstawie analizy SnPM, w tym prążkowia, jądro półleżące, wzgórze, ciało migdałowate, kora obręczy i kora przedczołowa. Nie przeprowadzono żadnych dodatkowych statystyk dotyczących analizy ROI, ponieważ stwierdzono, że regiony te były już znaczące przy użyciu SnPM.
Referencje
- 1.
Smyth, S. & Heron, A. Cukrzyca i otyłość: bliźniacze epidemie. Nat Med 12, 75 – 80, https://doi.org/10.1038/nm0106-75 (2006).
- 2.
Flegal, KM, Carroll, MD, Ogden, CL i Curtin, LR Częstość występowania i trendy w otyłości wśród dorosłych w Stanach Zjednoczonych, 1999–2008. JAMA 303, 235 – 241, https://doi.org/10.1001/jama.2009.2014 (2010).
- 3.
Davis, Kalifornia i wsp. Dopamina dla „chcących” i opioidy dla „lubić”: porównanie otyłych dorosłych z jedzeniem i bez jedzenia. Otyłość (srebrna wiosna) 17, 1220 – 1225, https://doi.org/10.1038/oby.2009.52 (2009).
- 4.
Drewnowski, A. Otyłość a środowisko żywności: gęstość energetyczna diety i koszty diety. Amerykański dziennik medycyny zapobiegawczej 27, 154 – 162, https://doi.org/10.1016/j.amepre.2004.06.011 (2004).
- 5.
Lenoir, M., Serre, F., Cantin, L. & Ahmed, SH Intensywna słodycz przewyższa kokainę. Jeden PUP 2, e698, https://doi.org/10.1371/journal.pone.0000698 (2007).
- 6.
Ahmed, S., Avena, NM, Berridge, KC, Gearhardt, A. & Guillem, K. In Neuronauka w 21 wieku (red. Phaff, DW) (Springer, 2012).
- 7.
Avena, NM, Gold, JA, Kroll, C. & Gold, MS Dalszy rozwój neurobiologii pożywienia i uzależnień: aktualizacja stanu nauki. Odżywianie 28, 341 – 343, https://doi.org/10.1016/j.nut.2011.11.002 (2012).
- 8.
Leyton, M.In Przyjemności mózgu (red. Kringelbach, ML & Berridge, KC) (Oxford University Press, 2010).
- 9.
Nathan, PJ i Bullmore, ET Od hedoniki smaku po motywację: centralne receptory opioidowe mu i zachowania związane z objadaniem się. Int J Neuropsychopharmacol 12, 995 – 1008, https://doi.org/10.1017/S146114570900039X (2009).
- 10.
Berridge, KC Nagroda żywnościowa: substraty mózgu do pożądania i sympatii. Neurobiologia i recenzje biobehawioralne 20, 1 – 25 (1996).
- 11.
Gjedde, A., Wong, DF, Rosa-Neto, P. & Cumming, P. Mapping neuroreceptors at work: o definicji i interpretacji potencjałów wiązania po 20 latach postępu. Int Rev Neurobiol 63, 1 – 20, https://doi.org/10.1016/S0074-7742(05)63001-2 (2005).
- 12.
Avena, NM, Bocarsly, ME & Hoebel, BG Zwierzęce modele objadania się cukrem i tłuszczem: związek z uzależnieniem od jedzenia i zwiększoną masą ciała. Metody Mol Biol 829, 351 – 365, https://doi.org/10.1007/978-1-61779-458-2_23 (2012).
- 13.
Jelsing, J. i wsp. Kora przedczołowa w mózgu świnki miniaturowej w Getyngi określona przez kryteria projekcji neuronowej i cytoarchitekturę. Brain Res Bull 70, 322 – 336, https://doi.org/10.1016/j.brainresbull.2006.06.009 (2006).
- 14.
Nichols, TE & Holmes, AP Nieparametryczne testy permutacji dla funkcjonalnego neuroobrazowania: elementarz z przykładami. Hum Brain Mapp 15, 1 – 25 (2002).
- 15.
Avena, NM, Rada, P. & Hoebel, BG Dowody na uzależnienie od cukru: behawioralne i neurochemiczne skutki przerywanego, nadmiernego spożycia cukru. Neurobiologia i recenzje biobehawioralne 32, 20 – 39, https://doi.org/10.1016/j.neubiorev.2007.04.019 (2008).
- 16.
Alonso-Alonso, M. i wsp. System nagradzania żywności: aktualne perspektywy i przyszłe potrzeby badawcze. Nutr Rev 73, 296 – 307, https://doi.org/10.1093/nutrit/nuv002 (2015).
- 17.
Figlewicz, DP, Bennett-Jay, JL, Kittleson, S., Sipols, AJ & Zavosh, A. Samo-podawanie sacharozy i aktywacja OUN u szczura. Am J Physiol Regul Integr Comp Physiol 300, R876-884, https://doi.org/10.1152/ajpregu.00655.2010 (2011).
- 18.
Tellez, LA i wsp. Oddzielne obwody kodują hedoniczne i odżywcze wartości cukru. Neurobiologia przyrody 19, 465 – 470, https://doi.org/10.1038/nn.4224 (2016).
- 19.
Colantuoni, C. i wsp. Nadmierne spożycie cukru zmienia wiązanie z receptorami dopaminy i mu-opioidów w mózgu. Neuroreport 12, 3549 – 3552 (2001).
- 20.
Pert, CB, Kuhar, MJ & Snyder, SH Receptor opiatowy: lokalizacja autoradiograficzna w mózgu szczura. Proc Natl Acad Sci USA 73, 3729 – 3733 (1976).
- 21.
Soderman, AR i Unterwald, EM Nagroda kokainowa i nadpobudliwość u szczura: miejsca modulacji receptora opioidowego mu. Neuroscience 154, 1506 – 1516, https://doi.org/10.1016/j.neuroscience.2008.04.063 (2008).
- 22.
Ward, SJ, Martin, TJ & Roberts, DC Beta-funaltreksamina wpływa na samopodawanie kokainy u szczurów, które reagują zgodnie z progresywnym współczynnikiem wzmocnienia. Farmakologia, biochemia i zachowanie 75, 301 – 307 (2003).
- 23.
Schroeder, JA i wsp. Rola receptorów opioidowych mu w indukowanej przez kokainę aktywności, uczuleniu i nagrodzie u szczura. Psychopharmacology 195, 265 – 272, https://doi.org/10.1007/s00213-007-0883-z (2007).
- 24.
Tang, XC, McFarland, K., Cagle, S. & Kalivas, PW Przywrócenie wywołane kokainą wymaga endogennej stymulacji receptorów opioidowych mu w brzusznej części bladej. The Journal of neuroscience: oficjalne czasopismo Society for Neuroscience 25, 4512 – 4520, https://doi.org/10.1523/JNEUROSCI.0685-05.2005 (2005).
- 25.
Tuulari, JJ i wsp. Karmienie uwalnia endogenne opioidy u ludzi. J Neurosci 37, 8284 – 8291, https://doi.org/10.1523/JNEUROSCI.0976-17.2017 (2017).
- 26.
Smith, KS & Berridge, KC Opioidowy obwód limbiczny dla nagrody: interakcja między hedonicznymi punktami gorącymi jądra półleżącego i brzusznej blady. J Neurosci 27, 1594 – 1605, https://doi.org/10.1523/JNEUROSCI.4205-06.2007 (2007).
- 27.
Pecina, S. & Berridge, KC Miejsce opioidowe w skorupie jądra półleżącego pośredniczy w jedzeniu i hedonicznym „lubieniu” pożywienia: mapa oparta na mikroiniekcjach pióropuszach Fos. brain Res 863, 71 – 86 (2000).
- 28.
Zhang, M. & Kelley, AE Spożycie sacharyny, soli i roztworów etanolu jest zwiększane przez wlew agonisty opioidowego mu do jądra półleżącego. Psychopharmacology 159, 415 – 423, https://doi.org/10.1007/s00213-001-0932-y (2002).
- 29.
Zhang, M., Gosnell, BA i Kelley, AE Spożycie wysokotłuszczowej żywności jest selektywnie zwiększane poprzez stymulację receptora opioidowego mu w jądrze półleżącym. Czasopismo farmakologiczne i eksperymentalne 285, 908 – 914 (1998).
- 30.
Levine, AS, Weldon, DT, Grace, M., Cleary, JP & Billington, CJ Naloxone blokują tę część karmienia powodowaną słodkim smakiem u szczurów objętych ograniczeniami żywieniowymi. Am J Physiol 268, R 248–252 (1995).
- 31.
Glass, MJ, Billington, CJ & Levine, AS Opioidy i spożycie pokarmu: rozproszone funkcjonalne ścieżki neuronowe? Neuropeptydy 33, 360 – 368, https://doi.org/10.1054/npep.1999.0050 (1999).
- 32.
Fantino, M., Hosotte, J. & Apfelbaum, M. Antagonista opioidów, naltrekson, zmniejsza preferencję dla sacharozy u ludzi. Am J Physiol 251, R91-96, https://doi.org/10.1152/ajpregu.1986.251.1.R91 (1986).
- 33.
Arbisi, PA, Billington, CJ & Levine, AS Wpływ naltreksonu na wykrywanie smaku i próg rozpoznawania. Apetyt 32, 241 – 249, https://doi.org/10.1006/appe.1998.0217 (1999).
- 34.
Drewnowski, A., Krahn, DD, Demitrack, MA, Nairn, K. & Gosnell, BA Naloxone, bloker opiatów, zmniejsza spożycie słodkich, wysokotłuszczowych pokarmów u otyłych i chudych kobiet objadających się. Am J Clin Nutr 61, 1206 – 1212 (1995).
- 35.
Wassum, KM, Ostlund, SB, Maidment, NT i Balleine, BW Wyraźne obwody opioidowe określają smakowitość i pożądanie satysfakcjonujących wydarzeń. Proc Natl Acad Sci USA 106, 12512 – 12517, https://doi.org/10.1073/pnas.0905874106 (2009).
- 36.
Colasanti, A. i wsp. Endogenne uwalnianie opioidów w układzie nagrody ludzkiego mózgu indukowane przez ostre podanie amfetaminy. Biol Psychiatry 72, 371 – 377, https://doi.org/10.1016/j.biopsych.2012.01.027 (2012).
- 37.
Mick, ja. i wsp. Indukowane przez amfetaminę endogenne uwalnianie opioidów w ludzkim mózgu wykryte za pomocą PET [11C] karfentanylu: replikacja w niezależnej kohorcie. Int J Neuropsychopharmacol, 1 – 6, https://doi.org/10.1017/S1461145714000704 (2014).
- 38.
Yeomans, MR & Gray, RW Peptydy opioidowe a kontrola ludzkiego zachowania pokarmowego. Neurobiologia i recenzje biobehawioralne 26, 713 – 728 (2002).
- 39.
Sprenger, T., Berthele, A., Platzer, S., Boecker, H. & Tolle, TR Czego się nauczyć in vivo opioidergiczne obrazowanie mózgu? Eur J Pain 9, 117 – 121, https://doi.org/10.1016/j.ejpain.2004.07.010 (2005).
- 40.
Unterwald, EM i Cuntapay, M. Interakcje dopaminy i opioidów w prążkowiu szczura: modulująca rola receptorów dopaminy D1 w transdukcji sygnału za pośrednictwem receptora opioidowego delta. Neuropharmacology 39, 372 – 381 (2000).
- 41.
Bencherif, B. i wsp. Regionalne wiązanie receptora opioidowego mu w korze wyspowej jest zmniejszone w bulimii i koreluje odwrotnie z zachowaniem na czczo. Dziennik medycyny nuklearnej: oficjalna publikacja, Society of Nuclear Medicine 46, 1349 – 1351 (2005).
- 42.
Karlsson, HK i wsp. Otyłość jest związana ze zmniejszoną dostępnością opioidów mu, ale niezmienioną dostępnością receptora dopaminy D2 w mózgu. J Neurosci 35, 3959 – 3965, https://doi.org/10.1523/JNEUROSCI.4744-14.2015 (2015).
- 43.
Karlsson, HK i wsp. Utrata masy ciała po operacji bariatrycznej normalizuje mózgowe receptory opioidowe w chorobliwej otyłości. Mol Psychiatry 21, 1057 – 1062, https://doi.org/10.1038/mp.2015.153 (2016).
- 44.
Burghardt, PR, Rothberg, AE, Dykhuis, KE, Burant, CF & Zubieta, JK Endogenne mechanizmy opioidowe są implikowane w otyłości i utracie wagi u ludzi. J Clin Endocrinol Metab 100, 3193 – 3201, https://doi.org/10.1210/jc.2015-1783 (2015).
- 45.
Majura, J. i wsp. Neurotransmisja dopaminy i opioidów w uzależnieniach behawioralnych: Porównawcze badanie PET w zakresie patologicznego hazardu i upijania się. Neuropsychopharmacology 42, 1169 – 1177, https://doi.org/10.1038/npp.2016.265 (2017).
- 46.
Vucetic, Z., Kimmel, J. & Reyes, TM Przewlekła dieta wysokotłuszczowa napędza poporodową epigenetyczną regulację receptora opioidowego mu w mózgu. Neuropsychofarmakologia: oficjalna publikacja American College of Neuropsychopharmacology 36, 1199 – 1206, https://doi.org/10.1038/npp.2011.4 (2011).
- 47.
Mena, JD, Sadeghian, K. & Baldo, BA Indukcja hiperfagii i spożycia węglowodanów przez stymulację receptora opioidowego mu w określonych obszarach kory czołowej. The Journal of neuroscience: oficjalne czasopismo Society for Neuroscience 31, 3249 – 3260, https://doi.org/10.1523/JNEUROSCI.2050-10.2011 (2011).
- 48.
Park, K., Volkow, ND, Pan, Y. & Du, C. Przewlekła kokaina tłumi sygnalizację dopaminy podczas intoksykacji kokainą i zaburza równowagę sygnalizacji receptora D1 nad D2. The Journal of neuroscience: oficjalne czasopismo Society for Neuroscience 33, 15827 – 15836, https://doi.org/10.1523/JNEUROSCI.1935-13.2013 (2013).
- 49.
Cumming, p. i wsp. Wpływ ostrej nikotyny na hemodynamikę i wiązanie racloprydu [11C] z receptorami dopaminy D2,3 w mózgu świni. NeuroImage 19, 1127 – 1136 (2003).
- 50.
Moore, RJ, Vinsant, SL, Nader, MA, Porrino, LJ & Friedman, DP Wpływ samopodawania kokainy na receptory dopaminy D2 u małp rezus. Synapse 30, 88–96, doi:10.1002/(SICI)1098-2396(199809)30:1<88::AID-SYN11>3.0.CO;2-L (1998).
- 51.
Volkow, ND i wsp. Wskazówki kokainowe i dopamina w prążkowiu grzbietowym: mechanizm głodu uzależnienia od kokainy. The Journal of neuroscience: oficjalne czasopismo Society for Neuroscience 26, 6583 – 6588, https://doi.org/10.1523/JNEUROSCI.1544-06.2006 (2006).
- 52.
Wong, DF i wsp. Zwiększone obłożenie receptorów dopaminy w ludzkim prążkowiu podczas wywoływanego przez kaszel głodu kokainy. Neuropsychopharmacology 31, 2716 – 2727, https://doi.org/10.1038/sj.npp.1301194 (2006).
- 53.
Hajnal, A., Smith, GP i Norgren, R. Doustna stymulacja sacharozą zwiększa ilość półleżącą dopaminy u szczurów. Am J Physiol Regul Integr Comp Physiol 286, R31-37, https://doi.org/10.1152/ajpregu.00282.2003 (2004).
- 54.
Volkow, ND, Fowler, JS, Wang, GJ, Baler, R. & Telang, F. Obrazowanie roli dopaminy w narkomanii i uzależnieniu. Neuropharmacology 56(Suplement 1), 3–8, https://doi.org/10.1016/j.neuropharm.2008.05.022 (2009).
- 55.
Wang, GJ i wsp. Dopamina mózgowa i otyłość. Lancet 357, 354 – 357 (2001).
- 56.
Wang, GJ, Volkow, ND, Thanos, PK i Fowler, JS Podobieństwo między otyłością a uzależnieniem od narkotyków oceniane za pomocą obrazowania neurofunkcjonalnego: przegląd koncepcji. Dziennik chorób uzależniających 23, 39 – 53, https://doi.org/10.1300/J069v23n03_04 (2004).
- 57.
Johnson, PM i Kenny, PJ Dopaminowe receptory D2 w dysfunkcji nagrody podobnej do uzależnienia i kompulsywnym jedzeniu u otyłych szczurów. Neurobiologia przyrody 13, 635 – 641, https://doi.org/10.1038/nn.2519 (2010).
- 58.
Berridge, KC i Kringelbach, ML Neuronauka afektywna przyjemności: nagroda u ludzi i zwierząt. Psychopharmacology 199, 457 – 480, https://doi.org/10.1007/s00213-008-1099-6 (2008).
- 59.
Berridge, KC i Kringelbach, ML Pleasure systems w mózgu. Neuron 86, 646 – 664, https://doi.org/10.1016/j.neuron.2015.02.018 (2015).
- 60.
Schultz, W. Przewidywalny sygnał nagrody neuronów dopaminowych. J Neurophysiol 80, 1 – 27, https://doi.org/10.1152/jn.1998.80.1.1 (1998).
- 61.
Val-Laillet, D., Layec, S., Guerin, S., Meurice, P. & Malbert, CH Zmiany w aktywności mózgu po otyłości wywołanej dietą. Otyłość 19, 749 – 756, https://doi.org/10.1038/oby.2010.292 (2011).
- 62.
Hajnal, A. & Norgren, R. Accumbens dopaminowe mechanizmy spożycia sacharozy. brain Res 904, 76 – 84 (2001).
- 63.
Rada, P., Avena, NM & Hoebel, BG Codzienne objadanie się cukrem wielokrotnie uwalnia dopaminę w powłoce półleżącej. Neuroscience 134, 737 – 744, https://doi.org/10.1016/j.neuroscience.2005.04.043 (2005).
- 64.
Bello, NT, Lucas, LR i Hajnal, A. Powtarzający się dostęp sacharozy wpływa na gęstość receptora dopaminowego D2 w prążkowiu. Neuroreport 13, 1575 – 1578 (2002).
- 65.
Alsio, J. i wsp. Ekspresja genu receptora dopaminy D1 zmniejsza się w jądrze półleżącym po długotrwałej ekspozycji na smaczny pokarm i różni się w zależności od fenotypu otyłości wywołanego dietą u szczurów. Neuroscience 171, 779 – 787, https://doi.org/10.1016/j.neuroscience.2010.09.046 (2010).
- 66.
Bassareo, V. & Di Chiara, G. Różnicowy wpływ asocjacyjnych i niezespolonych mechanizmów uczenia się na reakcję przedczołowej i półleżącej transmisji dopaminy na bodźce pokarmowe u szczurów karmionych do woli. J Neurosci 17, 851 – 861 (1997).
- 67.
Volkow, ND, Wang, GJ, Tomasi, D. & Baler, RD Niesymetryczne obwody neuronalne w uzależnieniu. Curr Opin Neurobiol 23, 639 – 648, https://doi.org/10.1016/j.conb.2013.01.002 (2013).
- 68.
Brogan, A., Hevey, D. & Pignatti, R. Anoreksja, bulimia i otyłość: wspólne deficyty decyzyjne w sprawie Iowa Gambling Task (IGT). J Int Neuropsychol Soc 16, 711 – 715, https://doi.org/10.1017/S1355617710000354 (2010).
- 69.
Davis, C., Levitan, RD, Muglia, P., Bewell, C. & Kennedy, JL Deficyty decyzyjne i przejadanie się: model ryzyka otyłości. Obes Res 12, 929 – 935, https://doi.org/10.1038/oby.2004.113 (2004).
- 70.
Volkow, ND i wsp. Nisko dopaminowe receptory prążkowia D2 są związane z metabolizmem przedczołowym u osób otyłych: możliwe czynniki. NeuroImage 42, 1537 – 1543, https://doi.org/10.1016/j.neuroimage.2008.06.002 (2008).
- 71.
Lingawi, NW & Balleine, BW Jądro centralne Amygdala oddziałuje z prążkowiem grzbietowo-bocznym, regulując nabywanie nawyków. J Neurosci 32, 1073 – 1081, https://doi.org/10.1523/JNEUROSCI.4806-11.2012 (2012).
- 72.
Granta, S. i wsp. Aktywacja obwodów pamięci podczas wywoływanego przez pamięć głodu kokainy. Proc Natl Acad Sci USA 93, 12040 – 12045 (1996).
- 73.
Childress, AR i wsp. Aktywacja limbiczna podczas indukowanego wskazówką głodu kokainy. Am J Psychiatry 156, 11 – 18, https://doi.org/10.1176/ajp.156.1.11 (1999).
- 74.
Mahler, SV & Berridge, KC Czego i kiedy „chcieć”? Oparte na amigdali skupienie się na bodźcach motywacyjnych na cukrze i seksie. Psychopharmacology 221, 407 – 426, https://doi.org/10.1007/s00213-011-2588-6 (2012).
- 75.
Koob, GF & Volkow, ND Neurobiology of addiction: a neurocircuitry analysis. Lancet Psychiatry 3, 760 – 773, https://doi.org/10.1016/S2215-0366(16)00104-8 (2016).
- 76.
Haase, L., Cerf-Ducastel, B. & Murphy, C. Aktywacja korowa w odpowiedzi na czyste bodźce smakowe podczas fizjologicznych stanów głodu i sytości. NeuroImage 44, 1008 – 1021, https://doi.org/10.1016/j.neuroimage.2008.09.044 (2009).
- 77.
Fotos, A. i wsp. Indukowane przez kokainę uwalnianie dopaminy w ciele migdałowatym i hipokampie: badanie PET o wysokiej rozdzielczości [(1) (8) F] fallypride u uczestników uzależnionych od kokainy. Neuropsychopharmacology 38, 1780 – 1788, https://doi.org/10.1038/npp.2013.77 (2013).
- 78.
Weiss, F. i wsp. Kontrola zachowań związanych z poszukiwaniem kokainy za pomocą bodźców związanych ze stosowaniem narkotyków u szczurów: wpływ na odzyskiwanie wygasłych poziomów dopaminy w komórkach migdałowatych i jądrze półleżącym odpowiadających na operanty i zewnątrzkomórkowych. Proc Natl Acad Sci USA 97, 4321 – 4326 (2000).
- 79.
Berglind, WJ, Case, JM, Parker, MP, Fuchs, RA & See, RE Dopaminowy antagonizm receptora D1 lub D2 w obrębie podstawno-bocznego ciała migdałowatego w różny sposób zmienia nabywanie skojarzeń kokainowych niezbędnych do przywrócenia poszukiwania kokainy przez sygnał. Neuroscience 137, 699 – 706, https://doi.org/10.1016/j.neuroscience.2005.08.064 (2006).
- 80.
Tuominen, L. i wsp. Nieprawidłowa mezolimbiczna interakcja dopamina-opiat w otyłości. NeuroImage 122, 80 – 86, https://doi.org/10.1016/j.neuroimage.2015.08.001 (2015).
- 81.
Schultz, W. Behawioralne sygnały dopaminowe. Trendy Neurosci 30, 203 – 210, https://doi.org/10.1016/j.tins.2007.03.007 (2007).
- 82.
Ting, AKR & van der Kooy, D. Neurobiology of opiate motivation. Cold Spring Harb Perspect Med 2, https://doi.org/10.1101/cshperspect.a012096 (2012).
- 83.
Mamaligas, AA, Cai, Y. & Ford, CP Regulacja przekazywania receptorów dopaminowych D2 w prążkowiu przez receptory nikotynowe i opioidowe. Sci Rep 6, 37834, https://doi.org/10.1038/srep37834 (2016).
- 84.
Nomur, Y. i wsp. Związany z wiekiem spadek dostępności receptora dopaminy D2 / 3 mierzony racloprydem [C-11] w niestriatalnych regionach ludzkiego mózgu: Porównanie czterech metod. NeuroImage 41, T133 – T133, https://doi.org/10.1016/j.neuroimage.2008.04.101 (2008).
- 85.
Alakurtti, K. i wsp. Długoterminowa niezawodność testu prążkowia i pozastriatalna wiązania receptora D2 / 3 dopaminy: badanie z użyciem racloprydu [(11) C] i PET o wysokiej rozdzielczości. J Cereb Blood Flow Metab 35, 1199 – 1205, https://doi.org/10.1038/jcbfm.2015.53 (2015).
- 86.
Piccini, P., Pavese, N. & Brooks, DJ Endogenne uwalnianie dopaminy po prowokacjach farmakologicznych w chorobie Parkinsona. Ann Neurol 53, 647 – 653, https://doi.org/10.1002/ana.10526 (2003).
- 87.
Sawamoto, N. i wsp. Deficyty poznawcze i prążkowo-czołowe uwalnianie dopaminy w chorobie Parkinsona. Mózg 131, 1294 – 1302, https://doi.org/10.1093/brain/awn054 (2008).
- 88.
Svensson, JE i wsp. Ważność i rzetelność kwantyfikacji pozaoperatowej [(11) C] racloprydu w żywym ludzkim mózgu. NeuroImage, 116143, https://doi.org/10.1016/j.neuroimage.2019.116143 (2019).
- 89.
Tsukada, H. i wsp. Znieczulenie izofluranem zwiększa hamujące działanie kokainy i GBR12909 na transporter dopaminy: badania PET w połączeniu z mikrodializą w mózgu małpy. brain Res 849, 85 – 96 (1999).
- 90.
Hassoun, W. i wsp. Badanie PET wiązania raclopridu [11C] w prążkowiu u przytomnego kota: skutki znieczulenia i rola mózgowego przepływu krwi. Europejskie czasopismo medycyny nuklearnej i obrazowania molekularnego 30, 141 – 148, https://doi.org/10.1007/s00259-002-0904-4 (2003).
- 91.
Serafini, G., Howland, RH, Rovedi, F., Girardi, P. & Amore, M. Rola ketaminy w depresji opornej na leczenie: przegląd systematyczny. Curr Neuropharmacol 12, 444 – 461, https://doi.org/10.2174/1570159X12666140619204251 (2014).
- 92.
Berman, RM i wsp. Przeciwdepresyjne działanie ketaminy u pacjentów z depresją. Biol Psychiatry 47, 351 – 354 (2000).
- 93.
Browne, CA i Lucki, I. Przeciwdepresyjne działanie ketaminy: mechanizmy leżące u podstaw szybko działających nowych leków przeciwdepresyjnych. Front Pharmacol 4, 161, https://doi.org/10.3389/fphar.2013.00161 (2013).
- 94.
Alto, S. i wsp. Ketamina nie zmniejsza prążkowia wiązania receptora dopaminowego D2 u człowieka. Psychopharmacology 164, 401 – 406, https://doi.org/10.1007/s00213-002-1236-6 (2002).
- 95.
Hashimoto, K., Kakiuchi, T., Ohba, H., Nishiyama, S. & Tsukada, H. Redukcja wiązania receptora dopaminowego D2 / 3 w prążkowiu po pojedynczym podaniu esketaminy, ale nie R-ketaminy: a PET badanie na przytomnych małpach. Eur Arch Psychiatry Clin Neurosci 267, 173 – 176, https://doi.org/10.1007/s00406-016-0692-7 (2017).
- 96.
Alstrup, AK i wsp. Wpływ znieczulenia i gatunków na pobieranie lub wiązanie radioligandów in vivo w minipig Getyngi. Międzynarodowe badania BioMed 2013, 808713, https://doi.org/10.1155/2013/808713 (2013).
- 97.
Lillethorup, TP i wsp. Wzdłużne monoaminergiczne obrazowanie PET przewlekłego hamowania proteasomów u świnek miniaturowych. Sci Rep 8, 15715, https://doi.org/10.1038/s41598-018-34084-5 (2018).
- 98.
Ichise, M., Toyama, H., Innis, RB i Carson, RE Strategie poprawy estymacji parametrów neuroreceptorów za pomocą analizy regresji liniowej. J Cereb Blood Flow Metab 22, 1271 – 1281, https://doi.org/10.1097/01.WCB.0000038000.34930.4E (2002).
- 99.
Logana, J. i wsp. Współczynniki objętości dystrybucji bez pobierania krwi z graficznej analizy danych PET. J Cereb Blood Flow Metab 16, 834 – 840, https://doi.org/10.1097/00004647-199609000-00008 (1996).
- 100.
Endres, CJ, Bencherif, B., Hilton, J., Madar, I. & Frost, JJ Quantification of brain opioid receptor with [11C] carfentanyil: reference-fabric methods. Nucl Med Biol 30, 177 – 186 (2003).
- 101.
Panksepp, J. & Bishop, P. An autoradiograficzna mapa wiązania (3H) diprenorfiny w mózgu szczura: skutki interakcji społecznej. Brain Res Bull 7, 405 – 410 (1981).
- 102.
Landau, AM i wsp. Stymulacja elektrowstrząsowa w różny sposób wpływa na wiązanie [(11) C] MDL100,907 z korowymi i podkorowymi receptorami 5HT2A w mózgu świni. J Psychopharmacol, 269881119836212, https://doi.org/10.1177/0269881119836212 (2019).
- 103.
Bjarkam, CR, Glud, AN, Orlowski, D., Sorensen, JCH & Palomero-Gallagher, N. The telencephalon of the Gettingen miniipig, cytoarchitecture and cortical surface anatomy. Brain Struct Funct 222, 2093 – 2114, https://doi.org/10.1007/s00429-016-1327-5 (2017).
- 104.
Orlowski, D., Glud, AN, Palomero-Gallagher, N., Sorensen, JCH & Bjarkam, CR Online histological atlas of the Gettingen minipig brain. Heliyon 5, e01363, https://doi.org/10.1016/j.heliyon.2019.e01363 (2019).
Podziękowania
Badanie sfinansowało Uniwersytet Aarhus „Grant na rozwój projektu AU Ideas” dla AML. Jesteśmy wdzięczni za wsparcie techniczne personelu Centrum PET w Szpitalu Uniwersyteckim w Aarhus i Farmy Uniwersyteckiej w Aarhus za pomoc w leczeniu zwierząt. Dziękujemy profesorowi Mortenowi Kringelbachowi, profesorowi Jørgenowi Scheel-Krugerowi i profesorowi nadzwyczajnemu Arne Møllerowi za pomoc w rozpoczęciu tych badań.
Deklaracje etyczne
Konkurencyjnymi interesami
Autorzy nie deklarują konkurencyjnych interesów.
Dodatkowe informacje
Nota wydawcy Springer Nature pozostaje neutralny w odniesieniu do roszczeń jurysdykcyjnych w opublikowanych mapach i powiązaniach instytucjonalnych.
Prawa i uprawnienia
Open Access Ten artykuł jest objęty licencją Creative Commons Uznanie autorstwa 4.0, która zezwala na używanie, udostępnianie, adaptację, dystrybucję i reprodukcję na dowolnym nośniku lub w dowolnym formacie, o ile odpowiednio przypisujesz autorowi oryginalnemu (autorom) i źródłu, link do licencji Creative Commons i wskaż, czy dokonano zmian. Obrazy lub inne materiały stron trzecich w tym artykule są objęte licencją Creative Commons tego artykułu, chyba że wskazano inaczej w linii kredytowej do materiału. Jeśli materiał nie jest objęty licencją Creative Commons, a zamierzone użycie nie jest dozwolone przez przepisy prawne lub przekracza dozwolone użycie, musisz uzyskać zgodę bezpośrednio od właściciela praw autorskich. Aby wyświetlić kopię tej licencji, odwiedź http://creativecommons.org/licenses/by/4.0/.