Disfuncția erectilă (DE) este frecventă odată cu îmbătrânirea. Anterior, tratamentul ED a fost oferit în principal de către urologi, dar aprobarea și utilizarea pe scară largă a inhibitorilor de fosfodiesteraza a permis medicilor de asistență medicală primară să ofere un tratament direcționat pentru ED. Deși studiile clinice mari, multicentrice au arătat eficacitatea și siguranța acestor medicamente, acestea sunt ineficiente la 30-35% dintre bărbați, pot provoca efecte secundare și nu îmbunătățesc patologia de bază. O înțelegere aprofundată a fiziologiei erectile și a cauzelor DE și un plan de tratament cuprinzător care abordează toți factorii contributivi pot fi mai eficiente decât managementul farmaceutic și pot îmbunătăți aspectele sănătății psihologice și fizice dincolo de problemele erectile.
Disfuncția erectilă (DE) – incapacitatea de a dezvolta și menține o erecție suficient de fermă pentru penetrare – este frecventă odată cu îmbătrânirea. Aproximativ 40% dintre bărbații în vârstă de 40 de ani și 70% dintre bărbații în vârstă de 70 de ani au o formă de DE.1 ED este asociată cu mai multe afecțiuni fizice, poate fi un precursor al bolilor metabolice sau vasculare și afectează sănătatea psihosocială. Inhibitorii de fosfodiesteraza de tip 5 (PDE5i) sunt cel mai frecvent tratament de primă linie pentru ED. Studiile clinice mari, multicentrice, au demonstrat eficacitatea și siguranța acestor medicamente; cu toate acestea, ele sunt ineficiente la 30-35% dintre pacienți,2 poate provoca reacții adverse și nu ameliorează patologia de bază. Tratamentul cuprinzător pentru ED care se concentrează pe toți factorii contributivi poate fi mai eficient decât managementul farmaceutic și poate îmbunătăți aspectele sănătății psihologice și fizice dincolo de problemele erectile.
DE apare din mecanisme complexe, multifactoriale, care implică sistemele nervos, vascular și endocrin. O revizuire de bază a anatomiei și fiziologiei erecțiilor va oferi un cadru pentru înțelegerea fiziopatologiei și rațiunea opțiunilor de tratament (Figura 1). Structura penisului constă din doi cilindri de țesut vascular (corpii cavernosi) care parcurg lungimea diafizei penisului împreună cu corpul spongios din jurul uretrei. Țesutul penian este inervat de aspectele autonome (simpatice și parasimpatice) și somatice (senzoriale și motorii) ale sistemului nervos periferic. Nervii simpatici provin din T11–L2 și sunt anti-erectili, controlând ejacularea și detumescitatea. Nervii parasimpatici provin din S2–S4 și sunt pro-erectili. Nervii simpatici și parasimpatici se îmbină pentru a forma nervi cavernoși care pătrund în corpurile cavernoase, corpul spongios și glandul penisului, reglând fluxul sanguin în timpul erecției. Nervul pudendal oferă senzație întregului pelvis și funcție motorie tuturor sfincterelor, podelei pelvine și mușchilor de rigiditate.
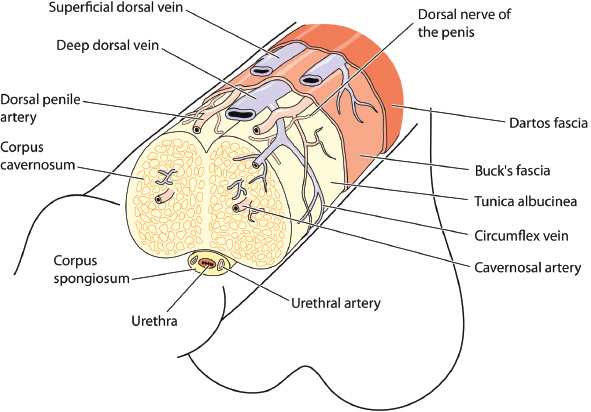
Figura 1:
Anatomia penisului care arată structurile majore, vasele de sânge și nervii.
Arterele pudendale interne asigură fluxul de sânge către penis, ramificându-se în arterele bulbouretrale, dorsale și cavernoase. Artera bulbouretrală trece prin fascia profundă a penisului (Buck), furnizând bulbul penisului și uretra penisului. Artera dorsală se deplasează între nervul dorsal și vena dorsală profundă dând ramuri circumflexe care însoțesc venele circumflexe cu ramuri terminale în gland. Penisul profund sau artera cavernosă pătrunde în corpul cavernos la crus și parcurge lungimea diafisului penian, aprovizionând arterele helicine specializate.
Stimularea sexuală declanșează nervii parasimpatici să elibereze acetilcolină. În interiorul celulelor endoteliale care căptușesc arterele penisului, oxid nitric sintetaza (NOS) catalizează oxidarea L-argininei în oxid nitric (NO) și L-citrulină. NO activează guanilat ciclaza în corpurile cavernoase și spongiose, care la rândul lor crește guanozin monofosfat ciclic (cGMP) conducând la relaxarea mușchilor netezi vasculari, vasodilatație și creșterea fluxului sanguin. Umplerea și extinderea rapidă a sistemului sinusoidal determină captarea sângelui prin ocluzia plexurilor venoase și a tunicii albuginee, ducând la ocluzia aproape totală a fluxului venos. Presiunea intracavernosa atinge 100 mmHg la erecția completă. Mușchii ischiocavernoși comprimă cavernoza plină de sânge pe măsură ce mușchii perineali se contractă, determinând presiunea finală să atingă câteva sute de mmHg. După ejaculare, eliberarea neurotransmițătorilor încetează din cauza excitației nervilor simpatici, iar enzimele fosfodiesterazei descompun cGMP, ducând la detumescitate și flaciditate (Figura 2).
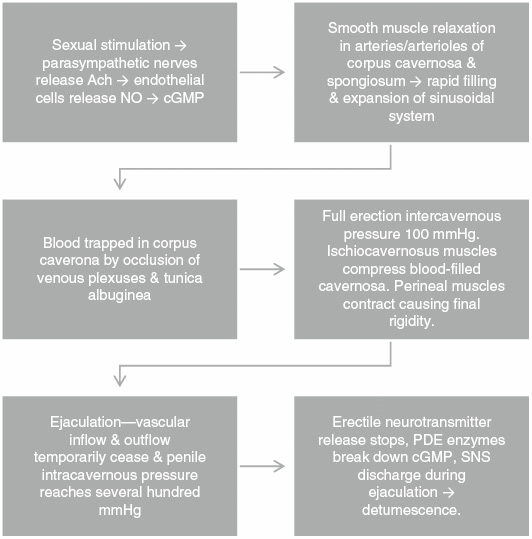
Figura 2:
Fiziologia erecțiilor.
Ach, acetilcolină; cGMP, guanozin monofosfat ciclic; NO, oxid nitric; PDE, fosfodiesteraza; SNS, sistem nervos simpatic.
Evaluarea amănunțită a DE necesită un istoric cuprinzător, utilizarea chestionarelor validate, examen fizic și lucrări de laborator. Imagistica, cum ar fi ultrasunetele doppler duplex, arteriografia penisului și RMN-ul trebuie efectuate de un urolog și rezervate pentru o eventuală intervenție chirurgicală.
ISTORIE
Realizarea unui istoric amănunțit oferă oportunitatea de a identifica toate cauzele/factorii care contribuie la DE. În ceea ce privește factorii psihosociali, este imperativ să se întrebe despre factorii de stres actuali și despre problemele relaționale.
Imaginea de sine a organelor genitale și așteptările privind frecvența sexuală sunt adesea subiecte neglijate atunci când se face un istoric sexual, dar afectează semnificativ performanța sexuală. Rezultatele dezvoltării și validării Scalei de auto-imagine genitală masculină (MGSIS), care a evaluat bărbații cu vârste cuprinse între 18 și 60 de ani, au constatat că bărbații cu o imagine de sine genitală mai bună au raportat mai puțină DE și 20% dintre bărbați au fost nemulțumiți de dimensiunea penisului.3 Bărbații care au o imagine de sine negativă a organelor genitale se pot întreba cum se compară dimensiunea penisului cu alți bărbați. Datele lui Alfred Kinsey privind 2500 de bărbați au raportat că lungimea medie a penisului flasc este de 1–4 inci și un penis erect mediu de 5–6.5 inci. Interesant este că bărbații au avut tendința să-și subestimeze dimensiunea penisului în comparație cu măsurarea reală.4
Discutarea așteptărilor cu privire la frecvența activității sexuale este relevantă pentru bărbații cu libido scăzut, sentimente de inadecvare sexuală sau curiozitate față de frecvența lor sexuală în comparație cu alți bărbați. Statisticile despre frecvența întâlnirilor sexuale sunt limitate. Un sondaj AARP pe 1670 de bărbați și femei cu vârsta peste 45 de ani a raportat că 41% dintre bărbații în vârstă de 50 de ani, 24% dintre bărbații în vârstă de 60 de ani și 15% dintre bărbații în vârstă de 70 de ani fac sex cel puțin o dată pe săptămână (reformularea acestor statistici). – 59% dintre bărbații de 50 de ani, 76% de 60 de ani și 85% dintre bărbații de 70 de ani fac sex mai rar decât o dată pe săptămână).5 Societatea Internațională pentru Medicină Sexuală (ISSM), raportând rezultatele din Sondajul Național de Sănătate și Comportament Sexual din 2010 al Institutului Kinsey, a remarcat că mai puțin de jumătate dintre bărbații căsătoriți cu vârsta cuprinsă între 25 și 49 de ani au făcut sex de câteva ori pe lună sau săptămânal, ceea ce era cea mai mare rată din orice categorie de vârstă.6 Un alt studiu publicat de ISSM care a chestionat bărbați și femei de peste 50 de ani a raportat că doar 20-30% dintre bărbați și femei rămân activi sexual până la 80 de ani.7
Utilizarea pornografiei este un subiect care poate fi inconfortabil pentru medici să discute cu pacienții lor de sex masculin. Deși diagnosticul dependenței de pornografie este controversat, există tot mai multe dovezi care leagă utilizarea frecventă a pornografiei cu un impact asupra satisfacției sexuale în partener, fericirea conjugală și relațională și disfuncția sexuală, inclusiv libidoul scăzut și ED.8-11 Pornografia pe internet oferă noutăți nelimitate și un format video la cerere care poate condiționa excitarea sexuală, făcând dificilă trecerea bărbaților la parteneri din viața reală.12 Nu a fost dezvoltat niciun instrument de screening validat pentru a identifica dificultățile legate de pornografie, inclusiv ED. După ce au întrebat despre frecvența utilizării pornografiei, furnizorii de asistență medicală ar trebui să întrebe despre capacitatea de a obține și de a menține o erecție în timpul sexului în parteneriat și al masturbării fără utilizarea sau rechemarea pornografiei. Dacă este necesară utilizarea sau rechemarea imaginilor pornografice pentru a produce o erecție adecvată, ED indusă de pornografie poate fi o problemă.
CHESTIONARE VALIDATATE
Chestionarele validate sunt utile în screening-ul pentru DE. Chestionarul cel mai des folosit în mediul clinic și în cercetările publicate este Indexul Internațional al Funcției Erectile (IIEF-15), cu 15 articole, validat în 32 de limbi.13 O versiune mai scurtă, IIEF-5 sau chestionarul Inventarului sănătății sexuale pentru bărbați (SHIM) poate fi, de asemenea, utilă pentru diagnostic și pentru a monitoriza eficacitatea tratamentului.14,15
EXAMENUL FIZIC
Examenul fizic ar trebui să includă un examen al penisului și al testiculelor, eventual puterea mușchilor planșeului pelvin (prin testări digitale), tensiunea arterială, semne de boală cardiovasculară, înălțimea, greutatea și circumferința taliei.
LUCRARE
Pe baza anamnezei și a examenului fizic, testele de laborator pot include panouri metabolice și lipidice cuprinzătoare, insulină a jeun, hemoglobina A1C, markeri inflamatori precum hsCRP, testosteron total și liber, teste tiroidiene și, la bărbații mai tineri cu suspiciune de hipogonadism, hormon luteinizant și prolactină. .
Cauzele și factorii care contribuie la ED se pot suprapune. Acestea includ probleme psihosociale, probleme neurologice, utilizarea excesivă a pornografiei, tulburări endocrine, efecte secundare ale medicamentelor și modificări vasculare.
PSIHOGENĂ
Stresul semnificativ, dificultățile de relație, depresia, anxietatea și tulburarea de stres post-traumatic pot contribui toate la ED. Anxietatea de performanță, descrisă pentru prima dată de Masters și Johnson în 1970,16 este o incapacitate de a obține o erecție din cauza experiențelor anterioare cu ED. Disfuncția sexuală, în special ED și scăderea dorinței sexuale, este semnificativ crescută la veteranii de sex masculin cu tulburare de stres post-traumatic.17 ED psihogenă apare de obicei în timpul sexului în parteneriat cu funcție erectilă normală în timpul masturbării. Debutul poate fi brusc, coincide cu stresul, cum ar fi pierderea locului de muncă, moartea unei rude sau probleme financiare. Erecțiile nocturne sau de dimineață sunt adesea normale.
NEUROLOGICE
Sistemul limbic, inclusiv amigdala; hipocampus; și gyri dințat și cingulat, este una dintre cele mai vechi zone ale creierului comune tuturor mamiferelor. Această regiune a creierului reglează emoțiile și încearcă să evite durerea și să caute plăcerea. Cercetările sugerează că stimulii vizuali plăcuti sexual activează mai mult amigdala și hipotalamusul la bărbați decât la femei.18 Intrarea din amigdală călătorește către striatul ventral, o parte majoră a ganglionilor bazali care funcționează ca parte a sistemului de recompensă. Nucleul accumbens din striatul ventral conține o concentrație mare de neuroni dopaminergici și este considerat centrul plăcerii al creierului. Semnalizarea dopaminei joacă un rol central în excitarea și motivația sexuală. Activarea receptorilor dopaminergici din nervii parasimpatici lombosacrali ai măduvei spinării facilitează erecțiile.19
Condițiile care perturbă semnalizarea normală a dopaminei sau neurotransmisia sau care pot afecta sistemul nervos central, de exemplu, boala Parkinson, scleroza multiplă, diabetul sau accidentul vascular cerebral, pot provoca, de asemenea, ED. Leziunea nervului cavernos în timpul prostatectomiei radicale duce la DE la mai mult de 50% dintre bărbați.20 Ciclismul pe distanțe lungi poate comprima nervul pudendal și vasele de sânge dintre șa și simfiza pubiană, limitând fluxul sanguin și oxigenul către penis.21,22 Bicicliștii pot prezenta disfuncționalitate arterială temporară și amorțeală genitală; cu toate acestea, este posibil să nu aibă un risc mai mare pentru DE. Rezultatele unui sondaj recent efectuat pe 5000 de bărbați sportivi au arătat că bicicliștii erau la fel de predispuși să sufere de ED ca și înotătorii și alergătorii.23
UTILIZAREA PORNOGRAFII
Deși utilizarea pornografiei poate fi considerată acceptabilă din punct de vedere social și normal, riscurile pentru sănătate ale utilizării frecvente nu sunt cunoscute. Pornografia pe internet oferă o noutate vizuală nelimitată exemplificând Efectul Coolidge, un fenomen biologic observat la animalele masculi când manifestă un interes reînnoit dacă sunt prezentate diferiților parteneri sexuali receptivi.24 Acest lucru oferă un posibil beneficiu evolutiv care îi permite unui mascul să fertilizeze mai multe femele. Stimulii vizuali sexuali noi provoacă excitare mai puternică, erecții mai ferme și ejaculare mai rapidă, cu o producție mai mobilă de spermă și spermă.25-27
Utilizarea excesivă a pornografiei pe internet poate influența neuroplasticitatea.28 Toate drogurile de abuz și dependențele comportamentale, cum ar fi jocurile pe internet și consumul excesiv de alimente, afectează calea dopaminei mezolimbice și nucleul accumbens.29 Noutatea promovează creșterea dopaminei în nucleul accumbens, declanșând eliberarea proteinei de legare a elementelor de răspuns cAMP (CREB). CREB reglează expresia genică a dinorfinei, o proteină care încetinește eliberarea de dopamină, atenuând sistemul de recompensă.30 Se crede că aceasta este baza moleculară a toleranței, deoarece sunt necesare cantități crescute de medicament sau comportament pentru a depăși cantitățile crescute de CREB. Când este abstinentă, reducerea dopaminei promovează anhedonia, potențial creând dependența de drog sau comportament.
În plus față de CREB, DeltaFosB este eliberat cu inundații repetate de dopamină a nucleului accumbens. DeltaFosB promovează întărirea pozitivă a comportamentului de dependență prin suprimarea eliberării de dinorfină și creșterea sensibilității la drog sau comportament. DeltaFosB persistă pentru o perioadă relativ lungă de timp, ceea ce îi face pe unii specialiști în dependență să se refere la el drept „comutatorul molecular pentru dependență”.31 Acest mecanism explică modul în care utilizarea repetată a pornografiei, ca și alte substanțe care creează dependență, determină desensibilizarea și reglarea în jos a receptorilor de dopamină, stabilind utilizatorul pentru un ciclu de agățare, poftă și erodare a voinței.32
ENDOCRIN
Pe lângă faptul că este necesar pentru dezvoltarea și creșterea penisului și pentru creșterea apetitului sexual, testosteronul reglează fiziologia erectilă prin mai multe mecanisme. Testosteronul promovează structura nervoasă sănătoasă, integritatea și funcția, în special a nervului cavernos.33 Studiile la animale și la oameni sugerează că testosteronul îmbunătățește expresia genei de sintetază de oxid nitric și producția de NO în arterele penisului, necesar pentru vasodilatație.34,35 Testosteronul modulează probabil activitatea PDE5, așa cum au demonstrat studiile pe animale care arată o reglare în sus a expresiei PDE5 cu suplimentarea cu testosteron.36,37
Nivelurile scăzute de testosteron liber și biodisponibil (dar nu total) sunt asociate cu disfuncția erectilă.38 Deși nivelul de testosteron necesar pentru a obține și menține erecțiile este necunoscut, o cantitate minimă pare să fie necesară pentru funcția erectilă.39,40 Suplimentarea cu testosteron poate să nu îmbunătățească DE la toți bărbații; cu toate acestea, unele studii au arătat că terapia cu testosteron poate fi utilă și poate permite inhibitorilor PDE-5 să funcționeze mai bine.41,42
Unii autori au documentat niveluri ridicate de estradiol la bărbați sau un raport ridicat de estradiol-testosteron asociat cu DE.43-45 Inhibitorii de aromatază previn conversia testosteronului în estradiol și pot crește testosteronul total și biodisponibil la bărbații în vârstă cu hipogonadism ușor, în timp ce scad ușor nivelurile de estradiol.46 În prezent, nu există dovezi că inhibarea aromatazei îmbunătățește funcția sexuală și nicio literatură care să susțină utilizarea inhibitorilor de aromatază pentru hipogonadism.47 În plus, unele studii au descoperit că raportul dintre estradiol și testosteron nu are legătură cu funcția erectilă sau cu dorința sexuală.48,49
Secreția ridicată de prolactină este o cauză mai puțin frecventă a testosteronului scăzut și a DE. Acest lucru se poate datora unei tumori hipofizare (prolactinom), marijuana sau medicamente precum amfetaminele, blocantele H2, risperidona, ISRS, inhibitorii MAO și unele antidepresive triciclice. Prolactina trebuie măsurată numai în cazurile de dorință sexuală scăzută, ginecomastie și/sau niveluri de testosteron total mai mici de 4 ng/ml (400 ng/dL).50
Atât hipotiroidismul, cât și hipertiroidismul pot duce la ED, iar ED este mai răspândită la bărbații cu distiroidism decât la martori.51 Tratamentul hipotiroidismului și hipertiroidismului poate îmbunătăți DE.52 Prin urmare, se recomandă screening-ul pentru disfuncția tiroidiană la bărbații care se prezintă cu DE.
VASCULARĂ
Sănătatea vasculară optimă este esențială pentru obținerea și menținerea erecțiilor. Disfuncția vasculară cauzează 70-80% din DE non-psihogenă la bărbații în vârstă. Deoarece ateroscleroza arterelor coronare, carotide, cerebrale sau periferice poate provoca simptome doar atunci când este avansată, ED poate fi cel mai precoce semn al bolii vasculare generalizate.53,54 În Studiul privind Cancerul de Prostată și Prevenirea, aproape 10,000 de bărbați randomizați în brațul placebo au fost evaluați la fiecare trei luni și urmăriți pentru DE și boli cardiovasculare din 1994 până în 2003. DE a fost un factor de risc la fel de mare pentru evenimente cardiovasculare viitoare precum fumatul și antecedentele familiale de atacuri de cord.55 Prezența DE poate fi, de asemenea, un predictor al mortalității de toate cauzele.56 ED împărtășește aceiași factori de risc ca și bolile cardiovasculare - hipertensiune arterială, lipsa exercițiilor fizice, alimentație proastă, fumat, diabet și hiperlipidemie. Mecanismul de bază pentru DE legată de vasculare implică disfuncția endotelială.57,58 Reglarea vasodilatației este o funcție a oxidului nitric (NO) eliberat de celulele endoteliale. NO inițiază producția de cGMP provocând relaxarea mușchilor netezi și vasodilatația arterelor din corpul cavernos. Disfuncția endotelială crește riscul de DE, indiferent de dovezile clinice ale bolilor cardiovasculare.59,60
EFECTE SECUNDARE MEDICAMENTE
Mulți agenți farmaceutici pot contribui la ED afectând neurotransmițătorii, hormonii, funcția nervoasă sau fluxul sanguin. Deși nu este o listă exhaustivă, vinovații obișnuiți includ antidepresivele (în special ISRS, cum ar fi fluoxetina, sertralina, citalopramul), anxioliticele, depresoarele SNC și relaxantele musculare (lorazepam, ciclobenzaprină). Diureticele (HCTZ, spironolactona, triamterenul, furosemid) și antihipertensivele și beta-blocantele (clonidină, enalapril, metoprolol) contribuie, de asemenea, în mod obișnuit la ED.
Este important să se dezvolte un plan cuprinzător de tratament pentru ED, deoarece este probabil mai eficient decât utilizarea unui singur agent pentru a trata numai simptomele.
CONSILIERE PSIHOSEXUALĂ
Trimiterea pentru terapie cognitiv-comportamentală, managementul stresului sau terapie de cuplu poate fi potrivită pentru unii bărbați cu ED. Relația cauzală dintre depresie și ED este neclară și probabil bidirecțională.61 De fapt, un studiu randomizat controlat (RCT) pe 152 de bărbați cu depresie concomitentă ușoară până la moderată și ED a arătat o stare de spirit îmbunătățită la bărbații cărora li s-a administrat sildenafil atunci când ED s-a îmbunătățit.62 ED cauzată de anxietatea de performanță sau depresia este cel mai bine tratată cu terapie cognitiv-comportamentală individuală, consiliere relațională sau colaborarea cu un terapeut sexual certificat. Există, de asemenea, dovezi că terapia de grup poate îmbunătăți funcția erectilă. O revizuire Cochrane a 11 studii clinice (dintre care nouă au fost randomizate) a concluzionat că terapia concentrată pe grupe de sex a fost mai eficientă decât niciun tratament pentru ED. O meta-analiză a studiilor care compară terapia de grup plus citrat de sildenafil versus sildenafil în monoterapie, a constatat că bărbații care au primit terapie de grup plus sildenafil au arătat o îmbunătățire semnificativă a actului sexual de succes și au mai puține șanse decât cei cărora li sa administrat doar sildenafil să abandoneze. Terapia de grup a îmbunătățit, de asemenea, semnificativ DE în comparație cu citratul de sildenafil în monoterapie.63
RECONDIȚIONARE DIN UTILIZARE EXCESIVA A PORNOGRAFII
Inversarea ED atribuită utilizării frecvente a pornografiei necesită ca pacientul să elimine toate pornografia, înlocuitorii pornografiei, rechemarea pornografiei și, în esență, orice stimulare sexuală artificială. Acest lucru permite recondiționarea excitației sexuale și a abilității erectile cu parteneri din viața reală. Deși timpul de „repornire” a creierului cu evitarea pornografiei este necunoscut, expertul în dependența de pornografie Gary Wilson sugerează că experiența clinică și forumurile online arată o recuperare mai rapidă pentru bărbații de peste 50 de ani, sugerând că 2 luni este tipic.64 Bărbații mai tineri pot avea nevoie de mai mult timp, eventual până la 5 luni, cu teoria că utilizarea pornografiei lor pe internet a început la o vârstă mai fragedă. Excitarea sexuală este condiționată, în special în timpul copilăriei și adolescenței, și poate fi mai puternică la bărbați decât la femei.65-67
FIZIOTERAPIE
Mușchii planșeului pelvin care joacă un rol în menținerea erecțiilor slăbesc odată cu vârsta. Terapia fizică pentru întărirea mușchilor bulbocavernos și ischiocavernos și a țesutului conjunctiv poate trata eficient DE la unii pacienți. Într-un studiu randomizat, controlat, 40 de bărbați cu DE au fost învățați să retragă maxim penisul și să-și ridice scrotul de două ori pe zi în timp ce stau în picioare, șezând și întinși și să-și strângă mușchii podelei pelvine după urinare. Rezultatele au fost surprinzătoare – până la 6 luni, 40% dintre participanți și-au recăpătat funcția erectilă normală și 35% au prezentat o oarecare îmbunătățire; 66% dintre bărbați au raportat, de asemenea, o scădere a driblingului după urinare. O tehnică mai simplă poate fi să-i înveți pe pacienții de sex masculin exerciții Kegel, punându-i să oprească urina în mijlocul fluxului pentru a identifica mușchii care vor fi necesari pentru a efectua exercițiul. Acești mușchi ar trebui să fie contractați timp de 5 secunde, de 10-20 de ori la rând, de trei ori pe zi. Bărbații pot fi stimulați să efectueze exerciții Kegel sau de întărire a podelei pelvine, datorită posibilei îmbunătățiri a calității orgasmului, un efect secundar comun documentat de Arnold Kegel, MD cu câteva decenii în urmă, la femeile care au efectuat frecvent Kegel.68
DISPOZITIV DE CONSTRECTARE A VACUUM
Dispozitivul de constricție cu vid (VCD), denumit în mod colocvial „pompă pentru penis” a fost proiectat de Geddings Osbon în 1974.69 Osbon s-a referit la el drept un „dispozitiv echivalent pentru tineret” și a pretins că l-a folosit personal timp de 20 de ani fără eșec. Primul dispozitiv de constricție a vidului a fost aprobat de FDA pentru ED în 1982.
VCD funcționează prin creșterea fluxului de sânge către penis prin generarea unei presiuni negative de 110-225 mmHg (manual sau cu o pompă acționată de baterii) și prevenirea ieșirii venoase cu un inel de constricție. Studiile sugerează că aproximativ 55-70% dintre bărbați pot obține erecții adecvate cu VCD.70, 71 Unii bărbați raportează că erecția obținută dintr-un VCD tinde să fie violet, rece sau amorțită, iar efectele secundare includ vânătăi ale diafului penian și captarea ejaculatului în timpul orgasmului din banda de constricție. Inelul de constricție nu trebuie lăsat pe loc mai mult de 30 de minute din cauza riscului de ischemie.
DIETA, EXERCIȚIILE ȘI SĂRBIREA ÎN GREUTATE
Căutarea afrodisiacelor pentru a stimula libidoul și a îmbunătăți performanța sexuală datează din antichitate. Într-adevăr, cuvântul afrodisiac provine de la zeița greacă a iubirii, Afrodita, care s-a născut din mare și adusă la țărm într-o scoică sau scoica de stridii. Deși stridiile conțin cantități mari de zinc necesare pentru producerea de testosteron, nu s-a demonstrat că consumul lor îmbunătățește libidoul sau capacitatea erectilă.
Cu toate acestea, anumite alimente îmbunătățesc sănătatea vasculară și, prin urmare, pot îmbunătăți funcția erectilă. De exemplu, alimentele bogate în nitrați, cum ar fi sfecla și legumele cu frunze verzi, cresc nivelul de oxid nitric, promovează funcția endotelială normală și scad tensiunea arterială.72-74 Semințele și sucul de rodie îmbunătățesc, de asemenea, funcția endotelială și scad tensiunea arterială, în timp ce scad LDL oxidat și glicat, minimizând astfel formarea plăcii aterosclerotice și atenuând grosimea și rigiditatea peretelui arterial.75-78 Siropul de porumb bogat în fructoză și băuturile răcoritoare cresc riscul de a dezvolta sindrom metabolic, ateroscleroză, diabet și ED.79 În plus, alimentele cu produse finale de glicație avansată, cum ar fi baconul, hamburgerii fast-food, hot-dog-urile, brânza, pizza și mâncarea prăjită, contribuie la diabet, boli cardiovasculare și ED.80-82 În loc să se concentreze pe evitarea anumitor alimente, ar putea fi cel mai benefic pentru pacienții cu disfuncționalități să adopte o dietă mediteraneană cu un aport abundent de legume, fructe, ulei de măsline extravirgin, cereale integrale, nuci și pește și un consum moderat de vin. Dovezile din patru studii clinice sugerează că dieta mediteraneană și stilul de viață influențează pozitiv funcția sexuală,83,84 precum și reducerea inflamației și întârzierea disfuncției sexuale la bărbații diabetici.
Există puține dezbateri despre faptul că exercițiile fizice îmbunătățesc câțiva factori de risc care contribuie la ED, inclusiv reducerea inflamației, îmbunătățirea funcției endoteliale, promovarea sensibilității la insulină, îmbunătățirea lipoproteinelor și creșterea pierderii de grăsime viscerală.85-89 O revizuire sistematică recentă și o meta-analiză confirmă că exercițiile fizice intense moderate până la viguroase pentru cel puțin 8 săptămâni pot îmbunătăți DE.90
Atât grăsimea corporală excesivă, cât și cea insuficientă sunt asociate cu ED. De exemplu, Studiul Hallym Aging a măsurat procentul de grăsime corporală și relația acestuia cu ED la bărbații coreeni.91 Bărbații cu cea mai scăzută și mai mare grăsime corporală au fost mai predispuși să aibă DE. Obezitatea centrală este asociată cu sindromul metabolic, disfuncția vasculară și testosteronul scăzut, toate contribuind la dezvoltarea DE.92,93 Țesutul adipos secretă peste 35 de hormoni și citokine, aproape toate promovând inflamația, rezistența la insulină și, în cele din urmă, bolile vasculare.94,95 Inflamația pare să fie un jucător cheie în cauza DE. Bărbații obezi cu ED au niveluri mai mari de markeri inflamatori (IL-6, IL-9, IL-18 și CRP) și funcția endotelială afectată decât bărbații obezi fără ED.96
Pierderea în greutate poate îmbunătăți semnificativ funcția erectilă. Într-un RCT, bărbații obezi care au slăbit în medie 33 de kilograme în decurs de 2 ani și-au îmbunătățit performanța sexuală.97 ED s-a îmbunătățit la mai mult de 30% din grupul de scădere în greutate, comparativ cu 5% din controale. Grupul de intervenție a primit consiliere nutrițională, sfaturi pentru creșterea activității fizice la aproximativ 3 ore pe săptămână și întâlniri lunare sau bilunare. Pe lângă o pierdere medie în greutate de 15%, bărbații din grupul de intervenție au prezentat și o reducere a markerilor inflamatori IL-6 și hsCRP, îmbunătățindu-și profilul de risc cardiometabolic.
BOTANICE ŞI AMINOACIZI
Utilizarea substanțelor botanice, nutrienților și a altor terapii naturale pentru a crește performanța sexuală a crescut considerabil datorită marketingului pe Internet. Puține terapii naturale au fost supuse unor studii clinice umane pentru a susține siguranța și eficacitatea. Cu toate acestea, următoarele substanțe botanice și aminoacizi pot fi de ajutor în tratarea ED, în special pentru bărbații care preferă să nu utilizeze medicamente PDE5i.
Pausinystalia yohimbe
Yohimbe este un veșnic verde originar din Africa centrală, care conține trei alcaloizi: rauwolscină, corynanthină și yohimbină. Cel mai activ constituent al yohimbe, yohimbina, este un produs farmaceutic cu un mecanism de acțiune bine conturat ca antagonist al α presinaptic.1 și α2-receptorii adrenergici și 5-HT(1B) și agonist parțial al receptorilor 5-HT(1A).98 Meta-analizele sugerează că yohimbina este eficientă pentru ED99,100 Yohimbina poate ajuta, de asemenea, cu capacitatea întârziată sau incapacitatea de a ejacula.101 Doza este de 15-30 mg, până la 100 mg pe zi. Yohimbe poate fi livrat cel mai bine la cerere, deoarece debutul este rapid, în 10-15 minute, cu un timp de înjumătățire de 35 de minute. Yohimbina pătrunde în sistemul nervos central cu posibile efecte secundare, inclusiv tahicardie, hipertensiune arterială, iritabilitate și anxietate. Transpirația, greața, amețelile, durerile de cap și înroșirea pielii sunt, de asemenea, frecvente. Ca și în cazul tuturor produselor botanice, multe mărci de suplimente fără prescripție medicală pot să nu fie de încredere. Un studiu care a testat 49 de mărci de yohimbe a constatat o variabilitate considerabilă a cantității de yohimbină – 0 până la 12.1 mg – per porție, cu 19 mărci care nu conțin rauwolscină și corynanthină, sugerând că acestea provin din extract de plante foarte procesate sau de origine sintetică.102
Tribulus terrestris
T. terrestris crește în Europa, Asia, Africa și Orientul Mijlociu. Rădăcina și fructele sunt utilizate pe termen lung atât în medicina chineză, cât și în cea ayurvedică. Se pretinde frecvent că Tribulus îmbunătățește producția de testosteron; cu toate acestea, studiile clinice nu au susținut această ipoteză decât în cazul utilizării intravenoase la primate.103-106 Studiile pe animale au arătat că Tribulus poate îmbunătăți funcția erectilă și producția de NO.107,108 Un RCT de 180 de bărbați cu DE ușoară până la moderată folosind 500 mg de T. terrestris luate de trei ori pe zi au raportat îmbunătățiri ale libidoului, ED, satisfacției actului sexual și calității orgasmului. Nu au fost raportate efecte adverse.109
Eurycoma longifolia
Eurycoma longifolia, cunoscut sub numele de ginseng malaysian sau Tongkat Ali, este o plantă cu flori originară din Indonezia, Malaezia, Thailanda, Vietnam, Laos și India. O meta-analiză a RCT sugerează E. longifolia ameliorează semnificativ DE.110 În plus, o analiză chineză a studiilor publicate sugerează E. longifolia îmbunătățește volumul spermei, libidoul și testosteronul.111 Planta poate avea o capacitate adaptogenă și s-a demonstrat că reduce oboseala, îmbunătățește starea de bine, scade cortizolul și crește testosteronul la subiecții stresați.112 Luat ca extract de rădăcină de apă, Eurycoma pare sigur, fără efecte secundare semnificative. Doza recomandată este de 200-300 mg o dată sau de două ori pe zi, cu o formă brevetată standardizată la 22% euripeptide și 40% glicozaponine.
Epimedium spp.
Epimedium spp. cresc în China și Coreea și aparțin familiei Berberidaceae (care conține și binecunoscutele plante botanice, Mahonia aquifolium, Hydrastis canadensis, și Berberis vulgaris). Au fost identificate cel puțin 50 de specii și sunt cunoscute în mod obișnuit sub denumirea de „buruiană de capră excitată”. Presupusul ingredient activ, icariina, este un flavonoid care îmbunătățește funcția erectilă în studiile pe animale prin inhibarea PDE5 și inducerea oxidului nitric.113-115 – Studii clinice pe oameni Epimedium lipsesc; prin urmare, recomandările de dozare nu sunt disponibile.
L-arginină
L-arginina este un aminoacid, esential in conditiile cu enzima arginaza crescuta, precum diabetul si insuficienta renala.116,117 Arginina este folosită de enterocitele intestinale și hepatocitele și transformată în L-citrulină sau L-ornitină. Variabilitatea absorbției L-argininei orale este considerabilă – o doză de 6 g este absorbită în aproximativ 68%, în timp ce o doză de 10 g este absorbită doar în proporție de 20%.118,119
Oxidul nitric este produsul secundar al conversiei L-argininei în citrulină. În plus, suplimentarea cu citrulină crește arginina plasmatică. Arginina poate îmbunătăți ED în doze mari; de exemplu, 5000 mg îmbunătățește DE, mai ales dacă metaboliții NO urinari sunt scazuți.120 Teoretic, L-arginina poate funcționa cel mai bine dacă nivelurile ADMA sunt crescute. Deoarece ADMA inhibă eNOS, enzima endotelială necesară pentru producerea de NO, suplimentarea cu L-arginină poate restabili raportul arginină-ADMA.121 Suplimentarea cu L-arginina poate fi mai eficienta pentru ED atunci cand este combinata cu yohimbina sau picnogenol (scoarta de pin de Pinus pinaster).122-124 Suplimentarea cu L-arginina poate activa herpesul și poate crește focarele. În plus, un RCT publicat în 2013 a raportat că 3000 mg de L-arginină luate de 3 ori pe zi a crescut riscul de mortalitate la pacienții cu IM recent.125
TERAPIILE FARMACOLOGICE
Principalele abordări farmacologice pentru DE sunt inhibitorii PDE5, apomorfina și terapiile prin injecție intracavernosă.
inhibitori PDE5
Inhibitorii de fosfodiesteraza de tip 5 (PDE5i) sunt cel mai frecvent tratament medicamentos pentru ED. Mecanismul lor de acțiune este bine cunoscut, inhibând enzima fosfodiesteraza de tip 5 care descompune cGMP, prelungind eficient activitatea NO în arterele penisului. Medicamentele din această clasă diferă prin selectivitatea lor pentru cele 11 izoenzime PDE diferite. Această reactivitate încrucișată cu izoenzimele PDE se găsește în special în mușchii netezi vasculari, viscerali și pulmonari și contribuie la efecte secundare.126 De exemplu, vardenafilul și sildenafilul au șanse de trei sau șapte ori mai mari de a se lega de PDE6, o enzimă din retină care transferă lumina în impulsurile nervoase. Inhibarea acestei enzime cauzează tulburări de percepție a culorii cunoscute sub numele de „cromatopsie”.
Patru medicamente PDE5i au fost aprobate de FDA – sildenafil în 1998, vardenafil și tadalafil în 2003 și avanafil în 2012. Nu au fost efectuate studii directe care să compare eficacitatea acestor medicamente. Aceste medicamente diferă în ceea ce privește debutul, durata acțiunii și efectele secundare.127 Debutul sildenafilului și vardenafilului este de 30-60 de minute cu o durată de 10-12 ore. Debutul tadalafilului este de 15-30 de minute, în funcție de doză, cu cea mai lungă durată de 36 de ore. Avanafil are cel mai scurt debut, în 15 minute, și durata, aproximativ 6 ore.
Utilizarea PDE5i poate reduce riscul de cancer de prostată, posibil pentru că bărbații care le folosesc pot ejacula mai frecvent, ceea ce protejează împotriva cancerului de prostată.128,129 Pe termen lung sildenafil Utilizarea citratului (Viagra) este asociată cu un risc ușor crescut de melanom.130 Cele mai frecvente efecte secundare ale PDE5i includ dureri de cap la până la 20% dintre bărbați, înroșirea feței în până la 15% și dispepsia și congestia nazală în până la 10%. Deși mai puțin frecvente, pot apărea amețeli și priapism. Toate PDE5i sunt contraindicate bărbaților care iau nitrați.
apomorfină
Apomorfina a fost utilizată din 1869 pentru boala Parkinson și a fost studiată pentru efectul său asupra funcției erectile. Deși derivată din morfină, apomorfina nu conține morfină și nu se leagă de receptorii opioizi. Are afinitate mare pentru receptorii de dopamină, iar mecanismul de îmbunătățire a apetitului sexual și erecțiilor este probabil printr-o afinitate moderată pentru receptorii D2 din hipotalamus și sistemul limbic.131 În studiile clinice de fază II și III la om, care au implicat 5000 de bărbați, 3-4 mg de apomorfină sublinguală au produs erecții suficient de ferme pentru penetrare în 10-25 de minute, cu aproximativ 20-25% îmbunătățire față de placebo.132,133 Singura apomorfina farmaceutica brevetata din SUA este Apokyn injectabil, aprobat de FDA pentru progresul bolii Parkinson; cu toate acestea, apomorfina poate fi combinată ca o pastilă sublinguală și poate fi combinată cu o PDE5i. Dozele de 2-3 mg pot fi la fel de eficiente ca cele de 4-6 mg fără efecte secundare, cum ar fi greață, dureri de cap sau amețeli. Apomorfina nu trebuie utilizată concomitent cu clorhidratul de ondansetron, un antiemetic frecvent prescris, din cauza posibilei hipotensiuni.
Injecții intracavernose
Introduse în 1983, injecțiile intracavernoase modulează funcția endotelială și sunt foarte eficiente chiar și la bărbații cu DE severă; alprostadil produce erecții la până la 93% dintre bărbați, cu eficacitatea mixurilor bi-, tri- și quad de până la 97.6%.134-136 Alprostadil, 20 sau 40 μg de prostaglandină E1, este singura injecție intracavernosă patentată aprobată de FDA, în timp ce alte două medicamente, fentolamină și papaverină, pot fi adăugate la PGE1 într-o formulă compusă. Cel mai frecvent efect secundar al PGE1 este durerea la 48.5% dintre bărbați. Bi-mix, care conține adesea 0.5–3.0 mg de fentolamină și 30 mg de papaverină, nu provoacă durere, dar poate să nu fie la fel de eficient. Tri-mix, care conține de obicei 5-10 μg (și până la 40 μg) de PGE1, 0.5-1.0 mg fentolamină și 15-30 mg papaverină, reduce probabilitatea durerii la 2.9%. Adăugarea a 0.15 mg de atropină în quad-mix, rezervat bărbaților la care tri-mix este ineficient, ameliorează semnificativ durerea. Cantitatea de amestec PGE1, bi-, tri- sau quad necesară variază de la 0.1 la 0.3 ml. Empiric (folosind PGE1 numai indiferent de etiologia sau severitatea DE, cu ajustări ale dozei sau formulei efectuate pe baza rezultatelor pacientului) și bazate pe risc (folosind bi-mix, tri-mix sau tri-mix cu doză mare pe baza unui algoritm care factorizează ED) etiologia și numărul de factori de risc ED) abordările de dozare par a fi similare în ceea ce privește eficacitatea și ratele de complicații și satisfacție.137 Efectele secundare includ durere la locul injectării, priapism și dezvoltarea țesutului cicatricial sau a bolii Peyronie. Pentru un articol excelent care analizează eficacitatea, dozele și efectele secundare ale injecțiilor intracavernose, consultați rezumatul Medscape „Algoritmul de injecție intracavernosă” de Jeffrey Albaugh.138
TERAPIA CU UNDE DE ȘOC EXTRACORPOREALE DE INTENSITATE JOZĂ
Unda de șoc extracorporală de intensitate scăzută (LI-ESW) a apărut în anii 1990, când s-a demonstrat că ultrasunetele induc angiogeneza în rănile șobolanului.139 LI-ESW folosește unde de șoc, un tip de undă acustică care transportă energie și induce reacții biologice atunci când este aplicată pe țesutul țintă.140 Procedura variază în ceea ce privește densitatea fluxului de energie, frecvența (numărul de impulsuri pe secundă în Hz) și numărul total de impulsuri furnizate. Mecanismul de acțiune pentru îmbunătățirea ED pare să fie regenerarea nervilor pozitivi ai oxidului nitric neuronal al penisului (nNOS), eliberarea îmbunătățită de oxid nitric și repararea celulelor musculare netede endoteliale și vasculare prin recrutarea celulelor stem mezenchimale.141 Tratamentul poate activa, de asemenea, celulele progenitoare locale ale penisului.142 În prezent, LI-ESW nu este aprobat de FDA pentru ED; cu toate acestea, multe studii clinice au fost efectuate cu un profil bun de siguranță și succes variabil.
Primul studiu pilot ED publicat în 2010 a folosit șase sesiuni LI-ESW la 20 de bărbați care nu au răspuns la inhibitorii PDE5 (PDE5i). Rezultatele au arătat o îmbunătățire a funcției erectile, a duratei erecțiilor și a rigidității penisului într-o lună. Au fost raportate îmbunătățiri pentru până la 1 luni de urmărire.143 Mai multe RCT au raportat rezultate pozitive folosind LI-ESW. Într-un studiu care a implicat 67 de bărbați cu ED care au răspuns la PDE5i, brațul de tratament a primit 12 sesiuni cu funcție erectilă îmbunătățită și hemodinamică penisului observate la aproximativ 50% dintre bărbați fără utilizarea PDE5i.144 Într-un RCT similar în India, care a inclus 135 de respondenți PDE5i tratați cu 12 ședințe, 78% dintre bărbații tratați au reușit să obțină erecții suficient de ferme pentru penetrare fără medicamente la 1 lună.145 Deși aceste rezultate au fost susținute la un an de urmărire, a existat o rată foarte mare de abandon, incluzând 1% din brațele de tratament simulat și 58% din brațele de tratament.
Bărbații care nu răspund la PDE5i pot deveni răspunsuri după tratamentul cu LI-ESW. Într-un studiu prospectiv deschis, cu un singur braț, pe 29 de bărbați care nu răspund la PDE5i, 12 tratamente au condus la 72% dintre bărbați capabili să obțină erecții suficient de ferme pentru penetrarea cu PDE5i.146 Într-un RCT mai recent, care a inclus 58 de non-răspunzători PDE5i, 54% au răspuns la PDE5i după 1 lună de terapie cu LI-ESW, comparativ cu 0% în grupul simulat.147
Îmbunătățirea susținută observată în studiile de urmărire mai lungă sugerează că, după tratament, unii bărbați pot inversa patologia de bază care le provoacă DE sau că LI-ESW poate oferi un anumit grad de reabilitare a penisului. Într-un RCT cu urmărire de 6 luni a 112 bărbați, toți dintre care au primit cinci ședințe de tratament, deoarece brațul placebo a primit tratament activ la 10 săptămâni, la 6 luni, aproximativ 20% din brațul de tratament inițial și 23% din brațul tratat inițial. grupul placebo a putut încă să aibă relații sexuale fără medicamente.148 Un alt an de urmărire a 1 de bărbați în vârstă (vârsta medie 50 de ani) cu factori de risc vascular, inclusiv diabet, hipertensiune arterială, dislipidemie și boală coronariană, a constatat o îmbunătățire susținută cu 65% a severității DE și a calității erecției auto-raportate.149
Nu se cunoaște numărul de tratamente LI-ESW pentru rezultatul ideal și cât timp rămâne eficient tratamentul. Un RCT recent efectuat pe 126 de bărbați într-un spital danez a comparat bărbați care au primit cinci ședințe față de zece la 6 și 12 luni; tratamentul a fost de aproximativ 38% eficient în ambele grupuri, ceea ce sugerează că ședințele suplimentare ar putea să nu îmbunătățească rezultatul.150,151 Într-o urmărire de 2 ani a unui studiu deschis pe 156 de bărbați, 63% s-au îmbunătățit la 4 săptămâni, cu 53% eficacitate susținută la 2 ani.152 Nu este surprinzător că bărbații cu DE severă au avut eșec mai devreme. Toți pacienții cu diabet zaharat și ED severă și-au pierdut efectul, în timp ce 76% dintre bărbații cu ED ușoară și fără diabet și-au păstrat eficacitatea.
Numărul de studii care utilizează LI-ESWT pentru ED a crescut dramatic în ultimii ani. O analiză narativă a literaturii publicate efectuată în 2013 a raportat că 60-75% dintre respondenții PDE5i ar putea obține erecții suficient de ferme pentru penetrare fără medicamente și 72% dintre cei care nu au răspuns la PDE5i au devenit respondenți.153 Meta-analize recente care au analizat 14 studii, inclusiv 7 RCT, au constatat că terapia LI-ESW este sigură și eficientă, cu rezultate care durează cel puțin 3 luni.154 Bărbații cu DE ușoară sau moderată par să aibă un răspuns mai bun decât bărbații cu DE severă, cu densitatea fluxului de energie, numărul de unde de șoc furnizate și durata tratamentului strâns corelată cu rezultatul.
PRP ȘI INJECȚIA CELULE STEM
Injectarea de plasmă bogată în trombocite (PRP) sau de celule stem mezenchimale în corpul cavernos promite să îmbunătățească ED și să restabilească funcția arterei și nervilor penian. Pentru a prepara PRP, trombocitele din sângele anticoagulant sunt centrifugate într-o centrifugă și concentrate. PRP conține peste 300 de proteine bioactive, factori de creștere și molecule de adeziune care pot îmbunătăți vindecarea țesuturilor și pot promova regenerarea țesutului nervos și vascular.155-157 Deoarece vascularizația penisului este regiunea cea mai bogată în endoteliu a corpului unui bărbat, iar fluxul de sânge în penisul flasc este mai lent în comparație cu circulația sistemică (permițând o retenție mai bună), teoretic, PRP poate oferi beneficii în țesutul penisului similar cu îmbunătățirile observate în leziunile ortopedice. .
Au fost publicate puține studii pilot de siguranță și fezabilitate care utilizează PRP pentru ED. Un studiu uman efectuat în Italia a evaluat 9 bărbați cu DE care au primit PRP în plus față de terapia cu vacuum. S-a observat o ușoară îmbunătățire cu singurul efect advers minor al durerii ușoare și vânătăilor la locul injectării.158
Nivelurile reduse de celule progenitoare endoteliale circulante (EPC), un tip de celule stem necesare pentru regenerarea mucoasei endoteliale vasculare, este un factor de risc independent pentru DE.159 EPC-urile sunt scăzute odată cu inflamația cronică observată în diabet, hipercolesterolemie, obezitate, boli cardiovasculare și fumatul de țigară.160 Studiile la animale sugerează că testosteronul stimulează mobilizarea EPC din măduva osoasă și îmbunătățește angiogeneza.161,162 Două recenzii ale studiilor publicate pe animale care implică injecții intracavernose cu celule stem derivate din măduva osoasă, țesutul adipos și mușchiul scheletic au raportat rezultate favorabile asupra funcției endoteliale, mușchilor netezi și nervoase în țesutul penian.163,164
PRP și terapia cu celule stem pot ajuta bărbații cu leziuni vasculare și nervoase cauzate de diabet sau prostatectomie radicală. Câteva studii pilot pe oameni sugerează că procedura poate fi sigură și eficientă. Un studiu a implicat 11 bărbați care au suferit prostatectomie radicală din cauza cancerului de prostată, rezultând că DE nu a răspuns la PDE5i.165 Celulele stem autologe derivate din adipos injectate în corpul cavernos și-au recuperat funcția erectilă la opt dintre cei unsprezece bărbați fără efecte adverse. Într-un alt studiu pilot care a folosit celule stem din cordonul ombilical uman neautologe, șase din șapte bărbați mai în vârstă cu diabet zaharat și ED care nu răspund la PDE5i, și-au recăpătat erecțiile de dimineață până în a treia lună, iar doi din șapte au fost încă capabili să obțină o erecție. cu PDE5i după 6 luni. Interesant este că glicemia a scăzut la 2 săptămâni după injectare, nivelul hemoglobinei A1C s-a îmbunătățit timp de până la 4 luni și nu au fost observate efecte adverse. Rezultate pozitive au fost, de asemenea, observate într-un studiu pilot pe oameni care a implicat 12 bărbați cu DE severă post-prostatectomie radicală care nu răspunde la alprostadil, PDE5i sau la dispozitivul de vid.166 Acest studiu de fază I a folosit doze crescânde de celule stem autologe derivate din măduva osoasă. Dozele mai mari au fost mai eficiente cu nouă din doisprezece bărbați capabili să obțină erecții suficient de ferme pentru penetrarea cu PDE5i; beneficiile au fost susținute la un an fără efecte adverse.
În timp ce PRP și injecțiile cu celule stem sunt considerate experimentale și nu au aprobarea FDA și acoperirea de asigurare, bărbații pot căuta practicieni care efectuează aceste proceduri. Posibilele efecte adverse includ infecția și dezvoltarea țesutului cicatricial sau boala Peyronie. Teoretic, celulele stem pot crește și tumorigeneza, deși amploarea acestui risc este necunoscută.167
Disfuncția erectilă este o problemă medicală comună cu mai mulți factori și cauze posibile, adesea suprapuse. Preluarea atentă și amănunțită a anamnezei, utilizarea chestionarelor validate, examenul fizic și lucrările de laborator sunt necesare pentru a dezvolta un plan de ameliorare a simptomelor, abordând în același timp cauzele subiacente. Opțiunile de tratament includ modificări ale dietei și ale stilului de viață, exerciții de terapie fizică, utilizarea dispozitivelor de constricție cu vid, suplimente alimentare botanice și de aminoacizi, medicamente, terapie cu unde de șoc extracorporală de intensitate scăzută și, posibil, injecții intracavernose cu plasmă bogată în trombocite sau celule stem.
- Efectuați istoricul amănunțit, documentarea chestionarului, examenul, lucrările de laborator relevante
- Discutați cauzele/factorii contributivi:
- psihogenă
- Neurologice
- Utilizarea excesivă a pornografiei
- Endocrin
- Efecte secundare ale medicamentelor
- Modificări vasculare
- Examinați opțiunile de tratament relevante:
- Consiliere psihosexuală
- Abstinenta pornografiei
- Terapie fizică (Kegel) sau utilizarea dispozitivului de constricție cu vid
- Modificări dietetice
- Recomandare de exerciții
- Opțiuni de pierdere în greutate
- Remedii pe bază de plante și aminoacizi
- medicamente:
- PDE5i: diferite debuturi, durata de acțiune și efecte secundare
- Poate fi acoperit sau nu de asigurare, poate fi costisitor
- Apomorfina, care nu este aprobată de FDA pentru ED, trebuie să fie combinată
- PDE5i: diferite debuturi, durata de acțiune și efecte secundare
- Undă de șoc extracorporală de intensitate scăzută
- Nu este aprobat de FDA pentru ED și lipsa acoperirii de asigurare
- Datele de siguranță sunt bune, majoritatea studiilor arătând rezultate pozitive
- Poate necesita tratamente repetate
- PRP și injecții cu celule stem
- Nu este recomandat din cauza lipsei de studii randomizate și a posibilelor probleme legate de siguranță
Nu a fost primită nicio finanțare pentru pregătirea și scrierea acestui articol.
- Feldman HA, Goldstein I, Hatzichristou DG, et al. Impotența și corelațiile sale medicale și psihosociale: rezultatele studiului Massachusetts Male Aging Study.
- McMahon CN, Smith CJ, Shabsigh R. Tratarea disfuncției erectile atunci când inhibitorii PDE5 eșuează.
- Herbenick D, Schick V, Reece M, et al. Dezvoltarea și validarea Scalei de auto-imagine a genitalelor masculine: rezultate dintr-un eșantion de probabilitate reprezentativ la nivel național de bărbați din Statele Unite.
- Gebhard P, Johnson A.
- Fisher L, Anderson G, Chapagain M, et al.
- Schick V, Herbenick D, Reece M, et al. Comportamente sexuale, utilizarea prezervativelor și sănătatea sexuală a americanilor peste 50 de ani: implicații pentru promovarea sănătății sexuale pentru adulții în vârstă.
- Berger J, Doan A, Kehoe J, et al. Sondajul PD69-12 al funcției sexuale și al pornografiei.
- Zillmann D, Bryant J. Impactul pornografiei asupra satisfacției sexuale 1.
- Sun C, Bridges A, Johnson JA, et al. Pornografia și scenariul sexual masculin: o analiză a consumului și a relațiilor sexuale.
- Poulsen FO, Busby DM, Galovan AM. Utilizarea pornografiei: cine o folosește și cum este asociată cu rezultatele cuplului.
- Perry SL. Vizionarea pornografiei reduce calitatea conjugală în timp? Dovezi din date longitudinale.
- Park B, Wilson G, Berger J, et al. Pornografia pe internet provoacă disfuncții sexuale? O revizuire cu rapoarte clinice.
- Rosen RC, Riley A, Wagner G, et al. Indicele internațional al funcției erectile (IIEF): o scară multidimensională pentru evaluarea disfuncției erectile.
- Rosen RC, Cappelleri JC, Smith MD, et al. Dezvoltarea și evaluarea unei versiuni prescurtate cu 5 articole a Indexului Internațional al Disfuncției Erectile (IIEF-5) ca instrument de diagnostic pentru disfuncția erectilă.
- Cappelleri JC, Rosen RC. Inventarul sănătății sexuale pentru bărbați (SHIM): o revizuire de 5 ani a cercetării și experienței clinice.
- Bruce T, Barlow D. Natura și rolul anxietății de performanță în disfuncția sexuală. În: Leitenberg H, ed.
- Bentsen I, Giraldi A, Kristensen E, et al. Revizuirea sistematică a disfuncției sexuale în rândul veteranilor cu tulburare de stres post-traumatic.
- Hamann S, Herman RA, Nolan CL, et al. Bărbații și femeile diferă în răspunsul amigdalei la stimulii sexuali vizuali.
- Simonsen U, Comerma-Steffensen S, Andersson KE. Modularea căilor dopaminergice pentru a trata disfuncția erectilă.
- Campbell J, Burnett A. Abordări neuroprotective și regenerative ale nervilor pentru tratamentul disfuncției erectile după leziunea nervului cavernos.
- Ricchiuti VS, Haas CA, Seftel AD, et al. Leziunea nervului pudendal asociată cu ciclismul avid.
- Oberpenning F, Roth S, Leusmann DB, et al. Sindromul Alcock: insensibilitate temporară a penisului din cauza comprimării nervului pudendal în canalul Alcock.
- Awad MA, Gaither TW, Murphy GP, et al. Ciclism și funcție sexuală și urinară masculină: rezultate dintr-un studiu amplu, multinațional, transversal.
- Ventura-Aquino E, Fernandez-Guasti A, Paredes R. Hormoni and the Coolidge effect.
- Koukounas E, Over R. Alocarea resurselor atenționale în timpul obișnuirii și dezhabituării excitării sexuale masculine.
- Kim SC, Bang JH, Hyun JS, et al. Modificări ale răspunsului erectil la stimularea sexuală audiovizuală repetată.
- Joseph P, Sharma R, Agarwal A, et al. Bărbații ejaculează volume mai mari de spermă, spermă mai mobilă și mai rapid atunci când sunt expuși la imagini cu femei noi.
- Volkow ND, Baler D. Stiinta dependentei: descoperirea complexitatii neurobiologice.
- Love T, Laier C, Brand M, et al. Neuroștiința dependenței de pornografie pe internet: o revizuire și o actualizare.
- Nestler EJ, Barrot M, Self DW. DeltaFosB: un comutator molecular susținut pentru dependență.
- Pitchers KK, Frohmader KS, Vialou V, et al. Recompensele naturale și medicamentoase acționează asupra mecanismelor comune de plasticitate neuronală cu ΔFosB ca mediator cheie.
- Traish A, Goldstein I, Kim N. Testosteronul și funcția erectilă: de la cercetarea de bază la o nouă paradigmă clinică pentru gestionarea bărbaților cu insuficiență androgenică și disfuncție erectilă.
- Park KH, Kim SW, Kim KD, et al. Efectele androgenilor asupra expresiei ARNm de oxid nitric sintază în corpul cavernos de șobolan.
- Mihail N. Are testosteronul un rol în funcția erectilă?
- Morelli A, Filippi S, Mancina R, et al. Androgenii reglează expresia fosfodiesterazei de tip 5 și activitatea funcțională în corpurile cavernoase.
- Zhang XH, Morelli A, Luconi M, et al. Testosteronul reglează expresia PDE5 și răspunsul in vivo la tadalafil în corpul cavernos de șobolan.
- Liao M, Huang X, Gao Y, et al. Testosteronul este asociat cu disfuncția erectilă: un studiu transversal la bărbați chinezi.
- Buena F, Swerdloff RS, Steiner BS, et al. Funcția sexuală nu se modifică atunci când nivelurile serice de testosteron sunt variate farmacologic în intervalul normal masculin.
- Armagan A, Kim NN, Goldstein I, et al. Relația doză-răspuns între testosteron și funcția erectilă: dovezi pentru existența unui prag critic.
- Jain P, Rademaker AW, McVary KT. Suplimentarea cu testosteron pentru disfuncția erectilă: rezultatele unei meta-analize.
- Aversa A, Isidori AM, Spera G, et al. Androgenii îmbunătățesc vasodilatația cavernoasă și răspunsul la sildenafil la pacienții cu disfuncție erectilă.
- Mancini A, Milardi D, Bianchi A, et al. Niveluri crescute de estradiol în tulburarea ocluzivă venoasă: un posibil mecanism funcțional al scurgerii venoase.
- Wu F, Chen T, Mao S, et al. Nivelurile de estradiol și testosteron sunt modificate la bărbații chinezi cu disfuncție sexuală.
- Srilatha B, Adaikan PG, Chong YS. Relevanța echilibrului estradiol-testosteron în prognosticul pacienților cu disfuncție erectilă.
- Leder BZ, Rohrer JL, Rubin SD, et al. Efectele inhibiției aromatazei la bărbații în vârstă cu niveluri scăzute sau limită de testosteron seric.
- Tan RBW, Guay AT, Hellstrom WJG. Utilizarea clinică a inhibitorilor de aromatază la bărbați adulți.
- Dastello-Porcar AM, Martinez-Jabaloyas JM. Raportul testosteron/estradiol, este util în diagnosticul disfuncției erectile și al dorinței sexuale scăzute?
- Gades NM, Jacobson DJ, McGree ME, et al. Asociațiile dintre hormonii sexuali serici, funcția erectilă și apetitul sexual: Studiul Olmsted Country despre simptomele urinare și starea de sănătate în rândul bărbaților.
- Buvat J, Lemaire A. Screening endocrin la 1,022 de bărbați cu disfuncție erectilă: semnificație clinică și strategie rentabilă.
- Gabrielson AT, Sartor RA, Hellstrom WJG. Impactul bolii tiroidiene asupra disfuncției sexuale la bărbați și femei.
- Krassas GE, Tziomalos K, Papadopoulou F, et al. Disfuncția erectilă la pacienții cu hiper și hipotiroidism: cât de frecvente și ar trebui să tratăm?
- Cheitlin M. Disfuncția erectilă: cel mai precoce semn al bolii vasculare generalizate?
- Billups KL. Disfuncția erectilă ca semn precoce al bolilor cardiovasculare.
- Thompson IM, Tangen CM, Goodman PJ, et al. Disfuncția erectilă și bolile cardiovasculare ulterioare.
- Böhm M, Baumhäkel M, Teo K, et al. Disfuncția erectilă prezice evenimente cardiovasculare la pacienții cu risc crescut care primesc telmisartan, ramipril sau ambele: Telmisartan în curs de desfășurare în monoterapie și în asociere cu Ramipril Global Endpoint Trial/Telmisartan Randomized Assessment Study la subiecții ACE iNtolerant cu boli cardiovasculare (ON TARGET)/TRANSCEND.
- Guay AT. ED2: disfuncție erectilă = disfuncție endotelială.
- Aversa A, Bruzziches R, Francomano D, et al. Disfuncția endotelială și disfuncția erectilă la bărbatul în vârstă.
- Kaya C, Uslu Z, Karaman I. Funcția endotelială este afectată la pacienții cu disfuncție erectilă?
- Kaiser DR, Billups K, Mason C, et al. Vasodilatație dependentă și independentă de endoteliu a arterei brahiale la bărbații cu disfuncție erectilă și fără altă boală cardiovasculară clinică.
- Seidman SN, Roose SP. Relația dintre depresie și disfuncția erectilă.
- Seidman SN, Roose SP, Menza MA, et al. Tratamentul disfuncției erectile la bărbații cu simptome depresive: rezultatele unui studiu controlat cu placebo cu citrat de sildenafil.
- Melnick T, Soares BG, Nasselo AG. Intervenții psihosociale pentru disfuncția erectilă.
- Wilson G.
- Brom M, Ambii S, Laan E, et al. Rolul condiționării, învățării și dopaminei în comportamentul sexual: o analiză narativă a studiilor pe animale și la om.
- Klucken T, Schweckendiek J, Merz CJ, et al. Activarea neuronală a dobândirii excitării sexuale condiționate: efectele conștiinței de urgență și a sexului.
- Griffee K, O'Keefe S, Beard K, et al. Dezvoltarea sexuală umană este supusă unei perioade critice de învățare: implicații pentru dependența sexuală, terapia sexuală și pentru creșterea copiilor.
- Kegel AH. Exercițiu de rezistență progresivă în refacerea funcțională a mușchilor perineali.
- Hoyland K, Vasdev N, Adshead J. Utilizarea dispozitivelor de erecție în vid în disfuncția erectilă după prostatectomie radicală.
- Vrijhof HJ, Delaere KP. Dispozitive de constricție a vidului în disfuncția erectilă: acceptare și eficacitate la pacienții cu impotență de etiologie organică sau mixtă.
- Kolettis PN, Lakin MM, Montague DK, et al. Eficacitatea dispozitivului de constricție a vidului la pacienții cu disfuncție ocluzivă venoasă corporală.
- Siervo M, Lara J, Ogbonmwan I, et al. Suplimentarea cu nitrați anorganici și suc de sfeclă roșie reduce tensiunea arterială la adulți: o revizuire sistematică și meta-analiză.
- Hord N, Tang Y, Bryan NS. Surse alimentare de nitrați și nitriți: contextul fiziologic pentru potențiale beneficii pentru sănătate.
- Hobbs DA, George TW, Lovegrove JA. Efectele tensiunii arteriale cu nitrați dietetici și ale funcției endoteliale: o revizuire a studiilor de intervenție umană.
- Fuhrman B, Volkova N, Aviram M. Sucul de rodie inhibă absorbția LDL oxidată și biosinteza colesterolului în macrofage.
- Aviram M, Rosenblat M, Gaitini D, et al. Consumul de suc de rodie timp de 3 ani de către pacienții cu stenoză de arteră carotidă reduce grosimea intima-media carotidă comună, tensiunea arterială și oxidarea LDL.
- Ignarro LJ, Byrns RE, Sumi D, et al. Sucul de rodie protejează oxidul de azot împotriva distrugerii oxidative și sporește acțiunile biologice ale oxidului de azot.
- Stowe CB. Efectele consumului de suc de rodie asupra tensiunii arteriale și a sănătății cardiovasculare.
- Adamowicz J, Drewa T. Există o legătură între băuturile răcoritoare și disfuncția erectilă?
- Neves D. Produse finale avansate de glicație: o cale comună în diabet și disfuncție erectilă legată de vârstă.
- Uribarri J, del Castillo MD, de la Maza MP, et al. Produse finale alimentare cu glicație avansată și rolul lor în sănătate și boală.
- Uribarri J, Woodruff S, Goodman S, et al. Produse finale avansate de glicație în alimente și un ghid practic pentru reducerea lor în dietă.
- Maiorino MI, Bellastella G, Chiodini P, et al. Prevenirea primară a disfuncției sexuale cu dieta mediteraneană în diabetul de tip 2: studiul randomizat MÈDITA.
- Di Francesco S, Tenaglia R. Dieta mediteraneană și disfuncția erectilă: o perspectivă actuală.
- Slentz CA, Houmard JA, Johnson JL, et al. Inactivitate, antrenament și dezinformare și lipoproteine plasmatice. STRRIDE: un studiu randomizat, controlat al intensității și cantității exercițiului.
- Di Francescomarino S, Sciartilli A, Di Valerio, et al. Efectul exercițiului fizic asupra funcției endoteliale.
- Walther C, Gielen S, Hambrecht R. Efectul antrenamentului fizic asupra funcției endoteliale în bolile cardiovasculare la om.
- Fuchsjager-Mayrl G, Pleiner J, Wiesinger GF, et al. Antrenamentul fizic îmbunătățește funcția endotelială vasculară la pacienții cu diabet zaharat de tip 1.
- Vina J, Sanchis-Gomar F, Martinez-Bellow V, et al. Exercițiul acționează un drog; beneficiile farmacologice ale exercițiilor fizice.
- Silva A, Sousa N, Azevedo LF, et al. Activitate fizică și exerciții fizice pentru disfuncția erectilă: revizuire sistematică și meta-analiză.
- Cho YG, Song HJ, Lee SK, et al. Relația dintre masa de grăsime corporală și disfuncția erectilă la bărbații coreeni: Studiul Hallym Aging.
- Diaz-Arjonilla M, Schwarcz M, Swerdloff RS, et al. Obezitate, niveluri scăzute de testosteron și disfuncție erectilă.
- Kapoor D, Clarke S, Channer KS, et al. Disfuncția erectilă este asociată cu niveluri scăzute de testosteron bioactiv și adipoziție viscerală la bărbații cu diabet zaharat de tip 2.
- Fantuzzi G. Țesut adipos, adipokine și inflamație.
- Mattu HS, Randeva HS. Rolul adipokinelor în bolile cardiovasculare.
- Giugliano F. Disfuncția erectilă se asociază cu disfuncția endotelială și nivelurile crescute de citokine proinflamatorii la bărbații obezi.
- Evans M. Pierde în greutate pentru a pierde disfuncția erectilă.
- Millan MJ, Newman-Tancredi A, Audinot V, et al. Acțiunile agoniste și antagoniste ale yohimbinei în comparație cu fluparoxan la receptorii alfa(2)-adrenergici (AR), serotonina (5-HT)(1A), 5-HT(1B), 5-HT(1D) și dopamină D( 2) și receptorii D(3). Semnificație pentru modularea transmisiei monoaminergice frontocorticale și a stărilor depresive.
- Ernst E, Pittler MH. Yohimbina pentru disfuncția erectilă: o revizuire sistematică și meta-analiză a studiilor clinice randomizate.
- Carey MP, Johnson BT. Eficacitatea yohimbinei în tratamentul tulburării erectile: patru integrări meta-analitice.
- Adeniyi AA, Brindley GS, Pryor JP, et al. Yohimbina în tratamentul disfuncției orgasmice.
- Cohen PA, Wang YH, Maller G, et al. Cantități farmaceutice de yohimbină găsite în suplimentele alimentare din SUA.
- Neychev V, Mitev V. Efecte pro-sexuale și de îmbunătățire a androgenilor Tribulus terrestris L.: Realitate sau ficțiune?
- Gauthaman K, Ganesan AP. Efectele hormonale ale Tribulus terrestris și rolul său în gestionarea disfuncției erectile masculine – o evaluare folosind primate, iepuri și șobolani.
- Qureshi A, Naughton DP, Petroczi A. O revizuire sistematică a extractului de plante Tribulus terrestris și rădăcinile presupusului său efect afrodisiac și de îmbunătățire a performanței.
- Neychev VK, Mitev Vi. Planta afrodisiacă Tribulus terrestris nu influențează producția de androgeni la bărbați tineri.
- Gauthaman K, Ganesan AP, Prasad RN. Efectele sexuale ale puncturevine (Tribulus terrestris) extract (protodioscin): o evaluare folosind un model de șobolan.
- Adaikan PG, Gauthaman K, Prasad RN, et al. Efectele farmacologice proerectile ale Tribulus terrestris extract pe corpus cavernosum de iepure.
- Kamenov Z, Fileva S, Kalinov K, et al. Evaluarea eficacității și siguranței Tribulus terrestris în disfuncția sexuală masculină – un studiu clinic prospectiv, randomizat, dublu-orb, controlat cu placebo.
- Kotirum S, Ismail SB, Chaiyakunapruk N. Eficacitatea lui Tongkat Ali (Eurycoma longifolia) privind îmbunătățirea funcției erectile: revizuire sistematică și meta-analiză a studiilor controlate randomizate.
- Joi HE, Mohamed IN, Hussain Z, et al. Eurycoma longifolia ca un potențial adoptogen al sănătății sexuale masculine: o revizuire sistematică a studiilor clinice.
- Talbott SM, Talbott J, George A, et al. Efectul Tongkat Ali asupra hormonilor de stres și asupra stării psihologice de dispoziție la subiecții stresați moderat.
- Dell'Agli M, Galli GV, Dal Cero, et al. Inhibarea puternică a fosfodiesterazei-5 umane de către derivații de icariină.
- Ning H, Xin ZC, Lin G, et al. Efectele icariinei asupra activității fosfodiesterazei-5 in vitro și a nivelului de guanozin monofosfat ciclic în celulele musculare netede cavernoase.
- Jiang Z, Hu B, Wang J, et al. Efectul icariinei asupra nivelurilor ciclice de GMP și asupra expresiei ARNm a fosfodiesterazei specifice de cGMP care leagă cGMP (PDE5) în cavernosul penian.
- Romero M, Platt DH, Tawfik HE, et al. Disfuncția vasculară coronariană indusă de diabet implică creșterea activității arginazei.
- Schramm L, La M, Heidbreder E, et al. Deficiența de L-arginină și suplimentarea în insuficiența renală acută experimentală și în transplantul de rinichi uman.
- Curis E, Nicolis I, Moinard C, et al. Aproape totul despre citrulină la mamifere.
- Bode-Böger SM, Böger RH, Galland A, et al. Vasodilatația indusă de L-arginina la oameni sănătoși: relație farmacocinetic-farmacodinamică.
- Chen J, Wollman Y, Chernichovsky T, et al. Efectul administrării orale a L-argininei donorului de oxid nitric în doze mari la bărbații cu disfuncție erectilă organică: rezultatele unui studiu dublu-orb, randomizat, controlat cu placebo.
- Bode-Böger SM, Scalera F, Ignarro LJ. Paradoxul L-argininei: importanța raportului L-arginina/dimetilarginina asimetrică.
- Lebret T, Hervé JM, Gorny P, et al. Eficacitatea și siguranța unei noi combinații de glutamat de L-arginină și clorhidrat de yohimbină: o nouă terapie orală pentru disfuncția erectilă.
- Akhondzadeh S, Amiri A, Bagheri A. Eficacitatea și siguranța combinației orale de yohimbină și L-arginină (SX) pentru tratamentul disfuncției erectile: un studiu clinic multicentric, randomizat, dublu orb, controlat cu placebo.
- Stanislavov R, Nikolova V. Tratamentul disfuncției erectile cu picnogenol și L-arginină.
- Schulman SP, Becker LC, Kass DA, Terapia cu L-arginina în infarctul miocardic acut: interacțiunea vasculară cu vârsta în infarctul miocardic (VINTAGE MI) studiu clinic randomizat.
- Saenz de Tejada I, Angulo J, Cuevas P, et al. Profiluri de selectivitate comparative ale tadalafilului, sildenafilului și vardenafilului utilizând un test de activitate a fosfodiesterazei in vitro.
- Evans J, Hill S. O comparație a inhibitorilor fosfodiesterazei-5 disponibili în tratamentul disfuncției erectile: un accent pe avanafil.
- Chavez A, Coffield KS, Rajab MH, Jo C. Rata de incidență a cancerului de prostată la bărbații tratați pentru disfuncție erectilă cu inhibitori ai fosfodiesterazei de tip 5: analiză retrospectivă.
- Rider JR, Wilson KM, Sinnott JA, et al. Frecvența ejaculării și riscul de cancer de prostată: rezultate actualizate cu un deceniu suplimentar de urmărire.
- Tang H, Wu W, Fu S, et al. Inhibitorii fosfodiesterazei de tip 5 și riscul de melanom: o meta-analiză.
- Chen KK, Chan JY, Chang LS. Neurotransmisia dopaminergică la nucleul paraventricular al hipotalamusului în reglarea centrală a erecției penisului la șobolan.
- Altwein JE, Keuler FU. Tratamentul oral al disfuncției erectile cu apomorfină SL.
- Heaton JP. Probleme cheie din studiile clinice ale apomorfinei SL.
- Linet OI, Ogring FG. Eficacitatea și siguranța alprostadilului intracavernos la bărbații cu disfuncție erectilă.
- Porst H, Buvat J, Meuleman E, et al. Alprostadil alfadex intracavernos – un tratament eficient și bine tolerat pentru disfuncția erectilă. Rezultatele unui studiu european pe termen lung.
- Baniel J, Israilov S, Engelstein D, et al. Rezultatul de trei ani al unui program de tratament progresiv pentru disfuncția erectilă cu injecții intracavernoase cu medicamente vasoactive.
- Bernie HL, Segal R, Le B, et al. Un algoritm de abordare empiric vs bazat pe risc pentru terapia cu injecție intracavernosă: un studiu prospectiv.
- Albaugh J. Algoritm de injectare intracavernosă.
- Young SR, Dyson M. Efectul ultrasunetelor terapeutice asupra angiogenezei.
- Lu Z, Lin G, Reed-Maldonado A, et al. Tratamentul cu undă de șoc extracorporeală de intensitate scăzută îmbunătățește funcția erectilă: o revizuire sistematică și meta-analiză.
- Qiu X, Lin G, Xin Z, et al. Efectele terapiei cu unde de șoc cu energie scăzută asupra funcției erectile și a țesutului unui model de șobolan diabetic.
- Lin G, Reed-Maldonado AB, Wang B, et al. Activarea in situ a celulelor progenitoare penisului cu terapie cu unde de șoc extracorporală de intensitate scăzută.
- Vardi Y, Appel B, Jacob G, et al. Poate terapia cu unde de șoc extracorporală de intensitate scăzută să îmbunătățească funcția erectilă? Un studiu pilot de urmărire de 6 luni la pacienții cu disfuncție erectilă organică.
- Vardi Y, Appel B, Kilchevsky A, et al. Terapia cu unde de șoc extracorporală de intensitate scăzută are un efect fiziologic asupra funcției erectile? Rezultatele pe termen scurt ale unui studiu randomizat, dublu-orb, controlat simulat.
- Srini VS, Reddy RK, Shultz T, et al. Terapia cu unde de șoc extracorporală de intensitate scăzută pentru disfuncția erectilă: un studiu la o populație indiană.
- Gruenwald I, Appel B, Vardi Y. Terapia cu unde de șoc extracorporale de intensitate scăzută – un nou tratament eficient pentru disfuncția erectilă la pacienții cu disfuncție erectilă severă care răspund slab la terapia cu inhibitor PDE5.
- Kitrey ND, Gruenwald I, Appel B, et al. Tratamentul cu unde de șoc de intensitate scăzută a penisului este capabil să transfere persoanele care nu răspund la PDE5i către cei care au răspuns: un studiu dublu-orb, controlat în mod simulat.
- Olsen AB, Persiani M, Boie S, et al. Poate terapia cu unde de șoc extracorporală de intensitate scăzută să îmbunătățească disfuncția erectilă? Un studiu prospectiv, randomizat, dublu-orb, controlat cu placebo.
- Bechara A, Casabé A, De Bonis W, et al. Eficacitatea și siguranța de douăsprezece luni a terapiei cu unde de șoc de intensitate scăzută pentru disfuncția erectilă la pacienții care nu răspund la inhibitorii fosfodiesterazei de tip 5.
- Fojecki GL, Tiessen S, Osther PJ. Efectul terapiei cu unde de șoc liniare cu energie scăzută asupra disfuncției erectile - un studiu clinic dublu-orb, controlat de simulare, randomizat.
- Fojecki GL, Tiessen S, Osther PJ. Efectul terapiei cu unde de șoc extracorporale liniare de intensitate scăzută pentru disfuncția erectilă - urmărire de 12 luni a unui studiu randomizat, dublu-orb, controlat de simulare.
- Kitrey ND, Vardi Y, Appel B, et al. Tratament cu undă de șoc de intensitate scăzută pentru disfuncția erectilă - cât durează efectul?
- Gruenwald I, Kitrey ND, Apel B, et al. Terapia cu unde de șoc extracorporală de intensitate scăzută în bolile vasculare și disfuncția erectilă: teorie și rezultate.
- Clavijo R, Kohn TP, Kohn JR, et al. Efectele terapiei cu unde de șoc extracorporale de intensitate scăzută asupra disfuncției erectile: o revizuire sistematică și meta-analiză.
- Pavlovic V, Ciric M, Jovanovic V, et al. Plasma bogată în trombocite: o scurtă prezentare a anumitor componente bioactive.
- Coppinger JA, Cagney G, Toomey S, et al. Caracterizarea proteinelor eliberate din trombocitele activate duce la localizarea de noi proteine plachetare în leziunile aterosclerotice umane.
- Yu W, Wang J, Yin J. Plasmă bogată în trombocite: un produs promițător pentru tratamentul regenerării nervilor periferici după leziuni ale nervilor.
- Banno JJ, Kinnick TR, Roy L, et al. Eficacitatea plasmei bogate în trombocite (PRP) ca terapie suplimentară pentru tratamentul disfuncției erectile (DE): rezultate inițiale.
- Baumhäkel M, Werner N, Bohm M, et al. Celulele progenitoare endoteliale circulante se corelează cu funcția erectilă la pacienții cu boală coronariană.
- Ichim TE, Warbington T, Cristea O, et al. Administrarea intracavernoasă a celulelor mononucleare ale măduvei osoase: o nouă metodă de tratare a disfuncției erectile?
- Franck-Lissbrant I, Häggström S, Damber JE, et al. Testosteronul stimulează angiogeneza și recreșterea vasculară în prostata ventrală la șobolanii adulți castrați.
- Sieveking DP, Chow RW, Ng MK. Androgeni, angiogeneză și regenerare cardiovasculară.
- Mingchao Li, Ruan Y, Wang T, et al. Terapia cu celule stem pentru disfuncția erectilă diabetică la șobolani: o meta-analiză.
- Lin CS, Xin ZC, Wang Z, et al. Terapia cu celule stem pentru disfuncția erectilă: o revizuire critică.
- Haahr MK, Jensen CH, Toyserkani NM, et al. Siguranța și efectul potențial al unei singure injecții intracavernoase de celule regenerative autologe derivate din adipos la pacienții cu disfuncție erectilă după prostatectomie radicală: un studiu clinic de fază I deschis.
- Yiou R, Hamidou L, Birebent B, et al. Siguranța celulelor mononucleare ale măduvei osoase intracavernoase pentru disfuncția erectilă postradicală de prostatectomie: un studiu pilot deschis de escaladare a dozei.
- Mousavinejad M, Andrews P, Shoraki E. Considerații actuale de biosecuritate în terapia cu celule stem.
