コメント:後の研究で明らかになるように、DeltaFosBは薬物依存症と行動依存症の両方に共通の分子スイッチです。 これは転写因子であり、どの遺伝子がオンまたはオフになるかに影響します。 他の場所で述べられているように、中毒性のある薬物は通常のメカニズムを乗っ取るだけです。 だから、行動中毒が存在できないと示唆するのはばかげています。
Proc Natl Acad Sci US A. 2001 9月25; 98(20):11042 - 11046。
土井:10.1073 / pnas.191352698。
Eric J. Nestler *、Michel Barrot、およびDavid W. Self
テキサス大学サウスウェストメディカルセンター、テキサス州ダラス、精神神経科および基礎神経科学センター5323-75390
抽象
薬物中毒を特徴付けるいくつかの行動異常の寿命は、乱用薬物が中毒状態を引き起こす過程に神経遺伝子発現の調節が関与している可能性があることを示唆している。 私ますます多くの証拠が、転写因子ΔFosBが、乱用薬物が中毒表現型の一因となる比較的安定した変化を脳内にもたらす一つのメカニズムを表すことを示唆している。 ΔFosB転写因子のFosファミリーのメンバーは、多くの種類の乱用薬物を繰り返し投与した後、側坐核および背側線条体(中毒に重要な脳領域)のニューロンのサブセット内に蓄積する。 ΔFosBの同様の蓄積は強制走行後にも起こり、これはΔFosBが多くのタイプの強制行動に応じて蓄積することを示唆している。。 重要なことに、ΔFosBは、その驚くべき安定性のために比較的長期間にわたってニューロン内に存続する。 したがって、ΔFosBは、薬物曝露が停止した後も長く続く遺伝子発現の変化を開始し、その後持続させることができる分子メカニズムを表しています。。 ΔFosBまたはタンパク質のドミナントネガティブインヒビターのいずれかを過剰発現する誘導性トランスジェニックマウスにおける研究は、ΔFosBが乱用薬物の行動効果に対する感受性の増加およびおそらく薬物探索行動の増加を引き起こすという直接的な証拠を提供する。 この研究は、ΔFosBが急性薬物反応を中毒の根底にある長期的な神経および行動の可塑性に寄与する比較的安定した適応に徐々に変換する一種の持続的「分子スイッチ」として機能するという見解を支持する。
依存症研究は、乱用薬物が脳を変化させて依存症を特徴付ける行動異常を引き起こす複雑な方法を理解することに焦点を当てています。 この分野における重大な課題の1つは、特に長命であるそれらの行動異常を説明するために比較的安定した薬物誘発性の脳内変化を同定することである。 例えば、人間の常習者は何年もの禁酒の後でさえも再発の危険性が高いかもしれません。
これらの行動異常の安定性は、少なくとも部分的には、遺伝子発現の変化(1〜3)によって媒介される可能性があることを示唆しています。 この見解によれば、乱用薬物への反復曝露は、薬物に敏感な脳内の特定のシナプスでの伝播を繰り返し混乱させる。 そのような摂動は最終的に細胞内メッセンジャーカスケードを介して核にシグナルを送り、そこでそれらは最初に特定の遺伝子の発現の変化を開始しそして次に維持する。 シグナル伝達経路が遺伝子発現に影響を与える主なメカニズムは、転写因子、すなわち遺伝子の調節領域に結合してそれらの転写を修飾するタンパク質の調節である。
したがって、依存症研究の目的の1つは、乱用薬物の長期投与後に依存症に関与すると考えられる脳領域で変化する転写因子を同定することです。 このような転写因子は過去10年間にいくつか同定されています(1〜6)。 このレビューの焦点は、ΔFosBと呼ばれる1つの特定の転写因子にあります。
乱用薬物によるΔFosBの誘導
fosB遺伝子によってコードされるΔFosBは、c − Fos、FosB、FraXNUMX、およびFraXNUMX(XNUMX)も含む転写因子のFosファミリーの一員である。 これらのFosファミリータンパク質は、Junファミリータンパク質(c-Jun、JunB、またはJunD)とヘテロ二量体化して、AP-1部位(コンセンサス配列:TGAC / GTCA)に結合する活性型AP-2(アクチベータータンパク質-7)転写因子を形成する。それらの転写を調節する特定の遺伝子のプロモーター。
これらのFosファミリータンパク質は、多くの乱用薬物の急性投与後に特定の脳領域で急速かつ一過性に誘発されます(図1)(8〜11)。 顕著な領域は、側坐核および背側線条体であり、これらは薬物に対する行動反応、特にそれらのやりがいおよび自発運動活性化作用の重要な媒介物質である(12、13)。 これらのタンパク質は薬物投与後数時間以内に基礎レベルに戻る。
図1
乱用薬物に反応してのΔFosBの漸進的蓄積対他のFosファミリータンパク質の急速で一過性の誘導を示すスキーム。 (A)オートラジオグラムは、慢性刺激(反復薬物曝露後の1日)に対する急性刺激(2〜1 1時間の薬物曝露後)によるこれらの様々なタンパク質の示差的誘導を示しています。 (B)Fos様タンパク質のいくつかの波(c-Fos(52-から58-kDaアイソフォーム)、FosB(46-から50-kDaアイソフォーム)、およびΔFosB(33-kDaアイソフォーム)、およびFra1またはFra2(からなる) XNUMX [kDa]]は、乱用薬物の急性投与によって側坐核および背側線条体ニューロンにおいて誘導される。 ΔFosBの生化学的に修飾されたアイソフォーム(40〜35 kDa)も誘導される。 それらもまた、(低いレベルではあるが)急性薬物投与後に誘発されるが、それらの安定性のために長期間脳内に持続する。 (C)反復(例えば、1日2回)薬物投与では、各急性刺激は低レベルの安定なΔFosBアイソフォームを誘導し、それは各急性刺激によって誘導されたΔFosBを示す下線の重なり線によって示される。 結果は、慢性治療の過程の間に刺激を繰り返すとΔFosBの総レベルが徐々に増加することであり、それはグラフ中の増加する階段状の線によって示される。
乱用薬物の長期投与後には、非常に異なる反応が見られます(図1)。。 ΔFosBの生化学的に修飾されたアイソフォーム(分子量35〜37 kDa)は、反復薬物曝露後に同じ脳領域内に蓄積しますが、他のすべてのFosファミリーメンバーは耐性を示します(つまり、初期薬物曝露と比較して誘導が減少します)。 このようなΔFosBの蓄積は、コカイン、モルヒネ、アンフェタミン、アルコール、ニコチン、およびフェンシクリジンについて観察されている。e(11、14 - 18) この誘導がこれらの脳領域に位置する中型有棘ニューロンのダイノルフィン/サブスタンスP含有サブセット(XNUMX、XNUMX)に対して選択的であるといういくつかの証拠があるが、これを確実に確立するためにはさらなる研究が必要である。 ΔFosBのXNUMX−からXNUMX − kDaのアイソフォームは、主にJunDと二量体化して、これらの脳領域内に活性で持続性のAP − XNUMX複合体を形成する(XNUMX、XNUMX)。 これらのΔFosBアイソフォームは、それらの異常に長い半減期(XNUMX)のために慢性的な薬物曝露と共に蓄積し、それ故、薬物投与の停止後少なくとも数週間はニューロン中に持続する。 これらのΔFosBアイソフォームは前初期遺伝子(fosB)の非常に安定な産物であることに注目することは興味深い。 ΔFosBアイソフォームの安定性は、比較的長期間の薬物中止にもかかわらずそれによって遺伝子発現における薬物誘導変化が持続することができる新規な分子機構を提供する。
側坐核は乱用薬物の有益な効果において重要な役割を果たすが、それは通常、食物、飲み物、性別、および社会的相互作用などの天然の強化剤に対する反応を調節することによって機能すると考えられている(12、13)。 結果として、他の強迫行動(例えば、病的過食、ギャンブル、運動など)におけるこの脳領域の可能な役割にかなりの関心が寄せられています。 この理由のために、我々は、ΔFosBが強制走行の動物モデルにおいて調節されるかどうかを調べた。 実際、ΔFosBの安定な35-to-37-kDaアイソフォームはラットの側坐核内で選択的に誘導され、強制的な走り行動を示します†。
安定なΔFosBアイソフォームの生化学的同一性
上記のように、乱用薬物または強制薬物療法の慢性投与後に蓄積するΔFosBアイソフォームは、35〜37 kDaの分子量を示す。 それらは、単一薬物曝露後に急速に、しかし一時的に誘導されるΔFosBの33-kDaアイソフォームと区別することができる(1、14、19)。 現在の証拠は、22-kDaアイソフォームがタンパク質の天然型であり、それがより安定な33〜35-kDa産物(37、19)を形成するように改変されていることを示唆している。 しかしながら、不安定なXNUMX − kDaアイソフォームを安定なXNUMX − 〜XNUMX − kDaアイソフォームに変換する生化学的修飾の性質は不明のままである。 リン酸化が原因であり得ると推測されている(XNUMX)。 例えば、ΔFosBの誘導は、DARPP-21、線条体濃縮タンパク質(33、35)を欠くマウスにおいて減弱する。 DARPP - XNUMXは、プロテインホスファターゼ-XNUMXおよびプロテインキナーゼA(XNUMX、XNUMX)の触媒活性を調節するので、安定なΔFosBアイソフォームの正常な蓄積に対するこのタンパク質の必要性は、これらの安定な生成物の生成におけるリン酸化の役割の可能性を示唆する。
薬物乱用に対する行動可塑性におけるΔFosBの役割
薬物依存症におけるΔFosBの役割への洞察は、ΔFosBが成体動物の側坐核および他の線条体領域内で選択的に誘導され得るトランスジェニックマウス(XNUMX、XNUMX)の研究から主にもたらされた。 重要なことに、これらのマウスは、薬物がタンパク質を誘導すると考えられているダイノルフィン/サブスタンスP含有中型有棘ニューロンにおいて選択的にΔFosBを過剰発現する。 ΔFosB過剰発現マウスの行動表現型は、多くの点で慢性薬物曝露後の動物に似ているが、表XNUMXに要約されている。 マウスは、急性および慢性投与後にコカインに対する自発運動反応の増強を示す(27)。 それらはまた、プレースコンディショニングアッセイ(28、1)におけるコカインおよびモルヒネのやりがいのある効果に対して高い感受性を示し、そしてΔFosBを過剰発現しない同腹仔よりも低用量のコカインを自己投与するであろう。モリス水迷路(28)におけるコカイン感作と通常の空間学習 Tこれらのデータは、ΔFosBがコカインおよびおそらく他の乱用薬物に対する動物の感受性を高め、薬物に対する比較的長期の感作のメカニズムを表している可能性があることを示しています.
 線条体
線条体
| 急性および反復コカイン投与に反応して自発運動が増加する。 |
| プレースコンディショニングアッセイにおけるコカインとモルヒネに対するやりがいのある反応 |
| 低用量コカインの自己投与量の増加。 |
| プログレッシブレシオアッセイにおけるコカインの動機づけの向上 |
| アルコールに対する抗不安反応の増加 |
| 強制的なランニング行動を増やしました。 |
参考文献のデータに基づく。 28 & 29.†‡¶
側坐核 - 背側線条体におけるΔFosBにより媒介される行動可塑性
Iさらに、ΔFosBの効果が薬物依存性それ自体の調節をはるかに超えて中毒プロセスに関連するより複雑な行動に及ぶ可能性があるという予備的証拠がある。 ΔFosBを発現するマウスは、プログレッシブレシオ自己投与アッセイにおいてコカインを自己投与することがより困難である。ΔFosBがコカインの動機付けとなる動機付け特性に対して動物を敏感にし、それによって薬物離脱後の再発傾向につながることを推測l。ΔFosB発現マウスはまた、アルコールの抗不安作用を示し、これはヒトにおけるアルコール摂取の増加と関連している表現型である。 まとめると、これらの初期の発見は、乱用薬物に対する感受性の増加に加えて、ΔFosBが薬物探索行動を促進する行動の質的変化を引き起こすことを示唆している。 したがって、ΔFosBは、嗜癖状態の重要な局面を開始し、次いで維持するのを助ける持続的な「分子スイッチ」として機能し得る。 現在の調査中の重要な問題は、薬物曝露中のΔFosB蓄積が、ΔFosBレベルが正常化した後でさえも、長期間の禁断期間後に薬物探索行動を促進するかどうかである(下記参照)。
成人 側坐核および背側線条体内で選択的にΔFosBを過剰発現するマウスは、対照同腹仔と比較してより強い強制走行を示す。おそらく、それらのニューロンが機能する神経回路の有効性を強化することによって。
ΔFosBは、コカインへの長期曝露後に側坐核および背側線条体の外側の特定の脳領域に蓄積する。 これらの間で著名な 領域は扁桃体および内側前頭前野である (15) 現在の研究の主な目的は、中毒表現型に対するこれらの領域におけるΔFosB誘導の寄与を理解することである。
fosBノックアウトマウスに関する初期の研究により、これらの動物はコカインの自発運動効果に対する感作を起こさないことが明らかになりました。これは、上記のΔFosB過剰発現マウスの発見と一致しています(22)。 ただし、fosB変異体は、コカインの急性効果に対する感受性の向上を示しました。これは、これらの他の発見と一致していません。 しかし、fosB変異体による所見の解釈は、これらの動物がΔFosBだけでなく完全長のFosBも欠いているという事実によって複雑になっています。 さらに、変異体は脳全体と発達の初期段階から両方のタンパク質を欠いています。 実際、より最近の研究は、ΔFosB過剰発現マウスからの結論を支持しています:側坐核および背側線条体において選択的にΔFosBのドミナントネガティブアンタゴニストとして作用するc-Junの短縮型変異体の誘導性過剰発現は、コカインの報酬効果に対する感受性の低下を示します.¶これらの発見は、構成的突然変異を有するマウスからの結果を解釈する際に使用しなければならない注意を強調し、成人の脳の可塑性の研究における誘導性および細胞型特異的突然変異を有するマウスの重要性を示しています。
ΔFosBの標的遺伝子
ΔFosBは転写因子であるため、おそらくこのタンパク質は他の遺伝子の発現の変化を通して行動的可塑性を引き起こす。 ΔFosBは、fosB遺伝子の選択的スプライシングによって生成され、そして全長FosB中に存在するC末端トランス活性化ドメインの一部を欠く。 その結果、ΔFosBが転写抑制因子(XNUMX)として機能することが当初提案された。 しかしながら、細胞培養における研究は明らかにΔを証明した。FosB 誘発または抑制できる 使用される特定のAP-1部位に応じたAP-1を介した転写(21、29〜31)。 全長FosBは、あるプロモーター断片に対してはΔFosBと同じ効果を発揮するが、他に対しては異なる効果を発揮する。 ΔFosBおよびFosBのこれらの多様な作用の根底にあるメカニズムを理解するためにはさらなる研究が必要である。
私たちのグループは、ΔFosBの標的遺伝子を特定するために3つのアプローチを使用しました。 5つは候補遺伝子アプローチです。 側坐核におけるグルタミン酸作動性伝達の重要な役割を考慮して、当初、α-アミノ-4-ヒドロキシ-2-メチル-2-イソキサゾールプロピオン酸(AMPA)グルタメート受容体を推定標的と見なしました。 これまでの研究により、特定のAMPAグルタミン酸受容体サブユニットであるGluR2がΔFosBの真正な標的である可能性があることが示されています(図28)。 GluR2の発現は、他のAMPA受容体サブユニットの発現ではなく、ΔFosBの過剰発現時に側坐核(背側線条体ではない)で増加し(1)、ドミナントネガティブ変異体の発現はコカインがタンパク質を誘導する能力を弱めます。さらに、GluR28遺伝子のプロモーターには、ΔFosBに結合するコンセンサスAP-2部位が含まれています(28)。 側坐核におけるGluR2の過剰発現は、ウイルスを介した遺伝子導入を使用することにより、コカインの報酬効果に対する動物の感受性を高め、それによってΔFosB発現マウスに見られる表現型の一部を模倣します(32)。 GluR2を含むAMPA受容体は全体的なコンダクタンスの低下とCa2 +透過性の低下を示すため、GluRXNUMXの誘導は、慢性コカイン投与後の側坐核ニューロンのAMPA受容体アゴニストに対する電気生理学的感受性の低下を説明できます(XNUMX)。 興奮性入力に対するこれらのニューロンの応答性の低下は、乱用薬物への応答を強化する可能性があります。 ただし、側坐核のドーパミン作動性およびグルタミン酸作動性シグナルが習慣性行動を調節する方法は不明のままです。 これには神経回路レベルの理解が必要ですが、これはまだ利用できません。
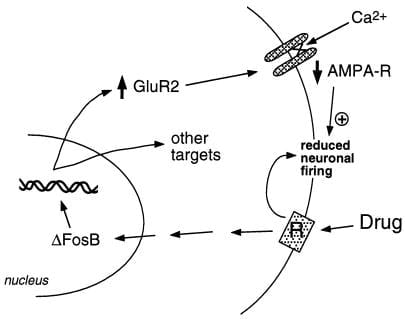
図2
AMPAグルタミン酸受容体サブユニットであるGluR2は、ΔFosBの推定標的です。 示されているのは、ΔFosBを介したGluR2の誘導が、側坐核ニューロンの生理学的反応性を変化させ、乱用薬物に対する感作反応を引き起こす可能性があることです。 このスキームによると、乱用薬物は側坐核ニューロンの抑制を介してそれらの急性強化効果を生み出します。 繰り返し曝露されると、薬物はΔFosBを誘導し、これはGluR2を含む多数の標的遺伝子を調節します。 これにより、GluR2サブユニットを含む側坐核ニューロン上のAMPA受容体(AMPA-R)の割合が増加し、全体的なAMPA電流とCa2 +電流が減少します。 この興奮性の低下は、ニューロンを薬物の急性抑制効果、ひいては薬物の強化効果に対してより敏感にする可能性があります。.
ΔFosBに対する別の推定標的は、ダイノルフィンをコードする遺伝子である。. 前述のように、ダイノルフィンは、ΔFosBの誘導を示す側坐核中型有棘ニューロンのサブセットで発現される。. ダイノルフィンは細胞間フィードバックループで機能するように見える:側坐核のドーパミン作動性神経終末および腹側被蓋野の細胞体および樹状突起に存在するκオピオイド受容体を介して中型有棘ニューロンを神経支配するドーパミン作動性ニューロンを阻害する (図3)(33 - 35)。 この考えは、これら2つの脳領域のいずれかに投与した際の、κ受容体作動薬の薬物耐性を低下させる能力と一致する。d(35)
Rこれまでの研究により、ΔFosBはダイノルフィンの発現を減少させることが示唆されており、これはΔFosBの誘導に見られる報酬メカニズムの強化に寄与し得る。 興味深いことに、もう1つの薬物制御転写因子CREB(cAMP応答配列結合タンパク質)(2、3)は、反対側の効果を発揮します:側坐核においてダイノルフィンの発現を誘導し、コカインとモルヒネの価値のある特性を低下させます (4)。**
BCREBの薬物誘発活性化は薬物投与後に急速に消散するため、CREBとΔFosBによるダイノルフィンの相互制御は、負の感情的症状と初期段階で優勢な薬物感受性の低下を伴って、離脱の初期と後期に起こる相互行動変化を説明できる離脱の兆候、および後の時点で優位を占める薬物のやりがいのある、動機付けの動機づけ効果への感作。
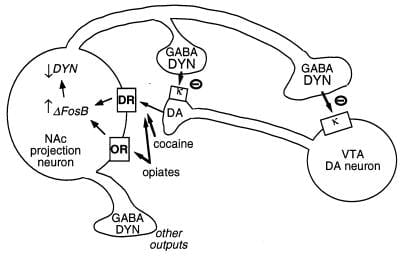
図3
ダイノルフィンはΔFosBの推定標的である。 ダイノルフィン(DYN)を発現する側坐核(NAc)GABA作動性投射ニューロンのクラスを神経支配する腹側被蓋野(VTA)ドーパミン(DA)ニューロンが示されている。 ダイノルフィンはこの回路においてフィードバック機構を果たす:NAcニューロンの末端から放出されるダイノルフィンは、神経末端およびDAニューロンの細胞体に位置するκオピオイド受容体に作用してそれらの機能を阻害する。 ΔFosBは、ダイノルフィン発現を阻害することによって、このフィードバックループを下方制御し、そして乱用薬物の有益な特性を増強し得る。 この系に対するCREBの相反効果は示されていない:CREBはダイノルフィン発現を増強し、それによって乱用薬物の有益な性質を弱める。 (4) GABA、γ-アミノ酪酸。 DR、ドーパミン受容体。 または、オピオイド受容体。
ΔFosBの標的遺伝子を同定するために使用される36番目のアプローチには、DNAマイクロアレイ分析が含まれます。 ΔFosBの誘導性過剰発現は、側坐核における多数の遺伝子の発現を増加または減少させます(5)。 これらの遺伝子のそれぞれをΔFosBの生理学的標的として検証し、依存症の表現型への寄与を理解するには、現在かなりの作業が必要ですが、重要な標的の5つはCdk5(サイクリン依存性キナーゼ-37)のようです。 したがって、Cdk5は、マイクロアレイを使用してΔFosBによって調節されるものとして最初に同定され、その後、慢性的なコカイン投与後に側坐核および背側線条体で誘導されることが示されました(1)。 ΔFosBは、遺伝子のプロモーター内に存在するAP-36部位を介してcdk5遺伝子を活性化します(5)。 一緒に、これらのデータは、コカインがΔFosBを介してこれらの脳領域でCdk32発現を誘導するスキームをサポートしています。 Cdk37の誘導は、Cdk1によるリン酸化の際にプロテインホスファターゼ-5の阻害剤からプロテインキナーゼAの阻害剤に変換されるDARPP-26(XNUMX)のリン酸化の増加を介して、ドーパミン作動性シグナル伝達を少なくとも部分的に変化させるようです(XNUMX)。
薬物乱用に対する「永久的」可塑性の仲介におけるΔFosBの役割
ΔFosBシグナルは比較的長命ですが、恒久的なものではありません。 ΔFosBは徐々に分解し、1〜2ヶ月間の薬物中止後、脳内では検出されなくなります。ただし、特定の行動異常がはるかに長期間続く場合でも同様です。 それ故、ΔFosBそれ自体はこれらの半永久的な行動異常を媒介することができないようである。 中毒に関連する非常に安定した行動変化の根底にある分子適応を見つけることの難しさは、学習と記憶の分野で直面する課題と類似しています。 洗練された細胞と分子の学習と記憶のモデルがありますが、今日まで非常に安定した行動記憶を説明するのに十分な長さである分子と細胞の適応を識別することは不可能でした。 確かに、ΔFosBは、乱用薬物に反応するだけでなく、他の摂動(病変を伴わない)にも反応して、成人の脳で発生することが知られている最も長命の適応です。 この不一致を説明するために、依存症と学習および記憶の両方の分野でXNUMXつの提案が展開されました。
1つの可能性は、ΔFosBまたは他の転写因子(例えばCREB)を介して媒介されるもののような、遺伝子発現におけるより一時的な変化であり、 神経細胞の形態およびシナプス構造のより長期にわたる変化を媒介する可能性があります。 たとえば、 樹状突起棘の密度の増加(特に両頭棘の増加)は、 グルタミン酸作動性シナプスの有効性の増加 長期増強中の海馬錐体神経細胞(38〜40)で、側坐核の中型有棘ニューロン(41)のレベルで仲介されるコカインに対する強化された行動感受性に匹敵する。 後者の変化が少なくとも1月の薬物禁断の間持続するが、そのような構造変化が非常に安定した行動変化を説明するのに十分に長寿命であるかどうかは知られていない。 最近の証拠は、ΔFosB、およびそのCdk5の誘導が、側坐核におけるシナプス構造の薬物誘導性変化の1つのメディエータであるという可能性を提起している(図4)。この領域で樹状突起棘密度を増加させるための反復コカイン暴露の能力。 これは、脳に富むCdkXNUMXが神経構造および成長を調節するという見解と一致する(参考文献XNUMXおよびXNUMXを参照のこと)。 決して証明されたわけではないが、そのようなニューロン形態の変化は、ΔFosBシグナルそれ自体に勝る可能性がある。
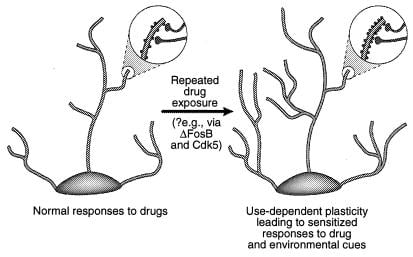
図4
乱用薬物による樹状構造の調節。 側坐核と前頭前野のコカインで観察されたように、乱用薬物への慢性的な曝露後のニューロンの樹状突起の拡大が示されています(41)。 拡大領域は樹状突起棘の増加を示しており、これは活性化された神経終末と関連して発生すると仮定されています。 樹状突起棘密度のこの増加は、ΔFosBとその結果としてのCdk5の誘導を介して媒介される可能性があります(テキストを参照)。 樹枝状構造のそのような変化は、いくつかの学習モデルで観察されたものと同様であり(例えば、長期増強)、乱用薬物または環境手がかりに対する長命の感作反応を媒介する可能性があります。 [参考文献の許可を得て複製。 3(Copyright 2001、Macmillian Magazines Ltd.)]。
他の可能性は、転写因子(例えばΔFosB、CREB)の一過性の誘導である。 染色分体の修飾により、遺伝子発現の恒久的な変化をもたらします。n。 これらおよび他の多くの転写因子は、遺伝子の近傍にあるヒストン(42)のアセチル化または脱アセチル化をそれぞれ促進することによって、標的遺伝子の転写を活性化または抑制すると考えられている。 ヒストンのそのようなアセチル化および脱アセチル化は明らかに非常に迅速に起こり得るが、ΔFosBまたはCREBはヒストンアセチル化を制御する酵素機構においてより長期にわたる適応を生じさせる可能性がある。 ΔFosBまたはCREBはまた、発生中に起こる遺伝子転写の永久的な変化に関与しているクロマチンの他の修飾(例えば、DNAまたはヒストンメチル化)を調節することによって遺伝子発現における長寿命の変化を促進し得る(参考文献XNUMXおよびXNUMXを参照)。 。 これらの可能性は推測的なままであるが、それらは乱用薬物(または他の何らかの摂動)への一時的な適応が本質的に一生の行動上の結果をもたらすメカニズムを提供する可能性がある。
参考文献
- ↵
- ネスラーEJ、
- BTさん、
- ウィドネルKL
(1993)ニューロン11:995 – 1006。
- ↵
- バークJD、
- ハイマンSE
(2000)ニューロン25:515 – 532。
- ↵
- ネスラーEJ
(2001)Nat Rev Neurosci 2:119 – 128。
- ↵
- Carlezon WA Jr、
- Thome J、
- オルソンVG、
- レーンラッドSB、
- ブロドキンES、
- Hiroi N、
- Duman RS、
- RLさん、
- ネスラーEJ
(1998)サイエンス282:2272 – 2275。
- オドノバンKJ、
- Tourtellotte WG、
- ミルブラントJ、
- バラバンJM
(1999)Neurosci 22のトレンド:167〜173。
- ↵
- マックラーSA、
- コルトラL、
- チャXY、
- Koebbe MJ、
- Fournier KM、
- バウワーズMS、
- カリバスPW
(2000)J Neurosci 20:6210 – 6217。
- ↵
- モーガンJI、
- カランT
(1995)Neurosci 18のトレンド:66〜67。
- ↵
- ヤングST、
- Porrino LJ、
- アイダローラMJ
(1991)Proc Natl Acad Sci USA 88:1291 – 1295。
- グレイビールAM、
- モラタラR、
- ロバートソンHA
(1990)Proc Natl Acad Sci USA 87:6912 – 6916。
- 希望B、
- コソフスキーB、
- ハイマンSE、
- ネスラーEJ
(1992)Proc Natl Acad Sci USA 89:5764 – 5768。
- ↵
- ケルズMB、
- ネスラーEJ
(2000)Curr Opin Neurol 13:715 – 720。
- ↵
- Koob GF、
- サンナPP、
- ブルームFE
(1998)ニューロン21:467 – 476。
- ↵
- ワイズRA
(1998)薬物アルコール依存症51:13 – 22。
- ↵
- BTさん、
- Nye HEさん、
- ケルズMB、
- 自己DW、
- Iadarola MJ、
- 中部屋Yさん、
- Duman RS、
- ネスラーEJ
(1994)ニューロン13:1235 – 1244。
- ↵
- Nye H、
- BTさん、
- ケルズM、
- Iadarola Mさん、
- ネスラーEJ
(1995)J Pharmacol Exp Ther 275:1671 – 1680。
- Nye HEさん、
- ネスラーEJ
(1996)Mol Pharmacol 49:636 – 645。
- ↵
- モラタラR、
- エリボルB、
- バジェホM、
- グレイビールAM
(1996)ニューロン17:147 – 156。
- ↵
- Pich EM、
- Pagliusi SR、
- テッサリM、
- タラボットアイエルD、
- Hooft van Huijsduijnen R、
- キアムレラC
(1997)サイエンス275:83 – 86。
- ↵
- 陳JS、
- Nye HEさん、
- ケルズMB、
- Hiroi N、
- 中部屋Yさん、
- BTさん、
- ネスラーEJ
(1995)Mol Pharmacol 48:880 – 889。
- ↵
- Hiroi N、
- ブラウンJ、
- はい、
- Saudou F、
- Vaidya VA、
- Duman RS、
- グリーンバーグME、
- ネスラーEJ
(1998)J Neurosci 18:6952 – 6962。
- ↵
- 陳J、
- ケルズMB、
- BTさん、
- 中部屋Yさん、
- ネスラーEJ
(1997)J Neurosci 17:4933 – 4941。
- ↵
- Hiroi N、
- ブラウンJ、
- ハイレC、
- はい、
- グリーンバーグME、
- ネスラーEJ
(1997)Proc Natl Acad Sci USA 94:10397 – 10402。
- ↵
- Fienberg AA、
- Hiroi N、
- メルメルシュタインP、
- ソングWJ、
- スナイナーGL、
- 西Aさん、
- ケラミーA、
- オキャラハンJP、
- ミラーD、
- コールDG、
- ら
(1998)サイエンス281:838 – 842。
- ↵
- Hiroi N、
- ファインバーグA、
- ハイレC、
- グリーンガードP、
- ネスラーEJ
(1999)Eur J Neurosci 11:1114 – 1118。
- ↵
- グリーンガードP、
- アレンPB、
- ネアンAC
(1999)ニューロン23:435 – 447。
- ↵
- ビブJA、
- スナイナーGL、
- 西Aさん、
- ヤンZ、
- マイヤーL、
- Fienberg AA、
- ツァイLH、
- クォンYT、
- ジローJA、
- Czernik AJ、
- ら
(1999)自然(ロンドン)402:669 – 671。
- ↵
- 陳JS、
- ケルズMB、
- Zeng GQ、
- 堺N、
- ステフェンC、
- Shockett PE、
- Picciotto M、
- Duman RS、
- ネスラーEJ
(1998)Mol Pharmacol 54:495 – 503。
- ↵
- ケルズMB、
- 陳JS、
- カルレゾンワシントン州、
- ウィスラーK、
- ギルデンL、
- ベックマン午前、
- ステフェンC、
- 張YJ、
- マロッティL、
- 自己SW、
- ら
(1999)自然(ロンドン)401:272 – 276。
- ↵
- ドブラザンスキーP、
- 野口Tさん、
- コヴァリーK、
- Rizzo CA、
- ラゾPS、
- ブラボーR
(1991)Mol Cell Biol 11:5470 – 5478。
- 中部屋Yさん、
- ネイサンズD
(1991)セル64:751 – 759。
- ↵
- 円J、
- 知恵RM、
- トラットナー私、
- Verma IM
(1991)Proc Natl Acad Sci USA 88:5077 – 5081。
- ↵
- ホワイトFJ、
- 胡XT、
- 張XF、
- オオカミ私
(1995)J Pharmacol Exp Ther 273:445 – 454。
- ↵
- ハイマンSE
(1996)ニューロン16:901 – 904。
- クリークMJ
(1997)Pharmacol Biochem Behav 57:551 – 569。
- ↵
- シッペンベルグTS、
- レアW
(1997)Pharmacol Biochem Behav 57:449 – 455。
- ↵
- 陳JS、
- 張YJ、
- ケルズMB、
- ステフェンC、
- Ang ES、
- Zeng L、
- ネスラーEJ
(2000)J Neurosci 20:8965 – 8971。
- ↵
- ビブJA、
- 陳JS、
- テイラーJR、
- Svenningsson Pさん、
- 西Aさん、
- スナイナーGL、
- ヤンZ、
- 佐川ZK、
- ネアンAC、
- ネスラーEJ、
- ら
(2001)自然(ロンドン)410:376 – 380。
- ↵
- ラッシャーC、
- ニコールRA、
- マレンカRC、
- ミュラーD
(2000)Nat Neurosci 3:545〜550。
- マリノウR、
- メインネンZF、
- 林Y
(2000)Curr Opin Neurobiol 10:352〜357。
- ↵
- Scannevin RH、
- フガニルRL
(2000)Nat Rev Neurosci 1:133 – 141。
Robinson、TE&Kolb、B。(1999)(1997) ユーロ。 J.Neurosci。11、 1598-1604。
- ↵
- キャリーM、
- スマイルST
真核生物における(2000)転写調節(Cold Spring Harbor Lab。Press、プレインビュー、NY)。
- ↵
- スペンサーバージニア州
- デイビーJR
(1999)Gene 240:1 – 12。
この記事を引用しているHighWire Press主催の記事
- 重要な仲介者としてのΔFosBを有する一般的な神経可塑性メカニズムに及ぼす天然および薬物報酬法 J.Neurosci。 2013 33(8)3434-3442
- 薬物、犯罪、そして快楽同盟のエピジェネティクス 現代刑事司法ジャーナル2012 28(3)314-328
- 抽象
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- 抽象
- フルテキスト(HTML)
- 全文(PDF)
- モルヒネは後根神経節ニューロン由来のF1細胞において細胞外シグナル調節キナーゼ1 / 2を介してE 26様転写因子11 /血清応答因子経路を活性化する J.Pharmacol。 経験値 その 2012 342(1)41-52
- ゲートウェイ薬物の分子機構:コカインによるニコチンプライム遺伝子発現により開始されるエピジェネティック変化 サイトランスルメディア2011 3(107)107ra109
- マウスの中脳ドーパミンニューロンにおけるVGLUTX NUM Xの喪失後のスクロースおよびコカイン自己投与の増強およびキュー誘発薬物探索 J.Neurosci。 2011 31(35)12593-12603
- 慢性間欠性低酸素は中枢自律神経系領域において血圧とFosB /ΔFosBの発現を増加させる 午前 J.Physiol。 よろしく。 積分器 比較 フィジオル。 2011 301(1)R131-R139
- GPR37 / PAEL受容体の欠如は線条体AktおよびERK2リン酸化、ΔFosB発現、ならびにアンフェタミンおよびコカインに対する条件付き場所優先性を損なう FASEB J. 2011 25(6)2071-2081
- 初期アルコール曝露期間と分子耐性の持続性との間の関係は著しく非線形である J.Neurosci。 2011 31(7)2436-2446
- in vivo生物発光イメージングは腎血管性高血圧症のマウスの室傍核におけるレドックス制御活性化蛋白質‐1活性化を明らかにする 高血圧症2011 57(2)289-297
- ΔFosBの線条体過剰発現は慢性レボドパ誘発不随意運動を再現する J.Neurosci。 2010 30(21)7335-7343
- 主要精神病性障害における環境影響のエピジェネティックな媒介 統合失調症雄牛2009 35(6)1045-1056
- 生体脳におけるアンフェタミンへの慢性曝露の特異的検出のためのDNAベースのMRIプローブ J.Neurosci。 2009 29(34)10663-10670
- コカイン離脱ラットにおける樹状突起棘可塑性の変化 J.Neurosci。 2009 29(9)2876-2884
- ショウジョウバエの過剰発現スクリーンはAP-3依存性発生可塑性の調節因子としてのGSK-1β/ shaggyの神経細胞的役割を同定する 遺伝学2008 180(4)2057-2071
- 転写MRI:生きている脳の新しい見方 神経科学者2008 14(5)503-520
- 眼窩前頭皮質におけるΔFosB誘導はコカイン誘導認知機能障害に対する寛容を仲介する J.Neurosci。 2007 27(39)10497-10507
- グリア細胞株由来神経栄養因子変異マウスにおけるメタンフェタミン探索行動の回復に対する持続性の脆弱性 FASEB J. 2007 21(9)1994-2004
- 側坐核のΔFosBは食品強化機器の挙動と動機を調節する J.Neurosci。 2006 26(36)9196-9204
- リン酸化によるΔFosB安定性の調節。 J.Neurosci。 2006 26(19)5131-5142
- ドーパミンD1受容体含有細胞における変異NMDA受容体の発現はコカイン感作を予防しコカイン嗜好性を低下させる J.Neurosci。 2005 25(28)6651-6657
- D1ドーパミン受容体は間欠的モルヒネ投与後のラット線条体におけるΔFosB誘導を調節する J.Pharmacol。 経験値 その 2005 314(1)148-154
- 高い自発的なホイールランニング活動のために選択されたマウスの神経生物学 積分器 比較 Biol。 2005 45(3)438-455
- ラット視索上核および終板領域におけるc-FosおよびFosB染色に対する水分欠乏および水分補給の影響 午前 J.Physiol。 よろしく。 積分器 比較 フィジオル。 2005 288(1)R311-R321
- 骨芽細胞における機械的ストレスによるFosB /ΔFosB遺伝子の転写誘導 Jバイオケム2004 279(48)49795-49803
- 慢性ストレス後の報酬関連脳構造におけるΔFosBの誘導 J.Neurosci。 2004 24(47)10594-10602
- Sim1遺伝子量はマウスの食物脂肪増加に対する恒常性摂食反応を調節する 午前 J.Physiol。 エンドクリノール。 メタブ 2004 287(1)E105 - E113
- 静水圧に応答したヒト視神経乳頭星状細胞における遺伝子発現のDNAマイクロアレイ解析 フィジオル。 ゲノミクス2004 17(2)157-169
- スーパーオキシドは心筋梗塞誘発性心不全の中枢神経系活性化および交感神経興奮に関与する サークル 結果 2004 94(3)402-409
- 反復ドーパミン作動性刺激への神経適応におけるアデノシンA2A受容体:パーキンソン病におけるジスキネジアの治療への影響 神経学2003 61(90116)S74-81
- カエル、Rana esculenta、精巣におけるFos関連蛋白質の細胞質対核局在:性腺刺激ホルモン放出ホルモンアゴニストのin vivoおよびin vitro直接作用 Biol。 再商品化します。 2003 68(3)954-960
- 思春期前後のマウスはコカインとアンフェタミンに反応して増強されたDelta FosBアップレギュレーションを示す J.Neurosci。 2002 22(21)9155-9159
- Delta FosBがホイールの回転を制御します J.Neurosci。 2002 22(18)8133-8138
- 側坐核の殻におけるCREB活性は感情的刺激に対する行動反応のゲーティングを制御する 手順 Natl。 アカド。 サイ。 アメリカ2002 99(17)11435-11440
- 心理ゲノム学:依存症を理解するための機会 J.Neurosci。 2001 21(21)8324-8327
