Främre. Psykiatri, 25 Februari 2016 | http://dx.doi.org/10.3389/fpsyt.2016.00024
Jarid Goodman och Mark G. Packard*
- Institutionen för psykologi, Texas A&M Institute for Neuroscience, Texas A&M University, College Station, TX, USA
Uppfattningen att anatomiskt distinkta minnessystem differentiellt bidrar till utvecklingen av drogberoende och återfall har fått omfattande stöd. Den nuvarande korta översynen granskar den här hypotesen eftersom den ursprungligen föreslogs för 20 år sedan (1) och belyser flera senaste utvecklingen. Omfattande forskning som använder olika djurinlärningsparadigmer indikerar att dissocierbara neurala system förmedlar olika typer av lärande och minne. Varje minnessystem bidrar potentiellt med unika komponenter till det lärda beteendet som stöder narkotikamissbruk och återfall. Speciellt kan övergången från användning av fritidsdrog till tvångsmissbruk misslyckas återspegla en neuroanatomisk övergång från kognitiv kontroll av beteende medierat av hippocampus / dorsomedial striatum mot vanligt kontroll av beteende medierat av det dorsolaterala striatum (DLS). Dessutom kan stress / ångest utgöra en kofaktor som underlättar DLS-beroende minne, och detta kan tjäna som en neurobeteende mekanism som ligger till grund för den ökade läkemedelsanvändningen och återfallet hos människor efter stressiga livshändelser. Bevis som stöder flera systemvyer av narkotikamissbruk kommer främst från studier av inlärning och minne som har använt som förstärkare beroendeframkallande ämnen som ofta beaktas inom ramen för narkotikamissbruk, inklusive kokain, alkohol och amfetaminer. Dessutom tyder nyligen på att minnessystemets strategi också kan vara till hjälp för att förstå aktuella källor till beroende som speglar nya hälsoproblem, inklusive användning av marijuana, fettsnål diet och videospel.
Beskrivning
Undersökare tittar ofta på mekanismer för inlärning och beteende för att förklara hur mänsklig psykopatologi förvärvas och uttrycks. Ett exempel på en sådan applikation tillhandahölls av Norman M. White som använde grunden för klassisk inlärningsteori och experimentella bevis som stödjer förekomsten av flera minnessystem i hjärnan för att tillhandahålla en ny, inflytelserik strategi för drogberoende (1). Specifikt indikerade White att droger kan spela rollen som ”förstärkare” som, precis som mat eller vatten i en lärande uppgift, stärker föreningarna bland narkotikarelaterade stimuli, sammanhang och beteende för att främja läkemedelsbruk och, med tiden, missbruk. White införlivade också den framväxande hypotesen att det finns olika typer av minne som förmedlas av dissocierbara neurala system. Enligt denna nya uppfattning kan läkemedel direkt modulera flera neurala system, och dessa neurala system går in på kodande distinkta komponenter i det läkemedelsrelaterade minnet som, när de uttrycks, främjar ytterligare läkemedelsintag.
Året 2016 markerar 20-årsjubileet för de flera minnessystemens uppfattning om narkotikamissbruk som beskrivits av White. Den nuvarande översynen granskar denna inflytelserika hypotes, samtidigt som den belyser en del viktiga utvecklingar på senare tid som inte bara har underbyggt den ursprungliga hypotesen utan också har gett ytterligare insikter i hur flera minnessystem potentiellt stöder drogberoende.
Det flera minnessystemet View of Addiction
Konvergerande bevis från studier som använde människor och lägre djur indikerar att däggdjursminnet medieras av relativt oberoende nervsystem [för recensioner, se Ref. (2-4)]. De tidiga experimenten som dissocierade flera minnessystem genomfördes främst i den radiella labyrinten och indikerade unika mnemoniska funktioner för hippocampus, dorsal striatum och amygdala (5, 6). Hippocampus förmedlar en kognitiv / rumslig form av minne, medan ryggstratum medierar stimulus – respons (S – R) -vaneminne. Amygdala förmedlar Pavloviska och stimulus-affekt-associerande relationer (6, 7), samtidigt som man underkastar sig den modulerande rollen som känslomässig upphetsning på andra typer av minne (8-12).
Inom ramen för flera systemvyer av minne, vit (1) föreslog att hippocampus, dorsal striatum och amygdala kodar unika komponenter i läkemedelsrelaterade minnen (se figur 1). Hippocampus kodar uttrycklig kunskap om förhållandet mellan ledtrådar och händelser (dvs. stimulus – stimulusassociationer) i läkemedelssammansättningen. Det är viktigt att hippocampus inte kodar för beteendespons, utan snarare den information som förvärvas av hippocampus kan användas för att generera lämpliga beteendespons för att få läkemedelsförstärkning. Å andra sidan kodar ryggstratumat för samband mellan läkemedelsrelaterade stimuli och beteendespons. Detta kan göra det möjligt för presentationen av en läkemedelsrelaterad ledning att aktivera ett automatiskt beteendespons som resulterar i läkemedelsupptagning (t.ex. körning eller instrumental spakpress). Amygdala kodar Pavlovian-associerande relationer, vilket gör att neutrala ledtrådar i läkemedelssammanhanget kan associeras med läkemedelsbelöningen. Djur reagerar senare på dessa konditionerade signaler på liknande sätt som de ursprungligen reagerade på läkemedlet. Specifikt aktiverar de konditionerade signalerna konditionerade känslomässiga svar, inklusive interna affektiva tillstånd och konditionerad inställning till (eller i vissa fall undvikande från) den konditionerade signalen. En annan kritisk komponent i Whites hypotes är att läkemedel kan modulera minnesfunktionen i vart och ett av dessa hjärnregioner. Således kan läkemedel potentiellt förbättra sin egen självadministrering genom att öka konsolideringen av de läkemedelsrelaterade minnen som kodas av hippocampus, amygdala och ryggstriatum (se figur 1).
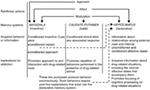
Bild 1. White's (1) flera minnessystemvy av narkotikamissbruk. Liksom naturliga förstärkare har beroendeframkallande läkemedel flera "förstärkande åtgärder", inklusive förmågan att åberopa positiva / negativa effekter, tillvägagångssätt och modulering av minnessystem. Amygdala, caudate – putamen (dvs. dorsal striatum) och hippocampus förmedlar dissocierbara minnessystem, och varje minnessystem kodar antagligen unika komponenter i läkemedelsrelaterade minnen. Med tanke på deras minnesmodulerande egenskaper kan beroendeframkallande läkemedel potentiellt förbättra sin egenadministrering genom att förbättra funktionen hos dessa system. (Omtryckt från White med tillstånd från John Wiley & Sons.)
I överensstämmelse med de flera minnessystemets syn på narkotikamissbruk tyder omfattande bevis på kritiska roller för hippocampus, dorsal striatum och amygdala när det gäller narkotikamissbruk och återfall för en mängd missbrukade ämnen [för granskning, se Ref. (13)]. Dorsal hippocampus verkar ha en roll i den kontekstuella kontrollen av läkemedelssökande efter kokain (14-16). Sidoregionen i dorsal striatum (DLS) förmedlar S-R-vanliga spakpressning för kokain och alkohol (17, 18), och den basolaterala amygdala (BLA) förmedlar konditionerat läkemedel som söker kokain, alkohol och heroin (19-22). Även i överensstämmelse med Whites hypotes, kan missbrukssubstanser modulera de mnemoniska funktionerna hos hippocampus, ryggstriatum och amygdala (23-31).
Nyligen genomförda studier har bidragit med nya ändringar i det flera minnessystemets strategi för narkotikamissbruk. Viktiga funktioner i denna samtida uppfattning inkluderar (1) en neuroanatomisk förskjutning över tid till DLS-beroende vaneminne, (2) konkurrenskraftiga interaktioner mellan minnessystem, (3) rollen som stress och ångest för att förbättra vanligt läkemedelssökande, och (4) tillämpningen av denna hypotese på nya framväxande källor till beroende.
Den neuroanatomiska förskjutningen från kognition till vana
I experimentella inlärningssituationer utnyttjar ämnen vanligtvis målmedvetet beteende när de initialt löser en uppgift. Men efter omfattande träning blir beteende autonomt och kan utföras med liten uppmärksamhet, avsikt eller kognitiv ansträngning, vilket utgör en ”vana” [för granskning, se Ref. (32)]. I tidiga demonstrationer av denna övergång från kognitiv kontroll av beteende till vana, tränades gnagare med matbelöning i en dubbellösning plus-labyrintuppgift (33-35). I denna uppgift släpptes råttor från samma utgångsläge (t.ex. sydarmen) och var tvungna att göra en konsekvent kroppsvängning vid labyrintkorsningen för att få matbelöning alltid belägen i samma målarm (t.ex. alltid vänster vänd dig för att hitta mat i västra armen). Råttor skulle kunna lösa denna uppgift genom att antingen lära sig ett konsekvent svar på kroppen-vändningen eller genom att göra något svar som krävs för att gå till samma rumsliga plats. För att bestämma vilken strategi som råttorna använde, implementerade utredare ett sondtest där djur släpptes från motsatt startarm (t.ex. norrarmen). Om djur gjorde motsatt kroppsvridning för att gå till den ursprungliga målplatsen, identifierades de som platselever. Om djur gjorde samma kroppsvängning som under träning (dvs att gå till armen mittemot den ursprungliga målplatsen) identifierades djur som svarstudenter. Bevis tyder på att efter en del träning visar de flesta djur platsinlärning, medan djur efter en omfattande träning övergår till vanligt svarinlärning (34-36). Intressant nog kan denna övergång från platsinlärning till responsinlärning återspegla en neuroanatomisk förändring. Den initiala användningen av platsinlärning i denna uppgift medieras av hippocampus och dorsomedial striatum [DMS (36, 37)], medan användningen av responsinlärning efter utökad utbildning medieras av DLS (36).
Förutom tidiga demonstrationer med plus-labyrint (34, 35) visades senare beteendeförskjutningen till vanligt minne med användning av operatörspaktryckningsparadigmer (38-42). I dessa instrumentella inlärningsuppgifter hävdar djur från början målmedvetet för att uppnå resultatet och kommer att upphöra med att trycka på när matutfallet har devalverats. Efter omfattande träningsdjur kommer emellertid växling till vanligt att reagera och fortsätter att trycka på spaken även efter att matutfallet har devalverats (40). Som ursprungligen visades i plus-labyrinten (36), kan övergången från kognition till vana i instrumentella inlärningsuppgifter också tillskrivas en neuroanatomisk förändring. Den initiala kognitiva kontrollen av beteende i dessa instrumentella inlärningsuppgifter medieras av hippocampus och DMS (43, 44), medan senare vanligt svar medieras av DLS (18, 45, 46).
Många utredare har föreslagit att den neuroanatomiska övergången till vanligt minne visat i labyrint och instrumentella inlärningsuppgifter också kan ligga till grund för övergången från narkotikamissbruk till tvångsmissbruk (13, 47-50). I överensstämmelse med denna hypotese har utredare visat för olika misshandlade ämnen att DMS förmedlar målriktad reaktion för läkemedelsförstärkning och DLS förmedlar vanligt svar på läkemedelsförstärkning (18, 31, 51-53).
Med tanke på den stora missbrukspotentialen för vissa droger har utredare föreslagit att beroendeframkallande läkemedel kan förbättra DLS-beroende vanliga minnesfunktioner och därmed påskynda övergången från kognitiv till vanligt kontroll av beteende. I överensstämmelse med den här hypotesen underlättar upprepad exponering för amfetamin eller kokain övergången från målinriktad till vanligt att svara på matförstärkning i instrumental spakpressningsuppgifter (31, 54-59). Dessutom har spakpressning för beroendeframkallande ämnen (t.ex. alkohol eller kokain) jämfört med livsmedelsbelöning förknippats med större vanliga svar mot målriktade svar (24, 60, 61). Hos människor visar alkoholberoende individer större vanliga svar i en instrumentell inlärningsuppgift, relativt till icke-beroende kontrollindivider (62). Denna förbättring av DLS-beroende vaneminne med beroendeframkallande läkemedel har också observerats i lärningsuppgifter för gnagare labyrint. Exponering av kokain, amfetamin och alkohol har associerats med förbättrad inlärning i DLS-beroende labyrintuppgifter eller större användning av DLS-beroende svarstrategier i versioner med dubbla lösningar av labyrinten (25, 63, 64). Hos människor har användningen av missbrukade ämnen, inklusive alkohol och tobak, korrelerats till den större användningen av ryggstratumberoende navigationsstrategier i en virtuell labyrint (65). Således kan vissa missbruk av droger förbättra DLS-beroende vaneminne, och detta ökade engagemang i DLS-minnessystemet kan påskynda övergången från rekreationsdroganvändning till vanligt drogmissbruk. Denna föreslagna mekanism är förenlig med White's (1) ursprungliga påståenden om att missbruk av droger ibland kan underlätta sin egen självadministrering genom att förbättra minnessystemens funktion.
Konkurrens mellan minnessystem
Även om det är möjligt att beroendeframkallande läkemedel förstärker vanligt minne direkt genom att förbättra funktionen hos DLS [t.ex. Ref. (29)], en annan möjlighet är att missbruk av droger förstärker vanligt minne indirekt via modulering av andra minnessystem. Denna alternativa mekanism åberopar hypotesen att i vissa inlärningssituationer konkurrerar minnessystem om kontroll av inlärning och att genom att försämra funktionen hos ett minnessystem kan funktionen hos ett annat intakt system förbättras (11, 66). Speciellt kan hippocampus och DLS ibland tävla om kontroll av inlärning, varvid lesion av hippocampus förbättrar DLS-beroende minnesfunktion (5, 6, 67, 68). Konkurrenskraftiga interaktioner kan också demonstreras i uppgifter med dubbla lösningar, när försämring av ett minnessystem resulterar i användningen av en strategi förmedlad av ett annat intakt system. Till exempel visar djur som får DMS-lesioner DLS-beroende vanligt svarande för matbelöning i instrumentella inlärningsuppgifter (44).
Med tanke på konkurrenskraftiga interaktioner som ibland uppstår mellan minnessystem, är en möjlighet att vissa missbruksläkemedel kan förstärka DLS-beroende vaneminne indirekt genom att försämra kognitiva minnesmekanismer medierade av DMS och hippocampus. Som tidigare nämnts, är alkohol förknippad med större användning av DLS-beroende vaneminne i labyrint och operatörspaktryckningsparadigmer (24, 61, 62, 64, 65). Bevis tyder också på att alkohol försämrar lärande i hippocampusberoende rumsliga minnesuppgifter [(64, 69-72); för granskning, se Ref. (73)], såväl som i DMS-beroende inlärningsuppgifter för reversering (74-77). I överensstämmelse med en konkurrenskraftig interaktion mellan minnessystem har det antagits att alkohol kan underlätta DLS-beroende vaneminne indirekt via försämrade kognitiva minnesmekanismer (78).
Det bör noteras att bortsett från alkohol har många droger associerats med kognitiva minnesunderskott. Exponering för morfin, heroin, metamfetamin, MDMA (ecstasy) eller kronisk kokain producerar på liknande sätt hippokampusberoende rumsliga minnesfunktioner i olika uppgifter (79-89). Det är frestande att spekulera i att, såsom föreslogs för alkohol, kan kognitiva minnesnedsättningar som produceras av beroendeframkallande medel indirekt förstärka DLS-beroende vaneminne, och att detta kan vara en mekanism som gör det möjligt för självadministrering av drog att bli vanligt hos mänskliga narkotikamissbrukare. Å andra sidan är det också möjligt att rumsliga inlärningsunderskott producerade av beroendeframkallande läkemedel kan inträffa indirekt genom förbättring av DLS-beroende minnesprocesser. I överensstämmelse med denna hypotese, stimulerar CREB-aktivitet i DLS hippocampusberoende rumsligt minne (90), medan hämning av CREB-aktivitet i DLS vänder de nedsatta rymdminnen som produceras av morfin (91).
Roll av stress och ångest
En ytterligare övervägande beträffande det multipla minnessystemet när det gäller narkotikamissbruk är stressens roll. Konvergerande bevis tyder på att robust känslomässig upphetsning underlättar DLS-beroende vaneminne hos gnagare och människor [för recensioner, se Ref. (9-12)]. Administration av ångestdödande läkemedel förbättrar DLS-beroende responsinlärning i vattnet plus labyrint (92-97). Denna förbättring av DLS-beroende vaneminne observeras också efter exponering för okonditionerade beteendestressorer [t.ex. kronisk återhållsamhet, svanschock, rovdjurlukt, etc. (98-101)] och exponering för räddkonditionerade stimuli [ton som tidigare parats med chock (102, 103)]. Även om de ursprungligen visades i gnagare (92), har denna förbättring av vanminnet inducerat av robust känslomässig upphetsning också visats i stor utsträckning hos människor (99, 104-110).
Mekanismerna som tillåter stress / ångest för att underlätta vanminnet är i stort sett okända bevis tyder dock på en kritisk modulerande roll hos BLA (93-95, 100). I överensstämmelse med en konkurrenskraftig interaktion mellan minnessystem tyder vissa bevis också på att stress / ångest kan förstärka DLS-beroende vaneminne indirekt genom att försämra hippocampal funktion (94, 95).
Förbättring av vanliga minne efter stress eller ångest kan vara relevant för att förstå några framstående faktorer som leder till drogmissbruk. Stressande livshändelser eller kroniska långvariga perioder av stress / ångest är nämligen förknippade med ökad sårbarhet för drogberoende och återfall hos människor (111-117), och liknande observationer har gjorts i djurmodeller för läkemedels självadministrering [för granskning, se Ref. (118)]. Utredare har föreslagit att det överensstämmer med påverkan av känslomässig upphetsning på flera minnessystem (10), akut eller kronisk stress kan öka läkemedelsberoende och återfall hos människor genom att engagera DLS-beroende vanliga minnesprocesser (9, 49, 119). I överensstämmelse med detta förslag är stress hos kokainberoende individer förknippat med minskad blod-syre-nivåberoende (BOLD) aktivitet i hippocampus och ökad aktivitet i ryggstratum, och dessa BOLD-aktivitetsförändringar är förknippade med stress-inducerade kokaintrang (120).
Emerging Sources of Addiction
Bortsett från missbruksläkemedel har hypotesen om flera minnessystem nyligen också använts för att förstå andra framväxande källor till missbruk. Till exempel har ökningen av fetma under de senaste decennierna lett till en jämförbar uppgång i experimentellt intresse, med många utredare som drar paralleller mellan narkotikamissbruk och överätande [för granskning, se Ref. (121-123)]. Några nyligen visade bevis har visat att liksom narkotikamissbruk kan matberoende delvis tillskrivas ökat engagemang i DLS-beroende vaneminne. Hos råttor underlättar binge-liknande matkonsumtion övergången från kognitiv till vanligt kontroll av beteende (124, 125). Dessutom är vanligt beteende hos djupgående djur förknippat med ökad DLS-aktivitet och kan förhindras genom att blockera AMPA eller dopamin D1-receptorer i DLS (125). Dietinducerad fetma har också nyligen varit associerad med användningen av vaneminne i en Y-labyrintuppgift (126).
En annan framväxande beteendestörning som är parallell med vissa funktioner i narkotikamissbruk är patologiskt videospel eller videospelberoende [för granskning, se Ref. (127)]. Liksom narkotikamissbruk har långvarig överdrivet videospel spelats ihop med reducerad dopamin D2-receptorbindning i ryggstratum (128). Videogamespelning är också korrelerad till ökad aktivering av ryggstriatumet (129, 130), och större ryggala dödliga volymer förutsäger högre nivåer av videospelförmåga (131). Människor som regelbundet spelar actionvideospel är mer benägna att använda dorsalt striatumberoende vanminne i en virtuell labyrint (132), och förhandsutbildning av videospel som leder till vanligt svar över målinriktat svar i en tvåstegs beslutsfattande uppgift (133). Såsom föreslagits för missbruk av droger kan spela videospel förbättra videospelberoende genom att engagera det DLS-beroende vanliga minnessystemet.
Slutligen kan flera system för flera minnessystem också vara användbara för att förstå marihuana-beroende. Även om marijuana kan ha lägre missbrukspotential än andra olagliga ämnen som klassiskt betraktas inom ramen för forskning om drogberoende (t.ex. kokain, morfin, heroin etc.), kan tung användning av cannabis ändå främja drogberoende och abstinenssymtom som observerats med andra droger av missbruk (134-137). Det har nyligen föreslagits att marijuana-beroende delvis kan tillskrivas ökat engagemang av DLS-beroende vaneminne (138). Medan akut exponering för cannabinoid försämrar DLS-beroende minnesfunktion (139, 140), upprepad cannabinoid exponering leder till större DLS-beroende vanliga svar i en instrumentell inlärningsuppgift (141). Dessutom visar tunga cannabisanvändare en större aktivering av ryggstratum, relativt till icke-användare, när de utför en marijuana-version av den implicita associeringsuppgiften (142), och deltagare med en historia av cannabisanvändning är mer benägna att använda dorsalt striatumberoende vanminne i den virtuella labyrinten (65).
Med tanke på den framgångsrika tillämpningen av minnessystemets tillvägagångssätt på nya källor till beroende, är det rimligt att anta att flera minnessystem också kan vara inblandade i andra beteendemässiga patologier som är förknippade med beroende, såsom tvångshopping, internetberoende och sexberoende. Huruvida minnessystemmetoden kan vara användbar för att förstå patologiskt spel har också fått viss uppmärksamhet (143, 144).
Slutsats
Tjugo år med experimentella bevis har till stor del bekräftat vita (1) flera minnessystem när det gäller narkotikamissbruk. Bevis tyder på att hippocampus förmedlar kontextuell kontroll av läkemedels självadministrering, DLS förmedlar S-R vanligt svarar för förstärkning av läkemedel, och amygdala förmedlar villkorad läkemedelssökning. Dessutom har efterföljande forskning lett till ytterligare insikter om synen på flera minnessystem om narkotikamissbruk inklusive övergången till vanliga minne, konkurrens mellan minnessystem och rollen som stress och ångest.
Framtida forskning bör försöka integrera minnessystemets strategi med andra teorier om beroende, såsom motståndares motiverande processer (145). Det skulle också vara användbart att införliva i minnessystemen visa ytterligare funktioner i beroende, såsom drogberoende, tolerans och tillbakadragande. Även om den aktuella översynen huvudsakligen fokuserade på hjärnregionerna som ursprungligen övervägs av White (dvs. hippocampus, ryggstriatum och amygdala), bör det noteras att ytterligare hjärnregioner relaterade till inlärning och minne också har kritiskt varit inblandade i drogberoende och återfall , inklusive den mediala prefrontala cortex och nucleus accumbens [för granskning, se Ref. (13)]. Slutligen, även om det ligger utanför ramen för den aktuella granskningen, bör det erkännas att omfattande bevis tyder på att cellulära och molekylära förändringar i det dopaminergiska systemet i mellanhjärnan också bidrar till missbruk (146).
Även om vanliga minnen kan vara särskilt svåra att kontrollera, tyder vissa bevis på att DLS-beroende minne, när det förvärvats, under vissa omständigheter kan undertryckas (147) eller till och med omvänd (148, 149). Således är det möjligt att de farmakologiska manipulationerna och beteendeförfarandena som leder till vändning eller undertryckande av vanligt minne i djurmodeller för inlärning potentiellt kan anpassas för att behandla drogberoende och återfall hos människor.
Författarbidrag
JG och MP bidrog båda med idéer och skrivande av den nuvarande mini-recensionen.
Intresseanmälan
Författarna förklarar att forskningen genomfördes i avsaknad av kommersiella eller finansiella relationer som kan tolkas som en potentiell intressekonflikt.
Referensprojekt
1. Vitt NM. Beroendeframkallande läkemedel som förstärkare: flera delvisa åtgärder på minnessystem. Addiction (1996) 91(7):921–50. doi: 10.1111/j.1360-0443.1996.tb03586.x
2. Vitt NM, McDonald RJ. Flera parallella minnesystem i råttans hjärna. Neurobiol Lär Mem (2002) 77(2):125–84. doi:10.1006/nlme.2001.4008
3. Squire LR. Hjärnans minnessystem: en kort historia och aktuellt perspektiv. Neurobiol Lär Mem (2004) 82(3):171–7. doi:10.1016/j.nlm.2004.06.005
4. White NM, Packard MG, McDonald RJ. Dissociation av minnessystem: berättelsen utvecklas. Behav Neurosci (2013) 127(6):813–34. doi:10.1037/a0034859
5. Packard MG, Hirsh R, White NM. Differentialeffekter av fornix och caudatkärnläsningar på två radiella labyrintuppgifter: bevis för flera minnessystem. J Neurosci (1989) 9(5): 1465-72.
6. McDonald RJ, White NM. En tredubbla dissociation av minnessystem: hippocampus, amygdala och ryggstratum. Behav Neurosci (1993) 107(1):3–22. doi:10.1037/0735-7044.107.1.3
7. Maren S. Neurobiology of Pavlovian fear conditioning. Annu Rev Neurosci (2001) 24(1):897–931. doi:10.1146/annurev.neuro.24.1.897
8. McGaugh JL. Amygdala modulerar konsolideringen av minnen från känslomässigt väckande upplevelser. Annu Rev Neurosci (2004) 27: 1-28. doi: 10.1146 / annurev.neuro.27.070203.144157
9. Packard MG. Ångest, kognition och vana: ett perspektiv med flera minnessystem. Brain Res (2009) 1293: 121-8. doi: 10.1016 / j.brainres.2009.03.029
10. Packard MG, Goodman J. Känslomässig upphetsning och flera minnessystem i däggdjurshjärnan. Front Behav Neurosci (2012) 6: 14. doi: 10.3389 / fnbeh.2012.00014
11. Packard MG, Goodman J. Faktorer som påverkar den relativa användningen av flera minnessystem. hippocampus (2013) 23(11):1044–52. doi:10.1002/hipo.22178
12. Schwabe L. Stress och engagemang av flera minnessystem: integration av djur- och mänskliga studier. hippocampus (2013) 23(11):1035–43. doi:10.1002/hipo.22175
13. Everitt BJ, Robbins TW. Neurala system för förstärkning för narkotikamissbruk: från handlingar till vanor till tvång. Nat Neurosci (2005) 8(11):1481–9. doi:10.1038/nn1579
14. Fuchs RA, Evans KA, Ledford CC, Parker MP, Case JM, Mehta RH, et al. Rollen för den dorsomediala prefrontala cortex, basolaterala amygdala och dorsal hippocampus vid kontextuell återinförande av kokain som söker hos råttor. Neuropsychopharmacology (2005) 30(2):296–309. doi:10.1038/sj.npp.1300579
15. Fuchs RA, Eaddy JL, Su ZI, Bell GH. Interaktioner mellan basolateral amygdala och dorsal hippocampus och dorsomedial prefrontal cortex reglerar läkemedelskontextinducerad återinförande av kokain-sökande hos råttor. Eur J Neurosci (2007) 26(2):487–98. doi:10.1111/j.1460-9568.2007.05674.x
16. Kramar CP, Barbano MF, Medina JH. Dopamin D1 / D5-receptorer i dorsal hippocampus krävs för anskaffning och uttryck av ett enda försökt kokainassocierat minne. Neurobiol Lär Mem (2014) 116: 172-80. doi: 10.1016 / j.nlm.2014.10.004
17. Zapata A, Minney VL, Shippenberg TS. Skift från målriktad till vanligt kokain som söker efter långvarig erfarenhet av råttor. J Neurosci (2010) 30(46):15457–63. doi:10.1523/JNEUROSCI.4072-10.2010
18. Corbit LH, Nie H, Janak PH. Vanlig alkoholsökande: tidskurs och bidraget från subregioner i ryggstratum. Biolpsykiatri (2012) 72(5):389–95. doi:10.1016/j.biopsych.2012.02.024
19. Whitelaw RB, Markou A, Robbins TW, Everitt BJ. Excitotoxiska lesioner av den basolaterala amygdala försämrar förvärvet av kokain-sökande beteende enligt ett andra ordningens förstärkningsschema. Psychopharmacology (1996) 127(1–2):213–24. doi:10.1007/BF02805996
20. Alderson HL, Robbins TW, Everitt BJ. Effekterna av excitotoxiska lesioner av den basolaterala amygdalaen på förvärv av heroinsökande beteende hos råttor. Psychopharmacology (2000) 153(1):111–9. doi:10.1007/s002130000527
21. Gabriele A, se RE. Vändbar inaktivering av den basolaterala amygdala, men inte den dorsolaterala caudat-putamen, dämpar konsolideringen av associerande lärande i kokain-cue i en återinföringsmodell för drogsökande. Eur J Neurosci (2010) 32(6):1024–9. doi:10.1111/j.1460-9568.2010.07394.x
22. Sciascia JM, Reese RM, Janak PH, Chaudhri N. Alkoholsökande utlöst av diskreta pavloviska ledtrådar förstärks av alkoholförhållanden och förmedlas av glutamatsignaler i basolaterala amygdala. Neuropsychopharmacology (2015) 40: 2801-12. doi: 10.1038 / npp.2015.130
23. Packard MG, Teather LA. Amygdala-modulering av flera minnessystem: hippocampus och caudate-putamen. Neurobiol Lär Mem (1998) 69(2):163–203. doi:10.1006/nlme.1997.3815
24. Dickinson A, Wood N, Smith JW. Alkoholsökning av råttor: handling eller vana? QJ Exp Psychol B (2002) 55(4):331–48. doi:10.1080/0272499024400016
25. Udo T, Ugalde F, DiPietro N, Eichenbaum HB, Kantak KM. Effekter av ihållande självadministrering av kokain på amygdala-beroende och rygg av ryggstrålning. Psychopharmacology (2004) 174(2):237–45. doi:10.1007/s00213-003-1734-1
26. Wood SC, Fay J, Sage JR, Anagnostaras SG. Kokain och pavlovsk rädsla: kondensanalys. Behav Brain Res (2007) 176(2):244–50. doi:10.1016/j.bbr.2006.10.008
27. Wood SC, Anagnostaras SG. Memory och psychostimulants: modulering av Pavlovian rädsla konditionering av amfetamin i C57BL / 6 möss. Psychopharmacology (2009) 202(1–3):197–206. doi:10.1007/s00213-008-1185-9
28. Iñiguez SD, Charntikov S, Baella SA, Herbert MS, Bolaños-Guzmán CA, Crawford CA. Exponering av kokain efter träning underlättar konsolidering av rumsligt minne i C57BL / 6-möss. hippocampus (2012) 22(4):802–13. doi:10.1002/hipo.20941
29. DePoy L, Daut R, Brigman JL, MacPherson K, Crowley N, Gunduz-Cinar O, et al. Kronisk alkohol producerar neuroadaptationer till främsta dorsal striatal lärande. Proc Natl Acad Sci USA (2013) 110(36):14783–8. doi:10.1073/pnas.1308198110
30. Leri F, Nahas E, Henderson K, Limebeer CL, Parker LA, White NM. Effekter av heroin och d-amfetamin efter utbildningen på konsolidering av lärande om win-stay och rädsla. J Psychopharmacol (2013) 27(3):292–301. doi:10.1177/0269881112472566
31. Schmitzer-Torbert N, Apostolidis S, Amoa R, O'Rear C, Kaster M, Stowers J, et al. Efter-träning kokainadministration underlättar vanliga inlärning och kräver infralimbic cortex och dorsolateral striatum. Neurobiol Lär Mem (2015) 118: 105-12. doi: 10.1016 / j.nlm.2014.11.007
32. Knowlton BJ. Basal ganglia: vanorbildning. I: Jaeger D, Jung R, redaktörer. Encyclopedia of Computational Neuroscience. New York: Springer (2014). s. 1-17.
33. Tolman EC, Ritchie BF, Kalish D. Studier i rumsligt lärande. IV. Överföring av platsinlärning till andra startvägar. J Exp Psychol (1947) 37(1):39–47. doi:10.1037/h0062061
34. Ritchie BF, Aeschliman B, Pierce P. Studier i rumsligt lärande. VIII. Platsprestanda och förvärv av platsdispositioner. J Comp Physiol Psychol (1950) 43(2):73–85. doi:10.1037/h0055224
35. Hicks LH. Effekter av överträning på förvärv och reversering av plats- och responsinlärning. Psychol Rep (1964) 15(2):459–62. doi:10.2466/pr0.1964.15.2.459
36. Packard MG, McGaugh JL. Inaktivering av hippocampus eller caudatkärna med lidokain påverkar på olika sätt uttrycket för plats- och responsinlärning. Neurobiol Lär Mem (1996) 65(1):65–72. doi:10.1006/nlme.1996.0007
37. Yin HH, Knowlton BJ. Bidrag från streatal subregioner till plats- och responsinlärning. Lär Mem (2004) 11(4):459–63. doi:10.1101/lm.81004
38. Adams CD, Dickinson A. Instrumental svarande efter förstärkningsdevaluering. QJ Exp Psychol (1981) 33B: 109-12. doi: 10.1080 / 14640748108400816
39. Adams CD, Dickinson A. Åtgärder och vanor: variationer i associerande representationer under instrumentellt lärande. I: Spear NE, Miller RR, redaktörer. Informationsbehandling hos djur: minnesmekanismer. Hillsdale, NJ: Erlbaum (1981). s. 143-65.
40. Adams CD. Variationer i känsligheten för instrumentell reaktion på förstärkningsdevaluering. QJ Exp Psychol (1982) 34B: 77-98. doi: 10.1080 / 14640748208400878
41. Dickinson A, Nicholas DJ. Irrelevant incitamentsinlärning under instrumentell konditionering: rollen som drivförstärkare och responsförstärkande relationer. QJ Exp Psychol (1983) 35B: 249-63. doi: 10.1080 / 14640748308400909
42. Dickinson A, Nicholas DJ, Adams CD. Effekterna av instrumental beredskap på mottaglighet för förstärkningsdevaluering. QJ Exp Psychol (1983) 35B: 35-51. doi: 10.1080 / 14640748308400912
43. Corbit LH, Balleine BW. Hippocampus roll i instrumentell konditionering. J Neurosci (2000) 20(11): 4233-9.
44. Yin HH, Ostlund SB, Knowlton BJ, Balleine BW. Den dorsomediala striatans roll i instrumentell konditionering. Eur J Neurosci (2005) 22:513–23. doi:10.1111/j.1460-9568.2005.04218.x
45. Yin HH, Knowlton BJ, Balleine BW. Lesioner av dorsolateralt striatum bevarar förväntningarna på utfallet men stör vanligtbildning i instrumentellt lärande. Eur J Neurosci (2004) 19:181–9. doi:10.1111/j.1460-9568.2004.03095.x
46. Quinn JJ, Pittenger C, Lee AS, Pierson JL, Taylor JR. Striatumberoende vanor är okänsliga för både ökningar och minskningar i förstärkningsvärde hos möss. Eur J Neurosci (2013) 37: 1012-21. doi: 10.1111 / ejn.12106
47. Yin HH. Från handlingar till vanor: neuro-anpassningar som leder till beroende. Alkohol Res Health (2008) 31(4): 340-4.
48. Belin D, Jonkman S, Dickinson A, Robbins TW, Everitt BJ. Parallella och interaktiva inlärningsprocesser i basala ganglier: relevans för förståelsen av missbruk. Behav Brain Res (2009) 199(1):89–102. doi:10.1016/j.bbr.2008.09.027
49. Schwabe L, Dickinson A, Wolf OT. Stress, vanor och drogberoende: ett psykoneuroendokrinologiskt perspektiv. Exp Clin Psychopharmacol (2011) 19(1):53–63. doi:10.1037/a0022212
50. Hogarth L, Balleine BW, Corbit LH, Killcross S. Associerande inlärningsmekanismer som ligger till grund för övergången från narkotikamissbruk till missbruk. Ann NY Acad Sci (2013) 1282(1):12–24. doi:10.1111/j.1749-6632.2012.06768.x
51. Murray JE, Belin D, Everitt BJ. Dubbel dissociation av dorsomedial och dorsolateral striatal kontroll över förvärv och prestanda av kokain sökande. Neuropsychopharmacology (2012) 37(11):2456–66. doi:10.1038/npp.2012.104
52. Clemens KJ, Castino MR, Cornish JL, Goodchild AK, Holmes NM. Beteende- och nervsubstrat för vanligt bildning hos råttor intravenöst självadministrerande nikotin. Neuropsychopharmacology (2014) 39: 2584-93. doi: 10.1038 / npp.2014.111
53. Corbit LH, Nie H, Janak PH. Vanligt svar på alkohol beror på både AMPA och D2-receptorsignaler i det dorsolaterala striatum. Front Behav Neurosci (2014) 8: 301. doi: 10.3389 / fnbeh.2014.00301
54. Schoenbaum G, Setlow B. Kokain gör handlingar okänsliga för resultat men inte utrotning: implikationer för förändrad orbitofrontal-amygdalar funktion. Cereb Cortex (2005) 15(8):1162–9. doi:10.1093/cercor/bhh216
55. Nelson A, Killcross S. Amfetamineksponeringen förbättrar bildningen av vanor. J Neurosci (2006) 26(14):3805–12. doi:10.1523/JNEUROSCI.4305-05.2006
56. Nordquist RE, Voorn P, De Mooij-van Malsen JG, Joosten RNJMA, Pennartz CMA, Vanderschuren LJMJ. Förstärkt förstärkningsvärde och accelererad vanliga bildning efter upprepad amfetaminbehandling. Eur Neuropsychopharmacol (2007) 17(8):532–40. doi:10.1016/j.euroneuro.2006.12.005
57. LeBlanc KH, Maidment NT, Ostlund SB. Upprepad kokaineksponering underlättar uttrycket av incitamentmotivering och inducerar vanligt kontroll hos råttor. PLoS One (2013) 8: E61355. doi: 10.1371 / journal.pone.0061355
58. Nelson AJ, Killcross S. Accelererad vanliga bildning efter exponering av amfetamin återförs av D1, men förbättras av D2, receptorantagonister. Främre Neurosci (2013) 7: 76. doi: 10.3389 / fnins.2013.00076
59. Corbit LH, Chieng BC, Balleine BW. Effekter av upprepad kokaineksponering på vanliga inlärning och reversering av N-acetylcystein. Neuropsychopharmacology (2014) 39(8):1893–901. doi:10.1038/npp.2014.37
60. Miles FJ, Everitt BJ, Dickinson A. Oral kokain som söker av råttor: handling eller vana? Behav Neurosci (2003) 117(5):927–38. doi:10.1037/0735-7044.117.5.927
61. Mangieri RA, Cofresí RU, Gonzales RA. Etanol som söker av Long Evans-råttor är inte alltid ett målstyrt beteende. PLoS One (2012) 7: E42886. doi: 10.1371 / journal.pone.0042886
62. Sjoerds Z, De Wit S, Van Den Brink W, Robbins TW, Beekman ATF, Penninx BWJH, et al. Beteende och neuroimaging bevis för över-förlust av vana inlärning hos alkoholberoende patienter. Transl Psychiatry (2013) 3(12): e337. doi: 10.1038 / tp.2013.107
63. Packard MG, McGaugh JL. Efterträning av quinpirol- och d-amfetaminadministration förbättrar minnet på rumsliga och ledde diskrimineringar i en vattenlaze. Psycho (1994) 22(1): 54-60.
64. Matthews DB, Ilgen M, White AM, Best PJ. Akut etanoladministration försämrar den rumsliga prestanda medan den underlättar nonspatialprestanda hos råttor. Neurobiol Lär Mem (1999) 72(3):169–79. doi:10.1006/nlme.1998.3900
65. Bohbot VD, Balso D, Conrad K, Konishi K, Leyton M. Caudate-kärnberoende navigationsstrategier är associerade med ökad användning av beroendeframkallande läkemedel. hippocampus (2013) 23(11):973–84. doi:10.1002/hipo.22187
66. Poldrack RA, Packard MG. Konkurrens mellan flera minnessystem: konvergerande bevis från djur- och människohjärnstudier Neuropsychologia (2003) 41(3):245–51. doi:10.1016/S0028-3932(02)00157-4
67. Matthews DB, Bästa PJ. Fimbria / fornix-lesioner underlättar inlärningen av en nonspatial responsuppgift. Psychon Bull Rev (1995) 2(1):113–6. doi:10.3758/BF03214415
68. Schroeder JP, Wingard JC, Packard MG. Vändbar inaktivering av hippocampus efter träning avslöjar störningar mellan minnessystem. hippocampus (2002) 12(2):280–4. doi:10.1002/hipo.10024
69. Matthews DB, Simson PE, Bästa PJ. Akut etanol försämrar rumsligt minne men inte stimulans / svarminne hos råtta. Alkoholklin Exp Exp (1995) 19(4):902–9. doi:10.1111/j.1530-0277.1995.tb00965.x
70. White AM, Elek TM, Beltz TL, Best PJ. Rymdprestanda är mer känslig för etanol än icke-patialprestanda oavsett signifikans närhet. Alkoholklin Exp Exp (1998) 22(9):2102–7. doi:10.1111/j.1530-0277.1998.tb05922.x
71. Matthews DB, Morrow AL, Tokunaga S, McDaniel JR. Akut administrering av etanol och akut administrering av allopregnanolone försämrar det rymliga minnet i Morris vattenuppgiften. Alkoholklin Exp Exp (2002) 26(11):1747–51. doi:10.1111/j.1530-0277.2002.tb02479.x
72. Berry RB, Matthews DB. Akut etanoladministration försämrar selektivt rumsligt minne i C57BL / 6J-möss. Alkoholer (2004) 32(1):9–18. doi:10.1016/j.alcohol.2003.09.005
73. Silvers JM, Tokunaga S, Berry RB, White AM, Matthews DB. Försämringar i rumsligt lärande och minne: etanol, allopregnanolone och hippocampus. Brain Res Rev (2003) 43(3):275–84. doi:10.1016/j.brainresrev.2003.09.002
74. Badanich KA, Becker HC, Woodward JJ. Effekter av kronisk intermittent etanolexponering på orbitofrontala och mediala prefrontala cortexberoende beteenden hos möss. Behav Neurosci (2011) 125(6):879–91. doi:10.1037/a0025922
75. Coleman LG Jr, He J, Lee J, Styner M, Crews FT. Adolescent binge drink förändrar vuxen hjärnneurotransmitter genuttryck, beteende, regionala volymer i hjärnan och neurokemi hos möss. Alkoholklin Exp Exp (2011) 35(4):671–88. doi:10.1111/j.1530-0277.2010.01385.x
76. Kuzmin A, Liljequist S, Meis J, Chefer V, Shippenberg T, Bakalkin G. Upprepade etanolutfall med måttlig dos försämrar den kognitiva funktionen hos Wistar-råttor. Addict Biol (2012) 17(1):132–40. doi:10.1111/j.1369-1600.2010.00224.x
77. Coleman LG, Liu W, Oguz I, Styner M, Crews FT. Behandling med ung etsol av ungdomar förändrar regionala volymer för hjärnor hos vuxna hjärnor, extracellulärt matrixprotein och beteendeflexibilitet. Pharmacol Biochem Behav (2014) 116: 142-51. doi: 10.1016 / j.pbb.2013.11.021
78. Matthews DB, Silvers JR. Användning av akut etanoladministration som ett verktyg för att undersöka flera minnessystem. Neurobiol Lär Mem (2004) 82(3):299–308. doi:10.1016/j.nlm.2004.06.007
79. Broening HW, Morford LL, Inman-Wood SL, Fukumura M, Vorhees CV. 3, 4-metylendioxymmetamfetamin (ecstasy) -inducerad inlärning och minnesnedsättning beror på exponeringsåldern under tidig utveckling. J Neurosci (2001) 21(9): 3228-35.
80. Williams MT, Morford LL, Wood SL, Wallace TL, Fukumura M, Broening HW, et al. Utvecklingsbehandling av d-metamfetamin inducerar selektivt rumsliga navigationssvårigheter i referensminnet i Morris-vattenlaze medan man sparar arbetsminnet. Synapsen (2003) 48(3):138–48. doi:10.1002/syn.10159
81. Vorhees CV, Reed TM, Skelton MR, Williams MT. Exponering för 3, 4-metylendioxymetamfetamin (MDMA) på postnatala dagar 11-20 framkallar referens men inte fungerar minnesunderskott i Morris vatten labyrint hos råttor: implikationer av tidigare inlärning. Int J Dev Neurosci (2004) 22(5):247–59. doi:10.1016/j.ijdevneu.2004.06.003
82. Cohen MA, Skelton MR, Schaefer TL, Gudelsky GA, Vorhees CV, Williams MT. Lärande och minne efter neonatal exponering för 3, 4-metylendioxymmetamfetamin (ecstasy) hos råttor: interaktion med exponering i vuxen ålder. Synapsen (2005) 57(3):148–59. doi:10.1002/syn.20166
83. Skelton MR, Williams MT, Vorhees CV. Behandling med MDMA från P11-20 stör störningar i rumsligt lärande och vägintegration hos ungdomliga råttor men endast rumsligt lärande hos äldre råttor. Psychopharmacology (2006) 189(3):307–18. doi:10.1007/s00213-006-0563-4
84. Ma MX, Chen YM, He J, Zeng T, Wang JH. Effekter av morfin och dess tillbakadragande rymdigenkänningsminne hos Y-labyrint hos möss. Neuroscience (2007) 147(4):1059–65. doi:10.1016/j.neuroscience.2007.05.020
85. Belcher AM, Feinstein EM, O'Dell SJ, Marshall JF. Metamfetamin påverkar igenkänningsminnet: jämförelse av eskalerande och en-dagars doseringsregimer. Neuropsychopharmacology (2008) 33(6):1453–63. doi:10.1038/sj.npp.1301510
86. Tramullas M, Martínez-Cué C, Hurlé MA. Kronisk administration av heroin till möss producerar uppreglering av hjärnapoptosrelaterade proteiner och försämrar rumsligt lärande och minne. Neuro (2008) 54(4):640–52. doi:10.1016/j.neuropharm.2007.11.018
87. North A, Swant J, Salvatore MF, Gamble-George J, Prins P, Butler B, et al. Kronisk exponering av metamfetamin ger ett försenat, långvarigt minneunderskott. Synapsen (2013) 67(5):245–57. doi:10.1002/syn.21635
88. Fole A, Martin M, Morales L, Del Olmo N. Effekter av kronisk kokainbehandling under tonåren hos råttor Lewis och Fischer-344: nedsatt nedsatt lägesigenkänning och förändringar i synaptisk plasticitet i vuxen ålder. Neurobiol Lär Mem (2015) 123: 179-86. doi: 10.1016 / j.nlm.2015.06.001
89. Zhou M, Luo P, Lu Y, Li CJ, Wang DS, Lu Q, et al. Obalans mellan HCN1 och HCN2-uttryck i hippocampal CA1-område försämrar rumsligt lärande och minne hos råttor med kronisk morfineksponering. Prog Neuropsychopharmacol Biolpsykiatri (2015) 56: 207-14. doi: 10.1016 / j.pnpbp.2014.09.010
90. Kathirvelu B, Colombo PJ. Effekter av lentivirusmedierat CREB-uttryck i det dorsolaterala striatum: minneförbättring och bevis för konkurrerande och kooperativa interaktioner med hippocampus. hippocampus (2013) 23(11):1066–74. doi:10.1002/hipo.22188
91. Baudonnat M, Guillou JL, Husson M, Vandesquille M, Corio M, Decorte L, et al. Störande effekt av läkemedelsinducerad belöning på rumslig men inte ledningsinriktad inlärning: implikation av striatal proteinkinas A / cAMP-svarelementbindande proteinväg. J Neurosci (2011) 31:16517–28. doi:10.1523/JNEUROSCI.1787-11.2011
92. Packard MG, Wingard JC. Amygdala och "emotionell" modulering av den relativa användningen av flera minnessystem. Neurobiol Lär Mem (2004) 82(3):243–52. doi:10.1016/j.nlm.2004.06.008
93. Elliott AE, Packard MG. Intra-amygdala ängslig infusion innan läkemedelsförspänningar råttor mot användning av vanligt minne. Neurobiol Lär Mem (2008) 90(4):616–23. doi:10.1016/j.nlm.2008.06.012
94. Wingard JC, Packard MG. Amygdala och känslomässig modulation av konkurrens mellan kognitivt minne och vaneminne. Behav Brain Res (2008) 193(1):126–31. doi:10.1016/j.bbr.2008.05.002
95. Packard MG, Gabriele A. Perifera ängslar injektioner av läkemedel påverkar differentiellt kognitivt minne och vaneminne: roll för basolateral amygdala. Neuroscience (2009) 164(2):457–62. doi:10.1016/j.neuroscience.2009.07.054
96. Leong KC, Goodman J, Packard MG. Buspirone blockerar den förstärkande effekten av det ängsliga läkemedlet RS 79948-197 på konsolidering av vaneminnet. Behav Brain Res (2012) 234(2):299–302. doi:10.1016/j.bbr.2012.07.009
97. Goodman J, Leong KC, Packard MG. Glukokortikoidförstärkning av dorsolateralt striatumberoende vanminne kräver samtidig noradrenerg aktivitet. Neuroscience (2015) 311: 1-8. doi: 10.1016 / j.neuroscience.2015.10.014
98. Kim JJ, Lee HJ, Han JS, Packard MG. Amygdala är avgörande för stressinducerad modulering av hippocampal långsiktig potentiering och inlärning. J Neurosci (2001) 21(14): 5222-8.
99. Schwabe L, Dalm S, Schächinger H, Oitzl MS. Kronisk stress modulerar användningen av rumsliga och stimulerande responsinlärningsstrategier hos möss och människor. Neurobiol Lär Mem (2008) 90(3):495–503. doi:10.1016/j.nlm.2008.07.015
100. Leong KC, Packard MG. Exponering för rovdjurlukt påverkar den relativa användningen av flera minnessystem: basolateral amygdala. Neurobiol Lär Mem (2014) 109: 56-61. doi: 10.1016 / j.nlm.2013.11.015
101. Taylor SB, Anglin JM, Paode PR, Riggert AG, Olive MF, Conrad CD. Kronisk stress kan underlätta rekryteringen av vanor och beroende-relaterade neurocircuitries genom neuronal omstrukturering av striatum. Neuroscience (2014) 280: 231-42. doi: 10.1016 / j.neuroscience.2014.09.029
102. Leong KC, Goodman J, Packard MG. Efterexponering av exponering för rädsla betingade stimuli förbättrar minneskonsolidering och förspänner råttor mot användning av dorsolateralt striatumberoende responsinlärning. Behav Brain Res (2015) 291: 195-200. doi: 10.1016 / j.bbr.2015.05.022
103. Goode TE, Leong KC, Goodman J, Maren S, Packard MG. Förbättring av striatumberoende minne med konditionerad rädsla förmedlas av beta-adrenerga receptorer i basolaterala amygdala. Neurobiologi av stress (i pressen). doi: 10.1016 / j.ynstr.2016.02.004
104. Schwabe L, Oitzl MS, Philippsen C, Richter S, Bohringer A, Wippich W, et al. Stress modulerar användningen av rumsliga kontra stimulans-respons inlärningsstrategier hos människor. Lär Mem (2007) 14(1–2):109–16. doi:10.1101/lm.435807
105. Schwabe L, Schächinger H, de Kloet ER, Oitzl MS. Kortikosteroider fungerar som en växel mellan minnessystem. J Cogn Neurosci (2010) 22(7):1362–72. doi:10.1162/jocn.2009.21278
106. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Samtidig glukokortikoid och noradrenergisk aktivitet förskjuter instrumentellt beteende från målstyrd till vanligt kontroll. J Neurosci (2010) 30(24):8190–6. doi:10.1523/JNEUROSCI.0734-10.2010
107. Schwabe L, Tegenthoff M, Höffken O, Wolf OT. Mineralokortikoidreceptorblockad förhindrar stressinducerad modulering av flera minnessystem i den mänskliga hjärnan. Biolpsykiatri (2013) 74(11):801–8. doi:10.1016/j.biopsych.2013.06.001
108. Schwabe L, Wolf OT. Stress uppmanar vanligt beteende hos människor. J Neurosci (2009) 29(22):7191–8. doi:10.1523/JNEUROSCI.0979-09.2009
109. Schwabe L, Wolf OT. Socialt utvärderad kallpressstress efter instrumental lärande gynnar vanor över målinriktad handling. Psychon (2010) 35(7):977–86. doi:10.1016/j.psyneuen.2009.12.010
110. Guenzel FM, Wolf OT, Schwabe L. Glukokortikoid stimulerar stimulans-responsminnesbildning hos människor. Psychon (2014) 45: 21-30. doi: 10.1016 / j.psyneuen.2014.02.015
111. Higgins RL, Marlatt GA. Rädsla för interpersonell utvärdering som en avgörande faktor för alkoholkonsumtionen hos manliga sociala dricker. J Abnorm Psychol (1975) 84(6):644–51. doi:10.1037/0021-843X.84.6.644
112. Marlatt GA, Gordon JR. Determinanter för återfall: konsekvenser för upprätthållandet av beteendeförändring. I: Davidson PO, Davidson SM, redaktörer. Beteendemedicin: förändrade livsstilar. New York: Brunne / Mazel (1980). s. 410-52.
113. Newcomb MD, Bentler PM. Påverkan av ungdomars droganvändning och socialt stöd på unga vuxnas problem: en longitudinell studie. J Abnorm Psychol (1988) 97:64–75. doi:10.1037/0021-843X.97.1.64
114. Wallace BC. Psykologiska och miljömässiga determinanter för återfall hos crack-kokainrökare. J Subst Abuse Treat (1989) 6(2):95–106. doi:10.1016/0740-5472(89)90047-0
115. Kaplan HB, Johnson RJ. Förhållanden mellan omständigheter kring initial olaglig droganvändning och upptrappning av droganvändning: moderera effekterna av kön och upplevelser från tidiga tonåringar I: Glantz M, Pickens R, redaktörer. Sårbarhet för missbruk av narkotika. Washington, DC: American Psychological Association (1992). s. 200-358.
116. Harrison PA, Fulkerson JA, Beebe TJ. Multipel substansanvändning bland ungdomars fysiska och sexuella övergreppsoffer. För missbruk av barnmissbruk (1997) 21:529–39. doi:10.1016/S0145-2134(97)00013-6
117. Chilcoat HD, Breslau N. Posttraumatisk stressstörning och läkemedelsstörningar: testning av kausalvägar. Arch Gen Psychiatry (1998) 55(10):913–7. doi:10.1001/archpsyc.55.10.913
118. Piazza PV, Le Moal M. Stressens roll vid självadministrering av läkemedel. Trends Pharmacol Sci (1998) 19(2):67–74. doi:10.1016/S0165-6147(97)01115-2
119. Goodman J, Leong KC, Packard MG. Emotionell modulering av flera minnessystem: implikationer för neurobiologin vid posttraumatisk stressstörning. Rev Neurosci (2012) 23(5–6):627–43. doi:10.1515/revneuro-2012-0049
120. Sinha R, Lacadie C, Skudlarski P, Fulbright RK, Rounsaville BJ, Kosten TR, et al. Neural aktivitet förknippad med stressinducerad kokaintrang: en funktionell magnetisk resonansavbildningstudie. Psychopharmacology (2005) 183(2):171–80. doi:10.1007/s00213-005-0147-8
121. Avena NM, Rada P, Hoebel BG. Bevis för sockerberoende: beteende- och neurokemiska effekter av intermittent, överdrivet sockerintag. Neurosci Biobehav Rev (2008) 32(1):20–39. doi:10.1016/j.neubiorev.2007.04.019
122. Gearhardt AN, Corbin WR, Brownell KD. Matberoende: en undersökning av de diagnostiska kriterierna för beroende. J Addict Med (2009) 3(1):1–7. doi:10.1097/ADM.0b013e318193c993
123. Smith DG, Robbins TW. De neurobiologiska förutsättningarna för fetma och binge ätande: en grund för att anta livsmedelsmodellen. Biolpsykiatri (2013) 73(9):804–10. doi:10.1016/j.biopsych.2012.08.026
124. de Jong JW, Meijboom KE, Vanderschuren LJ, Adan RA. Låg kontroll över smakligt matintag hos råttor är förknippat med vanligt beteende och återfallssårbarhet: individuella skillnader. PLoS One (2013) 8(9): e74645. doi: 10.1371 / journal.pone.0074645
125. Furlong TM, Jayaweera HK, Balleine BW, Corbit LH. Binge-liknande konsumtion av en smakrik mat påskyndar vanligt kontroll av beteende och är beroende av aktivering av det dorsolaterala striatum. J Neurosci (2014) 34(14):5012–22. doi:10.1523/JNEUROSCI.3707-13.2014
126. Hargrave SL, Davidson TL, Zheng W, Kinzig KP. Västra dieter inducerar läckage av blod-hjärnbarriär och förändrar rumsstrategier hos råttor. Behav Neurosci (2016) 130(1):123–35. doi:10.1037/bne0000110
127. Smith KL, Hummer TA, Hulvershorn LA. Patologisk videospel och dess förhållande till ämnesanvändningsstörningar. Curr Addict Rep (2015) 2(4):302–9. doi:10.1007/s40429-015-0075-6
128. Weinstein AM. Dator- och videospelberoende - en jämförelse mellan spelanvändare och icke-spelanvändare. Am J Drug Alcohol Abuse (2010) 36(5):268–76. doi:10.3109/00952990.2010.491879
129. Kätsyri J, Hari R, Ravaja N, Nummenmaa L. Motståndaren är viktig: förhöjda fMRI-belöningssvar för att vinna mot en människa kontra en datormotståndare under interaktiv videospel. Cereb Cortex (2013) 23(12):2829–39. doi:10.1093/cercor/bhs259
130. Kätsyri J, Hari R, Ravaja N, Nummenmaa L. Att bara titta på spelet är inte tillräckligt: striatal fMRI belöner svar på framgångar och misslyckanden i ett videospel under aktiv och vicarious spelning. Front Hum Neurosci (2013) 7: 278. doi: 10.3389 / fnhum.2013.00278
131. Erickson KI, Boot WR, Basak C, Neider MB, Prakash RS, Voss MW, et al. Striatal volym förutspår nivån på förvärv av videospel. Cereb Cortex (2010) 20: 2522-30. doi: 10.1093 / cercor / bhp293
132. West GL, Drisdelle BL, Konishi K, Jackson J, Jolicoeur P, Bohbot VD. Vanligt förekommande videospel spelas i samband med caudatkärnberoende navigationsstrategier. Proc R Soc B (2015) 282(1808). doi: 10.1098 / rspb.2014.2952
133. Liu S, Schad DJ, Kuschpel MS, Rapp MA, Heinz A. Musik och videospel under pauser: påverkan av vanligt kontra målriktat beslutsfattande. Uppsats presenterat vid 45th årsmöte i Society for Neuroscience. Chicago, IL: Society for Neuroscience (2015).
134. de Fonseca FR, Carrera MRA, Navarro M, Koob GF, Weiss F. Aktivering av kortikotropinfrisättande faktor i det limbiska systemet under uttag av cannabinoid. Vetenskap (1997) 276(5321):2050–4. doi:10.1126/science.276.5321.2050
135. Cornelius JR, Chung T, Martin C, Wood DS, Clark DB. Tillbakadragande av cannabis är vanligt bland behandlingssökande ungdomar med cannabisberoende och större depression och är förknippade med snabbt återfall till beroende. Addict Behav (2008) 33(11):1500–5. doi:10.1016/j.addbeh.2008.02.001
136. Greene MC, Kelly JF. Förekomsten av tillbakadragande av cannabis och dess påverkan på ungdomars behandlingsrespons och resultat: en prospektiv XNM-månaders utredning. J Addict Med (2014) 8: 359-67. doi: 10.1097 / ADM.0000000000000064
137. Wagner FA, Anthony JC. Från första läkemedelsanvändning till drogberoende; utvecklingsperioder med risk för beroende av marijuana, kokain och alkohol. Neuropsychopharmacology (2002) 26:479–88. doi:10.1016/S0893-133X(01)00367-0
138. Goodman J, Packard MG. Påverkan av cannabinoider på inlärning och minnesprocesser i dorsal striatum. Neurobiol Lär Mem (2015) 125: 1-14. doi: 10.1016 / j.nlm.2015.06.008
139. Rueda-Orozco PE, Soria-Gomez E, Montes-Rodriguez CJ, Martínez-Vargas M, Galicia O, Navarro L, et al. En potentiell funktion av endocannabinoider i valet av en navigationsstrategi av råttor. Psychopharmacology (2008) 198(4):565–76. doi:10.1007/s00213-007-0911-z
140. Goodman J, Packard MG. Perifera och intra-dorsolaterala striatuminjektioner av cannabinoidreceptoragonisten WIN 55,212-2 försämrar konsolideringen av stimulus-responsminnet. Neuroscience (2014) 274: 128-37. doi: 10.1016 / j.neuroscience.2014.05.007
141. Nazzaro C, Greco B, Cerovic M, Baxter P, Rubino T, Trusel M, et al. SK-kanalmodulering räddar striatal plasticitet och kontroll över vana vid cannabinoidtolerans. Nat Neurosci (2012) 15: 284-93. doi: 10.1038 / nn.3022
142. Ames SL, Grenard JL, Stacy AW, Xiao L, He Q, Wong SW, et al. Funktionell avbildning av implicita marijuanaföreningar under utförande på ett implicit associeringstest (IAT). Behav Brain Res (2013) 256: 494-502. doi: 10.1016 / j.bbr.2013.09.013
143. Redish AD, Jensen S, Johnson A. En enhetlig ram för beroende: sårbarheter i beslutsprocessen. Behav Brain Sci (2008) 31(04):415–37. doi:10.1017/S0140525X0800472X
144. Brevers D, Bechara A, Cleeremans A, Noël X. Iowa Gambling Task (IGT): tjugo år efter - spelstörning och IGT. Front Psychol (2013) 4: 665. doi: 10.3389 / fpsyg.2013.00665
145. Koob GF, Le Moal M. Neurobiologiska mekanismer för motståndares motivationsprocesser i beroende. Philos Trans R Soc B Biol Sci (2008) 363(1507):3113–23. doi:10.1098/rstb.2008.0094
146. Hyman SE, Malenka RC, Nestler EJ. Neurologiska missbruksmekanismer: rollen som belöningsrelaterat lärande och minne. Annu Rev Neurosci (2006) 29: 565-98. doi: 10.1146 / annurev.neuro.29.051605.113009
147. Goodman J, Packard M. Det minnessystem som används vid förvärv bestämmer effektiviteten hos olika utrotningsprotokoll. Front Behav Neurosci (2015) 9: 314. doi: 10.3389 / fnbeh.2015.00314
148. Palencia CA, Ragozzino ME. NMDA-receptors bidrag i det dorsolaterala striatum till egocentrisk responsinlärning. Behav Neurosci (2005) 119(4):953–60. doi:10.1037/0735-7044.119.4.953
149. Rueda-Orozco PE, Montes-Rodriguez CJ, Soria-Gomez E, Méndez-Díaz M, Prospéro-García O. Försämring av aktivitet av endocannabinoider i det dorsolaterala striatum försenar utrotning av beteende i en procedurminnesuppgift hos råttor. Neuro (2008) 55(1):55–62. doi:10.1016/j.neuropharm.2008.04.013
Nyckelord: minne, narkotikamissbruk, hippocampus, striatum, amygdala, stress, ångest
Citation: Goodman J och Packard MG (2016) Memory Systems and the Addicted Brain. Främre. Psykiatri 7: 24. doi: 10.3389 / fpsyt.2016.00024
Mottaget: 01 december 2015; Godkänd: 11 februari 2016;
Publicerad: 25 februari 2016
Redigerad av:
David Vincent, Centre National de la Recherche Scientifique (CNRS), Frankrike
Recenserad av:
Jacques Micheau, University of Bordeaux 1, Frankrike
Roberto Ciccocioppo, University of Camerino, Italien
Copyright: © 2016 Goodman och Packard. Detta är en artikel med öppen åtkomst som distribueras under villkoren för Creative Commons Attribution License (CC BY). Användning, distribution eller reproduktion i andra forum är tillåten, förutsatt att den ursprungliga författaren eller licensgivaren krediteras och att den ursprungliga publikationen i denna tidskrift är citerad i enlighet med godkänd akademisk praxis. Ingen användning, distribution eller reproduktion tillåts som inte överensstämmer med dessa villkor.
* Korrespondens: Mark G. Packard, [e-postskyddad]
